
Аляутдин большой
.pdf
Глава 24. Средства, применяемые при атеросклерозе |
533 |
|
|
|
|
|
|
|
|
кислот |
кислоты |
Секвестранты |
Жёлчные |
жёлчных |
Жёлчные |
средств |
кислоты |
|
|
Рис. 24.3. Механизмы действия гиполипидемических |
534 |
Часть II. Частная фармакология |
Захват ЛПНП периферическими тканями происходит путем рецепторозависимого эндоцитоза, который активирует содержащийся в ЛПНП Апо B-100 (этим же обусловлена высокая атерогенность ЛПНП). Гепатоциты также могут поглощать ЛПНП в случае недостатка ХС. Все классы липопротеинов, содержащие Апо B-100 и осуществляющие транспорт ХС от печени к периферическим тканям (ЛПОНП, ЛППП, ЛПНП), атерогенны.
После утилизации ХС периферическими тканями избыток его выводится на поверхность клеточных мембран. В плазме он соединяется с ФЛ, Апо А-1, Апо А-2, Апо E и Апо C. Таким образом формируются ЛПВП — транспортная система, осуществляющая транспорт избытка ХС от периферических тканей к печени. Этот класс липопротеинов содержит Апо Е, который обеспечивает поглощение ЛПВП печенью, пополняя депо свободного ХС. В то же время ЛПВП не содержат Апо B-100 и, таким образом, не захватываются периферическими тканями. Этими факторами объясняются их так называемые антиатерогенные свойства.
В патогенезе атеросклероза важную роль играет нарушение баланса между доставкой липидов к периферическим тканям и возвратом излишков в печень. Часто отмечают одновременное снижение содержания ЛПВП и увеличение ЛПНП. В результате возникает гиперлипопротеинемия (повышение уровня липопротеинов в плазме крови). Выделяют 5 типов гиперлипопротеинемий, причем не все типы атерогенны (табл. 24.2).
Таблица 24.2. Характеристика гиперлипопротеинемий
Тип |
Повышены |
Атерогенность |
Молекулярный дефект |
Группы |
|
|
|
|
препаратов |
|
|
|
|
|
I |
Хиломикроны, ХС (+) |
Отсутствует |
Липопротеинлипаза. |
– |
|
ТГ (+++) |
|
Апо С-2 |
|
IIa |
ЛПНП, ХС (++) |
Высокая |
Рецептор |
Статины + |
|
|
|
ЛПНП |
секвестранты |
|
|
|
Апо В-100 |
|
IIb |
ЛПНП (+) |
Высокая |
Неизвестен |
Фибраты, |
|
ЛПОНП, ХС (++) |
|
|
статины, |
|
ТГ (++) |
|
|
никотиновая |
|
|
|
|
кислота |
III |
3-ЛПОНП, ХС (++) |
Умеренная |
Апо E |
Фибраты |
|
ТГ (++) |
|
|
|
IV |
ЛПОНП, ХС (+) |
Умеренная |
Неизвестен |
Фибраты |
|
ТГ (++) |
|
|
|
V |
ЛПВП |
Отсутствует |
Неизвестен |
– |
Глава 24. Средства, применяемые при атеросклерозе |
535 |
При формировании атеросклеротических бляшек запускается местный воспалительный процесс, в ходе которого образуются активные формы кислорода. Это запускает процессы перекисного окисления (модификации) ЛПНП в зоне эндотелиального поврежедния. Мононуклеарные фагоциты поглощают модифицированные ЛПНП и превращаются в так называемые пенистые клетки, которые затем мигрируют в субэндотелиальный слой интимы, усиливая воспалительный процесс и продукцию активных форм кислорода. Погибая, они формируют некротический центр бляшки.
В соответствии с этим в фармакотерапии атеросклероза представляется целесообразным:
●уменьшение концентрации атерогенных липопротеинов в плазме крови (достигается применением гиполипопротеинемических средств);
●уменьшение перекисного окисления липопротеинов;
●снижение образования свободных радикалов (достигается применением антиоксидантов);
●уменьшение повреждения интимы сосудов (достигается применением эндотелиотропных ангиопротекторных средств) (см. главу «Ангиопротекторы»).
24.1.ГИПОЛИПИДЕМИЧЕСКИЕ СРЕДСТВА (АНТИГИПЕРЛИПОПРОТЕИНЕМИЧЕСКИЕ СРЕДСТВА)
Группу гиполипидемических средств составляют препараты, снижающие в плазме крови содержание атерогенных липопротеинов. При этом, как правило, происходит компенсаторное увеличение в плазме крови уровня ЛПВП, обладающих антиатерогенным действием.
К атерогенным липопротеинам относят ЛПНП, ЛПОНП, ЛППП. Пути их метаболизма и механизмы действия основных групп гиполипидемических средств представлены на рис. 24.3. В печени из ТГ и ХС синтезируются ЛПОНП. Они выделяются в системный кровоток и там под действием эндотелиальной липопротеинлипазы превращаются в ЛППП, а затем в ЛПНП.
Главная причина, приводящая к снижению концентрации всех типов атерогенных липопротеинов в плазме крови, — уменьшение запасов ХС в гепатоцитах. Это приводит к увеличению плотности (экспрессии) липопротеиновых рецепторов и увеличению рецепторозависимого эндоцитоза липопротеинов из плазмы крови (с целью пополнения запасов ХС в пе-
536 |
Часть II. Частная фармакология |
чени), а также снижению синтеза ЛПОНП. Конечным результатом этого становится уменьшение в плазме крови атерогенных липопротеинов.
Гиполипидемические средства представлены следующими группами препаратов:
●ингибиторы 3-гидрокси-3-метилглутарил-коэнзим А редуктазы (ГМГКоА редуктазы) (статины, ингибиторы синтеза ХС);
●средства, угнетающие всасывание ХС в кишечнике;
●секвестранты желчных кислот;
●производные фиброевой кислоты (фибраты, активаторы липопротеинлипазы);
●препараты никотиновой кислоты (ингибиторы триглицеридлипазы).
24.1.1. Ингибиторы 3-гидрокси-3-метилглутарил-коэнзим А редуктазы (статины)
В настоящее время это одна из наиболее часто применяемых групп гиполипидемических средств. Препараты этой группы — препараты выбора при различных типах гиперлипидемий в связи с высокой эффективностью
иотносительной безопасностью, а также наличием ряда других, так на-
зываемых плейотропных эффектов.
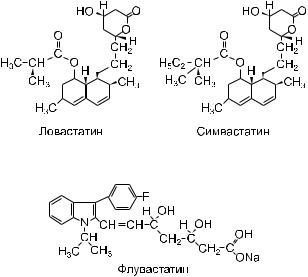
Представители группы статинов — ловастатин (мевакор♠), симвастатин
(зокор♠), правастатин (липостат♠), флувастатин (лескол♠), розувастатин
иаторвастатин (липримар♠, аторис♠).
Механизм гиполипидемического действия статинов заключается
вугнетении синтеза ХС (см. рис. 24.2). Статины конкурентно обратимо ингибируют ГМГ-КоА-редуктазу, что вызывает угнетение синтеза ХС на этапе образования мевалоновой кислоты. В результате запасы ХС
впечени уменьшаются, что приводит к экспрессии ЛПНП-рецепторов на гепатоцитах и увеличению рецепторозависимого эндоцитоза атерогенных липопротеинов. Кроме того, уменьшается образование в печени и выделение в кровь ЛПОНП. Увеличение захвата и уменьшение выделения печенью атерогенных липопротеинов приводит к снижению их концентрации в плазме крови (гиполипидемическому эффекту). Кроме того, при применении статинов повышается уровень ЛПВП в плазме крови.
Основное показание к применению статинов — гиперлипопротеинемия типов IIа и IIb. Препараты назначают внутрь 1 раз в сутки на ночь. При комбинированном применении с секвестрантами желчных кислот статины назначают либо за 1 ч, либо через 4 ч после приема секвестранта.
Статины применяют длительно (в течение нескольких месяцев), переносят их относительно хорошо. Побочные эффекты: диспептические рас-
Глава 24. Средства, применяемые при атеросклерозе |
537 |
стройства, бессонница, головная боль, эритема кожи, сыпь. Зависимый от дозы побочный эффект — гепатотоксичность (с повышением уровня трансаминаз или без него). Нечасто возникают, но наиболее тяжело протекают миопатия и рабдомиолиз.
Ловастатин получают из грибка Aspergillus terreus, а симвастатин и правастатин — его химические производные (полусинтетические препараты). Все три статина содержат в структуре гидронафталеновое кольцо (взаимодействует с ГМГ-КоА-редуктазой), а также оксикислоту (придает сходство
смевалонатом) в боковой цепи. Ловастатин и симвастатин (рис. 24.4) — пролекарства, неактивные лактоны, приобретающие фармакологическую активность в процессе гидролиза в β-оксикислоты.
Флувастатин (рис. 24.5) — синтетический препарат, производное мевалонолактона. Содержит в структуре фторфенилиндольную часть (придает сходство с коэнзимом А), а также боковую цепь (придает сходство
смевалонатом). Правастатин и флувастатин содержат в своей химической структуре оксикислоты, поэтому они фармакологически активны в исходном состоянии.
Биодоступность статинов при введении внутрь невелика, наиболее низкая у ловастатина и симвастатина — менее 5%, у аторвастатина — 14%, у правастатина — 18% и флувастатина — около 24%. Низкая биодо-
Рис. 24.4. Химические структуры ловастатина и симвастатина
Рис. 24.5. Химическая структура флувастатина
538 |
Часть II. Частная фармакология |
ступность статинов связана с их активным захватом печенью при первом прохождении. Взаимодействие статинов с пищей различно. Так, биодоступность ловастатина возрастает, если препарат принимают после еды, биодоступность симвастатина не зависит от приема пищи, а биодоступность правастатина и флувастатина уменьшается, если препараты приняты после еды. Максимальная концентрация в крови ловастатина и симвастатина достигается через 2–4 ч, а правастатина и флувастатина — через 0,75–1,5 ч и 0,5 ч соответственно. Через ГЭБ и плаценту хорошо проникают ловастатин и симвастатин (благодаря липофильности), а флувастатин, правастатин и аторвастатин практически не проходят через эти барьеры.
В настоящее время считают, что антиатеросклеротическое действие статинов обусловлено не только их гиполипидемическим эффектом, но и рядом других, так называемых плейотропных эффектов, к которым относят:
●восстановление функций эндотелия (препятствуют повреждающему действию окисленных ЛПНП на сосудистую стенку);
●сосудорасширяющий (экспрессия NO-синтетазы);
●антиишемический (увеличение толерантности к физической нагрузке);
●антитромбогенный (снижение количества и агрегации тромбоцитов, уменьшение количества тромбина, повышение фибринолиза);
●уменьшение пролиферации гладких мышц кровеносных сосудов (вероятно, за счет угнетения ГМГ-КоА редуктазы и синтеза ХС в ангиомиоцитах);
●противовоспалительный.
Наиболее эффективен среди статинов аторвастатин. При приеме внутрь он абсорбируется на 80%, биодоступность — 14% (ввиду пресистемного метаболизма). Препарат метаболизируется в печени системой цитохрома Р450 3А4. При этом образуются активные метаболиты (орто- и парагидроксилированные производные, продукты β-окисления), которые оказывают ингибирующее действие на ГМГ-КоА-редуктазу и сохраняются 20–30 ч. Выводится аторвастатин преимущественно с желчью, t½ составляет 14 ч. В качестве плейотропных эффектов вызывает:
●противоаритмическое действие и увеличение сердечного выброса (связаны с улучшением коронарного кровообращения);
●противовоспалительное действие (проявляется снижением уровня С-реактивного белка);
●стабилизацию и обратное развитие атеросклеротических бляшек, улучшение психического, физического самочувствия и качества жизни (связаны с улучшением мозгового кровообращения).

Глава 24. Средства, применяемые при атеросклерозе |
539 |
24.1.2. Средства, угнетающие всасывание холестерина в кишечнике
Относительно новая группа гиполипидемических средств, представитель которой — эзетимиб.
Эзетимиб (эзетрол♠, инеджи♠, мертенил♠) избирательно угнетает всасывание ХС в кишечнике, при этом не влияет на всасывание других стероидов (рис. 24.6). Избирательность связана с особенностями транспорта ХС через кишечную стенку (рис. 24.7). Транспорт ХС в эпителиоциты осуществляется при участии специфического транспортера NPС1L1. Кро-
ме того, в клетках эпителия кишечника |
|
существуют АТФ-связывающие кас- |
|
сетные переносчики АВСG5 и АВСG8, |
|
которые выводят стеролы (в том числе |
|
ХС) из эпителиоцитов в просвет ки- |
|
шечника. Эзетимиб угнетает NPС1L1 |
|
и активирует кассетные транспортеры. |
|
В результате всасывание ХС в кишеч- |
Рис. 24.6. Химическая структура |
нике с последующим его включением |
эзетимиба |
в хиломикроны снижается. |
|
При применении эзетимиба гиперхолестеринемия уменьшается на 18%. Эзетимиб метаболизируется на 80% с образованием активного метаболита эзетимиб-глюкуронида. Подвергается энтерогепатической циркуляции, благодаря чему долго не выводится из организма (t½ около 22 ч).
Наиболее эффективен эзетимиб в комбинации с симвастатином. Комбинированный препарат виторин♠ содержит эзетимиба 10 мг и симвастатина 10, 20, 40 или 80 мг.
Помимо гиполипидемического действия эзетимиб вызывает плейотропный эффект в виде противовоспалительного действия (при применении препарата более чем вдвое снижается уровень С-реактивного белка
вплазме крови).
24.1.3.Секвестранты желчных кислот
Колестирамин (квестран♠) и колестипол (холестид♠) — анионообменные смолы примерно одинаковой эффективности.
Секвестранты желчных кислот образуют в кишечнике невсасывающиеся комплексы с желчными кислотами, что приводит к усилению выведения желчных кислот из организма (см. рис. 24.2). Нарушение энтерогепатической циркуляции желчных кислот вызывает увеличение их синтеза

540 |
Часть II. Частная фармакология |
|
|
|
|
Рис. 24.7. Механизм действия эзетимиба

Глава 24. Средства, применяемые при атеросклерозе |
541 |
de novo в печени из эндогенного ХС. Запасы ХС в печени при этом истощаются, что приводит к экспрессии ЛПНП-рецепторов на мембране гепатоцитов и увеличению рецепторозависимого эндоцитоза атерогенных липопротеинов. Их содержание в плазме крови снижается. Концентрация ЛПВП в плазме крови либо не изменяется, либо несколько повышается.
Колестирамин (рис. 24.8) и колестипол
применяют при гиперлипопротеинемии
IIа типа внутрь в 2–3 приема в течение 14 дней. Действие препаратов начинается через 24–48 ч, продолжительность действия — 12–24 ч. Пик действия достигается в течение месяца. Эффект сохраняется в течение 2–4 нед после отмены препарата. Побочные эффекты: запоры, тошнота, изжога, метеоризм, головная боль.
24.1.4. Производные фиброевой кислоты (фибраты)
К препаратам этой группы относят гемфиброзил (регулип♠, иполипид♠), фенофибрат (липантил♠), безафибрат, ципрофибрат (липанор♠).
За счет активации PPARα (рецепторы, активируемые пероскисомными полифераторами) фибраты вызывают экспрессию эндотелиальной липопротеин липазы (см. рис. 24.2), что ускоряет катаболизм ЛПОНП
иЛППП. Кроме того, фибраты увеличивают синтез Апо А, угнетают синтез ХС в печени (возможно, ингибируя ГМГ-КоА-редуктазу) и синтез из него ЛПОНП. При применении фибратов увеличивается плотность липопротеиновых рецепторов в гепатоцитах, снижается уровень ЛПНП, а также повышается уровень ЛПВП.
Фибраты назначают при гиперлипопротеинемии II, IV и V типов, они эффективно снижают уровень ТГ. Из побочных эффектов отмечают диспептические расстройства, головную боль, затуманенное зрение, холелитиаз, миалгию, миопатии, реже — рабдомиолиз. Ввиду того, что фибраты
истатины вызывают сходные побочные эффекты со стороны мышечной ткани (миопатии), эти группы препаратов нельзя комбинировать.
Гемфиброзил (рис. 24.9) при приеме внутрь хорошо всасывается из ЖКТ в кровь, его биодоступность составляет 97%, пик плазменной концентрации достигается через 1–2 ч, метаболизируется в печени,
t½ после приема однократной дозы составляет 1,5 ч. Препарат выводится из организма почками в количестве 70% (большая часть в неизмененном виде). Гиполипидемический эффект гемфиброзила начинается через

542 |
Часть II. Частная фармакология |
2–5 дней, пик действия наступает через 4 нед. Препарат обычно назначают в 2 приема за 30–40 мин до еды.
Фенофибрат — пролекарство, превращающееся в тканях в фенофиброевую кислоту (см. рис. 24.9). При длительном применении препарат значительно снижает уровень общего ХС (на 16–35%) и ТГ (на 30–60%). Кроме того, препарат обладает урикозурическим действием. Пролонгированная форма содержит фенофибрат в микронизированной форме, имеет улучшенные фармакокинетические показатели, позволяющие назначать препарат 1 раз в сутки.
Ципрофибрат (см. рис 24.9) отличается от других фибратов большим значением t½ (48–120 ч), несколько лучше переносится, его назначают 1 раз в день после еды вечером.
Рис. 24.9. Химическая структура гемфиброзила, фенофибрата и ципрофибрата
24.1.5. Препараты никотиновой кислоты
В эту группу препаратов входят никотиновая кислота (рис. 24.10) (ниацин♠) и ее пролонгированные формы (эндурацин♠).
Гиполипидемическое действие никотиновой кислоты связано с тем, что она угнетает триглицерид липазу в адипоцитах (см. рис. 24.2). Как следствие, в жировой ткани снижается образование свободных жирных кислот, они не мобилизуются и не захватываются печенью. В результате в печени уменьшается биосинтез ТГ и образование из них ЛПОНП. Уровни ЛПОНП, ЛППП и ЛПНП в плазме крови снижаются, а уровень антиатерогенных ЛПВП повышается.
При приеме внутрь препарат быстро и хорошо всасывается из ЖКТ, биодоступность 72%. В организме препарат подвергается метаболизму в пе-
