- •Лекции №13-15 алкены
- •Изомерия и номенклатура алкенов
- •Методы получения алкенов
- •Физические свойства алкенов
- •Химические свойства
- •Реакция гидрирования.
- •2. Реакции электрофильного присоединения по двойной связи алкенов.
- •С другой стороны, ряд реакционной способности галогеноводородов
- •3. Взаимодействие с катионами металлов.
- •4. Гидроборирование алкенов.
- •5. Взаимодействие с с-электрофилами.
- •6. Реакции циклоприсоединения.
- •7. Реакции окисления алкенов.
- •8. Реакции полимеризации.
- •9. Гидроформилирование или оксосинтез
- •10. Радикальные реакции алкенов.
10. Радикальные реакции алкенов.
Выше уже упоминались радикальные реакции алкенов, такие как гидробромирование в присутствие пероксидов и радикальная полимеризация. Другими радикальными реакциями с участием алкенов являются:
а) теломеризация
Теломеризация – олигомеризация алкенов в присутствии веществ – передатчиков цепи (телогенов). В результате реакции образуется смесь олигомеров (теломеров), концевые группы которых представляют собой части телогена. Например, в реакции CCl4 с этиленом телогеном является CCl4.
CCl4 + nCH2=CH2 Cl(CH2CH2)4CCl3
Инициирование этих реакций может осуществляться радикальными инициаторами или -излучением. Это обусловливает свободнорадикальный характер реакций теломеризации:
Инициирование:
CCl4 hv;((( Cl + CCl3
Развитие цепей:
CH2=CH2 + CCl3 CH2CH2CCl3
CH2CH2CCl3 + CH2=CH2 CH2CH2CH2CH2CCl3
Передача цепи:
CH2CH2CH2CH2CCl3 + CCl4 CCl3 + Cl-CH2CH2CH2CH2CCl3
б) Присоединение H2S и RSH в присутствии инициаторов радикальных реакций.
RCH=CH2 + H2S ROOR;((((( RCH2CH2SH
RCH=CH2 + RSH ROOR;((((( RCH2CH2SR
Можно видеть, что такое присоединение идет против правила Марковникова. Обоснование такого порядка присоединения такое же, как и в случае свободнорадикального гидробромирования алкенов. (см. выше)
Осуществление гидробромирования, тиогидратации и других подобных реакций алкенов следует проводить в условиях избытка аддента (т.е. вещества, присоединяющегося к алкену), чтобы подавить побочную реакцию полимеризации. Необходимость такого решения можно проиллюстрировать на примере реакций тиогидратации:
Инициирование:
I2 2I
I + H2S HI + HS
Развитие цепей (тиогидратация)
RCH=CH2 + HS RCHCH2SH
![]()
Р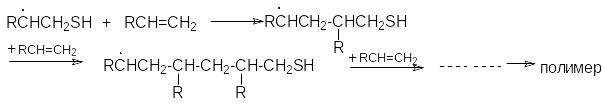 азвитие
цепи (полимеризация)
азвитие
цепи (полимеризация)
В кратком виде конкуренция реакций тиогидратации и полимеризации может быть представлена схемой:
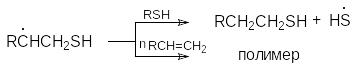
Из этой схемы очевидно вытекает необходимость применения избытка адденда для подавления побочной реакции полимеризации.
в) Галогенирование кратной связи.
Cl2 и Br2 могут присоединяться по двойной связи алкена по свободноразикальному механизму. Эти реакции протекают гораздо быстрее, чем реакции ионного галогенирования, но требуют химического или фотохимического инициирования.
Механизм этих реакций можно проиллюстрировать на примере бромирования:
Инициирование:
Br2 hv;((( 2Br
Развитие цепей:
RCH=CH2 + Br RCH-CH2Br
RCH-CH2Br + Br2 RCHBr-CH2Br + Br
Обрыв цепей:
B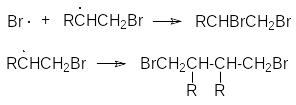 r
+ Br
Br2
r
+ Br
Br2
г) Аллильное замещение галогенами.
В условиях высоких температур (300-400оС) пропен и другие алкилзамещенные алкены хлорируются в паровой фазе в аллильное положение.
CH2=CH-CH3 + Cl2 t;(( CH2=CH-CH2Cl + HCl
Такое направление хлорирования связано со стабильностью аллильного радикала, образующегося при реализации радикально-цепного процесса:
Инициирование:
Cl2 + M 2Cl + M
Развитие цепей:
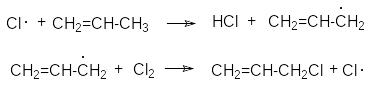
Обрыв цепей:
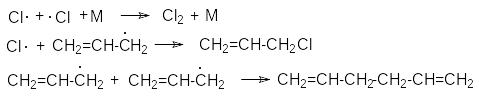
В то же время возможность присоединительного хлорирования путем реализации последовательности реакций
C H2=CH-CH3
+ Cl
Cl-CH2CH-CH3
H2=CH-CH3
+ Cl
Cl-CH2CH-CH3
Cl-CH2CH-CH3 + Cl2 Cl-CH2CHCl-CH3
практически исключена, поскольку высоко-экзотермическое равновесие присоединения хлор-радикала к двойной связи в условиях высоких температур практичеки нацело смещено в левую строну.
Аллильное бромирование можно провести в лабораторных условиях, используя N-бромсукцинимид и инициатор свободнорадикальных реакций