
- •Лекции №13-15 алкены
- •Изомерия и номенклатура алкенов
- •Методы получения алкенов
- •Физические свойства алкенов
- •Химические свойства
- •Реакция гидрирования.
- •2. Реакции электрофильного присоединения по двойной связи алкенов.
- •С другой стороны, ряд реакционной способности галогеноводородов
- •3. Взаимодействие с катионами металлов.
- •4. Гидроборирование алкенов.
- •5. Взаимодействие с с-электрофилами.
- •6. Реакции циклоприсоединения.
- •7. Реакции окисления алкенов.
- •8. Реакции полимеризации.
- •9. Гидроформилирование или оксосинтез
- •10. Радикальные реакции алкенов.
Методы получения алкенов
Дегидрирование и крекинг алканов.
CH3CH2CH2CH3 [Cr2O3];450 C;(((((( CH3CH=CH-CH3 + H2
При более высоких температурах происходит также разрыв связей С-С и получаются смеси различных алканов и алкенов, у которых молекулярная масса меньше, чем у исходных алканов (крекинг).

 СH2=CH2
+ CH3CH3
СH2=CH2
+ CH3CH3
CH4 + CH2=CH-CH3
CH3CH2CH2CH3 Cr2O3;500-600C;((((((( H2 + CH2=CH-CH2-CH3
H2 + CH3-CH=CH-CH3
Эти методы имеют промышленное значение.
2. Дегидратация спиртов.
R-CH2CH2OH cat;300-350 C;((((((( R-CH=CH2 + H2O
В качестве катализаторов используются Бренстедовские или Льюисовские кислоты, например H3PO4 и Al2O3. В первом случае фосфорную кислоту наносят на пористый носитель, например, силикагель.
Особенностью этих реакций является порядок отщепления воды, определяемый правилом Зайцева: при отщеплении воды наиболее легко отщепляется водород от соседнего наименее гидрированного атома углерода.
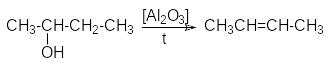
Такой характер отщепления может быть обоснован более высокой термодинамической стабильностью алкенов, у которых наибольшее число заместителей при двойной связи.
Реакции дегидратации имеют препаративное и промышленное значение. Так, в промышленности изобутилен получают дегидротацией изобутилового спирта.
3. Дегидрогалогенирование галогеналканов.
Эта реакция может осуществляться в двух вариантах:
а) щелочное дегидрогалогенирование
CH3CH2Br + KOH [спирт];t;(((((( CH2=CH2 + KBr + H2O
Порядок отщепления галогеноводорода в этих реакциях также определяется правилом Зайцева: при отщепление HHal наиболее легко отщепляется водород от наименее гидрированного атома углерода.
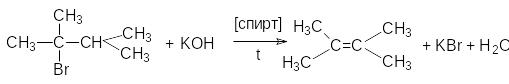
б) термическое дегидрогалогенирование в паровой фазе.
CH3CH2CH2Cl 400-500 C;((((((( CH3CH=CH2 + HCl
В отличие от щелочного дегидрогалогенирования эта реакция мало избирательна и при наличии нескольких неэквивалентных атомов водорода при вицинальном углеродном атоме образуется смесь алкенов.
Методы имеют препаративное и промышленное значение.
4. Отщепление галогенов от вицинальных дигалогеналканов металлическим цинком.
R-CHBr-CHBr-R' + Zn t;(( R-CH=CH-R' + ZnBr2
5. Селективное гидрирование диенов и алкинов.
CH2=CH-CH=CH2 + H2 [Ni];(((( CH3-CH=CH-CH3
R-CC-R' + H2 [Pb/PbCO3];(((((((( R-CH=CH-R'
6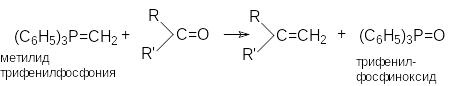 .
Реакция Виттига - взаимодействие
карбонильных групп с фосфоний - илидами.
.
Реакция Виттига - взаимодействие
карбонильных групп с фосфоний - илидами.
Сами фосфоний - илиды могут быть получены дегидрогалогенированием соответствующим галоидных солей фосфония под действия основания.
[(C6H5)3PCH3]+Br- + C6H5Li;((((((( (C6H5)3P=CH2 + LiBr + C6H6
7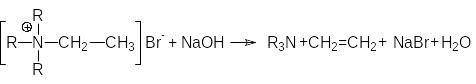 .
Реакция Гофмана - расщепление четвертичных
аммониевых солей под действием оснований.
.
Реакция Гофмана - расщепление четвертичных
аммониевых солей под действием оснований.
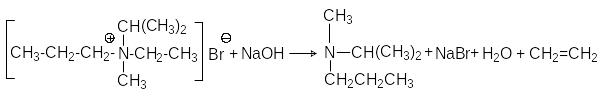
Характер образующихся продуктов определяется правилом Гофмана: при расщеплении образуется наименее замещенный алкен. Например:
Обоснованием правила Гофмана является относительная кислотность атомов водорода при -углеродных атомах: наименее кислыми являются атомы водорода при наиболее разветвленных углеродных атомах,так как образующиеся при отрыве от них анионы существенно дестабилизированы алкильными группами и такое отщепление становится энергетически невыгодным.
