- •Лекции №13-15 алкены
- •Изомерия и номенклатура алкенов
- •Методы получения алкенов
- •Физические свойства алкенов
- •Химические свойства
- •Реакция гидрирования.
- •2. Реакции электрофильного присоединения по двойной связи алкенов.
- •С другой стороны, ряд реакционной способности галогеноводородов
- •3. Взаимодействие с катионами металлов.
- •4. Гидроборирование алкенов.
- •5. Взаимодействие с с-электрофилами.
- •6. Реакции циклоприсоединения.
- •7. Реакции окисления алкенов.
- •8. Реакции полимеризации.
- •9. Гидроформилирование или оксосинтез
- •10. Радикальные реакции алкенов.
Лекции №13-15 алкены
План.
Изомерия и номенклатура алкенов.
Методы получения.
Физические и химические свойства.
Алкены (олефины) - углеводороды, в молекулах которых содержится одна двойная углерод-углеродная связь >C=C<, а все остальные атомы углерода находятся в sp3 - состояния.
Алкены образуют гомологический ряд соединений, состав которых выражается эмпирической формулой CnH2n.
Изомерия и номенклатура алкенов
Структурная изомерия алкенов начинается с четвертого члена ряда, однако, число структурных изомеров по сравнению с соответствующими алканами значительно больше. Это связано с тем, что структурная изомерия алкенов определяется двумя факторами: строением углеродного скелета и положением двойной связи углеродной цепи. У алкенов проявляется и другой вид изомерии - пространственная (геометрическая) или цис-транс-изомерия. Так как свободного вращения по двойной связи не происходит, определенные заместители могут фиксироваться по одной стороне двойной связи (цис-изомер), или по противоположным сторонам (транс-изомер):
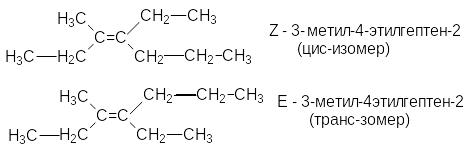
Н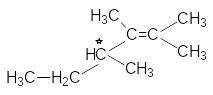 аличие
в молекулах алкенов третичных
углеводородных атомов с четырьмя
различными заместителями обусловливает
их хиральность и, как следствие, наличие
стереоизомеров.
аличие
в молекулах алкенов третичных
углеводородных атомов с четырьмя
различными заместителями обусловливает
их хиральность и, как следствие, наличие
стереоизомеров.
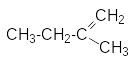
Название алкенов по номенклатуре IUPAC образуются из названий аналогично построенных алканов заменой окончания "ан" на "ен" с указанием цифрой местоположения двойной связи. В качестве родоначальной структуры выбирается самая длинная углеродная цепь, содержащая двойную связь. Нумерация атомов углерода в родоначальной структуре начинается с конца, к которому ближе расположена двойная связь. Иногда употребляется тривиальные и старые рациональные названия алкенов. Так, по рациональной номенклатуре алкены рассматриваются как результат замещения атомов водорода в этилене на алкильные группы.
Названия.
соединения |
IUPAC |
рациональная |
тривиальная |
СH2=СH2 |
этен |
этилен |
|
CH3CH=CH2 |
пропен |
метилэтилен |
пропилен |
CH2=CH-CH2 -CH3 |
1-бутен |
этилэтилен |
бутилен |
|
2-бутен |
симм. диметилэтилен |
псевдобутилен |
|
2-метилпропен |
несимм. диметилэтилен |
изобутилен |
CH2=CH-CH2CH2CH3 |
1-пентен |
пропилэтилен |
Амилен |
|
2-пентен |
симм. метилэтилен |
- |
|
3-метил-2-бутен |
изопропилэтилен |
- |
|
2-метил-2бутен |
триметилэтилен |
- |
|
2-метил-1-бутен |
несимм. метилэтилэтилен |
- |
|
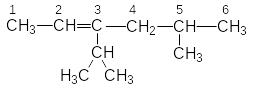
5-метил-3-изопропил-2-гексен |
- |
- |
Названия остатков алкенов (алкенильных групп) образуют присоединением к названию алкена суффикса "ил". Некоторые остатки алкенов сохраняют тривиальные названия:
CH2=CH- этенил или винил
3 2 1
CH2=CH-CH2- пропенил-2 или аллил
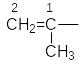
1-метилэтенил или изопропенил
3 2 1
CH3-CH=CH- пропенил-1
Для обозначения геометрических изомеров используется Z, E- номенклатура, согласно которой обозначения Z используется для цис-изомеров, а Е - для транс-изомеров. Обозначения Z и Е- выбираются по пространственному расположению самых старших групп. Старшинство углеводородных заместителей увеличивается в ряду:

Чтобы отнести изомер к Z- или Е- ряду необходимо среди четырех заместителей у двойной связи найти два самых старших. Если оба старших заместителя расположены по одну сторону плоскости, в которой лежит двойная связь, изомер относится к Z-ряду, в противном случае к Е-ряду. (см. пример названий выше).

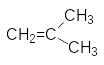 CH3-CH=CH-CH3
CH3-CH=CH-CH3
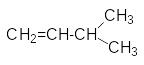 CH3-CH=CH-CH2-CH3
CH3-CH=CH-CH2-CH3