
- •Лекции №13-15 алкены
- •Изомерия и номенклатура алкенов
- •Методы получения алкенов
- •Физические свойства алкенов
- •Химические свойства
- •Реакция гидрирования.
- •2. Реакции электрофильного присоединения по двойной связи алкенов.
- •С другой стороны, ряд реакционной способности галогеноводородов
- •3. Взаимодействие с катионами металлов.
- •4. Гидроборирование алкенов.
- •5. Взаимодействие с с-электрофилами.
- •6. Реакции циклоприсоединения.
- •7. Реакции окисления алкенов.
- •8. Реакции полимеризации.
- •9. Гидроформилирование или оксосинтез
- •10. Радикальные реакции алкенов.
5. Взаимодействие с с-электрофилами.
А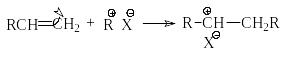 лкены
присоединяют сильные С-электрофилы, к
которым относятся карбкатионы, которые
генерируются в реакционной смеси обычно
в виде ионных пар:
лкены
присоединяют сильные С-электрофилы, к
которым относятся карбкатионы, которые
генерируются в реакционной смеси обычно
в виде ионных пар:
В результате образуется новый карбкатион, который может претерпевать дальнейшие превращения, например, присоединяться к следующей молекуле алкена. Многократное возобновление акта присоединения растущего карбкатиона к очередной молекуле алкена лежит в основе катионной полимеризации алкенов.
6. Реакции циклоприсоединения.
Алкены способны вступать в реакции, в которых образуется цикл. Такие реакции называются циклоприсоединением.
Эти реакции подразделяются в зависимости от числа атомов, участвующих в образовании цикла (цифры в квадратных скобках)
a) Циклоприсоединение [2+1].
К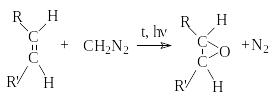 этому типу относятся реакции алкенов
с карбенами.
этому типу относятся реакции алкенов
с карбенами.
б) Циклоприсоединение [2+2].
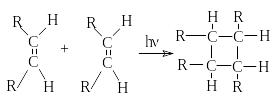
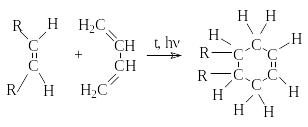
в) Циклоприсоединение [2+4].
7. Реакции окисления алкенов.
а) Окисление разбавленными растворами KMnO4 в слабощелочной среде (окисление по Вагнеру).
R-CH=CHR + KMnO4;H2O[OH-];((((((( R-CH(OH)-CH(OH)-R
Э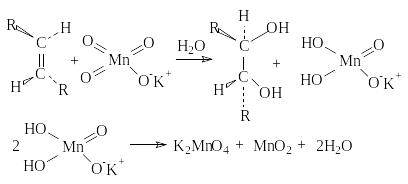 та
реакция протекает стереоселективно
как цис-присоединение двух гидроксильных
групп:
та
реакция протекает стереоселективно
как цис-присоединение двух гидроксильных
групп:
б) Окисление концентрированными растворами окислителей.
(KmnO4, CrO3, HNO3)
При действии этих окислителей происходит разрыв молекулы алкена по месту двойной связи с образованием кетонов и кислот.
(CH3)2C=CH-CH3 CrO3;(((( (CH3)2C=O + CH3COOH
ацетон уксусная кислота
CH3CH=CH-CH2CH3 KMnO4 конц.;[H2SO4];((((((((( CH3COOH + HOOC-CH2CH3
уксусная пропионовая
кислота кислота
Эта реакция широко используется для определения строения алкенов.
в) Озонолиз.
Озонолиз представляет собой комбинацию последовательных реакций озонирования и гидролиза:
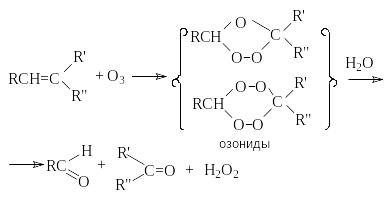
Озонолиз используют для установления строения алкена, так как его результаты является селективное расщепление молекулы алкена по месту двойной связи.
г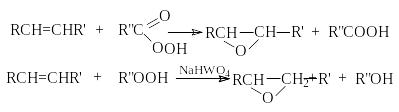 )
Окисление пероксикислотами и
гидропероксидами (реакция Прилежаева).
)
Окисление пероксикислотами и
гидропероксидами (реакция Прилежаева).
Результатом этих реакций является синтез эпоксидов, соединений, содержащих трехчленный оксидный цикл.
П ромышленный
вариант реакции эпоксидирования связан
с каталитическим окислением этилена
кислородом или воздухом на нанесенных
серебряных катализаторах.
ромышленный
вариант реакции эпоксидирования связан
с каталитическим окислением этилена
кислородом или воздухом на нанесенных
серебряных катализаторах.
д) Окисление алкенов в присутствии PdCI2.
CH2=CH2 + 1/2O2 PdCl2;100-300 C;((((((( CH3CHO ацетальдегид
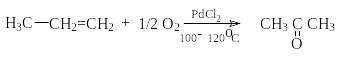
ацетон
Этот метод реализован в промышленности для получения ацетальдегида. В настоящее время это наиболее прогрессивный способ получения ацетальдегида (Вакер-процесс). Промышленный катализатор представляет собой трехкомпонентную систему PdCl2-CuCl2-HCl. Каталитический цикл состоит из трех сопряженных реакций:
окисления алкена хлорида палладия
CH2=CH2 + PdCl2 + H2O CH3CHO + Pd + 2HCl
регенерации хлорида палладия хлоридом меди (II)
Pd + 2CuCl2 PdCl2 + 2CuCl
регенерации CuCI2 кислородом в присутствии соляной кислоты
2CuCl + 2HCl + 1/2O2 2CuCl2 + H2O
П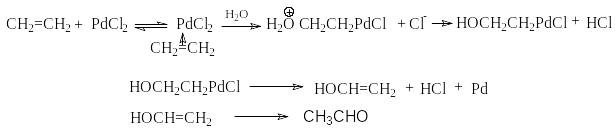 ервая
стадия этого цикла протекает через
образование -комплекса
PdCl2
с алкеном с последующим разложением
комплекса водой:
ервая
стадия этого цикла протекает через
образование -комплекса
PdCl2
с алкеном с последующим разложением
комплекса водой:
Замена в Вакер-процессе воды уксусной кислотой позволяет получать в промышленном масштабе винилацетат.
CH2=CH2 + CH3COOH + 1/2O2 PdCl2;((((( CH3COOCH=CH2 + H2O
