
metodichka_Lipidy_2020
.pdf
Ацетил-КоА образуется в матриксе как при распаде углеводов и кетогенных аминокислот, так и ВЖК. Синтез ВЖК происходит в абсорбтивный период, когда β-окисление выключается, поэтому именно избыток углеводов, поступающих в организм, трансформируется в жирные кислоты, а затем в жиры.
АсСоА образуются при декарбоксилировании пирувата в митохондиях, а используются на синтез ВЖК - в цитозоле. Внутренняя мембрана митохондрий непроницаема для ацетил-КоА, поэтому в роли переносчика ацетильных групп из митохондрий выполняет цитрат, концентрация которого в абсорбтивный период повышается. Это связано с образованием в абсорбтивный период больших количеств АТФ и NADH - аллостерических ингибиторов ферментов ЦТК: изоцитратдегидрогеназы и α-кетоглутаратдегидрогеназного комплекса, цикл Кребса замедляется и накапливается цитрат, образуемый в реакции переноса ацетильной группы на оксалоацетат (первая реакция ЦТК):
Далее цитрат переносится и в цитоплазме |
расщепляется под действием |
фермента цитратлиазы на ацетил-КоА и ОАА: |
|
Этот процесс является энергозависимым, поскольку связан с использованием
АТФ.
Оксалоацетат в цитозоле подвергается следующим превращениям:
+СО2
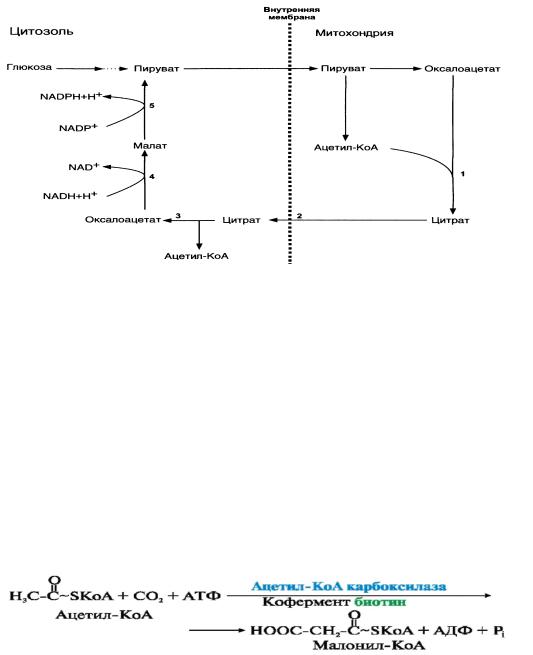
Пируват транспортируется обратно в матрикс митохондрий. Восстановленный в результате действия малик-фермента НАДФН используется как донор водорода для последующих реакций синтеза жирных кислот (другой источник НАДФН - окислительные стадии пентозофосфатного пути катаболизма глюкозы) (рис. 2.2.).
Перенос ацетильного остатка из митохондрий в цитозоль (Т-Транслоказа) при участии ферментов: 1-цитратсинтаза, 2-транслоказа, 3-цитратлиаза, 4- малатдегидрогеназа, 5-малик-фермент.
В цитозоле ацетил-КоА карбоксилируется и превращается в малонил-КоА - второй субстрат, необходимый для образования жирной кислоты. Реакцию катализирует биотин-зависимый фермент ацетил-КоА-карбоксилаза с участием АТФ. Реакция протекает в 2 этапа. На первом - СО2 связывается в активном центре с биотином, а на втором этапе - СО2 переносится на молекулу ацетил-КоА:
Фермент ацетил-СоА-карбоксилаза – регуляторный фермент, является сложным белком, содержащим в качестве простетической группы остаток фосфорилированного биотина (витамина Н).
После образования малонил-СоА синтез жирных кислот продолжается на мультиферментом комплексе – синтазе высших жирных кислот
(пальмитоилсинтазе).

Процесс синтеза жирной кислоты носит циклический характер. При каждом обороте цикла происходит удлинение жирной кислоты на два углеродных атома. Промежуточные продукты синтеза остаются связанными с ферментом вплоть до образования пальмитиновой
Рис. 2-3. Упрощенная схема биосинтеза кислоты. ВЖК
Мультиферментный комплекс - синтаза высших жирных кислот (пальмитоилсинтаза), состоит из 2 идентичных протомеров. Центральное место в каждом протомере занимает ацилпереносящий белок (АПБ, acyl-carrier protein, АСР), который последовательно соединяется с промежуточными продуктами биосинтеза и переносит их с одного активного центра на другой.

Простетической группой АПБ является производное пантотеновой кислоты – 4-фосфопантетеин (ФП) - фосфорилированное производное витамина пантотеновой кислоты, с которым связан остаток тиоэтаноламина. Простетическая группа АСР связывается с его полипептидной цепью через остаток серина. Структурно фосфопантотеиновая простетическая группа АПБ (АСР) соответствует аналогичной группе в коферменте А.
Протомеры синтазы ВЖК находятся в положении «голова к хвосту» и каждый содержит:
•7 активных центров и ацилпереносящий белок (АПБ)
•по две SH-группы (одна -у цистеина в составе кетоацилсинтазы, другая – у 4- фосфопантеината из АПБ)
Таким образом, в активном центре каждого из протомеров присутствуют 2 свободные SН-группы.
Реально синтезируются одновременно 2 жирных кислоты, но для упрощения в схемах изображают последовательность реакций для синтеза одной молекулы кислоты.
Мультиферментный комплекс синтазы ВЖК действует как роторный механизм по кругу: продукт, образованный на одном центре, с помощью АПБ перемещается в другой активный центр.
Началу синтеза высшей жирной кислоты предшествует перенос ацетильного и
малонильного остатков на SН-группы пальмитоилсинтазы |
: |
|
• |
ацетилтрансфераза осуществляет транспорт ацетил-СоА на SH-группу |
|
|
кетоацилсинтазного центра. |
|
• |
малонилтрансацилаза переносит малонил-СоА на SH-группу |
АПБ. |

После этого комплекс готов к первому циклу синтеза, состоящему из четырех реакций:
•декарбоксилирования малонильного остатка и конденсации ацетильной группы с остатком малонила по месту отделившегося СО2.
Продукт 2-оксобутирил-АПБ (2- оксоацил-АПБ) при участии
кетоацилсинтазного центра.
•восстановления 2-оксо группы с участием кофермента NADPH как донора водорода.
Продукт 2-оксибутирил-АПБ (2- оксиацил-АПБ) при участии
кетоацилредуктазного центра.
•дегидратации радикала с последующим образованием двойной связи при С2
Продукт – кротонил-АПБ (еноил-АПБ) при участии дегидратазного центра.

•восстановления с образованием бутирильного фрагмента при участии NADPH
Продукт бутирил–АПБ ( ацил-АПБ) при участии еноилредуктазного центра. (закончился 1-й цикл синтеза)
Далее следует прернос:
•радикала бутирила на SН-группу цистеина,
•малонила при участии малонилтрансацилазного центра
Затем остаток бутирила подвергается тем же превращениям и удлиняется на 2 углеродных атома, происходящих из малонил-КоА.

Аналогичные циклы реакций повторяются до тех пор, пока не образуется радикал пальмитиновой кислоты, который под действием тиоэстеразного центра гидролитически отделяется от ферментного комплекса, превращаясь в свободную пальмитиновую кислоту.
Суммарное уравнение синтеза пальмитиновой кислоты из ацетил-КоА и малонил-КоА имеет следующий вид:
Процесс биосинтеза жирных кислот является энергозависимым, поскольку использует АТФ для процессов карбоксилирования ацетил-СоА (при синтезе малонил-СоА) и транспорта ацетил-СоА из митохондрии (в цитратлиазной и пируваткарбоксилазной реакциях), и 2 НАДФН в восстановительных реакциях. Восстановленные NADPH организм получает частично из пентозофосфатного пути, а частично за счет работы малик-фермента.

Общая схема синтеза пальмитиновой кислоты.
1, 2- перенос ацетильной группы ацетил-КоА и малонила на АПБ; 3- декарбоксилирование малонильного остатка и конденсация 2 ацетильных остатков; 4 - восстановление β-карбонильной группы
5 - дегидратация - приводит к формированию двойной связи между α- и β- углеродными атомами;
6-восстановление и образование бутирильного фрагмента с участием NADPH.
1-й цикл синтеза закончился переносом радикала бутирила на SН-группу цистеина.
Представление о синтезе удлиненных и ненасыщенных ВЖК.
Жирные кислоты, радикал которых содержит более 16 атомов углерода, синтезируются в эндоплазматическом ретикулуме аналогично тому, как это

происходит на пальмитоилсинтазе: путем достраивания пальмитоила с помощью
малонил-КоА, доноров - NADPH + H+. Но |
каждую стадию процесса катализируют |
отдельные ферменты, а не комплекс. |
Первоначальным продуктом элонгации |
пальмитиновой кислоты является стеариновая кислота (С18:0), радикал которой в дальнейшем может увеличиваться до 24-26 углеродных атомов.
Стеариновая кислота является предшественником не только других высших насыщенных, но и ненасыщенных жирных кислот. В животных клетках
пальмитиновая |
|
|
и |
|
стеариновая |
кислоты |
могут |
использоваться |
|
только |
для |
образования |
моноеновых |
жирных |
кислот |
(пальмитолеиновой (С16:1) и олеиновой (С18:1). |
|
||
Моноеновые |
кислоты образуются |
при помощи десатуразной системы |
||
эндоплазматического ретикулума клетки. Функционирование этой ферментативной системы связано с существованием особых ферментов – оксигеназ со смешанной функцией - ацил-СоА-десатураз, которые одновременно окисляют два субстрата: НАДФН и насыщенную жирную кислоту (пальмитиновую или стеариновую).
Образование удлиненых и ненасыщенных ВЖК Образование полиеновых кислот в организме человека не происходит
(арахидоновая кислота синтезируется незначительно микрофлорой кисшечника). Комплекс полиеновых высших жирных кислот, основными компонентами которого служат линолевая и линоленовая кислоты, называют «витамин F».
 Полиеновые кислоты в растениях образуются из олеиновой и линолевой кислот, поэтому они для животных является незаменимым пищевым компонентом.
Полиеновые кислоты в растениях образуются из олеиновой и линолевой кислот, поэтому они для животных является незаменимым пищевым компонентом.

Синтез полиеновых кислот в растениях.
Регуляция биосинтеза ВЖК. Координированная регуляция синтеза и распада жирных кислот.
Ацетил-КоА-карбоксилаза - ключевой фермент биосинтеза ВЖК. В неактивной форме он представлен 3 отдельными тетрамерами. Активность фермента регулируется несколькими способами (рис. 2-6):
•ассоциацией/диссоциацией: объединение трех тетрамеров в единый комплекс из 12 субъединиц. Стимулирует ассоциацию и формирует активную форму фермента
-цитрат (активатор), подавляет - пальмитоил-КоА (ингибитор).
•фосфорилированием/дефосфорилированием: гормон глюкагон, передавая сигнал с помощью аденилатциклазной системы, активирует протеинкиназу А, которая фосфорилирует ацетил-КоА-карбоксилазу и переводит ее в неактивную
форму. Гормон инсулин активирует фосфопротеинфосфатазу (ФПФ), и ключевой
фермент |
переходит |
в |
дефосфорилированную |
форму: |
