
metodichka_Lipidy_2020
.pdf•в желудке, под действием желудочной липазы, продолжается частичное переваривание липидов (до 25 %), поскольку кислотность желудочного содержимого у младенцев сооветствует ее оптимуму (рН 5,5-7,5);
•В 12-перстной кишке эмульгированные желчью липиды на 50% расщепляются под влиянием липазы материнского молока. В коровьем молоке липазы мало,
поэтому |
скорость расщепления жиров в желудке детей, вскармливаемых |
искусственно, значительно меньше. |
|
Как и во взрослом организме, в кишечнике детей, происходит гидролиз большей части липидов с участием панкреатической липазы и колипазы до образования 2-МАГ (до 75%) и продуктов полного гидролиза - глицерина и жирных кислот.
До 7 лет активность панкреатической липазы невелика и достигает максимума к 8-9 годам.
Образование смешанной мицеллы и всасывание продуктов переваривания липидов
Плохо растворимые в водной среде, продукты гидролиза липидов: высшие жирные кислоты, 2-МАГ, холестерол, а также поступившие с пищей жирорастворимые витамины А, Д, Е, К включаются в мицеллы желчи, образуя смешанные мицеллы (рис. 1-5).
Мицелла – это сферический комплекс, в центре которого находятся транспортируемые гидрофобные продукты переваривания, окруженные желчными кислотами.
В состав гидрофобного ядра мицеллы входят: ацильные остатки жирных кислот, 2-моноацилглицеролов, неполярные группы холестерола и желчных кислот. Большую роль в формировании мицелл играют молекулы лизофосфатидной кислоты (продукт гидролиза фосфолипидов) и желчные кислоты, которые с помощью своих отрицательно заряженных групп образуют гидрофильную оболочку. Желчные
кислоты |
и их соли, стабилизируют смешанные мицеллы, |
способствуя их |
всасыванию в клетки кишечника. |
|
|
Смешанные мицеллы: |
|
|
• |
растворимы в водной фазе содержимого тонкой кишки |
|

•имеют малые размеры: в 100 раз меньше самых мелких эмульгированных жировых капель.
Рис. 1-5. Образование смешанной мицеллы Мицеллы перемещаются к всасывающей поверхности кишечного эпителия, а
затем, внутри клеток |
распадаются на составные компоненты. |
Проникновение |
мицелл в энтероцит регулируется гликокаликсом, |
покрывающим апикальную мембрану энтероцитов. Гликокаликс работает избирательно: отбрасывает назад в полость крупные гидрофобные молекулы и пропускает мелкие гидрофильные. Продукты ферментативного гидролиза липидов, которые хорошо растворимы в воде, такие как: глицерин, аминоспирты,
фосфорная кислота, жирные кислоты с короткой углеродной цепью (менее 10 атомов углерода) всасываются в кишечнике, попадая в энтероцит, а откуда поступают в кровь воротной вены и доставляются в печень.
Всосавшиеся продукты гидролиза в энтероцитах используются для синтеза липидов, близких по составу к липидам организма.
Желчные кислоты, оставшиеся в просвете кишечника и не вошедшие в состав мицелл, выводятся с калом (около 5%).
Потери желчных кислот в кишечнике (1-1,5 г) восполняются за счет их синтеза
в печени из холестерола. |
|
Основная масса |
желчных кислот (90-95%), поступивших из мицелл в |
энтероциты, всасывается и с кровью по воротной вене возвращаются обратно в печень. Откуда, через желчные протоки, они вновь поступают в желчный пузырь и затем, в составе простой мицеллы желчи, изливаются в кишечник. В этом случае имеет место постоянная циркуляция желчных кислот между печенью и кишечником. Данный процесс получил название энтерогепатической циркуляции желчных кислот (рис.1-6).
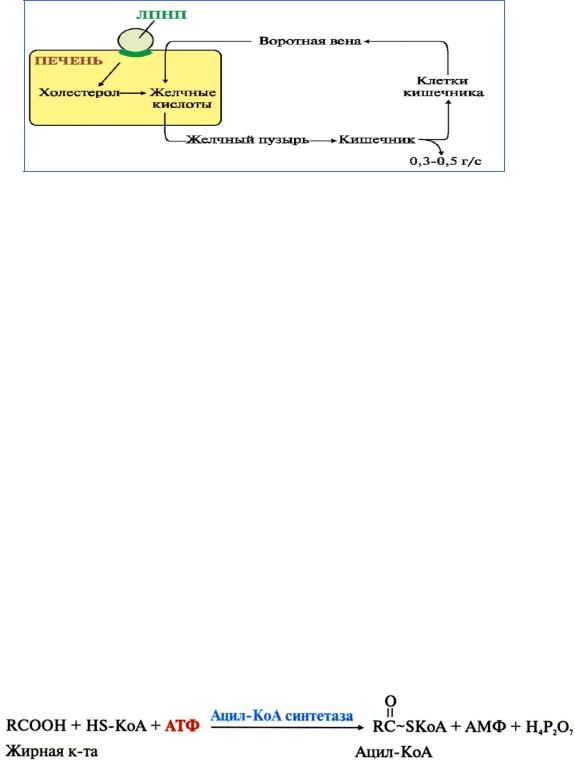
Рис.1-6. Энтерогепатическая циркуляция
Установлено, что у человека общий пул желчных кислот составляет примерно 2,8–3,5 г, при этом они совершают 6–8 оборотов в сутки, (в зависимости от количества жира в пище).
Биологическое значение энтерогепатической циркуляции: для эмульгирования липидов требуется меньшее количество желчных кислот.
I-й ресинтез липидов в энтероцитах и его биологическое значение.
Процесс синтеза жира в энтероцитах из продуктов гидролиза липидов, называется I-м ресинтезом жира.
Ресинтез ТАГ в энтероцитах протекает в гладком эндоплазматическом ретикулуме из 2-моноацилглицеролов и ВЖК. В ресинтезе жиров участвуют не только жирные кислоты, всосавшиеся из кишечника, но и жирные кислоты, синтезированные в организме, поэтому по составу ресинтезированные жиры отличаются от жиров, полученных с пищей.
Первая стадия ресинтеза жиров - реакция активации жирных кислот. Жирные кислоты активируются при участии ацил КоА-синтетаз, специфичных
к
Вторая стадия ресинтеза жиров - ацилирование 2-МАГ до ТАГ активированными жирными кислотами при участии ферментов — трансацилаз (или ацилтрансфераз):
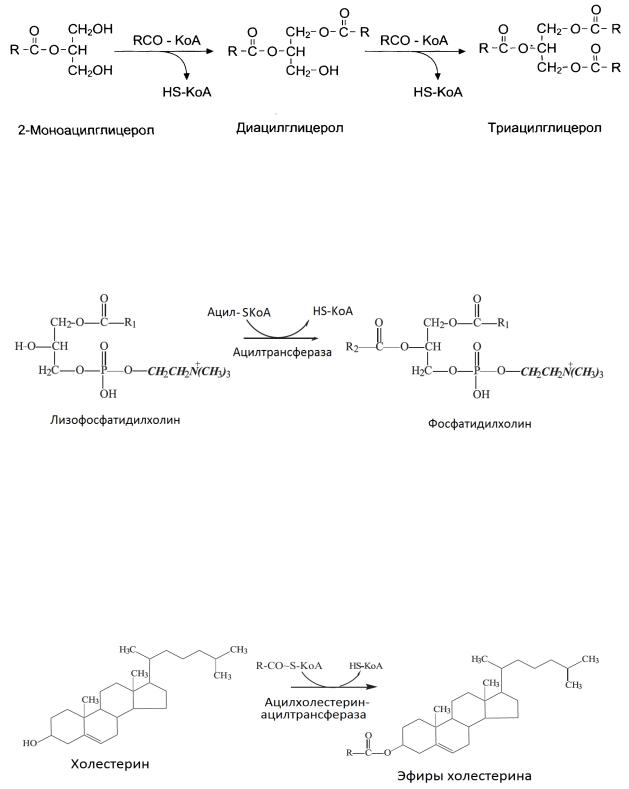
Ресинтез фосфолипидов в энтероцитах
Большая часть фосфолипидов содержимого тонкой кишки приходится на фосфатидилхолин (лецитин), поэтому в энтероцитах преимущественно этерифицируется именно лизофосфатидилхолин:
Ресинтез эфиров холестерина
В микросомах клеток слизистой оболочки тонкой кишки, всосавшиеся молекулы ХС превращаются в эфиры, путём взаимодействия с ацил-KоA при участии фермента ацилхолестеролацилтрансферазы (АХАТ). От активности данного фермента зависит скорость поступления экзогенного ХС в организм:
Биологическое значение ресинтеза липидов заключается в том, что синтезируются липиды, специфичные для организма человека.
Однако возможности «адаптировать» в процессе ресинтеза состав пищевых жиров к составу жиров организма человека ограниченны.
Понятие о липопротеинах. Хиломикроны: характеристика, функции, метаболизм.
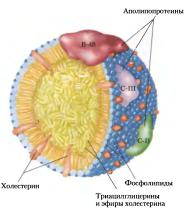
Липиды в водной среде (а значит, и в крови) нерастворимы, поэтому для их транспорта кровью в организме образуются комплексы липидов с белкамилипопротеины, отвечающие за транспорт триацилглицеринов, фосфолипидов, холестерина и его эфиров между органами.
Липопротеины - это сферические частицы, в которых можно выделить:
-гидрофобный центр, состоящий из:
триацилглицеролов и эфиров холестерина - гидрофильную оболочку, в составе которой
находятся фосфолипиды и белки. Холестерин обычно занимает промежуточное положение между оболочкой и сердцевиной. Компоненты частицы связаны слабыми типами связей,
находятся в состоянии постоянной диффузии и способны перемещаться друг относительно друга. Все липопротеины содержат: белки, липиды: ТАГ, фосфолипиды, холестерин, эфиры холестерина, но имеют различное соотношение компонентов в составе частицы, поэтому плотность их различна. Липопротеины разделяют по плотности методом ультрацентрифугирования, при этом они не осаждаются, а всплывают (флотируют). Мерой всплывания является константа флотации, обозначаемая Sf (Сведберг флотации). Чем выше содержание белка в липопротеине, тем больше его плотность. В соответствии с этим показателем различают следующие группы липопротеинов:
•хиломикроны (chylomicrons);
•липопротеины очень низкой плотности (ЛПОНП) (Very Low Density Lipoprotein, VLDL);
•липопротеины низкой плотности (ЛПНП) (Low Density Lipoproteins, LDL);
•липопротеины высокой плотности (ЛПВП) (High Density Lipoproteins, HDL). Каждый класс липопротеинов крови транспортирует определённые липиды:
•хиломикроны (ХМ) транспортируют триацилглицеролы, поступившие в организм с пищей, то есть триацилглицеролы экзогенного происхождения от кишечника к тканям;
•ЛПОНП переносят триацилглицеролы, синтезированные в печени (эндогенные

ТАГ) к другим органам и тканям;
•ЛПНП транспортируют свободный и эстерифицированный холестерол в клетки;
•ЛПВП переносят фосфолипиды и эфиры холестерола в печень.
Белки в составе липопротеинов называют апобелками или аполипопротеинами («апо» - означает отделенный, изолированный, т.е. белок без липида). Они отличаются структурой и функциями и обозначаются заглавными буквами латинского алфавита (А, В, С…) с указанием индекса (например, апо В100). Апобелки являются амфифильными веществами. Они принимают участие в метаболизме липидов и выполняют функции (табл.1):
• формируют липопротеины (например, В48 – основной белок ХМ, В100 – основной белок ЛПОНП, ЛППП, ЛПНП);
•взаимодействуют с рецепторами на поверхности клеток, определяя, с какими тканями будет захватываться данный тип липопротеинов (апопротеин В-100, Е);
•являются ферментами или активаторами ферментов, действующих на липопротеины (С-II – активатор ЛП-липазы, А-I – активатор лецитин:холестеролацилтрансферазы)
•осуществляют транспорт липидов из одного липопротеина в другой.
Таблица 1
Функции некоторых апобелков:
Апобелок |
Функция |
ЛП, в которых данный белок |
|
|
является главным |
А-I |
Активатор ЛХАТ |
ЛПВП |
B-100 |
Лиганд рецепторов В и Е |
ЛПОНП, ЛПНП |
B-48 |
Лиганд рецепторов В и Е |
ХМ |
C-I |
Активатор ЛХАТ |
ХМ, ЛПОНП |
C-II |
Активатор ЛПЛ |
ХМ, ЛПОНП, ЛПВП |
D |
Белок, переносящий эфиры |
ЛПВП |
|
холестерина |
|
E |
Лиганд рецепторов В и Е и |
ХМ, ЛПВП |
|
рецепторов, узнающих только |
|
|
апо-Е |
|
В метаболизме липопротеинов участвует |
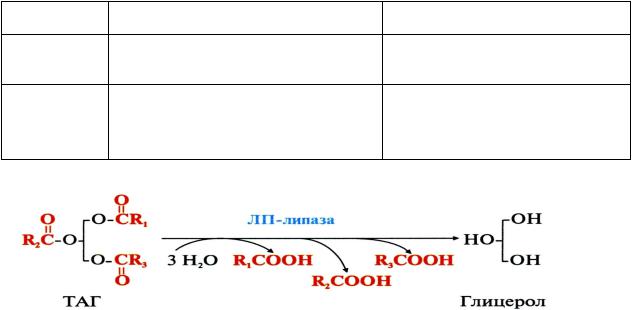
липопротеинлипаза – фермент, |
|
ЛП до ВЖК и
ЛП-липаза «захватывает» ХМ из кровотока и гидролизует ТАГ. Этот фермент синтезируется и секретируется жировой и мышечной тканями, клетками молочных желез. Секретируемая ЛПЛ связывается с поверхностью эндотелиальных клеток капилляров тех тканей, где она синтезировалась. Активаторами липопротеин (ЛП) липазы являются: апо-С-II в составе ХМ, инсулин (в жировой ткани) и гепарин.
Транспорт липидов из кишечника осуществляют хиломикроны (ХМ) и липопротеины очень низкой плотности (ЛПОНП). Их синтез происходит в клетках эпителия кишечника: хиломикроны синтезируются только в кишечнике, а ЛПОНП – в кишечнике на 10%, а в основном - в гепатоцитах (до 90%). ХМ после приема жирной пищи придают плазме крови опалесцирующий, похожий на молоко, вид.
Функция ХМ - транспорт экзогенных ТАГ из кишечника в ткани, запасающие и использующие жиры: жировую ткань (в основном), скелетные мышцы, миокард, легкие, печень, лактирующую молочную железу.
Хиломикроны, синтезируемые в энтероцитах (незрелые), имеют большие размеры, поэтому попадают в кровеносное русло через грудной лимфатический проток. Для их метаболизма требуются апобелки (апо Е и апоС-II), которые экспортируются с поверхности ЛПВП, циркулирующими в крови (рис. 1-7). Этот процесс носит название «дозревание», а образовавшиеся ХМзрелыми.
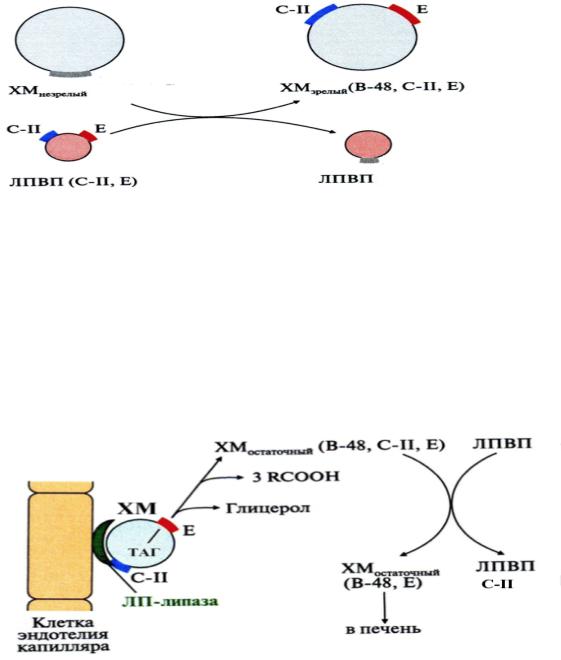
Рис. 1-7. Созревание ХМ в крови В результате действия ЛПЛ количество нейтральных жиров в ХМ снижается на
90%, они уменьшаются в размерах и возвращают белок апоС-II липопротеинам высокой плотности. Образовавшиеся частицы называются остаточными (ремнантами) ХМ (рис. 1-8). Далее они связываются с рецепторами на поверхности клеток печени, где полностью гидролизуется при участии лизосомальных ферментов.
Рис.1-8 Взаимодействие липопротеинлипазы (ЛПЛ) с ХМ Изоферменты ЛП-липазы в разных тканях отличаются по значению Km: ЛП-липаза жировой ткани имеет в 10 раз более высокое значение Km, чем, например, ЛП-липаза сердца, поэтому гидролиз жиров ХМ в жировой ткани происходит в абсорбтивный период. Жирные кислоты поступают в адипоциты и используются для синтеза жиров. В постабсорбтивном состоянии, когда количество жиров в крови снижается, ЛП-липаза сердечной мышцы продолжает гидролизовать жиры в составе ЛПОНП, которые присутствуют в крови в небольшом количестве, и жирные кислоты используются этой тканью как источники энергии, даже при низкой концентрации жиров в крови.
ЛП-липазы нет в печени, но на поверхности клеток этого органа имеется другой
фермент - печёночная липаза, которая не действует на зрелые ХМ, но гидролизует жиры в составе ЛППП, которые образуются из ЛПОНП в кровеносном русле.
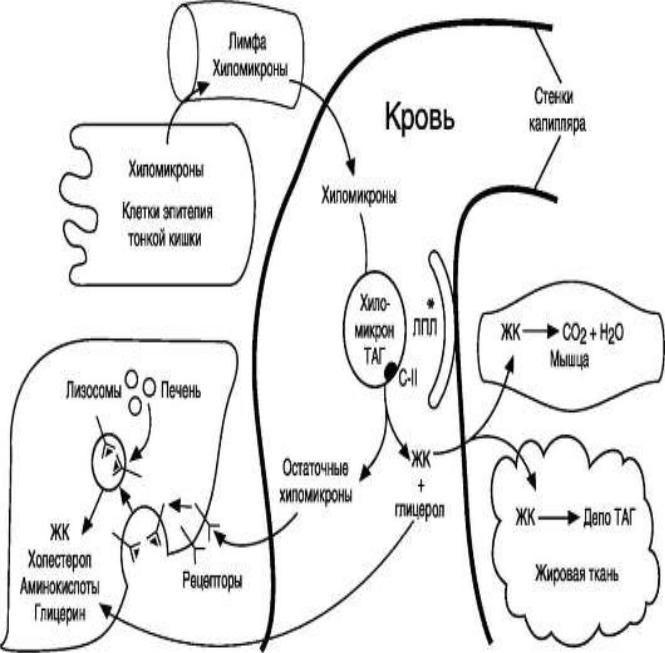
Рис. 1-9. Общая схема обмена ХМ
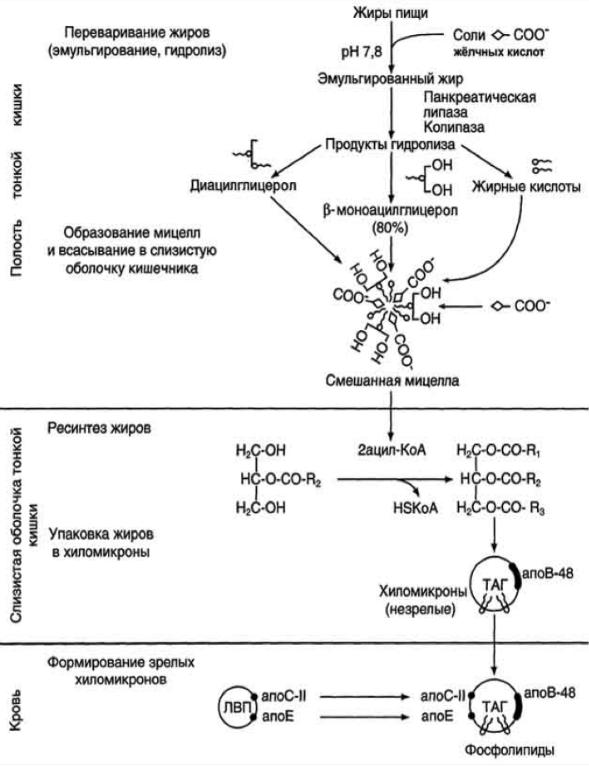
Общая |
схема |
переваривания |
липидов |
в |
ЖКТ |
Нарушение переваривания и всасывания липидов: стеаторея, гипертриацилглицеролемия, гиперхиломикронемия.
Поступившие с пищей жиры, если они приняты в умеренном количестве (не более 100-150 г), усваиваются почти полностью, и при нормальном пищеварении кал содержит не более 5% жиров.
