
metodichka_Lipidy_2020
.pdf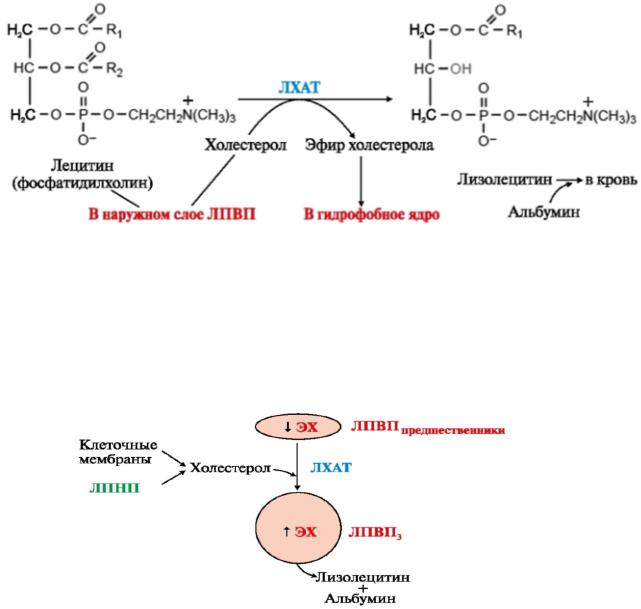
Образовавшиеся эфиры холестерина погружаются в гидрофобное ядро ЛПВП(нез), превращая их из дисковидных частиц и сферические. Наосвободившиеся
меспутемпростойадиффузииперемещаютновыемолекулыхолеизстеролая |
|
клеточныхмембраниЛПНП.Гидрофобноеядропополняетсяэфирам |
ихолестерола, |
покадисковиднратитсячастицанепресферическую(4 |
-5). |
Рис. 4 -5Образо. липопрвысокойаниеплотноститеиновзрелыхЛПВПз( ) |
|
|
|
Образованныйлизолецитинсвязываетсяальбуминомоситсяповерхности |
|
||
ЛПВП3 токомкрови.Недостатокфосф |
атидилхолинавнаружномслоеЛПВП |
3 |
|
устраняютлипид |
-переносящиебелки,котв сполняютрыеубыльэтого |
|
|
фосфолипида,такжечастичноосвобгидрядрождаютэфировфобное |
|
|
|
холест,перегонаЛПОНПро. сяла |
|
|
|
Изменениявсоставечастицвосстанавливаютих |
антиатерогенныесвойства, |
|
|
т.е.способ«»холестеролносиратьизЛПНПмембранклеток,такие |
|
|
|
липопротеиныназываютсяЛПВП |
|
2.Такимобразом,ЛПВПосв избыткабождают |
|
холестеролаклеточныемембраныЛПНПиснижаютверояразвитияность |
|
|
|
гиперхолестеролемииатеросклероза. |
|
|
|
Принедостаткефосфатидилхолинаможетзамедлятьсяформированиепечени
ЛПВП,чтоприведеткповышениюсодекрЛПНПжанияови,перегруженных
холестеролом,игиперхолестеролемии.
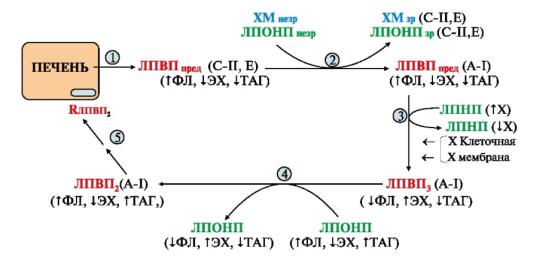
Рис. 4 -5Метаболизм. ЛПВП |
|
|
|
|
1 - в печениформируютсяЛПВП |
пред; 2 - вкронивитдаютапобелкиС |
|
-IIиЕ |
|
ХМиЛПОНП; 3 |
- ЛПВПзабираютхолестповерслояЛПНПхностногооли |
|
|
|
клеточныхмемб.ФеАХАТранпревращаментхолестацилхе.тролестерол |
|
|
|
|
Частприсферическуюобретцыформузсчеают |
|
тпополнениягидрофобногоядра |
|
|
эфирамихолестероланазываютсяЛПВП |
|
3; 4 - спомощьюлипид |
-переносящихбелков |
|
идетобменфосфолФЛ(),эфхолестеролаипидарамиЭХ()ТАГмиеждуЛПВП |
|
|
3 и |
|
ЛПОНП.Пополнивсодержаниефосфатидилхолиналецитина(),ЛПВП |
|
2 |
могут |
|
продолжитьсбх лестеролаизклеточныхмембраниЛПНП; 5 |
|
- катаболизмЛПВП |
|
|
происходвпечен. ит |
|
|
|
|
Богатые холестерином ЛПВП затем возвращаются и поглощаются клетками печени путем эндоцитоза, при этом “выгружая” холестерин. Часть ЛПВП поступает в другие ткани.
Желчные кислоты: строение, биологическая роль, этапы биосинтеза.
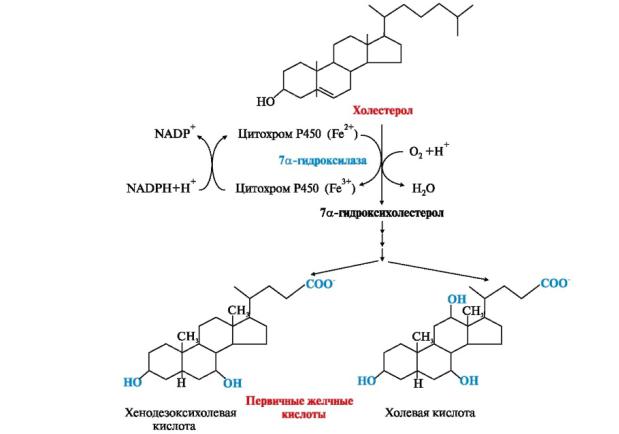
Жёлчные кислоты синтезируются из холестерина в печени. Известны четыре желчных кислоты, из них две кислоты первичные (синтезируются в печени): холевая, хенодезоксихолевая, а две другие – вторичные (синтезируются в кишечнике под действием ферментов микроорганизмов: дезоксихолевая и литохолевая.
Функции желчных кислот:
• являются мощными эмульгаторами липидов
•активируют липолитические ферменты: панкреатическую липазу, фосфолипазу А2
•снижают уровень холестерина, поскольку являются конечными продуктами его
распада и частично выводятся из организма.
Этапы биосинтеза желчных кислот
Синтез желчных кислот идет в эндоплазматическом ретикулуме печени при участии: цитохрома Р450, кислорода, НАДФН и аскорбиновой кислоты. В процессе синтеза жёлчных кислот холестерол подвергается гидроксилированию, восстановлению двойной связи в положении 5 и окислению боковой цепи. Образуется 2 типа первичных желчных кислот: холевая (гидроксильные группы в положениях 3, 7, 12 и хенодезоксихолевая (гидроксильные группы в 3, 7 положениях).
Рис.4-5 Синтез первичных жёлчных кислот |
|
|
Засуткиобразуется200 |
-600мгжелчныхкислот. |
Перед секрецией в просвет |
канальцев первичные желчные кислоты |
подвергаются конъюгации - связыванию |
|
с глицином и таурином. Это увеличивает их амфифильные и эмульгирующие свойства и снижает их цитотоксическое действие.
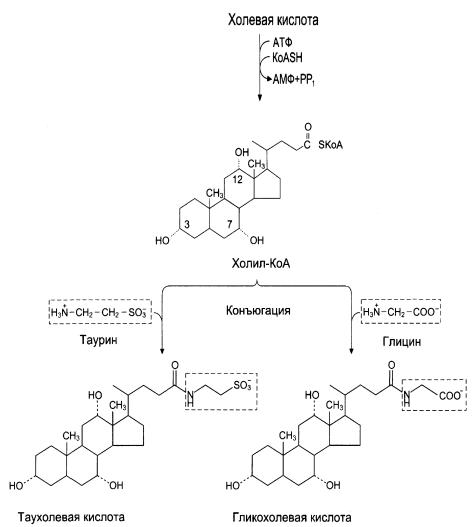
Конъюгация начинается с образования активной формы жёлчных кислот - производных КоА. Затем присоединяется таурин или глицин, и в результате образуется 4 варианта конъюгатов: таурохолевая и таурохенодезоксихолевая, гликохолевая или гликохенодезоксихолевая кислоты.
Рис.4-6. Конъюгация желчных кислот с глицином и таурином на примере холевой кислоты
Конъюгатов с глицином образуется в 3 раза больше, чем с таурином, так как количество таурина ограничено. Кислоты образуют натриевые или калиевые соли. В желчных протоках формируются мицеллы желчи состоящие из: желчных кислот, фосфолипидов, и холестерола в соотношении 12,5:2,5:1.
Регуляция синтеза желчных кислот
Ключевым ферментом процесса является 7а-гидроксилаза, которая катализирует первую реакцию синтеза желчных кислот. Активность 7а-гидроксилазы регулируется:
• фосфорилированием/дефосфорилированием и

• на уровне экспрессии гена:
Рис. 4-9. Регуляция синтеза желчных кислот в печени
Гормон глюкагон взаимодействует с мембранными рецепторами аденилатциклазной системы и активирует фермент протеинкиназу А (ПКА), который фосфорилирует и активирует 7а-гидроксилазу. Возрастает скорость ключевой реакции процесса. Таким образом, глюкагон в постабсорбтивный период стимулирует синтез желчных кислот.
Гормон инсулин в абсорбтивный период, взаимодействуя с рецепторами, активирует протеинфосфатазу, которая катализирует дефосфорилирование 7агидроксилазы и ее инактивацию.
Холестерол, его производные - желчные кислоты, эстрогены, а также гормон щитовидных желез тироксин регулируют количество фермента. Молекулы этих веществ связываются с определенными регуляторными зонами ДНК - энхансерами или сайленсерами, поэтому усиливают (+) или подавляют (- экспрессию гена 7агидроксилазы, соответственно изменяется количество этого фермента в клетке.
Желчные кислоты депонируются в желчном пузыре, из которого изливаются в двенадцатиперстную кишку после стимуляции кишечным гормоном холецистокинином во время приема пищи.
Образование вторичных желчных кислот. Энтерогепатический цикл.
В кишечнике большая часть желчных кислот под действием ферментов бактерий теряет глицин, таурин, ОН-группу в положении 7 и превращается во вторичные желчные кислоты литохолевую и дезоксихолевую. Отщепление полярных групп приводит к снижению растворимости кислот и затруднению их всасывания клетками кишечника.

Рис. 4-7. Образование вторичных желчных кислот в кишечнике
Далее желчные кислоты метаболизируются по одному из трех вариантов:
•выводятся с калом (0,3-0,5 г, 5-10%),
•всасываются в кишечнике и возвращаются в печень (большая часть)
•превращаются во вторичные кислоты (незначительно): литохолевую и
дезоксихолевую кислоты под действием ферментов бактерий кишечника.
Каждая |
образованная |
молекула |
желчной |
кислоты |
проходит |
энтерогепатический круг 6-8 |
раз, прежде |
чем выведется из |
организма. |
||
Рис. 4-8. Энтерогепатическая циркуляция желчных кислот
Желчь: состав, функции, желчнокаменная болезнь: причины, механизм камнеобразования.
В сутки образуется около 10 мл желчи на кг массы тела, таким образом, у взрослого человека это составляет 500-700 мл. Желчеобразование идет непрерывно, хотя интенсивность на протяжении суток резко колеблется.
В состав |
желчи входят желчные кислоты , |
фосфолипиды, |
холестерин в |
соотношении 12,5: 2,5: 1, которые формируют простую мицеллу. |
|
||
Желчь |
представляет собой раствор, в сухом остатке (3%) которого |
||
обнаруживается две группы веществ: |
|
|
|
• попавшие |
путем фильтрации из крови: ионы |
(натрий, калий, |
бикарбонат), |
молекулы (креатинин, холестерол, фосфатидилхолин), ,
•активно секретируемые гепатоцитами: билирубин, желчные кислоты.
Состав желчи:
•мицеллы желчи;
•билирубин;
•белки;
•минеральные соли; •Н2О.
Желчь:
•нейтрализует (совместно с панкреатическим соком) кислый химус, поступающий из желудка. (Основным компонентом желчи являются натриевые и калиевые соли желчных кислот, которые, будучи солями слабых кислот, подвергаются гидролизу и создают щелочную среду).
•эмульгирует жиры, обеспечивая их переваривание,
•усиливает перистальтику кишечника.
• |
образует смешанную мицеллу, в составе которой |
всасываются |
продукты |
|
|
гидролиза липидов и жирорастворимые витамины. |
|
|
|
• |
Выводит (экскретирует) продукты обмена: |
желчные пигменты, креатинин, |
||
|
ионы металлов (Zn, Cu, Hg), некоторые лекарственные |
препараты. |
|
|
|
Для холестерина - желчь – единственный путь его выведения, с ней может |
|||
выводиться до 1-2 г/сут. |
|
|
|
|
|
Желчнокаменная болезнь - патологический процесс, при котором в жёлчном |
|||
пузыре образуются камни в результате осаждения и кристаллизации компонентов желчи, основу которых составляет холестерол.
Причина - нарушение соотношения липидов, входящих в состав мицелл желчи (для поддержания холестерола в жёлчи в мицеллярном состоянии требуется определенное соотношение липидов). Это может быть вызвано:
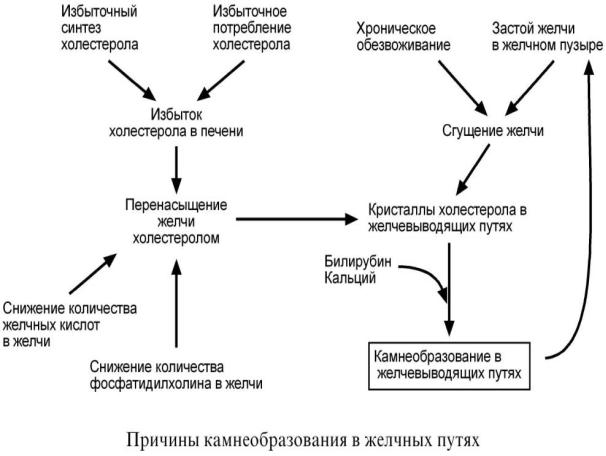
•повышением синтеза холестерола (из-за повышения активности ГМГ-КоА- редуктазы в печени) или
•снижением образования жёлчных кислот (из-за понижения активности 7агидроксилазы в печени).
Врезультате холестерол начинает осаждаться в жёлчном пузыре, образуя вначале вязкий осадок, который постепенно становится более твёрдым. Иногда он пропитывается билирубином - продуктом распада гема, белками и солями кальция.
Рис. 4-10. Механизм камнеобразования в почках
Камни, образующиеся в жёлчном пузыре, могут состоять только из холестерола (холестериновые камни) или из смеси холестерола, билирубина, белков и кальция. Холестериновые камни обычно белого цвета, а смешанные камни - коричневого цвета разных оттенков. Причин, приводящих к изменению соотношения жёлчных кислот и холестерола в жёлчи много: пища, богатая холестеролом, гиперкалорийное
питание, застой жёлчи в жёлчном пузыре, нарушение энтерогепатической циркуляции, нарушение синтеза жёлчных кислот, инфекции жёлчного пузыря.
Для лечения болезни на начальной стадии образования камней применяют хенодезоксихолевую кислоту, которая медленно растворяет осадок холестерола. Если камни неоднородные, то их удаляют в основном хирургическим путем.
При перемещении камней из жёлчного пузыря в жёлчные протоки наблюдается спазм жёлчного пузыря и протоков, что больной ощущает как приступ сильной боли.
Если камень перекрывает проток некоторое время, то нарушается поступление жёлчи в кишечник, жёлчные пигменты проходят через мембраны гепатоцитов в сторону синусоидов и попадают в кровь, что приводит к развитию обтурационной (подпечёночной желтухи).
Тесты по теме: «Обмен холестерина, желчных кислот и эйкозаноидов» Часть 1
1.Холестерол - стероид, характерный только для животных организмов:
1)расщепляется ферментами ЖКТ
2)поступает с пищей в количестве ~ 0,3 — 0,5 г ⁄ сутки
3)содержится преимущественно в жирах растительного происхождения
4)синтезируется в организме в количестве ~ 1 г ⁄сутки,
5)депонируется в эритроцитах
2.Холестерол синтезируется преимущественно в:
1) |
печени |
2) кишечнике 3) мозге |
4) эритроцитах 5) почках |
|
3. Субстратами синтеза холестерина в организме являются: |
||||
1) |
эфиры холестерина |
2) ацетил-КоА |
3) НАДН+Н+ |
|
4) |
НАДФН+Н+ |
5) ФАДН2 |
|
|
4. Снижение активности клеточной ГМГ-КоА- редуктазы у людей может быть результатом:
1) вегетарианской диеты 2)введения секвестрантов желчных кислот
3)диеты с низким содержанием холестерина
4)использования ингибиторов ГМГ-КоА редуктазы
5)длительной, высокохолестериновой диеты
5.У здорового человека при переходе на без холестериновую диету баланс холестерина:
1)в первые дни становится отрицательным
2) в первые дни становится положительным |
3) не изменяется |
4)через несколько дней равен нулю за счет увеличения синтеза холестерина
5)остается продолжительное время отрицательным
6.Эфиры холестерола - форма, в которой они:
1)входят в состав мембран клеток
2)окисляются в митохондриях клеток
3) выводятся из организма |
4) депонируются в клетках |
5) транспортируются кровью
7.В образовании эфиров холестерина принимают участие ферменты:
1) ЛХАТ 2) АХАТ 3) холестеролэстераза 4) холинэстераза 5) ЛП-липаза
8. В реакции превращения ГМГ-КоА в мевалоновую кислоту участвуют:
1) |
НАДФН |
|
2) ГМГ-КоА-редуктаза |
3) холестерин |
4) |
ГМГ-КоА-синтетаза |
|
5) АТФ |
|
9. Основное количество холестерина выводится из организма в виде: |
||||
1) |
желчных кислот |
2) стеринов фекалий |
3) секрета сальных желез |
|
4) |
стероидных гормонов |
5) в неизменном виде с мочой |
||
10.Промежуточные продукты, образующиеся при синтезе холестерола:
1) |
малонил-КоА |
2) геранилпирофосфат 3) сфингозин |
4) |
сквален |
5) карнозин |
11.Реакция, лимитирующая скорость биосинтеза холестерина:
1)циклизация сквалена
2)протекает с участием фермента ГМГ-КоА-синтаза
3)превращение β-гидрооксиметилглутарил-КоА в мевалонат
4)катализируется ферментом ГМГ-КоА-редуктаза
5)конденсация двух молекул ацетил-СоА с участием тиолазы
12.Высокие внутриклеточные концентрации холестерина:
1)повышают захват холестерина из крови клетками
