
metodichka_Lipidy_2020
.pdf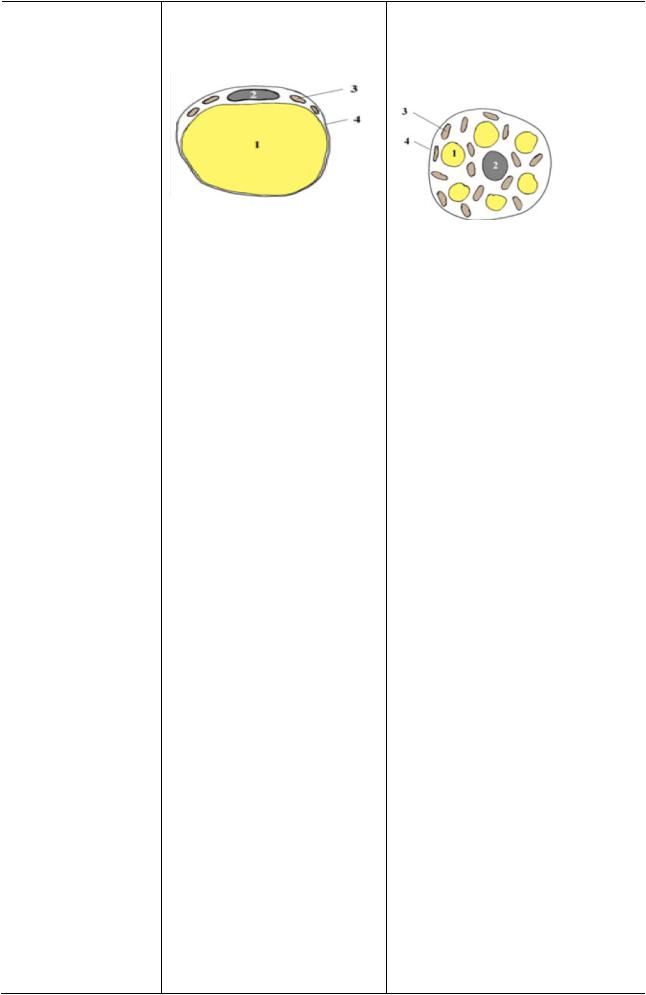
Структура |
Клетки имеет форму сферы |
Клетки меньшего размера, |
|
и содержат: |
имеют форму многогранника и |
|
|
содержат: |
- жир в виде крупной капли |
• |
жир в виде |
мелких жировых |
||||||
(1), |
который |
занимает |
|||||||
практически |
всю клетку, |
|
пузырьков, |
поэтому |
ядро ее |
||||
|
остается округлым. |
|
|||||||
делая ее сплюснутой |
|
|
|||||||
• |
на |
поверхности |
клеток |
||||||
- ядро (2) |
- |
сдвинуто к |
|||||||
оболочке клетки (4) |
|
располагается |
большое |
||||||
|
количество |
норадреналино- |
|||||||
|
|
|
|
|
|||||
|
|
|
|
|
вых рецепторов |
|
|||
|
|
|
|
• |
очень много митохондрий: |
||||
- с железосодержащими окрашенными цитохромами, придающими ткани коричневатый цвет; - содержание дыхательных
ферментов в них намного превышает содержание АТФсинтетазы.
- повышена активность гена, кодирующего термогенин - разобщающего митохондриального белка. На его долю приходится до 10-15% от общего белка митохондрий .

Функции |
• |
запасающая: 95% ТАГ –в • |
термогенез: выработка тепла |
|||||
|
|
жировой ткани, 5% - во |
при |
участии |
белка |
|||
|
|
внутренних органах и |
термогенина, |
|
который |
|||
|
|
костях, |
|
вызывает |
|
разобщение |
||
|
• |
теплоизоляционная |
процессов |
окисления |
и |
|||
|
• |
механическая: |
защита |
фосфорилирования |
|
в |
||
|
|
органов и тканей |
митохондриях. |
|
|
|||
|
• |
депонирующая: |
нако- |
|
|
|
|
|
|
|
пление жирораствори- |
|
|
|
|
|
|
|
|
мых витаминов: А,Д,Е, |
|
|
|
|
|
|
|
• |
эндокринная: |
секреция |
|
|
|
|
|
лептина, адипонекти-нов, эстрогенов
Химический состав белой жировой ткани
Состав жировой ткани зависит от ее локализации: чем глубже под поверхностью кожи она расположена, тем больше содержится насыщенных кислот в составе ТАГ.
В состав жировой ткани входят: ТАГ- 65-85%, вода – 22%, белки – 5,8%. ВЖК в составе ТАГ представлены кислотами: олеиновой – 42-51%, пальмитиновой – 5- 14%, олеопальмитиновой – 3-5%, миристиновой 3-5%, линолевой 1-5%.
Особенности метаболизма белой жировой ткани:
Белая жировая ткань слабо снабжена кровеносными капиллярами, поэтому к ней транспортируется мало кислорода, мало вырабатывается АТФ, которая тратится, в основном на транспорт веществ. Белковый и углеводный обмены протекают с невысокой скоростью. По скорости липидного обмена жировая ткань занимает второе место после печени.
Белковый обмен: белки синтезируются адипоцитами преимущественно для собственных нужд. На экспорт синтезируются: лептин, белки острой фазы воспаления (α1-кислый гликопротеин, гаптоглобин), компоненты системы комплимента (адипсин, комплемент С3, факторВ), интерлейкины.
Углеводный обмен: тесно связан с липидным обменом, преобладают катаболические процессы.
Липидный обмен: активно протекают реакции липолиза и липогенеза (в абсорбтивный период по глицерофосфатному пути).
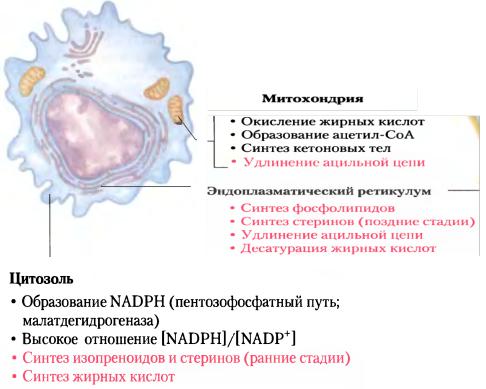
Обмен липидов в клетке локализован следующим образом:
Рис. 3-1. Внутриклеточная локализация метаболизма липидов.
Распад ТАГ в жировой ткани (липолиз).
ТАГ используется в организме после их предварительного расщепления (липолиза), в ходе которого освобождаются глицерин и свободные жирные кислоты. Мобилизация жиров, т.е. гидролиз до глицерола и жирных кислот, происходит в постабсорбтивный период при голодании и активной физической нагрузке. В клетках жировой ткани распад ТАГ происходит при участии липаз. ТАГ-липаза отщепляет одну жирную кислоту у первого углеродного атома глицерола с образованием диацилглицерола, который далее с участием
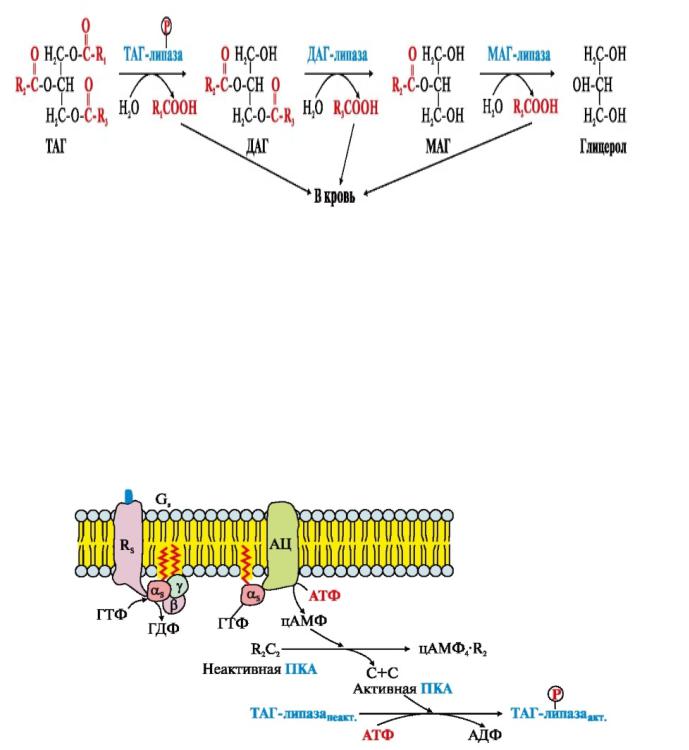
ДАГ- и МАГ липаз гидролизуется |
до глицерола и жирных кислот: |
Глицерол, как водорастворимое вещество, транспортируется кровью в свободном виде, а жирные кислоты (гидрофобные молекулы) - в комплексе с белком плазмы - альбумином.
ТАГ-липаза находится в неактивной форме и активируется гормонами (адреналином, норадреналином, глюкагоном, тироксином, глюкокортикоидами, СТГ, АКТГ) в ответ на стресс, голодание, охлаждение.
Активируется ТАГ липаза по каскадному механизму через аденилат-циклазную (АЦ) систему (рис 3-5) по типу фосфорилирования/дефосфорилирования:
Рис. 2-1. Регуляция активности ТАГ-липазы глюкагоном и адреналином. АЦаденилатциклаза, ПКА-протеинкиназа А В настоящее время известны свыше 200 природных жирных кислот, но наиболее
часто в организме человека встречаются не более десяти.
Распад фосфолипидов в тканях

Различные типы фосфолипаз, локализованных в клеточных мембранах или в лизосомах, катализируют гидролиз глицерофосфолипидов.
Рис. 3-11. Действия фосфолипаз
Хорошо известно, что фосфолипаза A1 атакует эфирную связь фосфолипидов в положении
•Фосфолипаза А2 катализирует гидролиз эфирной связи в положении 2 глицерофосфолипидов, в результате чего образуются свободная жирная кислота и лизофосфолипид.
•Фосфолипаза С атакует эфирную связь в положении 3, что заканчивается образованием 1,2-диглицерида и фосфорилированного основания.
•Фосфолипаза D катализирует отщепление от фосфолипида азотистого основания.
Гидролиз некоторых глицерофосфолипидов под действием фосфолипаз имеет значение не только как путь катаболизма, но и как путь образования вторичных посредников или предшественников в синтезе биологически активных веществ - эйкозаноидов. Кроме того, фосфолипазы А1 и А2 участвуют в изменении состава жирных кислот в глицерофосфолипидах, например при синтезе в эмбриональном периоде развития дипальмитоилфосфатидилхолина - компонента сурфактанта.
Таблица 1
Основные представители жирных кислот в организме человека
Название кислоты |
C m:n |
Структурная формула |
|
Насыщенные |
|
пальмитиновая |
С16:0 |
СН3(СН2)14СООН |
стеариновая |
С18:0 |
СН3(СН2)16СООН |

|
Ненасыщенные |
|
|
мононенасыщенные |
|
пальмитоолеиновая |
С16:1 (Δ9) |
СН3(СН2)5СН=СН(СН2)7СООН |
олеиновая |
С18:1 (Δ9) |
СН3(СН2)7СН=СН(СН2)-СООН |
|
полиненасыщенные (или полиеновые) |
|
линолевая (ω-6) |
С18:2 (Δ9, 12) |
СН3(СН2)4СН=СН-СН2-СН=СН-(СН2)7- |
|
|
СООН |
линоленовая (ω-3) |
С18:3 |
СН-СН2-(СН=СНСН2)3(СН2)6СООН |
|
(Δ9,12,15) |
|
|
эйкозаполиеновые кислоты |
|
арахидоновая (ω-6) |
С20:4 |
СН3(СН2)4(СН=СНСН2)4-(СН2)2СООН |
|
(Δ5,8,11,14) |
|
эйкозопентаеновая(ω3) |
С20:5, |
СН3(СН2)2-(СН=СН-СН2)5СООН |
|
5,8,11,14,17) |
|
Полиненасыщенные жирные кислоты почти не синтезируются в организме человека, а поступают только с пищевыми продуктами. Они для человека незаменимы и поэтому получили название эссенциальных жирных кислот, которые также объединяют термином витамин F. К ним относятся:
–линолевая (ω6), содержание которой в липидах человека составляет 10–15%,
–линоленовая (ω3) кислота,
–эйкозаполиеновые кислоты, включающие 20 углеродных атомов и несколько двойных связей.
Основной представитель — арахидоновая (ω6) кислота, частично синтезирующаяся в организме из линолевой кислоты. Ее содержание в составе липидов составляет около 8% от количества всех жирных кислот человека. В рыбьем жире, растительных маслах встречается эйкозапентаеновая (ω3) кислота с пятью двойными связями.
Насыщенные (пальмитиновая, стеариновая) и ряд мононенасыщенных жирных кислот могут синтезироваться в организме из углеводов и углеродного скелета аминокислот
Особенности структуры ВЖК организма:
• содержат четное число углеродных атомов в цепи,
• не имеют разветвлений в радикале,
• содержат двойные связи только в цис-конформации.
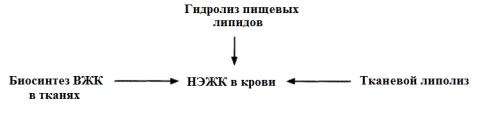
Свободные (неэтерифицированные) жирные кислоты (СЖК или НЭЖК): происхождение, транспортная форма в крови. Схема промежуточного обмена ВЖК в организме человека.
Свободные (неэстерифицированные) жирные кислоты (СЖК или НЭЖК) – это кислоты, не вступившие в реакцию этерификации с образованием сложных эфиров. СЖК - гидрофобные вещества, которые в кровяном русле транспортируются в комплексе с альбумином, повышающим их растворимость. Этот белок нековалентно (за счет гидрофобных, водородных, ионных связей) связывает жирные кислоты в соотношение 1:10. Пути образования НЭЖК:
Связанные с альбумином ВЖК переносятся к тканям, например: скелетным мышцам, сердцу, корковому веществу почек. В этих тканях кислоты отделяются от альбумина и с помощью белка-переносчика на плазматической мембране доставляются внутрь клеток, для выполнения своих функции (рис. 1-1.).
В организме ацетил-КоА подвергается следующим путям обмена:
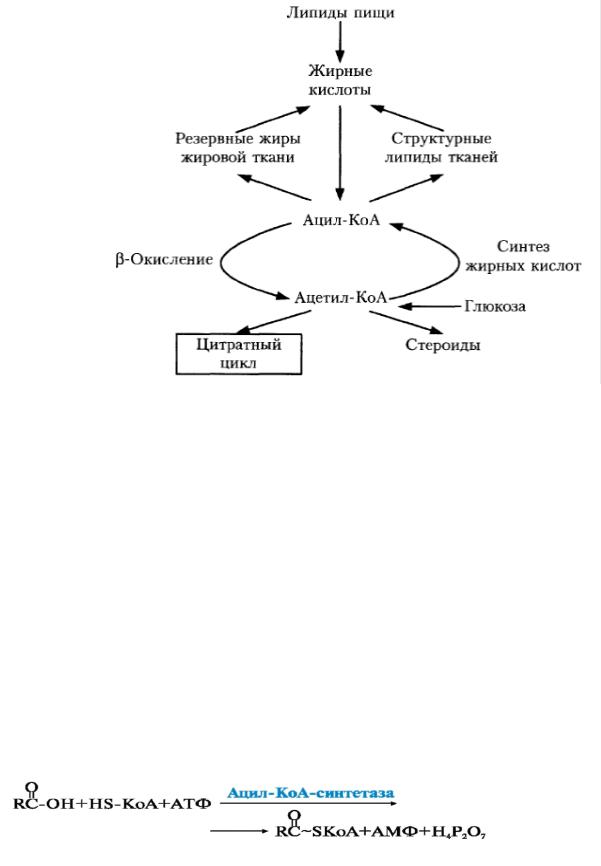
Схема промежуточного обмена ВЖК. Пути обмена ацетил-КоА.
Активация ВЖК и транспорт через митохондриальную мембрану. Роль карнитина.
Окисление жирных кислот в митохондриях до СО2 и Н2О – является одним из главных способов получения энергии. Окислению предшествует:
•активация ВЖК (для ослабления стабильности С-С связей),
•транспорт ацил-КоА через мембрану из цитозоля в матрикс митохондрий,
где локализованы ферменты окисления.
Активация ВЖК в цитозоле протекает при участии HSКоА, АТФ и фермента ацил-КоА синтетазы:
Далее пирофосфат гидролизуется ферментом пирофосфатазой: Н4Р2О7 + Н2О → 2 Н3РО4 и дополнительная энергия, выделенная при гидролизе макроэргической связи пирофосфата, обеспечивает полноту протекания реакции активации ВЖК.
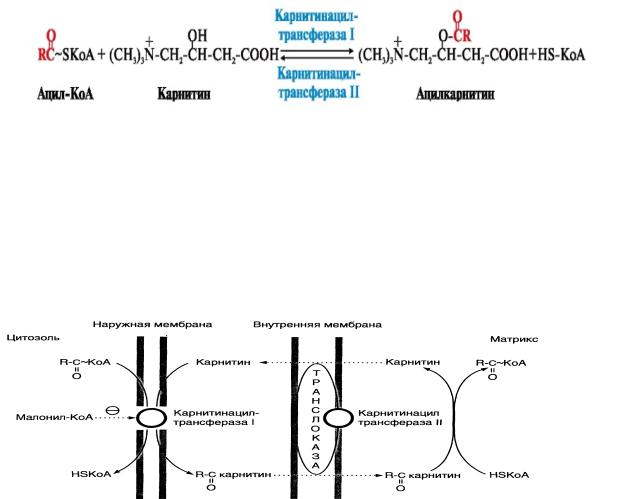
Ацил-КоА синтетазы находятся как в цитозоле, так и в матриксе митохондрий. Они отличаются специфичностью к жирным кислотам с различной длиной радикала.
Транспорт ВЖК из цитозоля в матрикс для коротко- и средне-цепочечных жирных кислоты (до С14) осуществляется без переносчиков, поскольку они легко проникают через мембрану митохондрий. Для переноса кислот с более длинным радикалом (их большинство) требуется специальная карнитиновая транспортная система.
На наружной мембране митохондрий имеется фермент карнитинацилтрансфераза I, которая катализирует образование сложноэфирной связи между ацильной и спиртовой группами карнитина:
Ацил-карнитин в цитозоле связывается с белком транслоказой, встроенной в наружную мембрану митохондрий и после прохождения через межмембранное простанство, на внутренней стороне митохондриальной мембраны происходит обратная реакция – образование ацил-СоА без затраты АТФ с участием фермента - карнитин-ацил-трансфераы II. Высвобождаемый карнитин возвращается назад за последующим остатком насыщенной жирной кислоты.
Рис.2-2. Транспорт жирных кислот через мембраны митохондрий.
C помощью карнитина происходит также удаление из митохондрий разветвленных ацильных остатков, которые образуются в результате распада аминокислот. В почках карнитин участвует в переносе и выведении ацильных групп, которые не могут метаболизироваться в организме.
 Карнитин поступает с пищей или синтезируется из незаменимых аминокислот лизина и метионина. В реакциях синтеза карнитина участвует витамин С (аскорбиновая кислота). При длительной физической нагрузке (тренировках спортсменов и др.) для повышения транспорта активных жирных кислот в матрикс митохондрий внутрь принимают препараты карнитина. Напротив, при ишемии миокарда блокируют β-окисление жирных кислот. Для этого вводят препараты, которые конкурентно ингибируют синтез карнитина. Недостаточность карнитина вследствие нарушения его синтеза отмечена при заболеваниях печени, голодании или употреблении в пищу только растительных продуктов, при беременности, некоторых инфекционных заболеваниях, травме, а также при проведении процедур гемодиализа, когда карнитин удаляется из крови. Дефицит ферментов карнитинацилтрансферазы I и II выражается в виде кардиомиопатии и мышечной слабости. Лечение заключается в приеме большого количества углеводов, карнитина и малого количества жирных кислот.
Карнитин поступает с пищей или синтезируется из незаменимых аминокислот лизина и метионина. В реакциях синтеза карнитина участвует витамин С (аскорбиновая кислота). При длительной физической нагрузке (тренировках спортсменов и др.) для повышения транспорта активных жирных кислот в матрикс митохондрий внутрь принимают препараты карнитина. Напротив, при ишемии миокарда блокируют β-окисление жирных кислот. Для этого вводят препараты, которые конкурентно ингибируют синтез карнитина. Недостаточность карнитина вследствие нарушения его синтеза отмечена при заболеваниях печени, голодании или употреблении в пищу только растительных продуктов, при беременности, некоторых инфекционных заболеваниях, травме, а также при проведении процедур гемодиализа, когда карнитин удаляется из крови. Дефицит ферментов карнитинацилтрансферазы I и II выражается в виде кардиомиопатии и мышечной слабости. Лечение заключается в приеме большого количества углеводов, карнитина и малого количества жирных кислот.
. Процесс β- окисления: локализация, последовательность реакций, ферменты. Биологическое значение. Регуляция процесса β-окисления. Энергетический эффект окисления ВЖК (на примере пальмитиновой кислоты).
Во многих тканях окисление жирных кислот - важный источник энергии. Это ткани с высокой активностью ферментов ЦТК и дыхательной цепи - клетки красных скелетных мышц, сердечная мышца, почки. Эритроциты, в которых отсутствуют митохондрии, не могут окислять жирные кислоты. Жирные кислоты не служат источником энергии для мозга и других нервных тканей, так как они не проходят через гематоэнцефалический барьер, как и другие гидрофобные вещества.
β-окисление - это аэробный процесс катаболизма жирных кислот путём последовательного отщепления двууглеродных фрагментов в виде ацетил-СоА. Ацетил-СоА может вступать в цитратный цикл и окисляться до СО2 и Н2О, а образовавшийся укороченный ацильный остаток вновь вовлекается в следующий цикл β-окисления.
