
- •Контроль чсс:
- •Диагностика
- •Классификация сссу
- •Медикаментозная противоаритмическая терапия.
- •1. Классификация e.Vaughan-Williams:
- •2. Препараты, не входящие в классификацию пас, но обладающие антиаритмическими свойствами:
- •Немедикаментозная противоаритмическая терапия.
- •2. Хирургические методы лечения аритмий:
- •Этиология орл.
- •Патогенез орл.
- •Клиника орл (“ревматизм лижет суставы и кусает сердце”).
- •3. Ревматический полиартрит
- •Лечение орл.
- •Профилактика орл.
- •Недостаточность митрального клапана.
- •Митральный стеноз.
- •Классификация марс
- •Диагностика пролапса митрального клапана
- •1. Воспалительные (артриты)
- •2. Дегенеративные артрозы
- •3. Особые формы
- •4. Артриты и артрозы, связанные с другими заболеваниями:
- •Клиника ра:
- •Диагностика ра:
- •Лечение ра.
- •Классификация св в зависимости от калибра пораженных сосудов:
- •1. Поражающие крупные сосуды:
- •2. Поражающие средние сосуды:
- •3. Поражающие мелкие сосуды:
- •2. Исследования, направленние на выяснение типа св:
- •Клинические признаки, которые позволяют заподозрить диагноз системного васкулита:
- •Профилактика гигантоклеточного артериита
- •70. Гемолитические анемии. Классификация. Механизмы гемолиза и основные причины развития гемолитических анемий.
- •I. Наследственные гемолитические анемии:
- •II. Приобретенные гемолитические анемии:
- •71. Наследственные гемолитические анемии: мембранопатии. Наследственный микросфероцитоз. Клиника, диагностика, принципы лечения.
- •I. Наследственные гемолитические анемии:
- •72. Наследственные гемолитические анемии: мембранопатии. Пароксизмальная ночная гемоглобинурия, клиника, диагностика, принципы лечения.
- •73. Аутоиммунные гемолитические анемии. Этиология. Патогенез. Классификация.
- •74. Аутоиммунные гемолитические анемии. Классификация. Клинические проявления. Лабораторные показатели. Дифференциальная диагностика. Лечение. Прогноз.
- •75. Геморрагические диатезы. Определение. Причины развития. Классификация.
- •Причины
- •76. Геморрагические диатезы. Общие признаки, типы кровоточивости. Методы исследования.
- •77. Иммунная тромбоцитопеническая пурпура. Основные этиологические факторы. Патогенез кровоточивости. Клиника. Диагноз.
- •78. Иммунная тромбоцитопеническая пурпура. Дифференциальная диагностика с симптоматическими тромбоцитопениями. Течение. Лечение.
- •79. Гемофилия. Значение наследственного фактора в развитии болезни. Патогенез кровоточивости. Клинические проявления и течение гемофилии. Диагноз. Прогноз. Лечение и профилактика.
- •80. Геморрагическая телеангиоэктазия (болезнь Рандю-Ослера). Патогенез кровоточивости. Роль наследственного фактора. Клиника. Лечение.
- •81. Гемобластозы. Значение наследственного фактора, радиации, химических веществ, вирусов в развитии гемобластозов. Молекулярные механизмы патогенеза гемобластозов.
- •82. Гемобластозы. Клинико-гематологические синдромы. Классификация. Миелопролиферативные и лимфопролиферативные заболевания.
- •83. Парапротеинемические гемобластозы. Этиология. Патогенез. Клиника, диагностика, лечение.
- •84. Острый лейкоз. Классификация. Основные клинические синдромы.
- •Морфологическая (fab) классификация олл
- •85. Острый лейкоз. Лабораторно-морфологическая диагностика, иммунологическое фенотипирование лейкозных клеток.
- •Методы исследований при острых лейкозах.
- •87. Агранулоцитоз. Этиология и патогенез. Классификация. Клинические варианты (миелотоксический и иммунный), лабораторная диагностика.
- •Диагностика агранулоцитоза
- •89. Хронический миелолейкоз. Патогенез. Стадии течения и клиническая картина. Лейкемоидные реакции.
- •90. Хронический миелолейкоз. Лабораторно-морфологическая диагностика. Осложнения. Лечение. Прогноз.
- •91. Хронический лимфолейкоз. Патогенез. Основные клинические синдромы, стадии течения.
- •92. Хронический лимфолейкоз. Лабораторно-морфологическая диагностика. Принципы лечения. Прогноз.
- •93. Полицитемия. Патогенез. Стадии течения болезни и основные клинические синдромы. Течение и исходы болезни. Прогноз.
- •94. Полицитемия. Дифференциальная диагностика с симптоматическими эритроцитозами. Лечение. Принципы лечения полицитемии и ее осложнений.
-
Инфекционный эндокардит. Определение. Эпидемиология. Этиология и патогенез. Патоморфология. Классификация. Группы и факторы риска. Клинические проявления основных синдромов, в том числе в зависимости от этиологического фактора, у лиц с протезированными клапанами, пожилого и старческого возраста, у ВИЧ-инфицированных и наркоманов.
ИЭ — воспалительное заболевание инфекционной природы, характеризующееся преимущественным поражением клапанов сердца, пристеночного эндокарда и эндотелия крупных сосудов, протекающее по типу сепсиса с токсическим поражением органов, развитием иммунопатологических реакций, эмболических и других осложнений.
Ранее ИЭ поражал пациентов молодого возраста, имеющих клапанные поражения, сейчас в большей степени заболевание затрагивает пациентов пожилого возраста
В развитых странах при современном уровне оказания медицинской
помощи появились новые предрасполагающие факторы развития ИЭ: протезы клапанов, внутривенное введение препаратов, расширение перечня
инвазивных диагностических процедур, сопряженных с риском бактериемии. Лидирующую позицию по этиологическому фактору в данных странах занял стафилококк.
Выделяют основные патогенетические факторы и патофизиологиче-
ские механизмы развития ИЭ:
1) повреждение эндотелия клапана;
2) бактериемия (преходящая бактериемия);
3) взаимодействие микро- и макроорганизма (адгезия и размножение
патогенных микроорганизмов, факторы защиты макроорганизма).;
4) развитие сердечной недостаточности.
Выделяют 2 патофизиологических механизма повреждения эндокарда.
Первый механизм представляет собой механическое повреждение эндокарда турбулентным потоком крови при пороках сердца, катетерами или электродами. Дегенеративные изменения клапанного аппарата у пожилых пациентов может способствовать адгезии микроорганизмов.
Вторым механизмом развития эндокардита является воспаление эндотелия без повреждения клапана.
В патогенезе ИЭ большое значение имеет факт быстрого разрушения клапанного аппарата сердца, септическое поражение миокарда, перикарда.
Это приводит к формированию недостаточности клапана, нарастанию СН, так как миокард не успевает приспособиться к резкому нарушению гемодинамики. Важным звеном патогенеза СН является увеличение постнагрузки при длительном повышении периферического сосудистого сопротивления.


В клин практике используется:
1. Клинико-морфологическая форма:
— первичный ИЭ — возникающий на интактных клапанах сердца;
— вторичный ИЭ — возникающий на фоне существующей патологии
клапанов сердца в результате предшествующего ревматического, атеро-
склеротического поражения, либо перенесенного ранее ИЭ.
2. По этиологическому фактору:
— стрептококковый;
— стафилококковый;
— энтерококковый и т. д.
3. По течению заболевания:
— острое (длительностью менее 2 месяцев);
— подострое (длительностью более 2 месяцев);
— затяжной ИЭ (употребляется крайне редко, в значении маломани-
фестного подострого течения ИЭ).
4. В особые формы ИЭ выделяют:
— нозокомиальный ИЭ;
— ИЭПК;
— ИЭ у лиц с имплантированными внутрисердечными устройствами
(ЭКС и/или КД);
— ИЭ у лиц с трансплантированными органами;
— ИЭ у наркоманов;
— ИЭ у лиц пожилого и старческого возраста (марантический).
Одной из характеристик патологического процесса при ИЭ является
степень его активности. Последняя устанавливается на основании клинических и лабораторных, в том числе иммунологических признаков, отражающих степень деструкции эндотелиальной поверхности. В национальных рекомендациях 2010 г. предложено три степени активности, во многом характеризующие клиническое течение и прогноз заболевания.
Первая (1) — минимальная — степень активности ИЭ диагностируется по наличию:
— субфебрильной температуры;
— минимальной длительной бактериемией;
— незначительной диспротеинемии (гамма-глобулины < 25 %);
— СОЭ до 30 мм/час;
— незначительной концентрации в крови — менее 40 мг % — СРБ.
Вторая (2) — умеренная — степень активности ИЭ характеризуется:
— фебрильной лихорадкой;
— массивной кратковременной бактериемией;
— значимой диспротеинемией (гамма-глобулины > 25 %);
— СОЭ до 40 мм/ч;
— анемией;
— тромбоцитопенией;
— высокими концентрациями СРБ (до 90 мг %).
Третья (3) — максимальная — степень активности ИЭ отличается:
— гектической лихорадкой;
— массивной, длительной (часто — полимикробной) бактериемией;
— увеличением концентрации альфа2-глобулинов (> 15 %);
— СОЭ свыше 40 мм/ч;
— анемией;
— тромбоцитопенией;
— крайне высокими (> 90 мг %) концентрациями СРБ
Категория высокого риска:
1) протезированные клапаны сердца;
2) предшествующий ИЭ;
3) врожденные пороки сердца «синего типа»;
4) хирургически установленный пульмональный шунт;
5) приобретенные пороки сердца (в том числе ревматические).
Категория умеренного (промежуточного) риска:
1) другие врожденные пороки сердца;
2) гипертрофическая кардиомиопатия;
3) ПМК с регургитацией и (или) утолщением его створок (миксома-
тозная дегенерация створок МК).
Категория минимального риска:
1) изолированный дефект межпредсердной перегородки;
2) хирургически корригированный дефект межпредсердной перего-
родки, дефект межжелудочковой перегородки;
3) предшествующее аортокоронарное шунтирование;
4) ПМК без регургитации;
5) предшествующая ревматическая лихорадка без клапанной дисфункции;
6) имплантированный ЭКС и/или КД.
В ситуации: бактериемия, повреждение эндокарда, иммунодефицит-
ное состояние — ИЭ также может развиваться при следующих состояниях:
— интоксикация; наркомания; алкоголизм; ВИЧ-инфекция;
— пожилой и старческий возраст;
— прием иммунодепрессантов (ГКС, цитостатики);
— длительно стоящие катетеры центральных вен;
— сахарный диабет;
— солидные опухоли;
— синдром диссеминированного внутрисосудистого свертывания;
— трансплантация органов;
— инфицированные кожные заболевания;
— программный гемодиализ;
— медицинские вмешательства на мочевыводящих путях и толстом
кишечнике.
Классическая клиническая картина ИЭ представлена рядом синдромов:
• Синдром воспалительных изменений и септицемии: лихорадка с
ознобами, геморрагические высыпания, петехии на коже конечностей, над ключицами, на слизистой оболочке щек, нѐба; подногтевые кровоизлияния, положительные симптомы жгута и щипка, наличие патогномоничных для ИЭ проявлений в виде симптома Лукина — Либмана (петехии с белым центром на переходной складке конъюнктивы нижнего века), пятен Дженуэя (безболезненные геморрагические пятна размером 1–4 мм, расположенные на ладонях и подошвах), узелков Ослера (болезненные узелки синюшно-красного цвета на ладонях и подошвах), пятен Рота (кровоизлияния овальной формы с бледным центром на сетчатке рядом с диском зрительного нерва) неспецифические острофазовые показатели, положительная гемокультура возбудителя.
• Интоксикационный синдром: общая слабость, повышенная потли-
вость, миалгии и артралгии, головные боли, снижение аппетита, бледность
кожных покровов вследствие развития анемии с желтушным оттенком из-за
присоединения гепатита приводит к формированию своеобразного цвета
кожи «кофе с молоком», похудание, деформация дистальных фаланг паль-
цев кистей и ногтей по типу «барабанных палочек» и «часовых стекол».
• Синдром клапанных поражений: формирование порока сердца, по
типу недостаточности клапана, за исключением случаев стеноза клапана
при формировании массивных вегетаций. Поражение клапанов проявляет-
ся в виде появления новых шумов регургитации или изменения характера,
интенсивности имевшихся ранее шумов, выявление вегетации на клапанах
при ЭхоКГ, прогрессирующая дилатация камер сердца с развитием сер-
дечной недостаточности, резистентной к лечению, появление нарушений
сердечного ритма.
• Синдром тромбоэмболических осложнений: наиболее частой ло-
кализацией тромбоэмболий при ИЭ считаются артерии почек, селезенки,
головного мозга и коронарные артерии. Клиническими проявлениями яв-
ляются очаговый нефрит, инфаркты миокарда, селезенки, кишечника, го-
ловного мозга, легкого, тромбоэмболия в сетчатку глаза, в сосуды нижних
конечностей с развитием гангрены пальца, конечности и т. д.
• Синдром иммунных нарушений: диффузный гломерулонефрит,
при котором могут регистрироваться высокие цифры артериального дав-
ления, миокардит, гепатит, васкулит, артрит, спленомегалия, которая мо-
жет сопровождаться явлениями гиперспленизма, кожными симптомами
(узелки Ослера, пятна Рота), выявление в крови циркулирующих иммун-
ных комплексов, специфических антител, ревматоидного фактора, гипер-
гаммаглобулинемии.
ИЭ может иметь острое течение с яркой клинической картиной, но не
редким является подострое течение с нормальной температурой тела, неспецифическими симптомами. У 85 % пациентов с ИЭ обнаруживаются шумы в сердце, до 90 % пациентов с лихорадкой отмечают общие симптмы интоксикации: озноб, отсутствие аппетита, снижение веса.
-
Инфекционный эндокардит. Диагностические критерии. Инструментальная диагностика (ЭхоКГ, КТ сердца, МРТ). Лабораторная диагностика: посев крови на гемокультуру, маркеры воспаления. Дифференциальная диагностика с другими заболеваниями, сопровождающимися лихорадкой (ОРЛ, системные заболевания соединительной ткани, гемобластозы, опухоли). Осложнения. Прогноз
ИЭ — воспалительное заболевание инфекционной природы, характеризующееся преимущественным поражением клапанов сердца, пристеночного эндокарда и эндотелия крупных сосудов, протекающее по типу сепсиса с токсическим поражением органов, развитием иммунопатологических реакций, эмболических и других осложнений.
Большие критерии:
-
Положительный посев крови:
-
возбудители типичные для ИЭ, выделенные из двух раздельно взятых проб крови: зеленящие стрептококки, Streptococcus gallolyticus, микроорганизмы НАСЕК-группы, Staphylococcus aureus или внебольничные энтерококки при отсутствии первичного очага;
-
Стойкая бактериемия (независимо от выявленного возбудителя), определяемая:
-
· или в двух и более пробах крови, взятых с интервалом 12 ч, · или в трех и более пробах крови, взятых с интервалом не менее 1 ч между первой и последней пробами
-
однократное выявление Coxiella burnetii или титра IgG к этому микроорганизму >1:800;
-
Доказательства поражения эндокарда:
-
вегетация, абсцесс или отхождение протеза при ЭхоКГ;
-
новая клапанная регургитация
-
Малые критерии:
-
Предрасположенность (предрасполагающее заболевание сердца или употребление наркотиков)
-
Лихорадка >38 °C,
-
Сосудистые феномены: эмболии крупных артерий, септические инфаркты лёгкого, микотические аневризмы, внутримозговые кровоизлияния, геморрагии на переходной складке конъюнктивы и повреждения Джейнуэя
-
Иммунологические феномены: гломерулонефрит, узелки Ослера, геморрагии Сплинтера(подногтевые кровоизлияния, не исчезают при нажатии), пятна Рота и ревматоидный фактор;
-
Микробиологические доказательства: положительный посев крови, который не соответствует большому критерию, или серологическое подтверждение активной инфекции, обусловленной потенциальным возбудителем ИЭ
Диагноз ИЭ считают достоверным при наличии двух больших, или одного большого и трёх малых, или пяти малых критериев. Диагноз ИЭ считают вероятным при наличии одного большого и одного малого или трёх малых критериев
В диагностике ИЭ определяют три основные составляющие:
1) клинические признаки;
2) эхокардиографию;
3) лабораторную (микробиологическую) диагностику.
Эхокардиография
Для инструментальной диагностики ИЭ в настоящее время доступно
выполнение трансторокальной и чреспищеводной ЭхоКГ.
Основными эхокардиографическими критериями ИЭ являются:
— вегетации (размер, подвижность, степень кальцификации);
— абсцессы;
— вновь возникшая недостаточность протезированного клапана.
В клинической ситуации, когда подозревается ИЭ, должно быть вы-полнено эхокардиографическое исследование. Показания и выбор методики выполнения ЭхоКГ

В зависимости от применяемой методики частота обнаружения возбудителя в крови составляет 30–70 %, при исследовании операционного материала — 52–90 %. Отрицательный результат микробиологического исследования может быть обусловлен:
— особенностями возбудителя;
— предшествующим забору анализа приемом антибактериальных лекарственных средств;
— не соблюдением микробиологической техники.
Правила взятия крови для микробиологического исследования
1. Забор крови производить до начала АБТ.
(В случае отсутствия возможности отменить АБТ — забор крови следует выполнять непосредственно перед очередным введением препарата).
2. Забор осуществляют из периферических вен разных конечностей (3
пробы) с интервалом 30 минут. Объем каждого образца (для взрослого пациента) должен быть не менее 15–20 мл.
3. При предшествующем коротком курсе АБТ забор анализа осуществляют не ранее, чем через 3 дня после прекращения лечения, при предшествующем длительном курсе — через 6–7 дней после отмены препарата.
4. В случае отрицательного результата первого исследования на гемо-
культуру при подозрении на ИЭ рекомендуется проведение 2-х или более дополнительных исследований через 48 ч.
5. Посев крови производить одновременно в два флакона для посева
на аэробные и анаэробные среды.
Алгоритм проведения микробиологической диагностики

Диф диагностика:
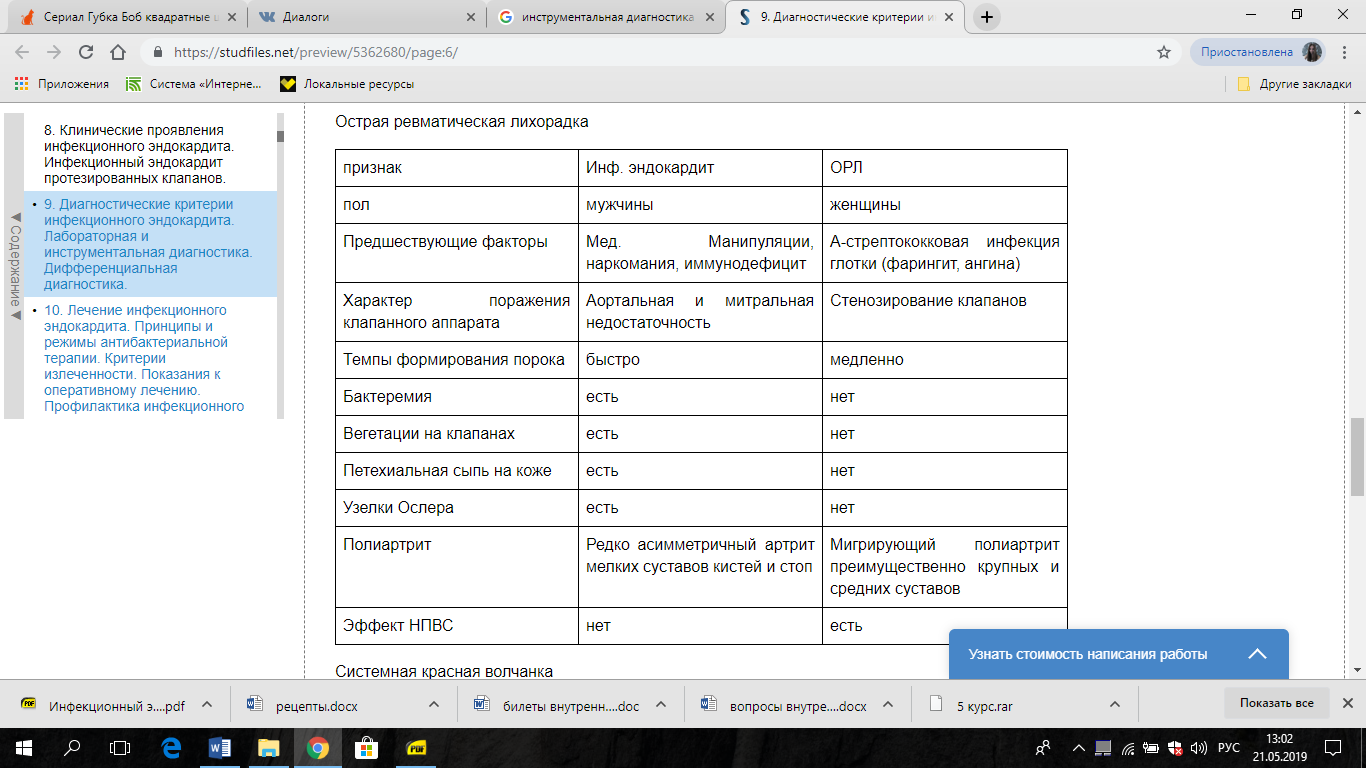
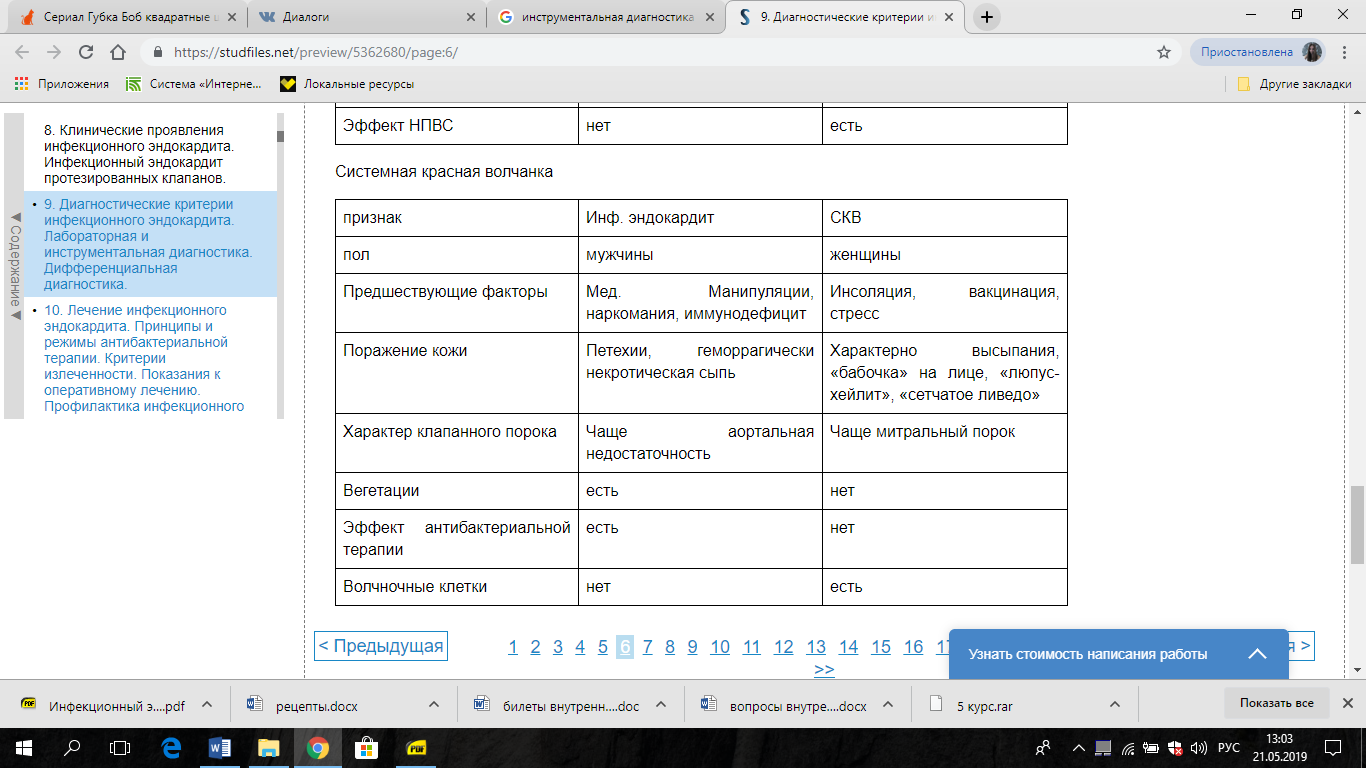
ПРОФИЛАКТИКА
Принципы профилактики ИЭ разработаны с учетом таких категорий как:
— оценка риска развития ИЭ у пациентов, страдающих сердечно-
сосудистой патологией;
— оценка риска бактериемии при медицинских вмешательствах (ди-
агностических, лечебных);
— оценка риска развития побочных эффектов антибактериальной те-
рапии, проводимой с профилактической целью;
— анализ экономической эффективности предлагаемых медикамен-
тозных схем профилактики.
ОСЛОЖНЕНИЯ ИНФЕКЦИОННОГО ЭНДОКАРДИТА
Сердечная недостаточность
Сердечная недостаточность наблюдается в 50–60 % случаев, является
самым частым осложнением ИЭ. СН может быть обусловлена: недостаточностью АК или МК, клапанной обструкцией или внутрисердечной фистулой. В патогенезе СН при ИЭ ведущую роль играет деструкция клапана, разрыв хорды, разрыв, перфорация створки. Клиническая картина характеризуется выраженной одышкой, отеком легких, возможна клиника кардиогенного шока. ЭхоКГ является обязательным методом для верификации причины, еѐ вызвавшей. СН может прогрессировать от легкой до тяжелой во время активной фазы заболевания, что является неблагоприятным в отношении прогноза фактором. Медикаментозная терапия СН при ИЭ осуществляется в соответствии с рекомендациями по лечению хронической СН.
Следует отметить, что у многих пациентов с ИЭ наличие СН является показанием к хирургическому вмешательству. Оперативное вмешательство показано пациентам с СН, развившейся вследствие тяжелой аортальной и митральной недостаточности, внутрисердечных свищей или обструкции клапана вегетацией.
Неврологические осложнения
Вторыми по частоте возникновения являются неврологические осложнения ИЭ. Клиническая картина неврологических осложнений включает ишемический и геморрагический инсульт, преходящие ишемические атаки, абсцессы мозга, менингит, токсические энцефалопатии, эпилепсию.
Неврологические осложнения чаще являются следствием эмболии вегетацией, развиваются у 20–40 % пациентов с ИЭ. После развития неврологического события большинство пациентов имеют показания к хирургическому лечению. После ишемического инсульта в случае, если неврологический прогноз не ухудшается, хирургическое лечение не противопоказано.
Нарушение мозгового кровообращения вследствие эмболических ос-
ложнений ИЭ ассоциировано с высокой летальностью. Таким образом,
своевременная диагностика, назначение адекватной АБТ имеют важное
значение для профилактики неврологических осложнений.
Острое повреждение почек
Острое повреждение почек встречается в 30 % случаев и является про-
гностически неблагоприятным фактором.
Выделяют две группы патогенетических факторов, вызывающих развитие острого повреждения почек при ИЭ:
1. Проявления заболевания ИЭ:
— инфаркт почек;
— иммунные комплексы и васкулитный гломерулонефрит;
— нарушение гемодинамики на фоне СН или сепсиса.
2. Лечебно-диагностические процедуры:
— нефротоксичность антибактериальных лекарственных средств;
— нефротоксичность контрастных веществ, используемых с диагно-
стической целью.
Вторая группа факторов должна быть особенно тщательно учтена с
точки зрения коррекции дозы антибактериальных препаратов по цифрам клиренса креатинина, анамнеза предыдущей почечной недостаточности.
При назначении диагностических процедур следует помнить о возможных побочных явлениях и осложнениях при выполнении рентген-контрастных исследований.
Иммунные осложнения
Частыми, до 15 % случаев симптомами ИЭ являются артралгии, миалгии, боль в спине. Указанные симптомы могут являться первыми проявлениями заболевания. При диагностике спондилита (наиболее часто встречается в случае стрептококковой инфекции) с магнитно-резонансно-томографической верификацией необходимо выполнить ЭхоКГ для исключения патологии сердца. И наоборот, у пациентов с ИЭ при возникновении болей в спине необходимо выполнение компьютерной томографии или магнитно-резонансной томографии для исключения пиогенного спондилодисцита.
Абсцесс селезенки
Абсцессы селезенки являются редким осложнением, несмотря на то, что эмболии селезенки встречаются довольно часто. У пациентов с ИЭ с сохранением стойкой лихорадки и бактериемией необходимо исключить данное осложнение. При наличии крупных абсцессов, не поддающихся лечению, разрыве селезенки может быть рассмотрен вопрос об удалении селезенки.
Миокардит, перикардит
Клинические проявления СН зачастую могут быть обусловлены по-
вреждением миокарда, развитием миокардита на фоне образования абсцессов. Ангиоспазм, эмболия коронарных артерий — причина развития инфаркта миокарда у пациентов с ИЭ без предшествующей патологии сердечно-сосудистой системы. Желудочковые нарушения ритма являются неблагоприятным прогностическим фактором.
Вовлечение в патологический процесс перикарда является редким ос-
ложнением ИЭ. При инфицировании золотистым стафилококком может развиваться гнойный перикардит, методом лечения которого является хирургическое дренирование.
Лечение указанных осложнений осуществляется посиндромно с учетом клинической картины
-
Инфекционный эндокардит. Медикаментозное лечение (этиотропное, патогенетическое, симптоматическое). Показания к хирургическому лечению. Профилактика в группах риска.
ИЭ — воспалительное заболевание инфекционной природы, характеризующееся преимущественным поражением клапанов сердца, пристеночного эндокарда и эндотелия крупных сосудов, протекающее по типу сепсиса с токсическим поражением органов, развитием иммунопатологических реакций, эмболических и других осложнений.
В терапии ИЭ выделяют консервативное и хирургическое лечение.
Медикаментозная терапия должна быть этиотропной, патогенетически обоснованной и по показаниям симптоматической. Успешное консервативное лечение зависит от ликвидации инфекционного агента антибактериальными препаратами. Хирургическое вмешательство способствует удалению зараженных тканей, дренированию абсцессов.
Основой консервативной терапии ИЭ являются антибактериальные
лекарственные средства. Эффективная АБТ возможна при выполнении
следующих условий:
— использование антибактериальных лекарственных средств с учетом
чувствительности к ним микроорганизмов;
— раннее начало приема в адекватных дозах;
— комбинированная терапия двух или трех бактерицидных антибио-
тиков с парентеральным путем введения;
— соблюдение оптимальных сроков лечения (не менее 4–6 недель при
своевременно начатом лечении и 8–10 недель при поздно начатом лечении);
— коррекция антибактериальной терапии, доз применяемых препара-
тов с учетом функции почек;
— определение антибиотикограммы при положительной гемокульту-
ре с последующей коррекцией терапии.
Эмпирическая терапия при установленном диагнозе ИЭ должна быть
начата незамедлительно. Три забора анализа крови из периферической вены с 30-минутным интервалом должно быть выполнено до начала анти-биотикотерапии. Для адекватного назначения стартовой терапии должны быть учтены несколько условий:
— необходимо уточнить принимал или нет пациент предварительную АБТ;
— уточнить нативный или протезированный клапан вовлечен в патологиче-
ский процесс (в случае протезированного — давность проведенной операции);
— эпидемиологическая обстановка, резистентность микроорганизмов к АБТ.
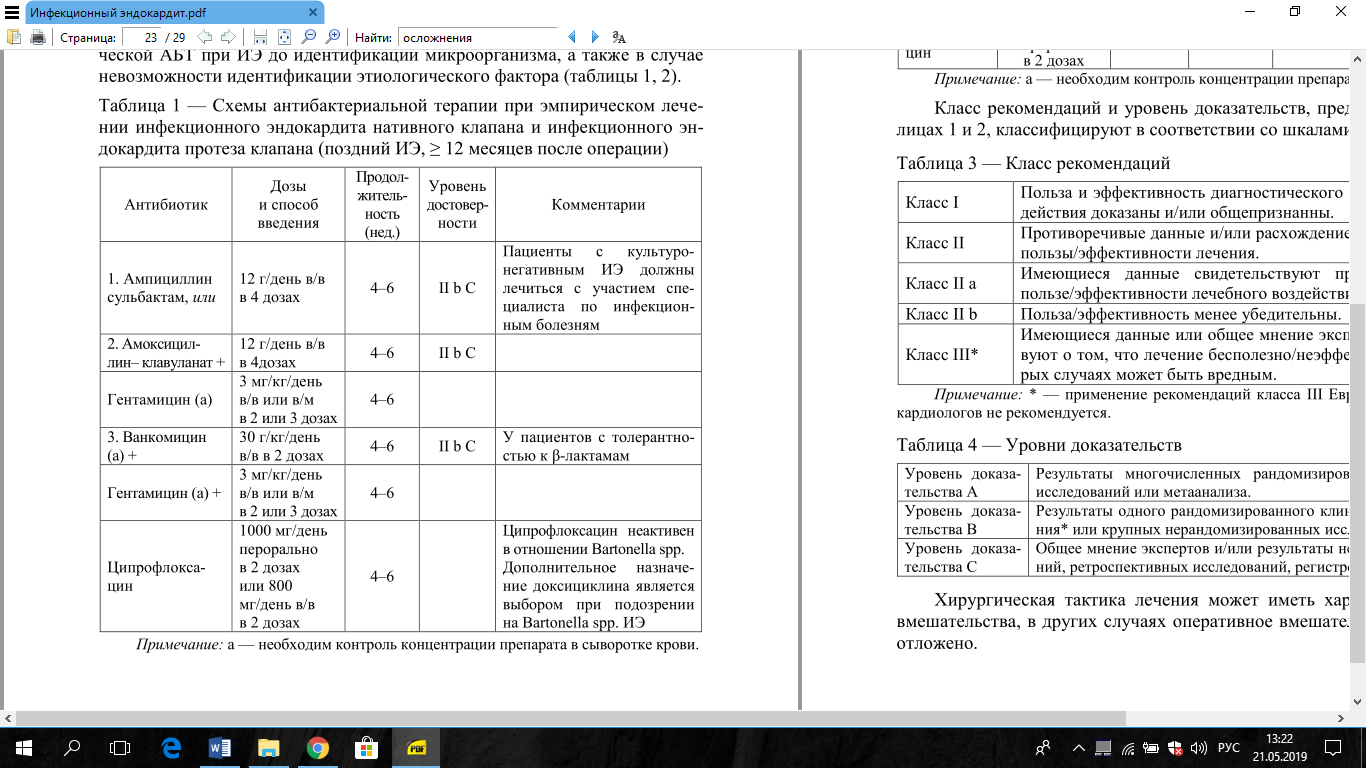

Хирургическая тактика лечения может иметь характер экстренного
вмешательства, в других случаях оперативное вмешательство может быть
отложено.
Тремя основными показаниями для выполнения раннего хирургического вмешательства при ИЭ являются:
— СН;
— неконтролируемая инфекция;
— профилактика эмболических осложнений.
Хирургическое лечение используется у половины пациентов с ИЭ. Так как выявление лиц, нуждающихся в раннем хирургическом вмешательстве, часто затруднено, консультация кардиохирурга рекомендована с целью определения лучшей стратегии лечения пациента в каждой индивидуальной ситуации.


-
Миокардиты. Определение. Классификация (инфекционные и неинфекционные миокардиты). Этиология и патогенез. Клинические проявления. Электро- и эхокардиографическая диагностика. Значение инструментальных (рентгенологических), лабораторных и морфологических методов диагностики. Дифференциальная диагностика.
Миокардит – это поражение сердечной мышцы, преимущественно воспалительного характера, обусловленное опосредованным через иммунные механизмы воздействием инфекции, паразитарной или протозойной инвазии, химических и физических факторов, а также возникающее вследствие аллергических и иммунных заболеваний.
Инфекционные:
• вирусные: вирусы Коксаки А и В, ЕСНО-вирусы, гриппа А и В, цитомегаловирус, вирусы полиомиелита, Эпштейна—Барр, иммунодефицита человека;
• бактериальные, риккетсиозные, спирохетозные: бета-гемолитические стрептококки, Corynobacterium diphtheriae , Mycoplasma pneumoniae , Coxiella burnetii (лихорадка Q), Rickettsia rickettsii (пятнистая лихорадка скалистых гор), Borrcllia burgdorferi (болезнь Лайма);
• протозойные: Tripanosoma cruzj (болезнь Чагаса), Toxoplasma gondii ;
• метазойные (трихинеллез, эхинококкоз);
• грибковые (кандидоз, криптококкоз, аспергиллез).
Неинфекционные:
• аллергические (антибиотики, сульфаниламиды, метилдопа, противотуберкулезные препараты, вакцины и сыворотки);
• токсические (кокаин, доксорубицин, антидепрессанты, при действии избытка катехоламинов — при феохромоцитоме и др.).
(ДРУГИЕ КЛАССИФИКАЦИИ, В ВОПРОСЕ ИХ НЕТ, НА ВСЯКИЙ)
По нозологической принадлежности:
• первичные (изолированные):
• вторичные (симптоматические) — как проявление системного (или общего) заболевания.
По патогенезу:
• инфекционные;
• токсические;
• аллергические (иммунные);
• смешанного характера.
По локализации:
• паренхиматозные;
• интерстициальные.
По распространенности:
• очаговые;
• диффузные.
По течению:
•Острый
•Абортивный
•Рецидивирующий
•Латентно текущий
• Хронический
По исходам:
• выздоровление
• миокардитический кардиосклероз (сердечная недостаточность, нарушения ритма сердца);
• дилатанионная кардиомиопатия.
Этиология инфекционных миокардитов представлена различными микроорганизмами:
-
•Вирусы: энтеровирусы (Коксаки А и В, ECHO, полиомиелита), аденовирусы, арбовирусы, цитомегаловирусы, ВИЧ, вирусы гепатитов, гриппа, паротита, краснухи, кори, ветряной оспы, герпеса, инфекционного мононуклеоза (Эпштейна—Барр) и др.
-
•Бактерии: стрептококки, стафилококки, пневмококки, менингококки, гонококки, бактерии дифтерии, туберкулеза, бруцеллеза и др.
-
•Спирохеты (сифилис, лептоспироз, возвратный тиф, боррелиоз).
-
•Риккетсии (сыпной тиф, лихорадка Q).
-
•Простейшие и гельминты (токсоплазмоз, трипаносомоз (болезнь Чагаса), трихинеллез, цистицеркоз и др).
-
•Грибки (актиномикоз, кандидоз, кокцидиоидомикоз, аспергиллез и др.).
Клиника во многом определяется этиологией, распространенностью и глубиной процесса. Его проявления могут варьировать от отсутствия признаков сердечной недостаточности до клинической картины тяжелой недостаточности кровообращения и сложных нарушений ритма и проводимости.
Жалобы: одышка, сердцебиение, кардиалгии, боль в правом подреберье.
Анамнез: хронологическая связь с перенесенной инфекцией, связь с другими потенциальными этиологическими факторами.
Осмотр, перкуссия: бледность, акроцианоз, патологические формы пульса, кардиомегалия, гепатомегалия, отеки.
Аускультация: тахикардия; реже - брадикардия, аритмия; ослабление 1-го тона, глухие тоны; систолический шум митральной регургитации, ритм галопа.
Лабораторные методы (анализ крови).Повышенная СОЭ (60%); лейкоцитоз (25%); повышение уровня МВ-изофермента КФК (12%); повышение концентрации тропонина J. По некоторым источникам чувствительность теста с сердечным тропонином J достигает 34%, специфичность – 89%, положительная диагностическая значимость – 82%.
ЭКГ: синусовая тахикардия, снижение вольтажа, изменения величины и продолжительности зубца Р, изменения фазы реполяризации (диффузные, локализованные), нарушения ритма, очаговые изменения в миокарде, блокады ножек пучка Гиса, блокады АV-проводимости, дисфункция синусового узла.
Эхокардиография (ЭхоКГ): увеличение полостей сердца, отечность миокарда, глобальные и сегментарные нарушения сократимости миокарда, дисфункции клапанов.
Рентген: увеличение размеров сердечной тени, признаки застоя в малом круге кровообращения.
Для диагностика острых диффузных миокардитов указанные диагностические критерии делятся на две группы: большие и малые.
К большим критериям относят хронологическую связь перенесенной инфекции с появлением в течение последующих 7-10 и более дней кардиомегалии, застойной сердечной недостаточности, кардиогенного шока, синдрома Морганьи - Адамса - Стокса, патологических изменений на ЭКГ (нарушения ритма, проводимости и др.), повышения активности кардиоспецифических ферментов в сыворотке крови.
Малые критерии - лабораторное подтверждение факта перенесенной инфекции, появление тахикардии, ослабления I тона, ритма галопа. Сочетание признаков перенесенной инфекции и двух больших критериев или одного большого и двух малых считается достаточным для постановки диагноза "миокардит".
(тут мало диф диагностики + инет)
При дифференциальном диагнозе миокардита с ишемической кардиомиопатией и постинфарктным кардиосклерозом с выраженными клиническими проявлениями недостаточности кровообращения следует обращать внимание на
-характер болевого синдрома в грудной клетке,
-его связь с физической нагрузкой
-и реакцию на прием коронарных вазодилататоров (нитраты, антагонисты кальция),
-сопутствующие симптомы воспаления,
-наличие стенокардии и инфаркта миокарда в анамнезе.
Выявление признаков рубцовых изменений на ЭКГ в этой ситуации может с равной вероятностью указывать как на перенесенный ранее инфаркт миокарда, так и на миокардит. В сложных случаях проводят коронароангиографию и биопсию миокарда.
Дифференцируя хронический миокардит с дилатационной кардиомиопатией, следует учитывать наличие общих симптомов воспаления (лихорадка, лейкоцитоз, увеличение СОЭ) и появление симптомов воспаления и аутоиммунного поражения других органов (артралгии, миалгии, плеврит, нефрит).
-
Принципы лечения миокардитов. Показания для применения глюкокортикостероидов. Исходы. Прогноз. Профилактика.
Принциты лечения миокардитов
Несмотря на то, что, теоретически, лечение миокардита должно быть направлено на устранение его причины, эффективность такой специфической терапии была подтверждена только в ходе выполнения ограниченного числа исследований, включавших больных с такими воспалительными заболеваниями миокарда, как саркоидоз и гигантоклеточный миокардит.
Специфическая терапия. Применяют иммуносупрессивную терапию, например, у больных с гигантоклеточным миокардитом или саркоидозом. В случае гигантоклеточного миокардита сочетанное применение иммуносупрессантов (циклоспорина и кортикостероидов) может улучшить в целом неблагоприятный прогноз.
Начальная лекарственная терапия должна соответствовать современным рекомендациям по лечению больных с СН. Стандартный режим терапии больных с СН, который включает применение -блокаторов, диуретиков, ингибиторов ангиотензинпревращающего фермента (АПФ) и блокаторов рецепторов ангиотензина II (БРА), должна начинаться и подбираться в зависимости от функционального состояния больного по результатам оценки функционального класса по классификации NYHA (New York Heart Association).
Ингибиторы АПФ и БРА. За счет рано начатого приема препаратов, блокирующих ренин-ангиотензиновую систему, возможно уменьшение выраженности дезадаптивного ремоделирования сердца, а также уменьшение вероятности прогрессирования заболевания до дилатационной кардиомиопатии. Применение ингибитора АПФ каптоприла, а также БРА лозартана и олмесартана приводит к статистически значимому уменьшению выраженности воспаления, некроза и фиброза.
Диуретики используют для предупреждения перегрузки жидкостью. Применение торасемида приводит к замедлению прогрессирования миокардита за счет уменьшения выраженности фиброза, размера миоцитов и уровня миокардиальных белков, трансформирующих фактор роста 1, а также уровней коллагена III типа, альдостеронсинтазы, которые не связаны с действием препарата на почки.
-блокаторы. В острой фазе декомпенсации СН следует избегать применения -блокаторов, так же как и в очень раннем периоде лечения больных с фульминантным миокардитом. Применение карведилола оказывает защитное действие на сердце с аутоиммунным миокардитом за счет подавления воспалительных цитокинов, а также реализации антиоксидантных свойств, в то время как применение метопролола и пропранолола не приводит к подобным эффектам. У больных с предполагаемым миокардитом были получены данные, которые позволяют предположить о том, что отсутствие применения -блокаторов сопровождается плохим прогнозом.
Антагонисты минералокортикоидных рецепторов рекомендуют пациентам с систолической дисфункцией ЛЖ и стойкой СН, тяжесть которой соответствует II-IV функциональному классу по классификации NYHA. Были подтверждены противовоспалительные эффекты применения эплеренона, которые проявлялись в подавлении протеиназ, выделяемых тучными клетками, что приводило у уменьшению выраженности ремоделирования сердца за счет подавления образования фиброза.
Известно, что применение сердечных гликозидов у больных с СН систолической дисфункцией ЛЖ, соответствующей II-IV функциональному классу по классификации NYHA, приводит к снижению частоты развития осложнений. Следует помнить о том, что применение высоких доз дигоксина приводит к образованию провоспалительных цитокинов и усилению выраженности повреждения миокарда. Кроме того, прием дигоксина может ограничивать применение максимальной дозы -блокатора вследствие развития брадикардии или АВ блокады. Следовательно, следует избегать применения дигоксина у больных с остро развившейся СН, которая обусловлена вирусным миокардитом.
Антагонисты кальция при лечении больных с остро развившейся СН не рекомендуются. Следует, однако, отметить, что применение амлодипина оказывает защитное действие от повреждения миокарда за счет подавления чрезмерного образования оксида азота.
Нестероидные противовоспалительные средства (НПВС) и колхицин применяют в качестве противовоспалительных средств при лечении перикардитов в качестве «неспецифической» противовоспалительной терапии, но отсутствуют показания для использования таких препаратов для лечения больных с миокардитом. Следовательно, применение НПВС в минимально необходимых дозах можно рассматривать только при лечении больных с перимиокардитом, у которых отсутствуют какие-либо нарушения функции ЛЖ и имеются выраженные боли в грудной клетке, обусловленные перикардитом.
Имплантация электрокардиостимулятора и дефибриллятора
Установка временного электрокардиостимулятора (ЭКС) показана больным с острым миокардитом, у которых развивается атриовентрикулярная блокада II или III степени с клиническими проявлениями. При миокардите, обусловленном болезнью Лайма, может отмечаться вариабельность степени нарушения атриовентрикулярной проводимости. В любом случае при стойкой атриовентрикулярной блокаде III степени, частота развития которой в целом низкая, требуется имплантация постоянного ЭКС. При болезни Чагаса характерно развитие нарушений проводимости, которые прогрессируют вплоть до развития полной атриовентрикулярной блокады; при этом заболевании часто развиваются и угрожающие жизни желудочковые аритмии.
Роль противовирусной терапии
Теоретическим основанием для применения противовирусных препаратов для лечения больных с миокардитом могут быть данные о том, что большая часть миокардитов обусловлена вирусной инфекцией.
Прогноз при миокардитах весьма вариабелен и зависит от множества факторов – этиологии, гистологических и иммунологических характеристик, клинической картины, наличия осложнений, возможности применения способов искусственного кровообращения. Известно, что часто миокардит протекает бессимптомно и заканчивается полным выздоровлением. Благоприятный прогноз обычен для пациентов с острым или фульминантным течением заболевания (в случае успешной коррекции гемодинамической нестабильности). При хроническом течении у значительного количества больных развивается дилатационная кардиомиопатия и в данном случае прогноз обусловлен наличием симптомов хронической сердечной недостаточности. При возникновении нарушений сердечного ритма прогноз часто зависит от возможности проведения специфических вмешательств, в том числе имплантации различных устройств. К числу предикторов плохого прогноза относят увеличение комплекса QRS более 120 мс, наличие синкопальных состояний, низкого систолического артериального давления, повышение давления в легочной артерии, дисфункция правого желудочка. Риск неблагоприятного исхода увеличивается при положительном иммуногистохимическом исследовании и отсутствии бета-адреноблокаторов в комплексной терапии. Выявление вирусного генома и положительный ответ по Далласским критериям на прогноз не влияют. Прогноз при специфических миокардитах (дифтерия, саркоидоз, болезнь Чагаса и др.) зависит от ранней диагностики и начала патогенетической терапии.
Исходы миокардита у выживших больных включают 4 основных варианта:
- выздоровление,
- миокардитический кардиосклероз,
- дилатационная кардиомиопатия,
- внезапная смерть.
У большинства больных, перенесших миокардит, наступает полное выздоровление в течение первого года от начала болезни. Однако у многих больных сохраняются остаточные изменения на ЭКГ, выявляемые в покое, при ортостатической пробе или велоэргометрии, указывающие на развитие очагового или диффузного миокардитического кардиосклероза (особенно часто миокардитический кардиосклероз становится исходом миокардита, вызванного вирусом Коксаки). Отсутствие клинико-инструментальных признаков поражения миокарда не исключает наличия миокардитического кардиосклероза как потенциальной причины внезапной смерти в ближайшем или отдаленном периоде после перенесенного миокардита, о чем свидетельствуют патоморфологические исследования умерших. В настоящее время накопилось достаточно оснований предполагать, что значительная часть случаев дилатационной кардиомиопатии является исходом вирусных миокардитов.
-
Первичные кардиомиопатии. Определение. Классификация. Этиология, патогенез нарушений внутрисердечной гемодинамики при разных формах первичных кардиомиопатий.
Кардиомиопатии - первичные невоспалительные поражения миокарда выясненной этиологии (идиопатические), не связанные с клапанными пороками или нутрисердечными шунтами, артериальной или легочной гипертензией, ишемической болезнью сердца или системными заболеваниями.
Классификация кардиомиопатий (1957 г.).
Выделяют следующие виды кардиомиопатий:
1. Дилатационная.
2. Гипертрофическая.
3. Рестриктивная.
4. Аритмогенная дисплазия правого желудочка.
5. Недифференцированные кардиомиопатии.
6. Специфические кардиомиопатии (ишемическая, клапанная, гипертензивная, воспалительная, метаболическая, кардиомиопатии при системных заболеваниях, кардиомиопатии при мышечных дистрофиях, кардиомиопатии при нейромышечных нарушениях, кардиомиопатии при гиперчувствительности и токсических реакциях, перипартальная кардиомиопатия).
Все варианты кардиомиопатий принято делить на три основные группы: дилатационная, гипертрофическая и рестриктивная.
Дилатационная кардиомиопатия характеризуется расширением полостей желудочков и нарушением их систолической функции. В основе данного типа лежит повреждение кардиомиоцитов, в связи с чем возникает уменьшение сократительной способности, дилатация сердечных полостей, компенсаторная гипертрофия миокарда, возможна недостаточность митрального клапана, коронарная недостаточность, переходящая в ишемию, развитие очагового и диффузного фиброза сердца.
Гипертрофическая форма отличается выраженным увеличением стенок левого желудочка при сохранении нормальных размеров его полости, часто асимметричная, по непонятным причинам. При этом нарушается диастолическая функция и сердечный ритм. Основные изменения гемодинамики следующие: повышение внутрижелудочкового давления, застой крови в лёгких, понижение сердечного выброса, коронарная недостаточность, электрическая нестабильность миокарда, приводящая к аритмии и внезапной смерти.
Рестриктивные кардиомиопатии обусловлены морфологическими нарушениями и выраженным фиброзом эндокарда и миокарда, что выражается в изменении диастолической функции сердца. Основными проявлениями считаются уплотнение и снижение эластичности эндокарда или миокарда, рестриктивное фиксированное нарушение наполнения кровью желудочков, расширение предсердий, связанное с их перегрузкой из-за уменьшения размера желудочковых полостей, как следствие возникновение внутрисердечных тромбов и возрастание риска тромбоэмболических осложнений.
-
Дилатационная кардиомиопатия. Клинические проявления. Значение эхокардиографии в диагностике. Течение и осложнения. Исходы. Прогноз. Принципы лечения. Медикаментозное лечение. Показания к хирургическому лечению.
Дилатационная кардиомиопатия (ДКМП) – первичное поражение сердца, характеризующееся диффузным расширением полостей сердца, преимущественно левого желудочка и нарушением сократительной функции.
Клиническая картина и диагностика.
Специфических признаков дилатационной кардиомиопатии нет. Клиническая картина полиморфна и определяется симптомами сердечной недостаточности, нарушениями ритма и проводимости, тромбоэмболическим синдромом.
жалобы на: повышенную утомляемость,
одышку при физической нагрузке, а затем и в покое.
По ночам - сухой кашель,
позже – типичные приступы удушья.
У 10% больных наблюдаются характерные ангинозные боли. При развитии застойных явлений в большом круге кровообращения появляются тяжесть в правом подреберье и отёки ног.
Одним из ранних проявлений дилатационной кардиомиопатии может быть пароксизмальная мерцательная аритмия, однако, больной часто долгое время не ощущает её.
Диагностические критерии дилатационной кардиомиопатии включают подтверждающие и исключающие признаки.
Подтверждающие признаки:
- прогрессирующая недостаточность кровообращения, резистентная к лечению;
- кардиомегалия с наличием относительной недостаточности митрального и трикуспидального клапанов;
- тромбоэмболический синдром;
- нарушение ритма, проводимости;
- относительно молодой возраст;
- отсутствие признаков воспалительного процесса;
- отсутствие связи заболевания с инфекционными или каким-либо другим этиологическим фактором.
Исключающие признаки:
- нормальные размеры сердца;
- ИБС (обструкция более 50 % просвета основных коронарных артерий);
- системная артериальная гипертензия (выше 160/100 мм.рт.ст.), документированная и подтвержденная при повторных измерениях и (или) доказательства поражения органов – мишеней;
- отсутствие в анамнезе врожденных пороков сердца и приобретенных изменений клапанного аппарата;
- указание в анамнезе на хроническое употребление алкоголя (более 40 г. в день для женщин и более 80 г. в день для мужчин в течение свыше 5 лет) с ремиссией дилатационной кардиомиопатии после 6 месяцев абстиненции;
- системные заболевания;
- поражения перикарда.
Важным признаком, подтверждающим данное заболевание, является значительное увеличение сердца, при этом артериальная гипертензия и клапанные пороки отсутствуют.
Кардиомегалия проявляется расширением сердца в обе стороны, определяемым перкуторно, а также смещением верхушечного толчка влево и вниз.
В тяжёлых случаях выслушиваются ритм галопа, тахикардия, шумы относительной недостаточности митрального или трёхстворчатого клапанов. Артериальное давление обычно нормальное или слегка повышено.
Лабораторные методы исследования длительное время не выявляют никаких изменений.
Рентгенологически выявляется значительное увеличение желудочков, усиление лёгочного рисунка, иногда появление транссудата в плевральных полостях.
Метод эхокардиографии позволяет выявить основной признак дилатационной кардиомиопатии – дилатацию полостей сердца с уменьшением фракции выброса левого желудочка. В допплеровском режиме можно обнаружить относительную недостаточность митрального и трёхстворчатого клапана, нарушения диастолической функции левого желудочка, увеличение конечного систолического и диастолического размеров левого желудочка.
На ЭКГ регистрируются признаки гипертрофии и перегрузки левого желудочка: депрессия сегмента ST и отрицательные зубцы Т в I, AVL, V5-V6; левого предсердия. ЭКГ – признаки носят неспецифический характер. К ним можно отнести нарушения проводимости (блокады ножек пучка Гиса), нарушение процессов реполяризации, мерцание предсердий, удлинение интервала QT.
Прижизненная биопсия миокарда малоинформативна при определении этиологии заболевания и оказывает помощь в дифференциальной диагностике дилатационной кардиомиопатии и заболеваний сердца, протекающих с кардиомегалией.
основным методом диагностики дилатационной кардиомиопатии служит эхокардиогрфия, позволяющая выявить дилатацию камер сердца и снижение сократимости левого желудочка, а также исключить поражение клапанов сердца и перикардиальный выпот.
Осложнения. К наиболее частым осложнениям дилатационной кардиомиопатии относятся тромбоэмболии, внезапная сердечная смерть, прогрессирующая сердечная недостаточность.
Основным направлением лечения является нормализации систолической функции сердца, устранение признаков недостаточности кровообращения, предупреждения тромбоэмболических проявлений заболевания, устранение нарушений ритма с помощью лекарственных препаратов.
1) Лечебный режим. т.к. это уменьшает воздействие ряда неблагоприятных факторов на сердечно-сосудистую систему.
Запрещается прием алкоголя и курения в связи с их повреждающим влиянием на миокард.
2) Лечение сердечной недостаточности:
-
сердечные гликозиды (при тяжелой сердечной недостаточности, но однако их следует назначать с большой осторожностью, ( повышена чувствительность может быть интоксикация);
-
негликозидные инотропные средства (допамин, амрион, милринон и др.) назначаются на непродолжительное время (4-6 дней) при крайне тяжелом течении сердечной недостаточности, а также с целью улучшения гемодинамики перед трансплантацией сердца;
-
периферические вазодилататоры – снижают преднагрузку и постнагрузку,
-
Применяются нитраты продленного действия одновременно с апрессином, празозин; Рекомендовано сочетать лечение тиазидными или петлевыми с калийсберегающими препаратами (верошпирон, триамтерем, адгальктон);
-
антиаритмическая терапия;
-
антикоагулянтная и антиагрегационная терапия: в качестве антикоагулянта рекомендуется гепарин внутривенно или под кожу живота, в качестве антиагрегантов - малые дозы ацетилсалициловой кислоты (0,165 – 0,325 г в сутки), дипиридамол (курантил, тиклид) трентал. Непрямые антикоагулянты применяются значительно реже (варфарин, пемитан и др.);
-
метаболическая терапия – проводится с целью улучшения метаболизма в миокарде, что опосредованно может положительно сказаться на его функциональном состоянии;
-
хирургическое лечение – пересадка сердца является единственным методом лечения дилатационной кардиомиопатии, обеспечивающим возможность полноценной жизни больных.
Прогноз: при ДКМП обусловлен выраженностью изменений левого желудочка и степени хронической сердечной недостаточности, а также индивидуальными особенностями течения заболевания. По данным различных клиник за 5-летний период заболевания и период наблюдения смертность составляет 35-50%, за 10-летний период – 70%.
-
Гипертрофическая кардиомиопатия. Клинические проявления. Значение эхокардиографии в диагностике. Течение и осложнения. Исходы. Прогноз. Принципы лечения. Медикаментозное лечение. Показания к хирургическому лечению.
Гипертрофическая кардиомиопатия (ГКМП)– заболевание миокарда неизвестной этиологии, характеризующееся гипертрофией межжелудочковой перегородки или стенок левого желудочка с уменьшением его систолического объёма и снижением его диастолической функции.
Выделяют 4 основных типа гипертрофической кардиомиопатии:
-
преимущественная гипертрофия базальных отделов межжелудочковой перегородки
-
асимметричная гипертрофия межжелудочковой перегородки на всём протяжении
-
концентрическая гипертрофия миокарда левого желудочка
-
гипертрофия верхушки сердца.
Различают обструктивную и необструктивную ГКМП. Гипертрофия может быть симметричной (увеличение с вовлечением всех стенок левого желудочка) и асимметричной (увеличение с вовлечением одной из стенок).
Характерными особенностями ГКМП являются высокая частота нарушений ритма сердца и нарушение диастолического наполнения левого желудочка, что может приводить к сердечной недостаточности. У 50% больных ГКМП наступает внезапная смерть, вызванная аритмией.
ГКМП встречается в молодом возрасте, более позднее выявление связано с нерезкой выраженностью гипертрофии миокарда и отсутствием значительных изменений внутрисердечной гемодинамики. При генетическом обследовании доказана роль наследственности в возникновении ГКМП (выявляется в 17-20% случаев).
Субъективные и обьективные признаки неспецифичны. Больных беспокоят одышка при физической нагрузке, боли за грудиной, учащённое сердцебиение, головокружение, обмороки.
Для ИГСС характерна триада симптомов, позволяющая поставить диагноз у постели больного на основании клинических признаков в сочетании с анамнестическими данными о семейном характере заболевания:
1) толчко-образный скачущий пульс;
2) поздний систолический шум над верхушкой сердца и по левому краю грудины;
3) пальпируемые сокращения левого предсердия
Осмотр внешних проявлений заболевания может не выявить. При выраженной сердечной недостаточности обнаруживают цианоз. Пальпаторно- усиленный верхушечный толчок, который в 34% случаев имеет «двойной характер»: вначале при пальпации ощущается удар от сокращения левого предсердия, затем от сокращения левого желудочка. Выявляется систолическое дрожание у левого края грудины, пульс высокий, скорый. Аускультативно определяются систолический шум на верхушке, в точке Боткина, который имеет характер нарастания-убывания и лучше выслушивается между верхушкой сердца и левым краем грудины.
К основным ЭКГ-признакам относят: гипертрофию левого желудочка, изменения сегмента ST и зубца Т, наличие патологических зубцов Q во II, III, AVF и грудных отведениях, трепетание предсердий, желудочковую экстрасистолию.
Основной метод диагностики – эхокардиография, с его помощью определяют локализацию гипертрофированных участков миокарда, степень выраженности гипертрофии. В 60% выявляют асимметричную гипертрофию, в 30%- симметричную, в 10% - апикальную. В доплеровском режиме определяют выраженность митральной регургитации, степень градиента давления между левым желудочком и аортой: градиент давления более 50 мм. рт.ст. считается выраженным.
К признакам ГКМП относят также малый размер полости левого желудочка, дилатацию левого предсердия.
Признаками обструктивной кардиомиопатии считают следующие: асимметричная гипертрофия межжелудочковой перегородки (толщина межжелудочковой перегородки должна быть на 4-6 мм больше нормы для данной возрастной группы); систолическое движение передней створки митрального клапана вперёд.
Рентгенологическое обследование больных с ГКМП выявляет увеличение левого желудочка и левого предсердия, расширение восходящей части аорты.
Проводится хирургическое и терапевтическое (медикаментозное) лечение.
-
Хирургическое лечение направлено на удаление гипертрофированных участков миокарда и устранения обструкции выходного тракта левого желудочка. Оно применяется при отсутствии эффекта от терапевтических методов, сохранении обструкции и клинической симптоматики заболевания. Цель – ликвидировать систолический градиент давления и снизить конечное диастолическое давление в левом желудочке. Применяют два вида операций: резекцию межжелудочковой перегородки и протезирование митрального клапана.
-
Медикаментозное лечение направлено на устранение или уменьшение признаков диастолической дисфункции левого желудочка, недостаточности кровообращения, купирование синдрома стенокардии и нарушений ритма.
Наиболее эффективны для этих целей β-адреноблокаторы, уменьшающие обструкцию, внутрижелудочковый градиент давления, улучшающие диастолическое расслабление левого желудочка, предупреждающие развитие мерцательной аритмии.
Используется пропранолон (обзидан, лидерал, анаприлин) в суточной дозе 160-320 мг, метопролол в суточной дозе 200 мг и выше.
При ГКМП применяются также антагонисты ионов кальция. Верапамил (изоптин, финоптин) улучшает диастолическое расслабление левого желудочка, увеличивает толерантность к физической (расслабление) нагрузке, обладает антиаритмическим действием. Применяется в дозе 160-320 мг в сутки. Дилтиазем используют в суточной дозе 180-360 мг.
Назначение производных дигидропиридинов короткого действия противопоказано, в связи с выраженным вазодилатирующим эффектом препаратов.
Все перечисленные препараты уменьшают симптоматику, улучшают качество жизни, но не влияют на выживаемость. При появлении признаков недостаточности кровообращения к лечению присоединяются диуретики. При нарушении ритма применяются соответствующие антиаритмические препараты. В этом случае препарат выбора амнадарон: в течение 5-7 дней суточная доза 1200 мг, затем 800 и 600 мг в течение недели в каждой дозе с переходом на поддерживающую терапию в дозе 200 мг в сутки.
Прогноз наиболее благоприятен при длительном бессимптомном течении заболевания, без отягощенного семейного анамнеза. Такое течение наблюдается у 1/3 больных.
-
Рестриктивная кардиомиопатия. Клинические проявления. Значение эхокардиографии в диагностике. Течение и осложнения. Исходы. Прогноз. Принципы лечения. Медикаментозное лечение. Показания к хирургическому лечению.
Рестриктивная кардиомиопатия (РКМП)
– это первичное или вторичное поражение миокарда неизвестной этиологии, характеризующееся нарушением диастолической функции сердца в результате морфологических изменений эндокарда, субэндокарда и миокарда (выраженного фиброза). РКМП характеризуется преимущественным нарушением диастолической функции и повышением давления наполнения желудочков при нормальной или малоизменённой сократительной функции миокарда и отсутствии его значимой гипертрофии и дилатации.
Клиника. Больные предъявляют жалобы на одышку при физической нагрузке, периферические отёки, боли в правом подреберье и увеличение живота.
При осмотре выявляются набухшие шейные вены, характерен симптом Куссмауля – увеличение набухания шейных вен на вдохе. Аускультативно выслушивается «ритм галопа», систолический шум недостаточности трёхстворчатого и митрального клапанов. При лёгочной гипертензии определяют её характерные аускультативные признаки, в лёгких выслушиваются хрипы. Характерны увеличение печени и асцит.
Наибольшее значение имеет эхокардиография. При РКМП размеры полостей сердца не изменены, в ряде случаев можно выявить утолщение эндокарда. Характерны нарушения диастолической функции левого желудочка: укорочение времени изоволюмического расслабления, при доплеровской эхокардиографии увеличение пика раннего наполнения, уменьшение пика предсердного наполнения. Особенностью рентгенологической картины лёгких считают нормальные контуры сердца при наличии признаков венозного застоя в лёгких. При эндомиокардиальном фиброэластозе Лёффлера возможны выраженная эозинофилия и бронхоспастический синдром, что в сочетании с умеренным увеличением сердца и симптомами сердечной недостаточности помогает поставить правильный диагноз.
Ранние стадии болезни могут быть выявлены при зондировании сердца и обнаружении повышенного конечного диастолического давления в левом желудочке.
Лечение
Проводится хирургическое и терапевтическое лечение.
Хирургическое заключается в иссечении плотной фиброзной ткани и протезировании клапанов при наличии показаний. Противопоказаниями для операции служат перикардит, активность заболевания, определяются по уровню гиперэозинофилии, рецидивирующий асцит.
Целью терапевтического лечения является уменьшение признаков недостаточности кровообращения. На ранних этапах заболевания при наличии гиперэозинофилии применяются глюкокортикоидные гормоны. Преднизолон назначают в дозе 40-50 мг с последующим переводом на поддерживающую терапию в дозе 10 мг.
Прогноз при раннем установлении диагноза относительно благоприятный, хирургическое лечение при сформировавшемся фиброзе позволяет продолжить жизнь больных.
-
Аритмогенная дисплазия сердца. Клинические проявления. Значение эхокардиографии в диагностике. Течение и осложнения. Исходы. Прогноз. Принципы лечения. Медикаментозное лечение. Показания к хирургическому лечению.
Аритмогенная дисплазия правого желудочка (АДПЖ) рассматривают как первичное поражение миокарда правого желудочка, характеризующее замещениями миоцитов жировой или фиброзно-жировой тканью. Этиология данной формы кардиомиопатии не установлена. Исследуется возможность генетической обусловленности заболевания, поскольку до 18% случаев приходится на семейные формы. Изучается влияние перенесенной вирусной или бактериальной инфекции, влияние химических факторов, физического перенапряжения.
Патогенез АДПЖ связан с развитием дезорганизации сердца, нарушением проведения импульсов в зонах фиброзно-жирового перерождения, что приводит как к созданию условий для возникновения нарушений ритма, так и снижения сократительной способности сердца.
Клиника и диагностика
Выделяют несколько клинически значимых форм заболевания. Первая форма характеризуется патологическими изменениями миокарда правого желудочка в сочетании с правожелудочковыми аритмиями. Выявляется в различных возрастных группах. Пациенты предъявляют жалобы на слабость, утомляемость, перебои в работе сердца, сердцебиение, головокружение, обморочные состояния, признаки правожелудочковой недостаточности. Пациенты с подобной клинической картиной представляют группу риска внезапной смерти. К факторам, увеличивающим этот риск, относят: молодой возраст, инверсия зубца Т в правых грудных отведениях, блокаду правой ножки пучка Гиса, синкопальные состояния, снижение фракции выброса правого желудочка; значительные физические нагрузки. Для второй клинической формы характерны правожелудочковые аритмии в виде желудочковой экстрасистолии, рецидивирующих пароксизмов желудочковой тахикардии, эпизодов фибрилляции желудочков. Она встречается реже, чем первая. Третья форма проявляется изменениями правого желудочка, характерными для АДПЖ, без нарушений ритма.
При ЭКГ-исследовании выявляются неспецифические изменения в виде увеличения амплитуды зубца Р, снижение амплитуды желудочкового комплекса QRS, полной блокады правой ножки пучка Гиса, двухфазного или отрицательного зубца Т в отведениях V1-V3, правожелудочковой экстрасистолии, правожелудочковой тахикардии, усиление интервала Q-Т. При проведении холтеровского мониторирования возможна регистрация не выявленных на ЭКГ- покоя эпизодов пароксизмальной желудочковой тахикардии типа «пируэт», фибрилляция желудочков.
Ультразвуковое исследование сердца выявляет дилатацию правого желудочка, дискинезию или гипокинезию его стенок, локальные аневризмы правого желудочка, снижение фракции выброса, признаки недостаточности трехстворчатого клапана. Радиоизотопная вентрикулография выявляет сегментарные нарушения сократительности, дилатацию правого желудочка. Электрофизиологическое исследование позволяет выявить аритмогенные зоны и контролировать адекватность антиаритмической терапии.
Эндомиокардиальная биопсия позволяет выявить фиброзно-жировую перестройку миокарда. Если в двух взятых образцах выявляется более 20% жировой ткани, диагноз считается достоверным, если процент жировой ткани колеблется от 5 до 20% - определяется высокий риск данной патологии.
Лечение направлено на профилактику и устранение аритмий, развитие хронической сердечной недостаточности. Наиболее часто используется амиодарон, сомалол, дигоксин при тахисистолической форме, трепетание предсердий. При развитии признаков хронической сердечной недостаточности возможно назначение диуретиков.
К хирургическому лечению относятся криодеструкция участка тахикардии при аритмогенной зоне меньшей, чем 4 см2, имплантация дефибрилятора или кардиостимуляторов, вентрикулотомия участков ранней актив.
Прогноз. Исходы АДПЖ по данным опубликованных исследований характеризовались выживаемостью за 11 лет наблюдения за 22 пациентами: 15 из них получали антиаритмическую терапию, 5 пациентам была проведена аблация аритмогенной зоны, 2-трансплантации сердца. Причиной летальных исходов у 3 больных была внезапная смерть, у 4-правожелудочковая недостаточность.
-
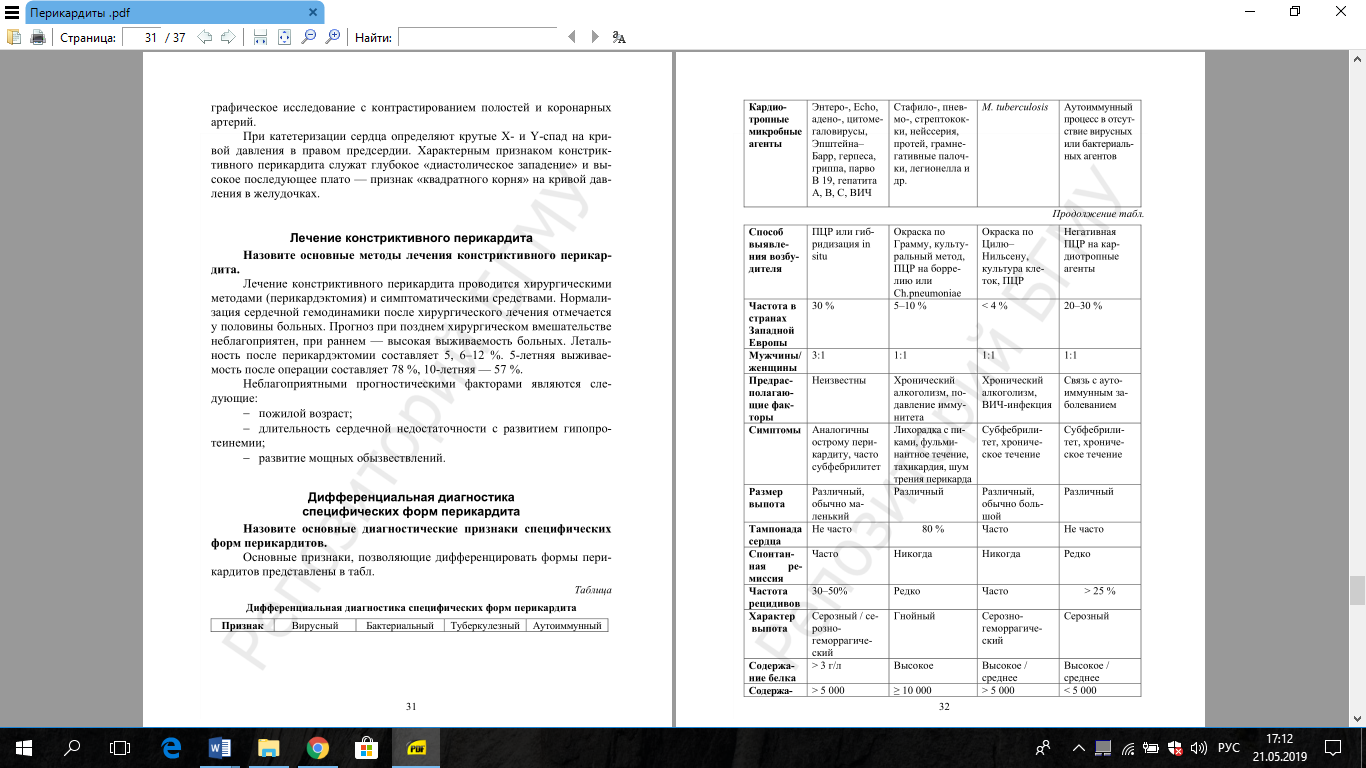
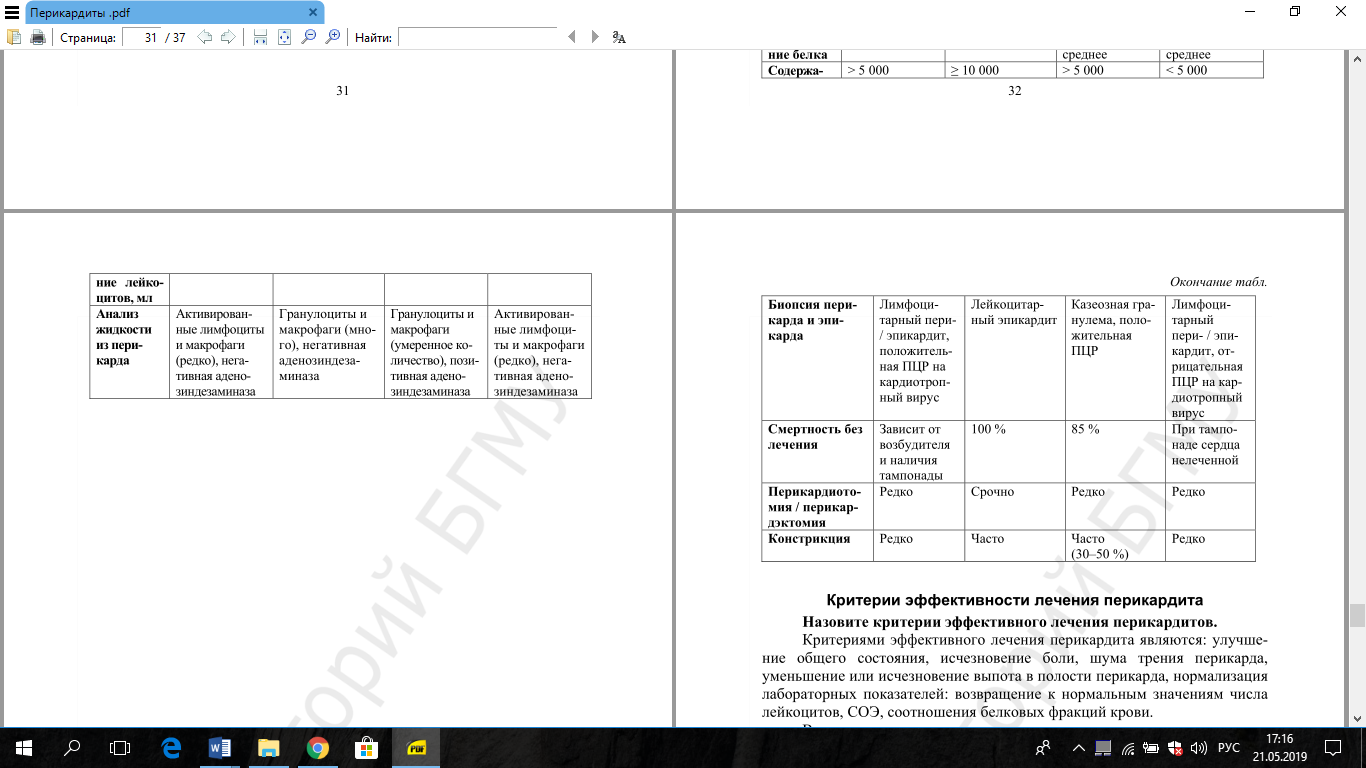
Перикардиты. Определение. Этиология и патогенез. Классификация. Дифференциальная диагностика.
Перикардит – это серозно-фибринозное, фибринозное, геморрагическое, гнойное или гнилостное воспаление перикардиальной полости (сердечной сорочки, околосердечной сумки).
!!!! До установления причины появления жидкости в перикардиальной полости и ее характера диагноз должен звучать как «синдром выпота в полости перикарда».
Классификация перикардитов
А. Клинико-морфологическая
-
Острый перикардит (до 6 нед)
-
Сухой, или фибринозный
-
Выпотной, или экссудативный:
-
-
без тампонады сердца
-
с тампонадой сердца
-
Подострый перикардит (6 нед-6мес)
1.Выпотной, или экссудативный
-
Хронический перикардит (более 6м)
1.Экссудативно-адгезивный
2. Адгезивный:
-
неконстриктивный
-
констриктивный
Б. По этиологии
I. Инфекционный перикардит
1. Бактериальный:
а) «неспецифический»
б) специфический, в том числе туберкулезный
2. Вирусный
3. Грибковый
4. При паразитарных и других инфекциях
II. Неинфекционный перикардит
1. Метаболический (при уремии, микседеме, аддисоническом кризе и др.)
2. Аллергический:
а) при ревматизме, диффузных заболеваниях соединительной ткани, системных васкулитах
б) при сывороточной болезни и лекарственный
в) связанный с повреждением сердца (при постинфарктном, постперикардиотомическом синдромах)
3. При остром инфаркте миокарда
4. При воздействии физических факторов:
а) травматический
б) радиационный
5. При опухолях перикарда
6. При некоторых других заболеваниях (семейная средиземноморская лихорадка, болезнь Уиппла, талассемия, панкреатит и др.).
Патогенез
В норме полость перикарда содержит перикардиальную жидкость, по составу близкую к плазме крови. Объём жидкости составляет 5-30 мл. Жидкость служит «смазкой», которая уменьшает трение между листками.
Первым развивается экссудативный перикардит. Происходит пропотевание дополнительной жидкости в полость перикарда. Увеличивается давление в полости перикарда, и, как следствие, сердце сдавливается снаружи. Нарушается диастолическая функция миокарда, сердце полностью не расслабляется в диастолу. Начинает нарастать сердечная недостаточность.
Если этот процесс развивается быстро, в течение часов или дней, развивается тампонада сердца. Это смертельно опасное осложнение, при котором жидкость в полости перикарда так сдавливает миокард, что он в диастолу не может расправиться, и, как следствие, больше не способен перекачивать кровь.
Вторым этапом перикардита является так называемый «сухой перикардит». Если накопление воспалительной жидкости было небольшим и не влияло на состояние больного, он может его не заметить. Постепенно, после затихания воспалительного процесса, объём жидкости в перикарде возвращается к норме, но содержащиеся в ней белковые включения остаются в полости перикарда. Формируются так называемые фибриновые спайки. Участки перикарда, где произошло активное отложение белка, слипаются, и впоследствии срастаются. Подобные спайки препятствуют свободному движению сердца в полости перикарда. При достаточно большом количестве спаек могут развиваться различные серьёзные осложнения, вызванные невозможностью сердца полноценно сокращаться.
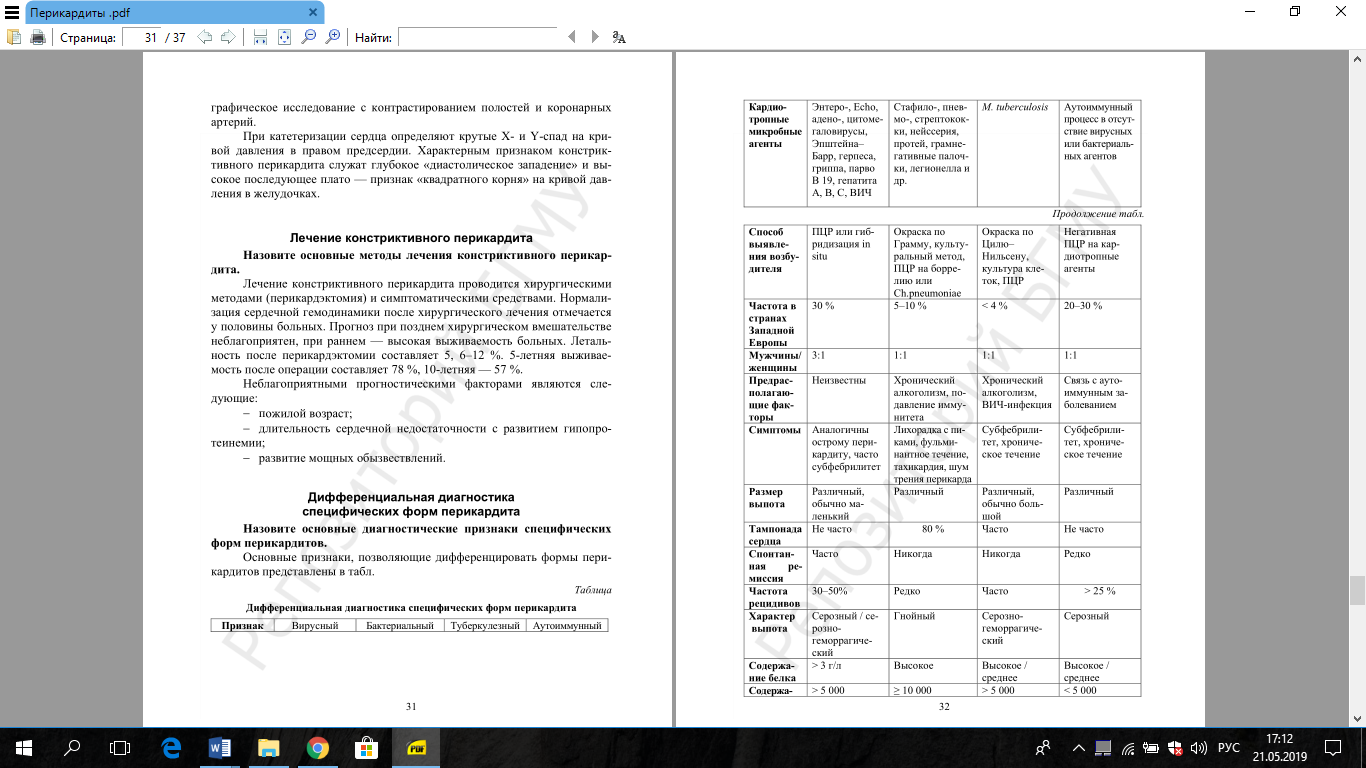

-
Сухой перикардит. Клиническая картина. Диагностика. Принципы лечения.
Острый фибринозный (сухой) перикардит
Клиника. Для фибринозного перикардита характерны триада: боль в грудной клетке, шум трения перикарда и изменения на ЭКГ.
Жалобы. Основным симптомом является боль в грудной клетке. Она связана с раздражением чувствительных рецепторов левого диафрагмального нерва.
Локализуется обычно за грудиной и может иррадиировать в шею, спину, левое плечо. Иногда она ощущается в надчревной области верхушки сердца. Боль носит постоянный характер, а по своей интенсивности варьирует от слабой до нестерпимой. Боль облегчается в положении сидя с наклоном туловища кпереди или в коленно-локтевом положении. Из-за болезненного вдоха больные часто дышат поверхностно, что может сопровождаться ощущением нехватки воздуха. Боль обычно возникает внезапно. Иногда за несколько дней ей предшествует неопределенное недомогание. У половины больных болевой синдром отсутствует или слабо выражен и быстро исчезает.
У ряда пациентов отмечаются также различные общие симптомы, связанные с основным заболеванием, - повышение температуры тела, слабость, иногда похудание. При объективном исследовании ведущим и патогномоничным признаком является шум трения перикарда. Он имеет характерный скребущий тембр.
Диагностика.
Изменения на ЭКГ, как и шум трения перикарда, могут быть единственным признаком заболевания. Отражается на ЭКГ в виде подъема сегмента ST и запаздывание реполяризации субэпикардиальных слоев вызывает инверсию зубца Т. Подъем сегмента ST является частым и ранним признаком, появляется у 90% больных в первые часы после возникновения болевого синдрома.
Его характерными особенностями являются:
1) конкордантность, т.е. регистрация в отведениях, отражающих потенциалы всех сегментов левого желудочка – 1,11, аVL, aVF, V2-6;
2) форма дугой книзу;
3) небольшая амплитуда – менее 5 мм.
Через несколько дней сегмент ST возвращается к изолинии, после чего на его месте формируются симметричные отрицательные зубцы Т. Они сохраняются несколько недель или месяцев, по-видимому, отражая относительно стойкое повреждение субэпикарда.
При рентгенологическом исследовании и эхокардиографии увеличение сердца или его отделов не характерно. Иногда как исход воспаления на ЭхоКГ может определяться утолщение перикарда.
Лабораторные изменения определяются основным заболеванием. Возможны неспецифические воспалительные сдвиги, иногда небольшое повышение активности изофермента МВ КФК в крови как следствие поверхностного миокардита.
Течение. Течение острого идиопатического перикардита у большинства больных доброкачественное. Полное выздоровление наблюдается даже без лечения. Возможны, однако, рецидивы, по-видимому, опосредованные аутоиммунными механизмами, и прогрессирование заболевания с развитием экссудативного перикардита.
Лечение этиотропное – основного заболевания и симптоматическое перикардита. Последнее заключается преимущественно в назначении нестероидных противовоспалительных препаратов. У единичных больных при отсутствии противопоказаний, связанных с активной инфекцией, в связи с выраженной болью и высокой лихорадкой прибегают к глюкокортикостероидам. Преднизолон по 40-60 мг в сутки внутрь назначают коротким курсом с полной отменой в течение 1-2 нед.
-
Экссудативный перикардит. Клиническая картина. Диагностика. Принципы лечения.
Острый экссудативный перикардит без тампонады сердца
Клиника.
Основными жалобами являются:
1) боль в грудной клетке;
2) одышка;
3) общие симптомы, связанные с причиной поражения перикарда.
Характерный для острого перикардита болевой синдром может исчезать при накоплении выпота либо, наоборот, появляться при его большом количестве, возможно, вследствие растяжения перикарда.
Одышка не выражена и связана с болью, механическим сдавлением бронхов и паренхимы легких.
Общие симптомы – повышение температуры тела, слабость, похудание и другие – могут быть резко выражены.
Реже при значительном объеме выпота отмечаются также симптомы сдавления соседних органов:
1) дисфагия из-за сдавления пищевода;
2) сухой кашель рефлекторного характера, связанный с увеличением давления на трахею;
3) осиплость голоса вследствие раздражения возвратного нерва.
При объективном исследовании определяются:
1) шум трения перикарда;
2) тахипноэ;
3) признаки наличия жидкости в полости перикарда. Шум трения перикарда может сохраняться даже при значительном выпоте, поскольку жидкость собирается преимущественно книзу и кзади от сердца, тогда как кпереди от него листки перикарда длительное время находятся в соприкосновении друг с другом.
Клинические признаки наличия выпота в перикарде без сдавления сердца и нарушения его диастолического наполнения (т.е. тампонады) включают:
1) набухание шейных вен и повышение ЦВД, обычно умеренное;
2) расширение тупости сердца во все стороны с изменением ее границ в зависимости от положения тела. (При переходе из горизонтального положения в положение стоя или сидя зона притупления во втором-третьем межреберье сокращается, расширяясь на 2- 4 см и более в третьем-четвертом межреберье. Угол между правой границей сердечной тупости и печеночной тупостью (угол Эбштейна) становится тупым.) Из-за наличия жидкости сердечная тупость приобретает выраженный, «деревянный» характер;
3) ослабление верхушечного толчка и его смещение кверху до третьего-четвертого межреберья и кнутри от границ сердечной тупости.
4) ослабление звучности сердечных тонов не является обязательным признаком и больше характерно для миогенной дилатации сердца;
5) притупление перкуторного тона с усилением голосового дрожания и бронхофонии и очагом бронхиального дыхания слева книзу от угла лопатки (признак Эварта). Обусловлено сдавлением экссудатом нижней доли левого легкого. При наклоне больного кпереди легкое расправляется.
Диагностика.
Изменения на ЭКГ, связанные с наличием выпота, неспецифичны и включают:
1) низкий вольтаж зубцов;
2) сглаженность, уплощение, двухфазность или инверсию зубцов Т как следствие давления жидкости на субэпикардиальный миокард и его воспаление;
3) электрическую альтернацию. Изменение амплитуды и полярности комплексов QRS в одном и том же отведении связано с увеличением амплитуды перемещения сердца в переполненной жидкостью полости перикарда;
4) синусовую тахикардию, не соответствующую выраженности повышения температуры тела и одышки, либо, реже, брадикардию в результате раздражения блуждающего нерва.
При рентгенологическом исследовании характерно увеличение тени сердца в обе стороны, которое в динамике развивается быстро и сердце может достигать огромных размеров (cor bovinum), не сопровождаясь выраженными клиническими признаками нарушения насосной функции. В передне-задней проекции сердце имеет шаровидную форму, образуя острый угол с диафрагмой, в отличие от треугольной формы при хроническом экссудативном перикардите. Дуги сердечной тени сглажены, пульсация ослаблена.
Эхокардиография. Скопление жидкости между листками перикарда вызывает их разъединение с образованием эхо-свободного пространства вокруг желудочков сердца. Выпот в перикард и утолщение его листков хорошо визуализируются при компьютерной томографии и ядерно-магнитном резонансе.
Осложнения. Основным осложнением острого экссудативного перикардита является тампонада сердца. Примерно в 1\3 случаев возникает пароксизмальная мерцательная аритмия или суправетрикулярная тахикардия, что связывают с распространением воспаления на миокард предсердий.
Лечение обязательно проводят в стационаре.
Оно зависит от причины перикардита и выраженности нарушений гемодинамики и включает:
1) лечение основного заболевания с помощью антибиотиков, туберкулостатических и химиопрепаратов, гемодиализа и др.;
2) симптоматическую и отчасти патогенетическую терапию нестероидными противовоспалительными средствами и глюкокортикостероидами. Лечение обычно начинают с относительно больших доз – 60-80 мг преднизолона в сутки внутрь – и проводят коротким курсом с быстрым снижением дозы до полной отмены в течение 2-4 нед.;
3) эвакуация выпота из полости перикарда. Показана при первых признаках тампонады сердца, а также при большом объеме выпота, который вызывает дискомфорт и не рассасывается в течение 2-3 нед. Обязательным показанием является также гнойный перикардит. Если, несмотря на повторные пункции, жидкость продолжает быстро накапливаться, прибегают к перикардэктомии.
-
Констриктивный перикардит. Клиническая картина. Диагностика. Принципы лечения.
Клиника. В основе лежит препятствие венозного притока к сердцу, преимущественно его правым отделам, и снижение МОС.
Пациенты жалуются на увеличение живота и чувство тяжести в правом подреберье, которые, в отличие от застойной сердечной недостаточности, предшествуют отекам нижних конечностей. Большинство пациентов беспокоят также слабость, утомляемость и одышка при физической нагрузке вследствие умеренной легочной гипертензии и фиксированного МОС. В запущенных случаях отмечаются похудание и диспепсия.
При физическом исследовании:
1. Гепатомегалия, асцит и периферические отеки.
2. Высокое венозное давление и изменения венного пульса. Шейные вены резко набухшие вследствие значительного повышения ЦВД, которое составляет обычно 250-300 мм.рт.ст. и является наиболее постоянным признаком заболевания. На вдохе набухание шейных вен и ЦВД возрастают. Этот феномен носит название признака Кусмауля.
3. Частый малый пульс.
4. Изменения верхушечного толчка. Верхушечный толчок обычно отсутствует. Такой диастолический верхушечный толчок образуется в момент резкого прекращения дальнейшего наполнения сердца из-за противодействия со стороны неподатливого перикарда.
5. Перикард-тон. Этот добавочный тон в период протодиастолы специфичен для констриктивного перикардита.
Диагностика.
На ЭКГ – низкий вольтаж комплекса QRS, уплощение или инверсия зубцов Т во многих отведениях, отклонение электрической оси сердца вправо, двухгорбый зазубренный зубец Р, напоминающий P-mitrale, и изредка – признаки гипертрофии правого желудочка.
При рентгенологическом исследовании размеры сердца не изменены или умеренно увеличены. Часто отмечается дилатация верхней полой вены, реже – небольшое увеличение предсердий. Пульсация сердца резко ослаблена. Патогномоничным рентгенологическим признаком является отложение в перикарде кальция в виде отдельных очагов или ободка в области атриовентрикулярной борозды, диафрагмальной и стернальной поверхностей правого или левого желудочка за исключением верхушки.
Изменения данных ЭхоКГ:
1) утолщение перикарда;
2) отсутствие расширения левого желудочка во второй половине диастолы;
3) парадоксальное движение межжелудочковой перегородки в период систолы при отсутствии объемной перегрузки правого желудочка.
Компьютерная томография и ядерно-магнитный резонанс служат надежным методами визуализации утолщения перикарда, которое является ценным диагностическим признаком констриктивного перикардита.
Катетеризация желудочков. Диагностическое значение имеет выявление нарушения позднего диастолического наполнения (синдрома рестрикции).
При лабораторном обследовании у значительной части больных определяются признаки печеночной недостаточности – гипоальбуминемия, повышение уровня билирубина и мочевины, положительная бромсульфолеиновая проба.
Течение и осложнения. К возможным осложнениям констриктивного перикардита относятся:
1) мерцательная аритмия. Отмечается в 30-40% случаев и обусловлена, вероятно, вовлечением в патологический процесс миокарда предсердий;
2) миокардиальная недостаточность. Развивается при длительном течении заболевания и наиболее ярко проявляется после перикардиоэктомии, ухудшая ее результаты;
3) кардиальный цирроз печени. Возникает при длительном и выраженном венозном застое в печени;
4) энтеропатия вследствие нарушения лимфатического оттока от тонкой кишки из-за выраженного повышения венозного давления. Может приводить к значительной потере белка, что усугубляет асцит и периферические отеки, вплоть до развития нефротического синдрома.
Лечение. Единственно эффективным является хирургическое лечение – перикардэктомия. Активная мочегонная терапия и парацентез связаны с риском резкого снижения давления наполнения желудочков и падения МОС, вплоть до развития гиповолемического шока.
-
Осложнения перикардитов. Тампонада сердца. Показания к пункции перикарда и хирургическому лечению. Исходы перикардитов. Прогноз.
Тампонада сердца
Тампонада сердца – это осложнение экссудативного перикардита, при котором давление в перикарде повышается настолько, что создает значительное препятствие притоку крови в желудочки и вызывает нарушение их диастолического наполнения.
Этиология. Наиболее частой причиной тампонады сердца является кровотечение в перикард (гемоперикард) после хирургических операций.
Клиника. Проявления тампонады сердца обусловлены малым МОС и застоем в системным венах.
Жалобы неспецифичны. Наблюдаются одышка, слабость, головокружение, а при медленном развитии тампонады – также чувство тяжести или боль в надчревной области и в правом подреберье и увеличение живота. АД имеет тенденцию к снижению, но в начальных стадиях может сохраняться в пределах свыше 100 мм.рт.ст. за счет артериолярной вазоконстрикции.
Важное диагностическое значение имеет парадоксальный пульс вследствие снижения систолического АД на вдохе более чем на 10 мм.рт.ст. Верхушечный толчок ослаблен, иногда не определяется. Тоны сердца глухие, может сохраняться шум трения перикарда. Добавочные тоны, как и застойные хрипы в легких, не характерны. При хронической тампонаде отмечаются увеличение печени и асцит. Асцит предшествует периферическим отекам, что имеет важное дифференциально-диагностическое значение.
Основным осложнением тампонады является шок.
Лечение. Как угрожающее жизни состояние тампонада сердца требует неотложного лечения – перикардиоцентеза. Он показан во всех случаях тампонады и снижения систолического АД более чем на 30 мм.рт.ст. от его обычного уровня. Чаще всего перикардиоцентез производят из субксифоидального доступа или при пункции в четвертом межреберье слева. Особенно выраженный клинический эффект дает аспирация первых 25-50 мл жидкости.
Прогноз. Нераспознанная тампонада сердца является фатальной. Однако при своевременном оказании помощи ближайший прогноз обычно благоприятен. Исключение составляют случаи разрыва сердца, его значительной травмы и расслоения аневризмы аорты. Отдаленный прогноз зависит от генеза поражения перикарда.
Исходы перикардитов:
-
сухожильные бляшки
-
интраперикардиальные спайки
-
сращения перикардиальных листков
-
экстраперикардиальные спайки
-
панцирное сердце
-
Электрофизиологические механизмы аритмий и блокад сердца. Классификация нарушений ритма сердца. (Очень дурацкий вопрос про эл.физиол.механизмы. я хз, что тут нужно!)
Классификация аритмий
Вследствие нарушений автоматизма:
Номотопные:
● синусовая тахикардия;
● синусовая брадикардия;
● синусовая аритмия;
● синдром слабости синусового узла.
Гетеротопные аритмии:
● миграция наджелудочкового водителя ритма;
● медленные выскальзывающие ритмы: предсердный медленный ритм, атриовентрикулярный ритм (узловой ритм), идиовентрикулярный (желудочковый) ритм;
● выскальзывающие комплексы;
● атриовентрикулярная диссоциация.
Вследствие нарушений проводимости:
Замедление проведения (блокады):
● синоаурикулярная блокада;
● внутрипредсердная блокада;
● атриовентрикулярная блокада;
● нарушения внутрижелудочковой проводимости;
● блокады ножек пучка Гиса и ветвей левой ножки.
Ускорение проведения:
● синдром Вольфа-Паркинсона-Уайта (WPW);
● синдром Клярка-Леви-Кристеско (CLC).
Вследствие нарушений возбудимости (комбинированные):
Экстрасистолия:
● наджелудочковая;
● атриовентрикулярная;
● желудочковая.
Пароксизмальная тахикардия:
● наджелудочковая;
● атриовентрикулярная;
● желудочковая.
Трепетание и мерцание предсердий.
Трепетание и мерцание желудочков.
К сердечным аритмиям относят изменения нормальной частоты, регулярности и источника возбуждения сердца, а также расстройства проведения импульса, нарушения связи или последовательности между активацией предсердий и желудочков.
Электрофизиология миокарда
Основными понятиями в электрофизиологии миокарда являются:
-
потенциал покоя (ПП);
-
потенциал действия (ПД);
-
возбудимость и рефрактерные периоды (РП) структуры;
Этиологические факторы развития аритмий
1) функциональные факторы, связанные с дисбалансом вегетативной нервной системы, при физическом и эмоциональном напряжении, в пубертатный период: гормональные нарушения (гипотиреоидизм, гипертиреоидизм), курение табака, употребление алкоголя, употребление кофеина;
2) органическое поражение миокарда, которое сопровождается его гипертрофией, ишемией, очаговым и диффузным кардиосклерозом, а также дилатацией полостей предсердий и желудочков: ИБС (стенокардия, инфаркт миокарда, постинфарктный кардиосклероз), сердечная недостаточность, кардиомиопатии, приобретённые и врождённые пороки сердца, миокардиты, гипоксия, врождённые аномалии структуры (дополнительное атриовентрикулярное соединение) или функции (наследственные нарушения в ионных каналах) проводящей системы;
3) нарушения электролитного обмена (гипокалиемия, гипомагниемия, гиперкалиемия, гиперкальциемия);
4) ятрогенные факторы (антиаритмические препараты, сердечные гликозиды, диуретики, симпатомиметики).
Нарушения ритма сердца могут возникать в результате:
1. Нарушений формирования импульса:
● повышение нормального автоматизма;
● патологический автоматизм;
● триггерная активность.
2. Нарушений проведения возбуждения:
● замедление проведения и блокады;
● однонаправленная блокада и повторный вход волны возбуждения (re-entry).
3. Сочетанных нарушений образования и проведения импульса — парасистолии.
-
Синусовая тахикардия, синусовая брадикардия, синусовая аритмия. Клинические проявления. Диагностика. Суточное мониторирование электрокардиограммы. Медикаментозное лечение.
Синусовая тахикардия – увеличение автоматизма синусового узла и нарушение его регуляции.
Критерии: синусовая тахикардия ЧСС > 100 в мин. И выраженное увеличение ЧСС во время активности. Непароксизмальный характер тахикардии,отсутствие вторичных причин тахикардии,характерная морфология зубцов P. Лечение-б-адреноблокаторы
Синусовая брадикардия-замедление ритма сердца меньше 60 в мин.
Импульсы возникают в синусовом узле,зубцы P имеют обычную амплитуду. Обычно сопровождается нерегулярными сердечными сокращениями. При остро возникшей брадикардии вводят 0,5 мг атропина внутривенно. ЭКС при выраженном нарушении гемодинамики.
Синусовая аритмия-периодическое изменение деятельности синусового сердечного цикла, когда разница между максимальным и минимальным интервалом PP больше 120 мс, а отношение этой разницы к минимальному интервалу PP составляет больше 10%.
Формы:
1. Дыхательная,когда интервал PP укорачивается при вдохе(подавление тонуса блуждающего нерва) и удлиняется при выдохе.
2. Недыхательная, когда вариабельность интервала PP не связана с дыхательным циклом. Специального лечения не требует.
-
Фибрилляция предсердий. Классификация. Клинические проявления. Диагностика. Медикаментозное лечение.
Фибрилляция предсердий представляет собой состояние, при котором наблюдается частое (до 400–700 уд./мин), беспорядочное, хаотичное возбуждение и сокращение отдельных групп мышечных волокон предсердий.
При брадисистолической форме фибрилляции предсердий число желудочковых сокращений меньше 60 уд./мин;
при нормосистолической — от 60 до 100 уд./мин;
при тахисистолической форме — от 100 до 200 уд./мин.
Классификация фибрилляции предсердий:
-
Пароксизм фибрилляции предсердий
-
Рецидивирующая фибрилляция предсердий: при наличии 2 или более пароксизмов
-
Пароксизмальная: если фибрилляция предсердий проходит спонтанно, то рецидивирующую фибрилляцию предсердий называют пароксизмальной
-
Персистирующая: если рецидивирующая фибрилляция предсердий сохраняется более 7 дней, относят также случаи длительно сохраняющейся аритмии (например, более 1 года)
-
Постоянная фибрилляция предсердий: более 1 года
-
Впервые выявленная: фибрилляция предсердий может быть пароксизмальной или персистирующей
(Выше была классификация из методы, ниже – интернет! ЛУЧШЕ МЕТОДА, но мало-ли что)

ЭКГ признаки фибрилляция предсердий: отсутствие во всех ЭКГ-отведениях зубца Р. Наличие на протяжении всего сердечного цикла беспорядочных мелких волн f, имеющих различную форму и амплитуду. Волны f лучше регистрируются в отведениях V1, V2, II, III и aVF. Нерегулярность желудочковых комплексов QRS — неправильный желудочковый ритм (различные по продолжительности интервалы R-R). Наличие комплексов QRS, имеющих, в большинстве случаев, нормальный неизмененный вид без деформации и уширения.
Фибрилляция предсердий может проявляться сердцебиением, вызывает нарушения гемодинамики и тромбоэмболические осложнения или протекает бессимптомно.
Симптомы фибрилляции предсердий зависят от правильности и частоты желудочкового ритма, состояния сердца, длительности фибрилляции предсердий и индивидуальных факторов.
Первым проявлением фибрилляции предсердий могут быть тромбоэмболия или нарастание сердечной недостаточности, однако большинство пациентов жалуются на учащенное сердцебиение, боль в груди, одышку, утомляемость, головокружение или обморок.
Лечение фибрилляции предсердий
Выделяют три цели лечения пациентов с фибрилляцией предсердий: контроль ЧСС, профилактика тромбоэмболии и контроль ритма.
-
Купирование пароксизма (контроль ритма) проводится в зависимости от длительности пароксизма, показателей гемодинамики и эффективности применения лекарственных средств для контроля ритма в анамнезе. При длительности пароксизма < 48 часов фармакологическая или электрическая кардиоверсия может быть выполнена без длительной антикоагулянтной подготовки, при длительности пароксизма > 48 часов – антикоагулянтная подготовка в течение > 3 недели: варфарином (под контролем МНО = 2,0–3,0),:
При длительности пароксизма < 48 часов:
-
Пропафенон 1–2 мг/кг внутривенно за 10 минут;
-
прокаинамид 10 % 5–10 мл (до 17 мг/кг) внутривенно капельно;
-
пропафенон 150–450 мг однократно
-
этацизин 50–100 мг однократно;
-
амиодарон внутрь 600–1000 мг/сут.;
-
амиодарон 5–7 мг/кг (300–450 мг) внутривенно медленная (за 30–60 минут) инфузия или
-
ЭИТ 100–360 Дж (при наличии неотложных показаний).
-
Контроль чсс:
-
Метопролола тартрат 0,1 % раствор 2,5–5 мл (2,5–5,0 мг со скоростью 1–2 мг/мин);
-
Бисопролол 2,5–10 мг/сут.;
-
Метопролол 25–100 мг 2–4 раза в день;
-
дигоксин (при отсутствии WPW) – 0,25 мг (0,025 % – 1 мл) внутривенно медленно;
-
При синдроме WPW – Амиодарон 150 мг в/в в течение 10 минут с последующей инфузией 0,5–1,0 мг/мин;
-
При нарушении центральной гемодинамики и неконтролируемой тахисистолии или трепетании предсердий ЭИТ разрядом 100–360 Дж.
-
Профилактика пароксизмов: (подбор эффективного препарата):
1. метопролол 25–200 мг/сут. внутрь, бисопролол 2,5–10 мг/сут. бетаксолол 5–40 мг/сут.
2. пропафенон – 450–600 мг/сут. или этацизин – 150–200 мг/сут.;
3. соталол 80–320 мг/сут.;
4. при неэффективности указанных выше лекарственных средств и наличии выраженных симптомов фибрилляции предсердий – амиодарон 100–400 мг/сут.
-
Профилактика тромбоэмболических осложнений: определяется степенью риска тромбоэмболии (по шкале CHA2DS2-VASc).
-
варфарин 2,5–5 мг/сут. под контролем МНО (= 2,0–3,0, целевой 2,5).
-
дабигатран (при неклапанной фибрилляции предсердий) – 150 мг х 2 раза/сут.
-
ривароксабан (при неклапанной фибрилляции предсердий) 20 мг 1 раз в сутки
-
комбинация аспирина и клопидогреля или, что менее эффективно, аспирин
-
-
Трепетание предсердий. Классификация. Клинические проявления. Диагностика. Медикаментозное лечение.
Трепетание предсердий возникает при тех же патологических состояниях, однако, причиной этого нарушения ритма сердца несколько чаще бывают заболевания, характеризующиеся перегрузкой правого предсердия (дилатация, гипертрофия, дистрофические изменения), в т. ч. тромбоэмболии легочной артерии, хроническая обструктивная болезнь легких и др.
При трепетании предсердий мышечные волокна предсердий возбуждаются и сокращаются также с большой частотой (около 300 уд./мин), но при этом обычно сохраняется правильный предсердный ритм.
Классификация
По состоянию АВ-проведения различают следующие формы трепетания предсердий:
-
Правильная форма - ритмичная, регулярная.
-
Неправильная форма.
В силу наличия эффективного рефрактерного периода АВ узла к желудочкам проводится обычно каждый второй (2:1) или каждый третий (3:1) предсердный импульс. Такая функциональная АВ-блокада, развивающаяся при трепетании предсердий, предотвращает слишком частую и неэффективную работу желудочков. Например, если частота регулярных возбуждений предсердий составляет 300 уд./мин, то при соотношении 2:1 ритм желудочков — только 150 уд./мин.
Если степень замедления АВ-проводимости постоянна, на ЭКГ регистрируется правильный желудочковый ритм, характеризующийся одинаковыми интервалами R-R (правильная форма).
Если наблюдается скачкообразное изменение степени АВ-блокады и к желудочкам проводится то каждый второй, то лишь третий или четвертый предсердный импульс, на ЭКГ регистрируется неправильный желудочковый ритм (неправильная форма).
Симптомы исходно зависят от частоты желудочковых сокращений и природы лежащего в основе заболевания сердца. При желудочковом регулярном ритме <120 уд/мин симптомов может быть мало или не быть совсем. Более быстрая частота и меняющееся АВ-проведение обычно обусловливают сердцебиение и снижение сердечного выброса, которое может вызывать нарушение гемодинамики (например, дискомфорт в грудной клетке, одышку, слабость, обмороки). При подробном обследовании яремного венозного пульса обнаруживаются a волны трепетания.
