
- •1.Органикалық қосылыстардың жіктелуі.
- •1.Массаалмасу аппараттары. Насадкалы ректификациялық колонна және оның негізгі элементтері. Насадкалардың түрлері.
- •1.Парафиндер. Жалпы сипаттамасы. Төменгі және жоғарғы парафиндер. Төменгі парафиндердің бөліну технологиясы.
- •1.Мұнайды ұңғылар басында тасымалдауға және өңдеуге дайындау. Мұнайларды сусыздандыру және тұзсыздандыру процестерінің теориялық негіздері мен технологиясы.
- •2.Алкандар. Изомерлері. Номенклатурасы. Физикалық қасиеттері.
- •Изомерлері
- •2.Массаалмасу аппараттары. Клапанды табақшалы ректификациялық колонна және оның негізгі элементтері, жұмыс істеу принципі.
- •2.Олефиндердің жалпы сипаттамасы. Төменгі және жоғарғы олефиндер. Көмірсутегі атомдары бірдей олефиндермен парафиндердің айырмашылықтары.
- •2.Мұнай эмульсияларының түрі мен оларды ыдырату әдістері.
- •3.Алкендер. Изомерлері. Номенклатурасы. Алыну тәсілдері.
- •Изомерлері
- •3.Массаалмасу аппараттары. Қалпақшалы табақты ректификациялық колонна және оның негізгі элементтері, жұмыс істеу принципі.
- •3 Парафиндерді изомерлеу процесінің маңызы және жалпы сипаттамасы. Процестің катализаторлары мен температурасы.
- •3 Мұнай және мұнайөнімдерінің физико-химиялық қасиеттері (Мұнай мен мұнайөнімдерінің компонентік құрамдарын, қаныққан буларының қысымдарын, критикалық параметрлерін анықтау.)
- •4 Алкандардың химиялық қасиеттері.
- •Нитрлеу реакциясы.
- •Тотығу реакциясы.
- •Крекинг реакциясы.
- •4.Массаалмасу аппараттары. Қалпақсыз табақты ректификациялық колонна және оның негізгі элементтері, жұмыс істеу принципі.
- •4 Ароматты көмірсутектерді алудың басты әдістері. Пиролиз өнімдері - ароматты көмірсутектердің негізгі көзі.
- •4 Мұнай мен мұнайөнімдерінің жылулық қасиеттерін анықтау (энтальпия, жылусиымдылык, жану жылуы).
- •5 Алкиндер. Изомерлері. Номенклатурасы. Ацетилен алу. Алкиндердің химиялық қасиеттері.
- •5.Жылу аппараттары. Қапталған құбырлы (кожухтрубчатый) жылу алмастырғыш, олардың түрлері және жұмыс істеу принципі.
- •5 Жоғары парафиндер. Жоғары парафиндерді бөліп алу әдістері және технологиясы.
- •5 Мұнайды біріншілік өңдеудің негізгі өнеркәсіптік қондырғылары (мұнайды біріншілік өңдеудің комбинирленген қондырғысы – элоу-авт-екіншілік айдау).
- •6.Алкадиендер. Изопрен мен дивинилдің алыну жолдары. Диендердің физикалық және химиялық қасиеттері.
- •6.Ауамен салқындатқындатылатын жылуалмастырғыш. Конструкциялық ерекшеліктері және олардың қолданылу аймақтары.
- •6.Олефиндерді алудың технологиялық жолдары (термиялық, каталитикалық, парафиндерді дегидрлеу).
- •6.Мұнайды біріншілік өңдеу өнімдері.
- •7.Алкендердің химиялық қасиеттері.
- •7.«Құбыр ішіндегі құбыр» жылу алмастырғыштары. Конструкциялық ерекшеліктері және құбырларды бекіту түрлері. Оларды қолдану аймақтары.
- •7.Риформинг процесінің маңызы мен жалпы сипаттамасы.
- •7.Тауарлық мұнайөнімдерінің сипаттамасы. Отынның негізгі қасиеттері (бензиндердің, реактивті және дизелді отындардың).
- •8.Алифатты қатардың көмірсутектерінің галоген туындылары.
- •8.Псевдосұйытылған катализатор қабаты бар каталитикалық крекинг процесінің реакторы. Оның жұмыс істеу принципі және конструкциялық элементтері.
- •8 Ацетилен алу процесінің жалпы сипаттамасы. Ацетиленді кальций карбидінен алу.
- •9. Біратомды қаныққан спирттер. Изомерлері, номенклатурасы. Біріншілік, екіншілік, және үшіншілік спирттер туралы түсінік. Алынуы. Физикалық қасиеттері.
- •9.Псевдосұйытылған катализатор қабаты бар каталитикалық крекинг процесінің регенераторы. Оның жұмыс істеу принципі және конструкциялық элементтері.
- •9. Ацетилен алу процесінің жалпы сипаттамасы. Пиролиз газдарының құрамы және оларды бөлу әдістері.
- •9. Көмірсутекті шикізаттарды екіншілік өңдеу процесстері. Олардың жіктелуі. Термиялық деструктивті процесстер.
- •10.Алифатты қатары спирттерінің химиялық қасиеттері. Біріншілік, екіншілік, және үшіншілік спирттердің химиялық ерекшеліктері..
- •10.Циркуляциялық қабатты катализаторы бар каталитикалық крекинг реакторы. Оның жұмыс істеу принципі және конструкциялық элементтері.
- •10.Синтез-газ алу процесінің жалпы сипаттамасы. Көмірсутектердің каталитикалық конверциясы.
- •10.Көмірсутекті шикізатты байытудың каталитикалық гидрогендеу процесінің технологиясы.
- •4. Дизельдік отынды гидротазалаудың принципті технологиялық кескіні
- •11.Алифатты қатардың альдегидтері мен кетондары.
- •11.Циркуляциялық қабатты катализаторы бар каталитикалық крекинг регенераторы. Оның жұмыс істеу принципі және конструкциялық элементтері.
- •11.Көмірсутектерді каталитикалық конверциялау арқылы синтез- газ алу. Катализаторлары, процестің температурасы, оларға қойылатын талаптар.
- •11.Каталитикалық крекинг процесінің технологиясы мен теориялық негіздері.
- •12.Алифатты қатардың альдегидтері мен кетондарының химиялық қасиеттері.
- •12.Каталитикалық риформинг қондырғысының реакторы. Оның қолданылу аймақтары және конструкциялық элементтері.
- •12.Тотығу процесінің маңызы және жалпы сипаттамасы. Тотығудың қазіргі органикалық синтездегі алатын орны.
- •12.Каталитикалық риформинг процесінің технологиясы мен теориялық негіздері.
- •13.Бірнегізді қаныққан карбон қышкылдары. Изомерлері. Номенклатурасы. Қышқылдарды алу тәсілдері, физикалық және химиялық қасиеттері.
- •13.Дизель отынын гидротазалау реакторы. Оның жұмыс істеу принципі және конструкциялық элементтері.
- •13.Хлорлау процесінің маңызы және жалпы сипаттамасы.
- •13.Бутан-бутилен фракциясының каталитикалық алкилдеу процесінің технологиясы.
- •14.Бірнегізді қанықпаған карбон қышкылдары және олардың туындылары Химиялық қасиеттері және қолданылуы.
- •14.Құбырлы пештердегі отынды жағуға арналған форсункалар. Олардың құрылысы және жұмыс істеу принциптері.
- •14.Сұйық фазалы хлорлау технологиясы, процестің жағдайлары және реакторлардың түрлері.
- •14.Пентан-гександы фракциясының каталитикалық изомерлену процесінің технологиясы.
- •15.Алифатты қатардың нитроқосылыстары. Изомерлері, номенклатурасы, алыну тәсілдері, физикалық және химиялық қасиеттері.
- •Изомерлері мен аталуы.
- •Алу әдістері.
- •Химиялық қасиеттері.
- •15.Жалынсыз құбырлы пештер. Қабырға панелінің конструкциялық ерекшелігі. Пештің конструкциялық элементтері.
- •15.Радикалды – тізбекті тотығу процесінің жалпы сипаттамасы. Тотығу өнімдері.
- •15.Каталитикалық гидрокрекинг процесінің технологиясы.
- •16.Алифатты қатардың аминдері. Изомерлері, номенклатурасы. Алифатты аминдердің алыну тәсілдері, физикалық және химиялық қасиеттері.
- •Алыну жолдары.
- •16.Күкіртқышқылымен алкилдеу қондырғысының жазықты және тік түріндегі контакторлары. Олардың жұмыс істеу принципі және конструкциялық элементтері.
- •16.Гидроформилдеу процесінің маңызы және жалпы сипаттамасы. 263(520)
- •16.Тығыздығы жоғары полиэтилен өндірісі.
- •Изомерлері. Бір негізді оксиқышқылдардың гомологтық қатары оксиқұмырсқа немесе көмір қышқылынан басталады. Одан
- •Алу әдістері.
- •Физикалық қасиеттері.
- •Химиялық қасиеттері.
- •17.Құбырлы пештер. Олардың жіктелуі және қолдану аймақтары. Екі камералы, екі жағы да құламалы (двухскатные) пештер.
- •17.Сұйық фазалы хлорлаудың технологиялық сатылары.
- •17.Тығыздығы орташа полиэтилен өндірісі.
- •18.Көпатомды спирттер. Физикалық және химиялық қасиеттері.
- •18.Құбырлы пештер. Тік құрылымды құбырлы пеш. Пештердің негізгі элементтері мен гарнитурасы.
- •18.Тотығу реакциялары және олардың жіктелуі (көмірсутек тізбегі үзілмей тотығу, деструктивті тотығу, тотығу конденсациясы, толық тотығу).
- •18.Тығыздығы төмен полиэтилен өндірісі.
- •19.Көмірсулар. Жіктелуі. Моносахаридтердің физикалық және химиялық қасиеттері.
- •Моноқанттарды алу әдістері.
- •Физикалық қасиеттері.
- •Химиялық қасиеттері.
- •19.Массаалмасу процестеріндегі абсорберлер мен десорберлер. Олардың жұмыс істеу принципі және конструкциялық элементтері.
- •19.Тотығу процесінің тотықтырғыш агенттері, оларға қойылатын талаптар, активтілігі және селективтілігі.
- •19.Полистирол алу технологиясы. Полимер қасиетіне технологиялық процесс параметрлерінің әсері.
- •20.Циклоалкандар. Изомерлері. Алыну тәсілдері, физикалық және химиялық қасиеттері.
- •20.Экстракторлар. Негізгі конструкциялық элементтері.
- •20.Өндірістік оксосинтез процесінің технологиясы.
- •20.Полиизобутилен. Технологиясының ерекшеліктері.
- •21.Алифатты қатардың амин қышқылдары. Номенклатурасы. Физикалық және химиялық қасиеттері.
- •21.Химиялық процестердің негізгі реакторлары. Адиабаттық реакторлар, Олардың жұмыс істеу принципі және конструкциялық ерекшеліктері.
- •21.Бензолды алкилдеу процесінің технологиялық сызбанұсқасы және жағдайлары.
- •21.Поливинилхлорид өндірісінің процесін технологиялық жабдықтау мен қондырғылары. Пвх негізіндегі пластмассалар
- •22.Ароматтық көмірсутектер. Бензолдың гомологтық қатары. Изомерлері мен номенклатурасы. Алыну тәсілдері, физикалық және химиялық қасиеттері.
- •22.Химиялық процестердің негізгі реакторлары. Құбырлы реакторлар. Олардың құрылысынң негізгі конструкциялық элементтері.
- •22.Олефиндердің тура гидратациясы, этанол өндірісі.
- •22.Стиролдың сополимерлері. Акрилонитрилдің, бутадиеннің және стиролдың үшкомпонентті сополимерлері.
- •23.Бензолды ядросындағы орынбасу ережелері. I және II текті орынбасарлар.
- •23.Полимерлеу процестерге арналған реакциялық аппараттар. Араластырғышы бар реакциялық қазандар. Олардың негізгі бөлшектері.
- •23.Алкилдеу процесінің сипаттамалары. Алкилдеуші агенттер және катализаторлар.
- •23.Поликонденсация реакциясының жалпы ерекшеліктері. Поликонденсация процесінің сипаттамасы.
- •24.Ароматты көмірсутектердің галоген- және сульфотуындылары. Алыну тәсілдері, химиялық қасиеттері және қолданылуы.
- •24.Жылуалмастырғыш аппаратары. Қатаң бекітілген қапталған құбырлы жылуалмастырғыш. Оның негізгі болшектері жұмыс істеу принциптері.
- •24.Винилдеу процесінің сипаттамасы, ацетиленнен және сірке қышқылынан винилацетат алу.
- •24.Фенол-альдегидті полимерлер. Новолакты және резолды олигомерлер мен полимерлердің түзілу механизмі.
- •25.Фенолдар мен ароматты спирттер. Изомериясы және номенклатурасы. Алыну тәсілдері, физикалық және химиялық қасиеттері.
- •25.Полимерлеу процестеріндегі «идеалды ығыстыру» аппараттары. Колонна түрдегі және құбырлы реакторлардың конструкциялық ерекшеліктері.
- •25.Сульфирлеу процесінің сипаттамасы. Ароматты қосылыстарды сульфирлеу процесінің технологиясы мен талаптары, химизмі.
- •25.Новолакты фенол-формальдегидті шайыр өндірісі процесінің кескіні (үздіксіз әдіс).
- •26.Ароматты нитроқосылыстар. Изомериясы және номенклатурасы. Алыну тәсілдері, физикалық және химиялық қасиеттері.
- •26.Жылуалмастырғыш аппаратары. Негізгі органикалық синтездегі тоңазытқыштар мен конденсаторлар. Олардың негізгі конструкциялық элементтері.
- •26.Новолакты фенол-формальдегидті шайыр өндірісі процесінің кескіні (үздікті әдіс).
- •27.Ароматты аминдер. Изомериясы және номенклатурасы. Алыну тәсілдері, физикалық және химиялық қасиеттері.
- •27.Жылуалмастырғыш аппаратары. Булы кеңістікті қыздырғыштар. Қолданылу аймақтары, негізгі конструкциялық элементтері.
- •27.Изобутиленді формальдегидпен конденсациялау арқылы изопрен өндіру. Конденсация процесінің температурасы, қысымы және катализаторлары.
- •27.Полигексаметиленадипамид өндірісінің процесінің технологиялық кескіні.
- •28.Гетероциклды қосылыстар. Бес- және алты мүшелі гетероциклды қосылыстар. Алынуы, химиялық қасиеттері, оргсинтезде қолданылуы.
- •28.Мұнайхимиялық өндірістегі кристализаторлар. Олардың жұмыс істеу принципі және конструкциялық элементтері.
- •28.Стирол өндірісінің шикізаттары мен өнеркәсіптік әдістері.
- •28.Термопластарды өңдеу. Термопластар өңдеудің әдістерін жіктеу.
- •29.Конденсирленген және конденсирленбеген ароматтық қосылыстар. Алынуы. Химиялық қасиеттері.
- •29.Қапталған құбырлы (кожухтрубчатый) жылу алмастырғыш. Құбыры u- тәрізді жылуалмастырғыш, оның жұмыс істеу принципі.
- •29.Этилбензолды дегидрлеу арқылы стирол өндіру. Дегидрлеу процесінің температурасы, қысымы және катализаторлары.
- •29.Қысыммен құю. Процестің негізгі заңдылықтары.
- •30.Диазо- және азоқосылыстар. Диазоттау реакциясы. Азоқосылыстар дың химиялық қасиеттері. Азотты бөле және бөлмей жүретін химиялық реакциялар.
- •30.Қатты отындардың шығу тегі және олардың жалпы сипаттамасы.
- •30.Эластомерлер өңделуі. Техникалық каучук пен резиналы қоспалардың ингредиенттері.
9. Көмірсутекті шикізаттарды екіншілік өңдеу процесстері. Олардың жіктелуі. Термиялық деструктивті процесстер.
Заманауи мұнайөңдеуде термиялық процестердің келесі типтері қолданылады:
Термиялық крекинг – қайнауы жоғары мұнай шикізатын жоғары температура әсерінен газтәрізді және сұйық өнімге айналдыру. Қазіргі кезде термиялық крекингті сажа алу үшін шикізат – термогазойль өндірісі мен кокстену қондырғысы үшін шикізаттың дистилятты түрін термодайындау процесі ретінде қолдану артықшылығы бар. Ауыр мұнай қалдықтары үшін висбрекинг процесінің өнеркәсіптік маңызы зор. Висбрекинг – бұл жеңіл крекинг, оның термолиз тереңдігі шектеулі, төмен температура мен қысымда (1,5-3МПа) котелдік отын тұтқырлығын төмендету мақсатында.
Кокстену – жоғары емес қысымда және 470-540°С температурада ауыр қалдықтардың ұзақ термолиз процесі. Кокстенудің мақсатты белгіленуі – өңделетін шикізат сапасынан тәуелді әртүрлі өлшемді мұнай кокстерінің өндірісі. Қосымша өнімдер – құндылығы төмен газ, сапасы төмен бензин мен газойль.
Пиролиз – көмірсутек шикізатының жоғарытемпературалық (750-800°С) термолизі, төмен қысымда жүргізіледі және тек жеңіл өнеркәсіпте. Мақсаты белгіленуі - олефинқұрамды газдар өндірісі. Қосымша өнім – қанықпаған көмірсутектердің құрамы үлкен фракциялық құрамы кең жоғарыароматтанған сұйық.
Пектену (мұнай пектері – байланыстырушы, сіңдіруші, талшықтүзуші және т.б.) – мұнай пектерін алу процесі төмен қысымда, қалыпты температурада (360-420°С) және ұзақ мерзімде жүргізіледі. Қосымша өнімдер – газдар мен керосинді-газойльді фракциялар.
Мұнай битумдарын алу процесі – атмсофералық қысымда және 250-300°С температурада жүргізілген ауыр қылдықтардың (гудронов, асфальтитов) тотыға дегидроконденсациялануының (карбонизации) ұзаққа созылған процесі.
6- билет
10.Алифатты қатары спирттерінің химиялық қасиеттері. Біріншілік, екіншілік, және үшіншілік спирттердің химиялық ерекшеліктері..
Химиялық қасиеттері.Спирттердің химиялық қасиеттерін құрамындағы гидроксил тобы анықтайды. Бұлар өте активті химиялық заттар. Себебі көміртек - оттек - сутек байланысы химиялық реакцияның пәрменділігіне /С-О-Н/ қарай әр жерден үзіліп, реакцияға түсуі мүмкін.
А) Гидроксил тобының тек сутегі атомының қатысуымен жүретін реакциялар.
Б) Гидроксил тобының толық қатысуымен жүретін реакциялар
В) Гидроксил тобы және сол топтағы сутегі атомы мен бірге көміртегі атомының қатысуымен жүретін тотығу реакциялары.
А. Гидроксил тобындағы сутегі атомының қатысуымен жүретін реакциялар.
1. Сілтілік металдармен әрекеттесу реакциясы
2ROH+2Na→2R-ONa+H2
спирт алкоголят
немесе
2CH3OH+2Na→2CH3Na+H2
натрий алкоголяты
Су ерітіндісі үстіне Na салғанда оның қаншалықты жылдам қозғалып еритіндігін білеміз. Бірақ спирттермен Na суға қарағанда аз жылдамдықпен реакцияға түседі. Және де спирт құрамындағы радикалдар саны артқан сайын, бұл реакция жылдамдығы онан әрі төмендей түседі. Бұл реакцияда спирттер аздап та болса қышқылдық қасиет көрсетеді.
2. Спирттер мен органикалық қышқылдар қосылып күрделі эфирлер түзеді.
CH3OH+OH-OC-CH3←→CH3 –CO-OCH3+H2O
сірке қышқылының метил эфирі
Бұлреакцияэфирленуреакциясыдепаталады. Бұлқайтымдыреакция, себебіпайда болған күрделі эфирсудаыдырапқайтаданқышқылменспирттібереді. Мұндайреакцияныгидролизреакциясыдепатайды.
Солсияқтыспирттерминералдықышқылдармендеәрекеттесіпкүрделіэфирлертүзеді.
Мысалы, этилспиртіменазотқышқылыныңарасындағыреакцияныжазыпкөрейік.
CH3CH2OH+HONO2→CH3CH2-ONO2+HOH
азот қышқылының этил эфирі(этилнитрат)
Б. Гидроксил тобы арқылы жүретін реакциялар:
1. Спирттерге галогентуындыларының әсері
CH3 – CH2 – OH + PCI5→CH3 – CH2 – CI + POCI3 + HCI
Бұл реакцияда қайтымды реакцияға қатарына жатады. Күкірт қышқылын катализатор есебінде қолдану арқылы реакция тепе-теңдігін оңға қарай жылжытуға болады.
2. Спиртті күкірт қышқылы мен немесе хлорлы мырышпен Al2O3 алюминий тотығының қатысында қыздырғанда 3500-5000 сусызданады.
Мысалы:
CH3 – CH2 –OH + AI2O3+ H2SO4→CH2 = CH2+ H2O
Зайцев ережесі бойынша үшіншілік спирт, екіншілік немесе біріншілік спирттерге қарағанда оңай сусызданады.
![]()
екіншілік ацетон
пропилспирті
![]() +3О→
+3О→ +НОН?
+НОН?
үшіншілік спирт ацетонқышқыл
Үшіншілік спирт көміртегінде сутегі болмағандықтан олар екіншілік және біріншілік спирттерге қарағанда қиын тотығады.
В. Тотығу реакциясы
Біріншілік, екіншілік және үшіншілік спирттер тотыққанда әр түрлі заттар түзіледі. Мысалы, біріншілік спирттер тотыққанда, әруақытта альдегидтер пайда болады.

біріншілік альдегид
спирт
![]()
Этил спирті сірке альдегиді
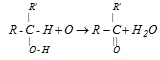
екіншілік кетон
спирт
