
Современные проблемы и методы биотехнологии
.pdf
ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
Потенциалы ионизации лежат в пределах 3,98 эВ (Fr)− 24,58 эВ (Не), для большинства органических соединений – 7–11 эВ. Используя моноэнергетические пучки электронов и снижая их энергию до пороговых значений, можно определять потенциалы ионизации вещества и потенциалы появления ионов − критическую энергию электронов, при которой в спектре появляются линии соответствующих осколочных ионов. При ионизации электронным ударом происходит перераспределение энергии возбуждения по колебательным степеням свободы иона, прежде чем этот ион распадается. Предположение о квазиравновесном распределении энергии возбуждения позволяет полуэмпирическим путем рассчитать масс-спектры некоторых веществ, согласующиеся с экспериментальными данными. Однако во многих случаях, особенно для длинных молекул, эта теория не подтверждается.
Для двухатомных молекул изменения колебательного состояний объясняют, исходя из принципа Франка− Кондона. При взаимодействии низкоэнергетических электронов (менее 10 эВ) с веществом могут осуществляться процессы резонансного захвата электронов молекулами с образованием отрицательно заряженных ионов. Масс-спектр электронного удара− высок о- чувствительный метод анализа, он позволяет анализировать пикомольные количества вещества, его предпочитают использовать для исследования структуры соединений. Существуют «библиотеки» масс-спектров, содержащие спектры более 350 000 органических соединений, по которым можно проводить их идентификацию с применением ЭВМ. Недостатки метода: молекулярные ионы образуются лишь у 20 % органических соединений; метод применим только для определения легколетучих термически стабильных соединений; в значениях полного ионного тока на ионы с большими значениями m/z, дающими информацию о молекулярной массе и наличии функциональных групп, приходится меньшая часть; отрицательно заряженные ионы, имеющие большое значение в структурном анализе, образуются в очень небольшом количестве и в ограниченном числе органических соединений.
Для решения части проблем применяют метод химической ионизации, которая осуществляется при столкновении молекул исследуемого вещества с ионами реагентного газа, в качестве которого используются индивидуальные вещества или их смеси. Реагентный газ находится в источнике под давлением 65–130 Па, парциальное давление исследуемого вещества – 0,1–0,01 Па. При бомбардировке такой смеси электронами с энергией 70–500 эВ преимущественно ионизируются молекулы реагентного газа. Образовавшиеся положительно заряженные ионы в результате ионно-молекулярных столкновений с неионизированными молекулами реагентного газа преобразуются в реактантные ионы, которые, в свою очередь, взаимодействуют с молекулами исследуемого вещества и ионизируют их, образуя ионы МН+. Наиболее используемые реагентные газы и их характеристики приведены в табл. 6.3. Химическая ионизация с образованием положительно заряженных ионов может осуществляться также в результате переноса заряда с реактантных ионов, например, Не+' , Ar+' , N2+', СО+', NO+' на молекулы исследуемого вещества; при этом образуется молекулярный ион М+. Масс-спектры химической иониза-
Современные проблемы и методы биотехнологии. Учеб. пособие |
331 |

ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
ции с реагентными газами Ar и N2 напоминают спектры электронного удара. Метод химической ионизации позволяет оценивать кислотно-основные свойства органических соединений в газовой фазе. Химическая ионизация с образованием отрицательно заряженных ионов осуществляется в результате взаимодействия исследуемых молекул с ионами NH2-, OH-, CH3O-(сродство к протону, соответственно, 1682, 816 и 778 кДж/моль).
Таблица 6.3
Реагентные газы и их характеристики
Газ-реагент |
Сродство к протону, |
Реактивный ион |
Ион исследуемого |
|
кДж/моль |
вещества |
|||
|
|
|||
СН4 |
536 |
CH5+ |
MH+ |
|
Н2О |
724 |
H3O+ |
MH+, MH3O+ |
|
(СН3)3СН |
828 |
(СН3)3С+ |
MH+ |
|
NH3 |
858 |
NH4+ |
MH+, MNH4+ |
Последние образуются при захвате молекулами NH3, H2O и СН 3ОН электронов с пониженной энергией (около 6 эВ) с последующим распадом образовавшихся молекулярных ионов М- (диссоциативный захват). Ионы OH-, CH3O- образуются в значительном количестве при электронной бомбардировке смесей N2O с СН4 или (СН3)3СН, Н2О и N2O с СН3ОН. Часто метод химической ионизации более чувствительный, чем метод ионизации электронным ударом, т. к. практически все имеющиеся в ионизационной камере электроны используются для ионизации. Метод позволяет анализировать пространственные и оптические изомеры. Его важное достоинство – большой выход протонированных молекулярных ионов МН+ при малом выходе осколочных ионов.
Другим методом мягкой ионизации является полевая десорбция. Полевая десорбция – это образование ионов в сильном электростатическом поле (108 В/см) за счет квантово-механического туннельного эффекта. Полевая десорбция может происходить при низких температурах эмиттера и не сопровождаться диссоциацией. В результате образуются в основном молекулярные и квазимолекулярные ионы. Так, например, в масс-спектре электронного удара ацетилсалициловой кислоты преобладают продукты диссоциативной ионизации с m/z, равным 140 и 120, а в масс -спектре полевой десорбции есть только два пика: молекулярный с М = 180 и квазимолекулярный с М = 181, образованный путем присоединения протона к молекуле ацетилсалициловой кислоты. Однако несмотря на определенные успехи, этот метод не получил достаточно широкого применения в связи с его избирательностью.
Далеко не все молекулы отдают поверхности электрон при низких температурах. Для ионизации труднолетучих соединений в масс-спектрометрии применяются искровая и лазерная ионизация вещества. Ионизации подверга-
Современные проблемы и методы биотехнологии. Учеб. пособие |
332 |

ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
ется твердое вещество. В искровом источнике испарение и ионизация исследуемого вещества происходят за счет искрового разряда, зажигающегося между электродами при разности потенциалов между ними от 3 до 5 кВ. На одном из электродов находится сам образец. Лазерная ионизация производится путем импульсного лазерного нагрева твердого вещества, и образующийся плазменный пучок направляется в масс-анализатор. В этих условиях происходит полное разрушение химических соединений, и в масс -спектре фиксируются лишь атомные ионы и определяется элементный состав образца. Похожие результаты можно получить, производя испарение и ионизацию твердого вещества ионами или нейтральными атомами с энергией в несколько киловольт. Эти методы широко применяются для элементного анализа.
Масс-анализаторы – устройства для пространственного или временного разделения ионов с различными значениями m/z в магнитном или электрических полях или их комбинациях. Различают статические и динамические анализаторы. В статических ионы разделяются в постоянных или практически не изменяющихся за время их движения через анализатор магнитных полях. Ионы с различным значениями m/z движутся в таком анализаторе по разным траекториям и фокусируются последовательно на щель детектора в результате плавного изменения напряженности электрического и магнитного полей анализатора. В динамических анализаторах разделение ионов происходит под воздействием импульсных или радиочастотных электрических полей с периодом изменения, меньшим или равным времени пролета ионов через масс-анализатор. Ионы с различным значениями m/z, как правило, разделяются по времени пролета определенного расстояния. Давление в анализаторах должно быть достаточно низким (~10-5Па), чтобы избежать рассеяния ионов на молекулах остаточных газов.
Основные характеристика масс-анализатора – его разрешающая способность, или разрешающая сила R. Она характеризует способность анализатора разделять ионы с незначительно отличающимися друг от друга массами и определяется отношением значения массы иона М к ширине его пика ∆М (выраженной в атомных единицах массы) на определенном уровне высоты пика (обычно 50 или 10 %): R = М/∆М. Например, R = 10 000 означает, что масс-анализатор может разделять ионы с массами 100,00 и 100,01. Наиболее часто применяют статистические масс-анализаторы с однородным магнитным полем (одинарная фокусировка) или комбинацией электрических и магнитных полей (двойная фокусировка). В масс-анализаторах с одинарной фокусировкой ионный луч, сформированный в источнике ионов, выходит из щели шириной S1 в виде расходящегося ионного пучка и в магнитном поле разделяется на пучки ионов с различным значениями m/z.
Под действием поля, силовые линии которых направлены перпендикулярно направлению движения ионного пучка, ионы двигаются по круговой траектории с радиусом
r = (2Vmn/zH2)1/2,
Современные проблемы и методы биотехнологии. Учеб. пособие |
333 |

ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
где V – напряжение, ускоряющее ионы; mn – масса иона; z – заряд иона; H – напряженность магнитного поля.
Ионы с одинаковой кинетической энергией, но с разными массами или зарядами проходят через анализатор по различным траекториям. Обычно развертка масс-спектра (регистрация ионов с определенными значениями m/z) осуществляется изменением Н при постоянном V. Разброс ионов, вылетающих из ионного источника, по кинетическим энергиям, а также несовершенство фокусировки по направлениям приводят к уширению ионного пучка, что сказывается на разрешающей способности. Для статического массанализатора
R = r/(S1 + S2+ δ),
где S1 и S2 – соответственно, ширина входной и выходной щелей; δ – уширение пучка в плоскости выходной щели.
Уменьшение размера щелей для увеличения разрешающей способности прибора трудно осуществимо технически и, кроме того, приводит к очень малым ионным токам, поэтому обычно конструируют приборы с большим радиусом траектории ионов (r = 200–300 мм). Разрешающая способность может быть повышена также при использовании масс-анализаторов с двойной фокусировкой. В таких приборах ионный пучок пропускают сначала через отклоняющее электрическое поле специальной формы, в котором осуществляется фокусирование пучка по энергиям, а затем через магнитное поле, в котором ионы фокусируются по направлениям.
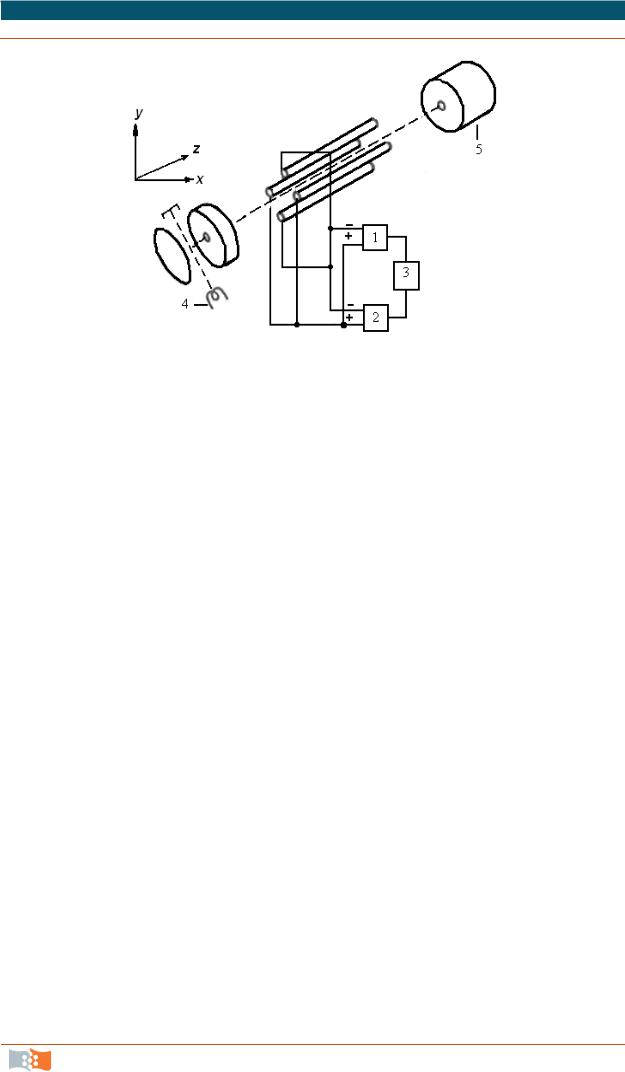
Существует более 10 типов динамических масс-анализаторов: квадрупольный, время-пролетный, циклотронно-резонансный, магнитно-резонансный, радиочастотный, фарвитрон, омегатрон и др. Наиболее широко применяемый масс-анализатор – квадрупольный. Этот масс-анализатор представляет собой квадрупольный конденсатор (рис. 6.16), к парам параллельных стержней которого приложены постоянное напряжение V и переменное высокочастотное
V0cos ωt (ω частота– ; t – время); их суммы для каждой пары равны по величине и противоположны по знаку.
Современные проблемы и методы биотехнологии. Учеб. пособие |
334 |
ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
Рис. 6.16. Схема квадрупольного масс-анализатора: 1 – высокочастотный генератор; 2 – генератор постоянного напряжения; 3 – генератор развертки; 4 и 5 – источник и детектор ионов
Ионы, вылетевшие из ионного источника, движутся в камере анализатора вдоль оси z, параллельной продольным осям стержней, по сложным объемным спиралевидным траекториям, совершая поперечные колебания вдоль осей x и у. При фиксированных значениях частоты и амплитуды переменного напряжения ионы с определенными значениями m/z проходят через квадрупольный конденсатор, у ионов с другими значениями m/z амплитуда поперечных колебаний достигает такой величины, что они ударяются о стержни и разряжаются на них. Развертка масс-спектра производится путем изменения постоянного и переменного напряжения или частоты. Для современных квадрупольных масс-спектрометров R = 8000. Первый квадрупольный прибор построен В. Паули и X. Штайнведелем (ФРГ, 1953).
Время-пролетный масс-анализатор представляет собой эквипотенциальное пространство, в котором дрейфуют ионы, разделяясь по скоростям движения. Ионы, образующиеся в ионном источнике, очень коротким электрическим импульсом «впрыскиваются» в виде «ионного пакета» через сетку в анализатор. В процессе движения исходный ионный пакет расслаивается на пакеты, состоящие из ионов с одинаковыми значениями m/z. Скорость дрейфа отслоившихся ионных пакетов и, следовательно, время их пролета через анализатор длиной L вычисляется по формуле
t = L |
, |
(6.32) |
где V – напряжение.
Совокупность таких пакетов, поступающих в детектор, образует массспектр. Для современных приборов R = 5 000–10 000. Первый прибор создан А. Камероном и Д. Эгтерсом (США, 1948), а в СССР – Н.И. Ионовым (1956).
Современные проблемы и методы биотехнологии. Учеб. пособие |
335 |

ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
Детекторы (приемники) ионов помещают на выходе прибора. Для детектирования используют электрометрические усилители, позволяющие измерять ионные токи до 10-14А, электронные умножители и сцинтилляционные детекторы с фотоумножителем, которые обеспечивают счет отдельных ионов (ток 10-19А) и имеют малую постоянную времени. Обработка данных на современных приборах идет на компьютере.
Применение масс-спектрометрии. Масс-спектрометрия широко при-
меняют в различных областях науки и техники. Большие успехи достигнуты при анализе биологически важных продуктов биотехнологии; показана возможность структурного анализа полисахаридов с молекулярной массой до
15000, белков – до 45 000 и т.д.
Большие принципиальные возможности масс-спектрометрии появляются при сочетании её с другими методами. Сочетание методов значительно расширяет возможности каждого из них, позволяя получать больше информации об объекте исследования. Созданы тандемные масс-спектрометры, позволяющие двукратное, трехкратное, четырехкратное и т.д. разделение по массам.
Хромато-масс-спектрометры – одни из наиболее распространенных современных аналитических приборов. В них различные типы газовых, жидкостных или ионных хроматографов (электрофореза) обеспечивают предварительное разделение вещества, а индикацию разделенных веществ и измерение их содержаний осуществляет масс-спектрометр. Поэтому массспектрометры в хромато-масс-спектрометрах большей частью имеют дело не со смесью соединений, а с индивидуальными соединениями.
Весьма плодотворным, но далеко не в полной мере реализованным,
оказалось совместное применение лазеров и масс-спектрометрии, которое может идти по двум – трем направлениям: применение лазеров в массспектрометрии, применение масс-спектрометрии для диагностики и изучения работы лазеров, масс-спектрометрический контроль работы установок по лазерному разделению изотопов.
Более распространенным и относительно простым является применение масс-спектрометрии в аналитических целях. Условия ионизации в этих слу-
чаях, как правило, либо остаются неизменными, либо контролируемым образом переключаются между несколькими значениями. Масс-спектрометрия как область аналитических измерений требует довольно сложных приборов, основательного методического и метрологического обеспечения. Она объединяет и согласует длинную цепочку объектов, методов и процессов: объект исследования; подготовку эталонов, поверочных смесей или образцов сравнения; метод отбора и подготовки проб; ионизацию вводимого вещества; разделение ионов по массам; их детектирование; обработку и представление полученной информации; её анализ и последующие выводы. Работы по осуществлению этой цепочки требуют использования разнообразных систем и узлов масс-спектрометров. Эти методы обладают хорошей наглядностью, большой универсальностью и информативностью, позволяют достигать высокой чувствительности, разрешающей способности и точности, что спо-
Современные проблемы и методы биотехнологии. Учеб. пособие |
336 |
ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
собствует их широкому распространению в различных отраслях науки и технологии.
Масс-спектрометрия в сочетании с газовой хроматографией активно используется в СФУ для решения ряда биотехнологических задач.
а
б
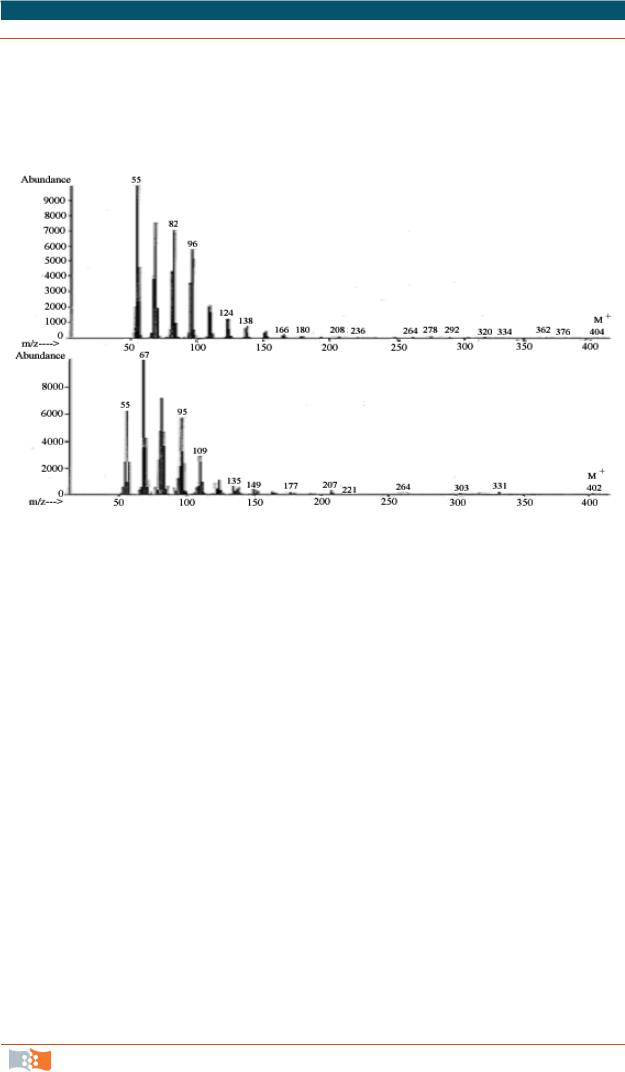
Рис. 6.17. Масс-спектры основных диеновых углеводородов изолята Botryococcus озера Шира: а – 29:2; б – 29:3 [3, 22]
Так, например, с помощью масс-спектрометрии были идентифицированы углеводороды двух представителей Botryococcus – музейного штамма и изолята озера Шира. На рис. 6.17 представлены масс-спектры основных углеводородов, выделенных из природного штамма Botryococcus braunii. На данных спектрах четко видны основные молекулярные ионы, характерные для доминирующих диенового и триеного углеводородов С29:2 и С29:3, а фрагментация молекул соответствует углеводородным цепям с двумя и тремя ненасыщенными связями.
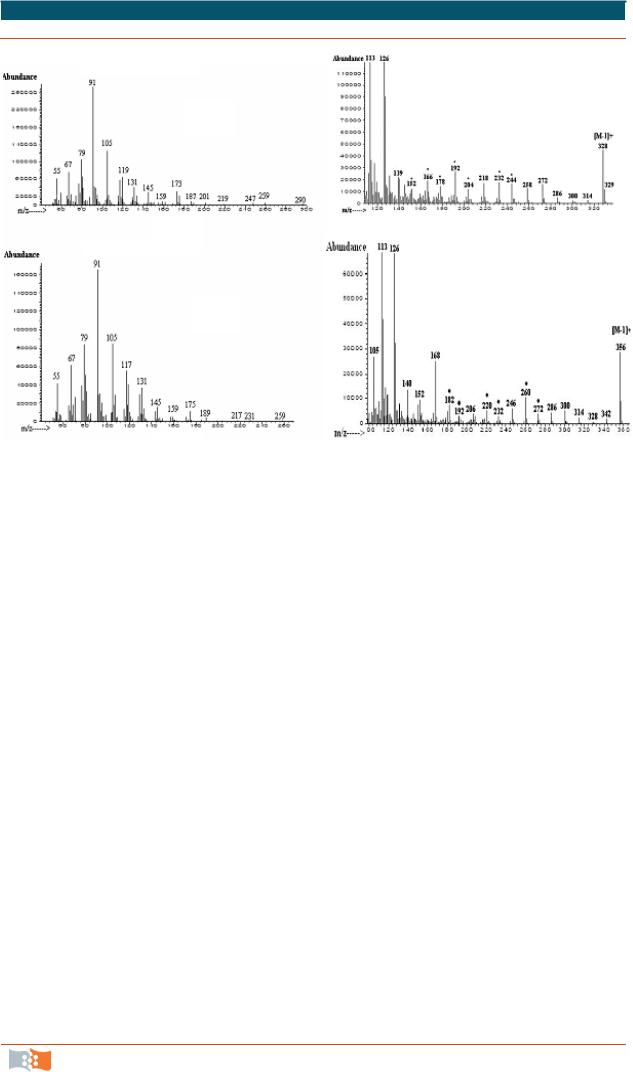
Идентификацию ацетиленовых кислот, синтезируемых водным мхом, проводили также по масс-спектрам. Но положение двойных и тройных связей в ненасыщенных кислотах определяли после получения диметилоксазолиновых производных фракции жирных кислот (ДМОК) и последующего хроматографирования их в тех же условиях, что и метиловые эфиры жирных кислот. На рис. 6.18 приведены масс-спектры метиловых эфиров двух ацетиленовых кислот и их ДМОК.
Современные проблемы и методы биотехнологии. Учеб. пособие |
337 |
ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
а |
в |
б |
г |
Рис. 6.18. Масс-спектры метиловых эфиров основных ацетиленовых кислот липидов
Fontinalis antipyretica: а – 6a, 9, 12–18:3 (А1); б – 8a, 11, 14–20:3 (А5) и их димети-
локсазолиновых производных: в – 6a, 9, 12–18:3 (А1); г – 8a, 11, 14–20:3 (А5). Точками отмечены диагностические фрагменты, молекулярный вес которых отличается на 10 или 12 ам [12]
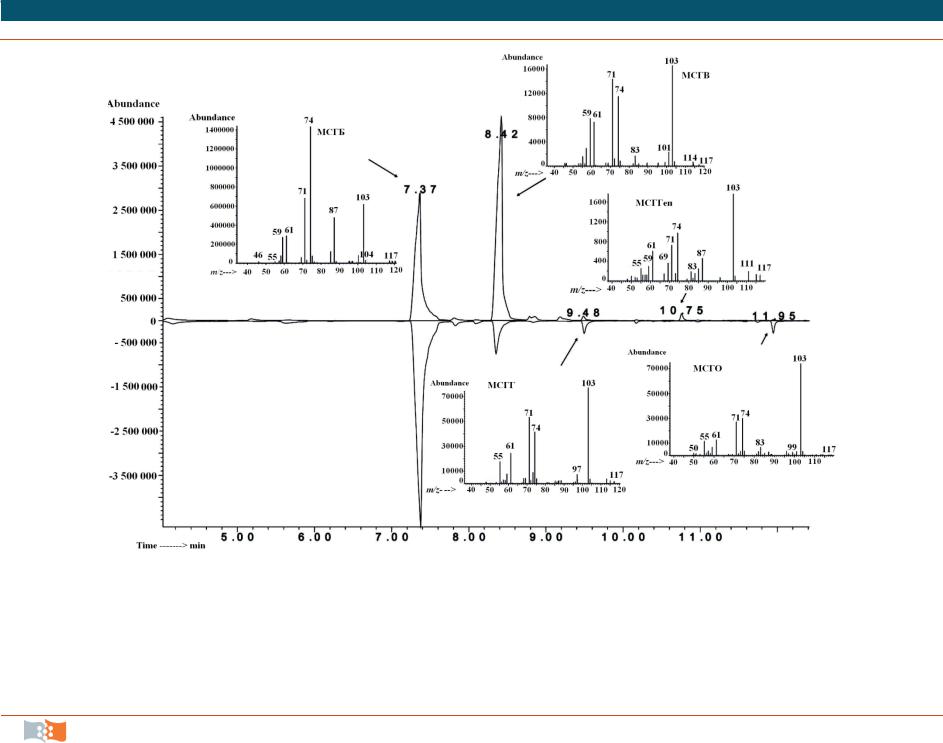
Совершенная масс-спектрометрическая техника позволяет изучать полимерные молекулы, синтезируемые бактериями – полигидроксиалканоаты. На рис. 6.19 приведены две ионные хроматограммы 4- и 5-компонентных полимеров и масс-спектры соответствующих мономеров, из которых состоят полимеры.
Современные проблемы и методы биотехнологии. Учеб. пособие |
338 |
ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
Рис. 6.19. Ионные хроматограммы полимеров, выделенных из биомассы Ralstonia eutrophа В5786 с добавкой гептаноата (верх) и добавкой октаноата (зеркально внизу) и масс-спектры соответствующих мономеров – ГБ – β- гидроксибутират с временем удерживания 7,37; ГВ – β-гидроксивалерат – 8,42; ГГ– β-гидроксигексаноат – 9,48;
ГГеп – β-гидроксигептаноат – 10,75; ГО – β-гидроксиоктаноат – 11,95 [5]
Современные проблемы и методы биотехнологии. Учеб. пособие |
339 |

ГЛАВА 6. СОВРЕМЕННЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЦЕЛЕВЫХ ПРОДУКТОВ
6.3. Масс-спектрометрия в биотехнологии
Масс-спектры β-гидрокси-кислот характеризуются наличием базового иона 103 m/z . Следовательно, все отмеченные на хроматограмме пики относятся кβ-гидроксикислотам, а их длина определена по их временам удерживания.
Фундаментальные физические законы, передовые научные и инженерные разработки, высокотехнологичные вакуумные системы, самые лучшие материалы, высочайшее качество их обработки, современнейшая быстродействующая цифровая и аналоговая электроника и компьютерная техника, а также программное обеспечение – основы современных массспектрометров.
Без масс-спектрометрии немыслим контроль над незаконным распространением наркотических и психотропных средств, криминалистический и клинический анализ токсичных препаратов, анализ взрывчатых веществ. С ее помощью стала возможным разработка новых лекарственных средств, контроль их производства. Она дала существенное продвижение в области генной инженерии, биохимии и протеомике.
Целый ряд техногенных (т.е. не существующих в природе, а появившихся в результате индустриальной деятельности человека) веществ являются супертоксикантами (имеющими отравляющее, канцерогенное или вредное для здоровья человека действие в предельно низких концентрациях). Примером является хорошо известный диоксин. Существование ядерной энергетики немыслимо без масс-спектрометрии. С ее помощью определяется степень обогащения расщепляющихся материалов и их чистота. Конечно, и медицина не обходится без масс-спектрометрии. Изотопная масс-спектрометрия углеродных атомов применяется для прямой медицинской диагностики инфицированности человека Helicobacter pylori и является самым надежным из всех методов диагностики.
Таким образом, масс-спектрометрия в настоящее время является одним из наиболее информативных, чувствительных и надежных аналитических методов. Любая крупная физическая, химическая или биологическая лаборатория имеет в своем распоряжении масс-спектрометр, ориентированный на те или иные специфические исследования. Совершенствование техники позволило создать приборы, способные исследовать молекулы с огромными массами порядка 100 000 а.е.м. и выше, что, несомненно, открывает просторы для изучения таких сложных биологических молекул, как белки и нуклеиновые кислоты. Масс-спектрометрия способна обнаруживать примеси на уровне 0,0001 % и ниже, что актуально при контроле синтеза высокочистых веществ, например в микроэлектронике и медицинской биотехнологии.
Современные проблемы и методы биотехнологии. Учеб. пособие |
340 |
