
- •Инфекционные болезни Учебник для медицинских вузов
- •Содержание
- •Предисловие
- •Список условных сокращений
- •Общая часть учение об инфекционных болезнях
- •Воздействие на возбудителя
- •Нежелательные эффекты взаимодействия антибактериальных препаратов и других лекарственных средств (по с. В. Яковлеву)
- •Бактериальные кишечные инфекции брюшной тиф
- •Паратифы а и в
- •Сальмонеллез
- •Пищевые токсикоинфекции
- •Дизентерия
- •Эшерихиозы
- •Отравления бактериальными токсинами ботулизм
- •Столбняк
- •Бактериальные кокковые инфекции ангина
- •Скарлатина
- •Менингококковая инфекция
- •Спирохетозы тиф возвратный вшивый
- •Лептоспироз
- •Боррелиозы клещевой лайм-боррелиоз
- •Клещевой возвратный тиф
- •Бактериальные зоонозы чума
- •Туляремия
- •Сибирская язва
- •Бруцеллез
- •Псевдотуберкулез
- •Кишечный иерсиниоз
- •Кампилобактериоз
- •Листериоз
- •Эризипелоид
- •Дифтерия
- •Легионеллезы
- •Риккетсиозы
- •Эпидемический сыпной тиф
- •Болезнь брилля-цинссера
- •Клещевой сыпной тиф северной азии
- •Эндемический (крысиный) сыпной тиф
- •Лихорадка цуцугамуши
- •Пятнистая лихорадка скалистых гор
- •Марсельская лихорадка
- •Клещевой пароксизмальный риккетсиоз
- •Осповидный риккетсиоз
- •Болезнь кошачьей царапины
- •Хламидиозы
- •Мочеполовой хламидиоз
- •Перинатальный хламидиоз
- •Венерическая лимфогранулема
- •Трахома
- •Пневмохламидиоз
- •Микоплазмозы
- •Вирусные болезни острые респираторные заболевания
- •Парагрипп
- •Аденовирусные заболевания
- •Острые респираторные заболевания (недифференцированные)
- •Энтеровирусные болезни
- •Ротавирусные гастроэнтериты и диареи
- •Другие вирусные гастроэнтериты и диареи
- •Вирусные гепатиты
- •Гепатит а (га)
- •Гепатит в (гв)
- •Гепатит с (гс)
- •Гепатит е (ге)
- •Микст-гепатиты
- •Геморрагические лихорадки
- •Геморрагическая лихорадка с почечным синдромом
- •Геморрагическая лихорадка крым-конго
- •Омская геморрагическая лихорадка
- •Желтая лихорадка
- •Лихорадка денге
- •Геморрагическая лихорадка ласса
- •Геморрагическая лихорадка марбург
- •Лихорадка эбола
- •Москитная лихорадка (лихорадка паппатачи)
- •Вирусные менингоэнцефалиты и энцефаломиелиты
- •Японский энцефалит
- •Клещевой энцефалит
- •Калифорнийский энцефалит
- •Лихорадка западного нила
- •Бешенство
- •Оспа натуральная
- •Краснуха
- •Эпидемический паротит
- •Герпетическая инфекция
- •Оспа ветряная
- •Инфекционный мононуклеоз
- •Паразитарные болезни малярия
- •Амебиаз
- •Лейшманиозы
- •Токсоплазмоз
- •Гельминтозы
- •Нематодозы аскаридоз
- •Энтеробиоз
- •Трихинеллез
- •Трематодозы описторхоз
- •Цестодозы дифиллоботриоз
- •Тениаринхоз
- •Тропические гельминтозы
- •Шистосомозы
Список условных сокращений
АГА — агрегатагглютинация;
АКТГ — адренокортикотропный гормон;
ВВК — военно-врачебная комиссия;
ВИЧ — вирус иммунодефицита человека;
ВИЭФ — реакция встречного иммуноэлектрофореза;
ВПИГ — военно-полевой инфекционный госпиталь;
ГБО — гипербарическая оксигенация;
ГЛПС — геморрагическая лихорадка с почечным синдромом;
ДВС — диссеминированное внутрисосудистое свертывание;
ДС — дегидратационный синдром;
ЖКТ — желудочно-кишечный тракт;
ИБ — иммунный блоттинг;
ИБЭСМП — инфекционная бригада экстренной специализированной медицинской помощи;
ИВЛ — искусственная вентиляция легких;
ИНФ — интерферон;
ИТ — интенсивная терапия;
ИТШ — инфекционно-токсический шок;
ИТЭ — инфекционно-токсическая энцефалопатия;
ИФА — иммуноферментный анализ;
КИЗ — кабинет инфекционных заболеваний;
КЛБ — клещевой Лайм-боррелиоз;
КОД — коллоидно-осмотическое давление;
КЭ — клещевой энцефалит;
ЛЗН — лихорадка Западного Нила;
МП — медицинский пункт;
МПК — минимальная подавляющая концентрация;
ОДН — острая дыхательная недостаточность;
ОИПЗИ — отделение инфекционно-паразитарных заболеваний
и профилактики;
ОМедБ — отдельный медицинский батальон;
ООИ — особо опасная инфекция;
ОПечН — острая печеночная недостаточность;
ОПН — острая почечная недостаточность;
ОПЭ — острая печеночная энцефалопатия;
ОРВИ — острая респираторная вирусная инфекция;
ОРЗ — острое респираторное заболевание;
ОРИТ — отделение реанимации и интенсивной терапии;
ОССН — острая сердечно-сосудистая недостаточность;
ПИТ (БИТ) — палата (блок) интенсивной терапии;
ПЦР — полимеразная цепная реакция;
РА — реакция агглютинации;
РАЛ — реакция агглютинации латекса;
РЗГА (РТГА) — реакция задержки (торможения) гемагглютинации;
РИА — радиоиммунный анализ;
РКА — реакция коагглютинации;
РИГА (РПГА) — реакция непрямой (пассивной) гемагглютинации;
РСК — реакция связывания комплемента;
СМЖ — спинномозговая жидкость;
СПК — санитарно-противоэпидемическая комиссия;
СПЭБ — специализированная противоэпидемическая бригада;
СТГ — соматотропный гормон;
ЦВД — центральное венозное давление;
ЦГ — церебральная гипертензия;
ЭД — экстракорпоральная детоксикация.
Общая часть учение об инфекционных болезнях
Инфекционные болезни возникли задолго до появления человека. На костях динозавров, мамонтов, пещерных медведей и других древних животных имеются следы остеомиелита. Из предков человека инфекционные поражения костей отмечены у питекантропов с острова Ява, живших 1—2 млн лет тому назад. Таким образом, человечество еще на заре своего существования встречалось с многочисленными инфекционными болезнями.
По мере возникновения общества и развития социального образа жизни человека многие инфекции получили широкое распространение. «Моровые заболевания» людей описаны еще врачами древности. Упоминания о поветриях, повальных, заразных болезнях можно отыскать в индийских ведах, иероглифическом письме Древнего Китая и Японии, в Библии и в русских летописях. Широко известен факт, что на лице мумифицированного фараона Рамзеса V, умершего три тысячи лет тому назад, были обнаружены рубцы от перенесенной натуральной оспы. Следы оспы изображены на глиняных человеческих фигурках, найденных в Мексике и изготовленных в 600-е гг. до н. э. Древние рукописи сообщают об эпидемиях оспы в Китае и Индии, где еще 2500 лет тому назад пытались проводить профилактику оспы путем прививок содержимого пузырьков от больного в кожу здоровых людей, которые переносили заболевание в более легкой форме.
Опустошительные эпидемии и пандемии различных инфекционных болезней были свойственны всем историческим периодам развития человечества. Первая достоверно документированная пандемия чумы наблюдалась в VI веке (527—565 гг.), так называемая «чума Юстиниана», поразившая ряд стран в районе Средиземного моря. В средние века от новой пандемии чумы, известной тогда под названием «черной смерти», вымерла треть населения Европы. В XIV веке от этого заболевания погибли более 50 млн человек. Эпидемии сыпного тифа были постоянными спутниками войн того времени, а потери погибшими от этой болезни превышали боевые.
Давно известны и другие инфекционные болезни. Так, малярия описана н древнеегипетских папирусах и индийской «Книге жизни» (750—700 гг. до п. э.). В сочинениях Гиппократа помимо малярии можно найти описания возвратного тифа, столбняка, рожи, эпидемического паротита, дизентерии, сибирской язвы (anthrax — дословный перевод —«уголь»). Бешенство было описано в V веке до н. э. (Демокрит, Ксенофонт). Четкое описание клиники холеры и опустошений, приносимых этим заболеванием, найдено в одном из древних документов храма Куржат в Западной Индии во времена нашествия войск Александра Македонского (327—326 гг. до н. э.).
Интересно, что еще Лукреций (99—55 гг. до н. э.) высказал предположение, что моровые болезни вызываются живыми болезнетворными семенами. Однако еще очень долго причины повальных болезней оставались неясны, строились различные догадки и предположения, иногда весьма близкие к истине. Например, лишь в 1784 г. русский ученый Самойлович (Данило Самойлович Сущинский), изучая причину распространения чумы, пришел к выводу, что болезнь вызывается «неким особливым и совсем отменным существом». На основании своих предположений он построил чрезвычайно действенную для того времени систему защитных мероприятий, проведение которых позволяло пресекать распространение эпидемий.
Постепенно врачи научились отличать отдельные инфекционные болезни. Особое значение имели труды таджикского ученого, врача и мыслителя Ибн Сины (Авиценны), родившегося в Бухаре в 980 г. Из пяти написанных им медицинских книг одна была целиком посвящена инфекциям. Он разграничивал чуму и холеру, оспу и корь. Однако еще долго врачи смешивали под одним названием различные болезни (например, «тиф», «горячка»). В дальнейшем из этого обобщенного понятия выделялись и описывались отдельные нозологические формы. Первое описание сыпного тифа было сделано итальянцем Фракасторо в XVI веке. Однако детальную характеристику клиники сыпного тифа дали русские врачи А. Шировский (1811) и Я. Говоров (1812), которые назвали его головным тифом (или нервной горячкой). Французские ученые Бретоно, Труссо, Луи в 1813—1826 гг. дали описание клиники и патологоанатомических особенностей брюшного тифа. Обстоятельное разграничение этих тифов (брюшного и сыпного) было сделано Мерчисоном (1862) и С. П. Боткиным (1867). Патологоанатомические изменения головного мозга, характерные для сыпного тифа, описал сотрудник Военно-медицинской академии Л. В. Попов (1875), а через год русский врач Осип Осипович Мочутковский героическим опытом самозаражения доказал, что возбудитель сыпного тифа циркулирует в крови больных. В историю мировой науки вошли и другие самоотверженные опыты по самозаражению русских врачей: Григорий Николаевич Минх — и 1874 г. и Илья Ильич Мечников — в 1881 г. привили себе кровь возвратно-тифозных больных в целях изучения этих болезней.
В XIX веке активно описываются все новые и новые нозологические формы инфекционных болезней: краснуха (Вагнер, 1834), бруцеллез (Мэрстон, 1861), орнитоз (Юргенсен, 1875), лихорадка паппатачи (Пик, 1886). В 1884 г. Нилом Филатовым под названием железистой лихорадки был описан инфекционный мононуклеоз. В 1888 г. ученик С. П. Боткина Н. П. Васильев подробно описал клинику тяжелых (желтушных) форм лептоспироза, за два года до него немецкий врач Вайль (1886) дал краткое описание лишь четырех случаев подобного заболевания. В честь этих ученых тяжелые формы лептоспироза называют болезнью Васильева—Вайля.
В изучение инфекционных болезней большой вклад внесли выдающиеся русские ученые С. П. Боткин, А. А. Остроумов, Г. А. Захарьин, Н. Ф. Филатов. Отечественные ученые нередко были пионерами в организации профилактической и лечебной работы во время эпидемий инфекционных болезней. Так, в 1830—1831 гг. для борьбы с холерой был создан специальный комитет во главе с М. Я. Мудровым (умер от холеры 8 июля 1831 г.). Материалы изучения холеры были опубликованы в «Трактате о повально-заразной болезни — холере, бывшей в России в 1830 и 1831 годах», который использовался во многих странах. В борьбе с холерой, возникшей в Петербурге в 1848 г., активное участие принимал известный хирург Н. И. Пирогов, который за 1,5 месяца вскрыл более 400 трупов людей, погибших от холеры, дал детальное описание патологоанатомических изменений, создал атлас с пояснительными записками.
Таким образом, клиницисты дали подробное описание инфекционных болезней, изучили патологоанатомические изменения, свойственные той или иной болезни, доказали контагиозность инфекционных заболеваний и разработали ряд профилактических рекомендаций. В ряду последних следует назвать предложенную в 1876 г. английским врачом Дженнером эффективную профилактику натуральной оспы путем прививки коровьей оспы (вакцины). Однако отсутствие знаний о возбудителях не позволяло решить многих вопросов диагностики, лечения и профилактики.
Новый толчок к развитию учения об инфекционных болезнях дало открытие и изучение их возбудителей, вначале микробов (Л. Пастер), а затем и вирусов (Д. И. Ивановский). Луи Пастер провел серию блестящих исследований, он открыл ряд возбудителей гнойных и септических заболеваний, разработал метод аттенуации (ослабления) микроорганизмов, предложил называть ослабленные культуры возбудителя вакцинами. Пастер создал вакцину против сибирской язвы, бешенства, причем последняя была получена им без выделения культуры возбудителя (использовался мозг инфицированных животных). Учреждения, в которых проводились прививки против бешенства, с тех пор называются пастеровскими станциями.
Большое значение имели работы немецкого ученого Роберта Коха: в 1882 г. он открыл возбудителя туберкулеза, в 1883 г.- возбудителя холеры. В этом же году Клебс и Леффлер открыли возбудителя дифтерии, а в 1884 г. Гаффки получил чистую культуру возбудителя брюшного тифа. В 1886 г. английский врач Брюс открыл возбудителя мальтийской лихорадки (сейчас это заболевание называют бруцеллезом, а возбудителя — бруцеллой).
В изучение этиологии инфекционных болезней большой вклад внесли и русские ученые. Уже в 80-е гг. XIX столетия С. П. Боткин утверждал, что многие известные заболевания, например катаральная желтуха, сыпной тиф, несомненно, имеют инфекционную природу. На это указывали одновременное поражение многих органов больного, лихорадочное состояние, случаи групповых заболеваний. Убежденный в этом, Боткин длительное время проводил за микроскопом в поисках возможных возбудителей болезни, а в 1884 г. создал при терапевтической клинике бактериологическую лабораторию, в которой впервые началось систематическое изучение нового раздела науки.
80-90-е гг. XIX века отмечены серией блестящих открытий. В 1875 г. приват-доцент Медико-хирургической (Военно-медицинской) академии Ф. А. Леш открыл дизентерийную амебу (возбудителя амебиаза). В 1891 г. военный врач А. В. Григорьев открыл возбудителя бактериальной дизентерии (через 7 лет японский ученый Шига получил возбудителя в чистой культуре, и сейчас этот вид называют палочкой Григорьева-Шига). Врач ташкентского военного госпиталя П. Ф. Боровский в 1898 г. открыл возбудителя пендинской язвы (лей-шмании), а в 1901 г. Н. С. Соловьев доказал, что язвенные поражения кишечника могут быть обусловлены инфузорной балантидией.
К этому же времени относится появление вирусологии. Первооткрывателем вирусов был русский ученый Д. И. Ивановский (1892). Развитие вирусологии позволило выделить возбудителей многих хорошо известных клиницистам инфекционных болезней (кори, натуральной и ветряной оспы, краснухи, эпидемического паротита, гриппа и других заболеваний).
Понимание сущности ряда заболеваний меняло и существо подхода к изучению больного и выбору средств лечения. С. П. Боткин писал: «Мы в клинике на каждом шагу убеждаемся в действительном существовании тех неизвестных нам физиологических условий в организме, которые дают возможность
бороться с заболеванием, а потому считаем себя вправе предположить в животном организме условия, более или менее неблагоприятные для специфических низших микроорганизмов». То, что Боткин предвосхитил, И. И. Мечников сумел расшифровать. Он перекинул мост от бактериологии к патологии и явился создателем раздела науки, имеющей большое значение для понимания инфекционного процесса,— иммунологии. Выдающийся русский микробиолог И. И. Мечников на основании своих открытий в области сравнительной патологии воспаления в 1903 г. создал стройное учение об иммунитете при инфекционных болезнях. В 1909 г. ему была присуждена Нобелевская премия.
Изучение возбудителей, их антигенов и токсинов позволило выяснить ряд вопросов патогенеза инфекционных болезней и тем самым обосновать новое патогенетическое направление в клинике инфекционных болезней. Пионером этого направления явилась первая в России кафедра инфекционных болезней, созданная в Военно-медицинской академии в 1896 году. Более двадцати лет она оставалась единственной в стране. В последующем от нее отпочковались кафедры микробиологии (1923) и эпидемиологии (1936). Первым профессором кафедры инфекционных болезней был избран Сергей Сергеевич Боткин, перенесший в клинику передовые принципы клинической школы своего отца С. П. Боткина; в дальнейшем его сменил Николай Яковлевич Чистович — ученик И. И. Мечникова. Введение патогенетического направления облегчалось тем, что в то время кафедра включала не только клинику инфекционных болезней, но и микробиологию с учением об иммунитете. С другой стороны, при оценке клинических симптомов и синдромов давался глубокий патофизиологический анализ всех проявлений болезни. Этот подход, особенно при Николае Константиновиче Розенберге, стал традицией кафедры, которая сохраняется до настоящего времени.
Одним из практических достижений иммунологии явилась серотерапия. Позже, помимо введения готовых антител (пассивный иммунитет), стали использовать и активную иммунизацию — вакцинотерапию. В разработку ее принципов и методов большой вклад сделан коллективом кафедры инфекционных болезней Военно-медицинской академии, в том числе ее руководителями Николаем Ивановичем Рагозой и Петром Алексеевичем Алисовым. В частности, Н. И. Рагоза предложил оригинальный метод вакцинотерапии бруцеллеза, а П. А. Алисов разработал принцип внутрикожной вакцинотерапии, который он применял при лечении различных инфекционных болезней. На основании этих принципов на кафедре при активном участии Александра Павловича Казанцева в период руководства ею Валерием Сергеевичем Матковским были разработаны и применены методы вакцинотерапии больных брюшным тифом (внутрикожно и электрофорезом), токсоплазмозом, орнитозом, доброкачественным лимфоретикулезом. Широкое применение этиотропных средств не вытеснило вакцинотерапию. Наоборот, сочетание антибиотиков с вакцинами (антибиотикоиммунотерапия) получило значительное распространение. В этот период была расшифрована псевдотуберкулезная природа дальневосточной лихорадки. Владимиром Александровичем Знаменским в стенах клиники был проведен героический опыт самозаражения псевдотуберкулезной палочкой.
В 80-90-е гг. XX века появились и были использованы новые возможности воздействия на иммунитет — применение цитокинов (тималин, тимоген и другие). Это направление активно разрабатывалось в период руководства кафедрой Константином Сергеевичем Ивановым (1985—1994 гг.). Большую роль играли исследования, имеющие четко выраженную военную направленность. Разработаны принципы организации медицинской помощи инфекционным больным в мирное и военное время, в том числе в условиях массового поступления больных по опыту локальных войн и военных конфликтов. Предложена классификация инфекционных болезней, могущих возникнуть при массовом поражении средствами бактериологического оружия (заболевания с общетоксическими проявлениями, с преимущественным поражением органов дыхания, желудочно-кишечного тракта и признаками очагового поражения нервной системы). Такое разделение пораженных бактериальными рецептурами облегчало мероприятия по сортировке больных, оказанию им своевременной и полноценной медицинской помощи. Кафедра участвовала в разработке штатной структуры и медицинского оснащения инфекционных полевых госпиталей и тыловых госпиталей МЗ РФ. Все эти работы имеют большое значение для подготовки военных и гражданских специалистов не только в лечебном деле, но и в области противоэпидемической защиты.
В последние годы появились новые (ВИЧ-инфекция, болезнь Лайма - клещевой боррелиоз, эрлихиоз, вирусный гепатит С и др.) и возвратились «старые» инфекции (малярия, амебиаз, дифтерия и др.). Кафедра Военно-медицинской академии стала одним из ведущих центров России по клещевым иксодовым боррелиозам, микст-инфекциям и другим новым и хорошо знакомым «старым» инфекционным болезням.
Существенное значение в развитии учения об инфекционных болезнях и их преподавания имеют кафедры инфекционных болезней, научно-исследовательские институты и Академия медицинских наук с ее подразделениями.
Среди признанных корифеев отечественной науки необходимо назвать имена таких выдающихся ученых, как С. С. Златогоров, Г. А. Ивашенцов, Г. П. Руднев, А. Ф. Билибин, К. В. Бунин, В. И. Покровский, В. А. Никифоров, Е. С. Кетиладзе, Е. П. Шувалова, О. А. Дунаевский, К. М. Лобан, Н. И. Нисевич.
На рубеже XX и XXI веков возникли новые отечественные школы инфекционистов во главе с крупными учеными Н. Д. Ющуком, В. Ф. Учайкиным, В. В. Малеевым, С. Г. Паком, В. В. Ивановой, М. X. Турьяновым, В. И. Лучшевым, А. К. Токмалаевым, А. Г. Рахмановой, Б. С. Нагоевым и другими.
Переходя к общей характеристике и классификации инфекций, необходимо остановиться на семантике и определениях некоторых основных понятий.
Инфекция (от лат. infectio — загрязнение, заражение и inficio — загрязняю) представляет собой широкое общебиологическое понятие, характеризующее проникновение патогенного возбудителя (вирус, бактерия и др.) в другой, более высокоорганизованный, растительный или животный организм и последующее их антагонистическое взаимоотношение.
Инфекционный процесс — это ограниченное во времени сложное взаимодействие биологических систем микро- (возбудитель) и макроорганизма, протекающее в определенных условиях внешней среды, проявляющееся на молекулярном, субклеточном, клеточном, тканевом, органном и организменном уровнях и закономерно заканчивающееся либо гибелью макроорганизма, либо его полным освобождением от возбудителя.
Инфекционная болезнь — это конкретная форма проявления инфекционного процесса, отражающая степень его развития и имеющая характерные нозологические признаки.
Инфекционные болезни - это обширная группа болезней, вызванных патогенным возбудителем. В отличие от других заболеваний инфекционные болезни могут передаваться от зараженного человека или животного здоровому (контагиозность) и способны к массовому (эпидемическому) распространению. Для инфекционных болезней характерны специфичность этиологического агента, цикличность течения и формирование иммунитета. В общей структуре заболеваний человека на инфекционные болезни приходится от 20 до 40%. Следует подчеркнуть, что инфекционный процесс — один из самых сложных биологических процессов в природе, а инфекционные болезни являются грозными, разрушительными факторами для человечества, наносящими ему колоссальный экономический ущерб.
Эйфория 50—70-х гг. XX столетия по поводу успешной борьбы с инфекциями и полной ликвидации части из них оказалась преждевременной. Лишь одну инфекционную болезнь — натуральную оспу — можно считать условно ликвидированной на планете, поскольку, несмотря на почти тридцатилетний срок отсутствия ее официальной регистрации, вирус заболевания сохраняется в ряде лабораторий, а прослойка не иммунных людей весьма значительна и постоянно возрастает.
С другой стороны, увеличивается число известных науке инфекций. Достаточно напомнить, что если в 1955 г. их насчитывалось 1062 (В. М. Жданов), то в настоящее время — более 1200 [Покровский В. И. и др., 1994]. Отсюда — возникновение новых проблем (СПИД и др.) как для специалистов, так и для общества в целом.
К инфекционным болезням традиционно относят также заболевания, вызываемые не живым возбудителем, а продуктами его жизнедеятельности, накопленными вне макроорганизма (например, в пищевых продуктах). При этом инфекционный процесс, как правило, не развивается, а наблюдается лишь интоксикация. В то же время наличие этиологического агента, формирование иммунитета (антитоксического) и возможность развития инфекционного процесса позволяют относить эти заболевания к инфекционным (ботулизм и др.).
Общепризнанным является положение о том, что инфекционный процесс — суть взаимодействие возбудителя и макроорганизма в определенных условиях окружающей среды. Однако окружающая среда в этой триаде занимает особое место и обычно лишь косвенно влияет на инфекционный процесс. Во-первых, она оказывает предварительное опосредованное воздействие путем влияния как на возбудителя (физические, химические, биологические и другие факторы среды), так и на макроорганизм (те же факторы плюс социальные условия). Во-вторых, любые терапевтические воздействия также можно расценивать как текущее влияние факторов внешней среды на инфекционный процесс. И в-третьих, сам комплекс взаимных приспособительных реакций микро-и макроорганизма можно рассматривать в конечном итоге как направленный на восстановление нарушенного гомеостаза и биологического равновесия с окружающей средой.
Возбудитель определяет не только возникновение инфекционного процесса, но и его специфичность. Так, возбудитель чумы вызывает чуму, холеры — холеру и т. д. Интересно, что поскольку инфекционные болезни стали известны человечеству раньше, чем микроорганизмы, их вызывающие, то их возбудитель, как правило, получал название, соответствующее заболеванию. В то же время, специфичность не является абсолютной. Например, одно инфекционное заболевание могут вызвать разные возбудители (сепсис), и напротив, один возбудитель (стрептококк) может вызывать разные болезни (скарлатина, рожа, ангина).
На протяжении всей своей жизни человек контактирует с огромным миром микроорганизмов, но вызывать инфекционный процесс способна лишь ничтожно малая часть этого мира (примерно 1/30 000). Эта способность в значительной степени определяется патогенностью возбудителя.
Патогенность (болезнетворность) — видовой признак микроорганизма, закрепленный генетически и характеризующий способность вызывать заболевание. По этому признаку микроорганизмы подразделяются на патогенные, условно-патогенные и непатогенные (сапрофиты). Главными факторами, определяющими патогенность, являются вирулентность, токсигенность и инвазив-ность.
Вирулентность — это степень, мера патогенности, индивидуально присущая конкретному штамму патогенного возбудителя.
Токсигенность — это способность к выработке и выделению различных токсинов (экзо- и эндотоксины).
Инвазивность (агрессивность) — способность к проникновению в ткани и органы макроорганизма и распространению в них.
Считается, что свойства патогенности определяются генами, входящими в состав мобильных генетических элементов (плазмиды, транспозоны и др.). Преимущество мобильной организации генов заключается в возможности быстрой адаптации бактерий к условиям окружающей среды. Такой механизм изменчивости объясняет формирование новых типов возбудителей инфекционных болезней. Ген, детерминирующий синтез фактора патогенности, при попадании в другую бактерию может по-иному взаимодействовать с уже имеющимися факторами патогенности, обусловливая различную степень вирулентности и, следовательно, изменение картины инфекционного процесса.
Факторы и способы «агрессии» возбудителей инфекции весьма разнообразны. Среди них — индукция стресса, геморрагических реакций (повреждение сосудов), аллергических и иммунопатологических реакций, аутоиммунитета (вплоть до системных тяжелых поражений), прямой токсический эффект на клетки и ткани, иммунодепрессия, развитие опухолей и др. Нередко вторичные изменения превышают повреждения, вызываемые непосредственно возбудителями. Это связано преимущественно с патологическим действием экзо- и эндотоксинов, продуцируемых возбудителем и антигенемией. В то же время, возбудители болезней обладают свойствами, препятствующими воздействию на них защитных факторов макроорганизма (наличие капсулы, продуцирование факторов угнетения фагоцитоза, антигенная мимикрия, внутриклеточное расположение, антигенные вариации и др.).
Состояние макроорганизма и его свойства определяют не только возможность возникновения и характер течения инфекционного процесса, но и вероятность проявления последнего в форме инфекционного заболевания. Следует подчеркнуть, что при любом способе воздействия патогенного возбудителя на организм в ответных реакциях в той или иной степени участвуют все физиологические системы макроорганизма, а не только иммунная система. Эти реакции организма как единого целого определяются его реактивностью, под которой понимают способность организма приводить в действие физиологические механизмы, направленные на инактивацию, разрушение и выведение возбудителя и связанных с ним субстанций, а также и на компенсацию нарушенных функций.
Защитные факторы организма (резистентность) подразделяются на специфические (иммунные) и неспецифические, составляя в целом комплекс полученных наследственно и индивидуально приобретенных механизмов.
Важно, что в большинстве случаев микроорганизму еще до вступления в непосредственный контакт с макроорганизмом приходится преодолевать мощный защитный барьер в виде нормальной микрофлоры. Микрофлора макроорганизма подразделяется на две основные группы:
— микрофлора (микробиоценоз), характерная для данного вида (эндогенная, аутохтонная, облигатная, резидентная);
— микрофлора случайная (временная, транзиторная, факультативная).
Механизмами формирования микробных экосистем, регуляции микрофлоры, взаимодействия с организмом хозяина занимается новая наука — микроэкология. Среди различных микробиотопов (определенная сфера, площадь, субстрат для жизнедеятельности микрофлоры) организма человека ведущими являются кишечник (общая площадь — 200—300 м2), легкие (80 м2) и кожа (2 м2). Кишечная микроэкологическая система является важнейшей частью гомеостатической системы организма (представлена более чем 400 видами микроорганизмов, из них 98% — облигатные анаэробы). Она располагает многими механизмами, обеспечивающими подавление патогенной микрофлоры (стимуляция перистальтики, конкуренция за места адгезии к эпителию кишечника, выработка антибиотических веществ, индукция иммунологических механизмов защиты и др.). Интегральным показателем специфических и неспецифических механизмов защиты желудочно-кишечного тракта (ЖКТ) является колонизационная резистентность (состояние эпителия, активного лизоцима, кислотность и ферментативная активность желудочного сока, содержание комплемента, интерферонов, макрофагов, иммуноглобулинов). Снижение ее (дисбактериоз) приводит к более частому заболеванию различными кишечными инфекциями.
Аналогично выполняет свои защитные и барьерные функции кожа (непроницаемость ее для большинства микробов, бактерицидные свойства) и респираторный тракт (реснички эпителия респираторного тракта, механическое удаление возбудителей из дыхательных путей при кашле, секреция иммуноглобулинов и др.).
Далее в процесс защиты включаются такие факторы естественного иммунитета, как фагоциты (микро- и макрофаги), предшествующие (естественные) антитела, лизоцим, интерферон и т. д. И наконец, в большинстве случаев развивается реакция приобретенного иммунитета (клеточного и гуморального), а также иммунологическая толерантность.
В то же время хорошо известны видовая и индивидуальная невосприимчивость к инфекционным болезням. Особую роль при этом играют гены, располагающиеся в главном комплексе гистосовместимости (гены системы HLA). К настоящему времени уже картирован ряд локусов, определяющих высокую и низкую чувствительность к некоторым инфекционным заболеваниям. Так, доказано, что отсутствием в организме генетически детерминированного синтеза нормального полипептида цепи β-гемоглобина обусловливается устойчивость человека к возбудителю малярии.
Важнейшую роль в развитии и течении инфекционного процесса играют нервная система и, прежде всего, нейрогуморальная регуляция. Хорошо известно, что регуляторами нейроэндокринного воздействия на иммунную систему являются адренокортикотропный гормон (АКТГ), соматотропный гормон (СТГ), кортикостероиды, катехоламины, энкефалины и многие другие гормоны и нейромедиаторы. На иммунокомпетентных клетках имеются рецепторы для кортикостероидов, катехоламинов, энкефалинов, эндорфина, серотонина, ацетилхолина и других нейроэндокринных медиаторов. Нарушения нейроэндокринной регуляции способствуют развитию инфекционных заболеваний и осложнений.
Взаимодействие патогенного возбудителя и восприимчивого организма происходит в течение определенного временного промежутка и характеризуется цикличностью, т. е. закономерной сменой фаз развития, нарастания и убывания проявлений инфекционного процесса. В этой связи при развитии инфекционной болезни принято различать несколько последовательных периодов: инкубационный (латентный), начальный, разгара и выздоровления.
Инкубационный период (от момента заражения до начала заболевания), как правило, не имеет клинических проявлений, лишь при некоторых заболеваниях (сыпной тиф, корь) и у немногих больных в последние дни этого периода появляются самые общие и неопределенные симптомы (предвестники, продромальные явления), на основании которых при отсутствии эпидемиологических данных трудно даже заподозрить инфекционную болезнь. Каждому инфекционному заболеванию присуща своя длительность инкубационного периода (с небольшими вариациями в зависимости от вирулентности, дозы возбудителя и реактивности организма). Она исчисляется от нескольких часов (грипп, токсикоинфекции) до нескольких недель, месяцев (столбняк, бешенство, вирусные гепатиты) и даже лет (ВИЧ-инфекция).
Начальный период характеризуется большим количеством разнообразных признаков, которые в совокупности составляют клинический или клинико-лабораторный симптомокомплекс, позволяющий установить предварительный или, реже, окончательный диагноз болезни.
Период разгара характеризуется типичными для данной болезни симптомами, достигающими своей максимальной выраженности и определяющими все ее своеобразие (например, сыпь при брюшном тифе, желтуха при вирусном гепатите, бубон при туляремии).
Периоду выздоровления свойственны угасание клинических проявлений болезни и постепенное восстановление нарушенных функций организма. В этом периоде при некоторых инфекционных заболеваниях возможны рецидивы (возврат болезни). Так, например, при псевдотуберкулезе они столь характерны, что нередко сам период называют периодом рецидивов. Рецидивы следует отличать от обострений, которые развиваются не после болезни, а на фоне сохраняющейся клинической симптоматики. Повторное заболевание, развивающееся в результате нового заражения тем же возбудителем, называется реинфекцией.
КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ. Классификация, которую принимают все или большинство врачей, работающих в этой области, до настоящего времени отсутствует. Предлагается огромное число различных вариантов систематизации. Они обусловливаются главным образом той практической точкой зрения и конечными целями, которые преследуются при классифицировании.
Важным является число видов возбудителей, вызвавших инфекционный процесс. При этом инфекционные болезни, вызванные одним видом микроорганизмов (таких абсолютное большинство), называются моноинфекцией, вызванные одновременно несколькими видами — смешанными, или микст-инфекциями. Очевидно, что взаимодействие организма человека с двумя и более возбудителями является более сложным процессом и не исчерпывается простым суммированием эффектов отдельных представителей микрофлоры. В последние годы накапливается и анализируется значительный опыт по изучению смешанных инфекций, представляющих собой различные сочетания вирусного гепатита, брюшного тифа, малярии, амебиаза, дизентерии и других болезней |Ляшенко Ю. И., Иванов А. И., 1989].
Другим подходом в классификации является деление всех инфекций на экзогенные и эндогенные (аутоинфекция). Абсолютное большинство инфекционных болезней являются экзогенными, т. е. вызываемыми вследствие проникновения возбудителя извне. Под эндогенной понимается инфекция, вызываемая собственной условно-патогенной флорой и приобретающая значение самостоятельной формы заболевания. Аутоинфекция чаще всего развивается в миндалинах, толстой кишке, бронхах, легких, мочевыводящих путях, на кожных покровах вследствие снижения защитных сил организма, вызванного неблагоприятным воздействием факторов окружающей среды, длительной антибиотикотерапией и др.
Рассматривая экзогенные инфекции с чисто эпидемиологических позиций по такому критерию, как контагиозность, можно выделить следующие группы инфекционных болезней:
— неконтагиозные, или незаразные (псевдотуберкулез, ботулизм, отравление стафилококковым энтеротоксином, малярия и др.);
— малоконтагиозные (инфекционный мононуклеоз, орнитоз, ГЛПС, бруцеллез);
— контагиозные (дизентерия, грипп, брюшной тиф и др.);
— высококонтагиозные (натуральная оспа, холера).
С позиций организационных и противоэпидемических мероприятий выделяют также карантинные инфекции. Согласно Международным медико-санитарным правилам, принятым на XXII сессии ВОЗ в Женеве в 1972 г., к карантинным болезням отнесены три инфекционных заболевания — холера (в том числе Эль-Тор), чума и желтая лихорадка. Натуральная оспа к настоящему времени выведена из этого перечня. Уведомление ВОЗ о каждом случае заболевания осуществляется в течение 24 ч от момента выявления. В течение следующих 24 ч должно последовать уведомление о границах зараженного района. Действие этих правил на территории России регламентируется Приказом МЗ. Помимо указанных трех заболеваний в перечень включены:
— контагиозные вирусные геморрагические лихорадки (Ласса, Марбург, Эбола);
— малярия;
— другие болезни, передающиеся комарами (лихорадки денге, долины Рифт, Западного Нила; энцефаломиелиты лошадиные — западный американский, восточный американский, венесуэльский; энцефалиты — японский, калифорнийский, Сент-Луис, долины Муррея).
Можно классифицировать экзогенные инфекции по месту внедрения в организм возбудителя (входные ворота). Входными воротами для одних возбудителей является кожа (малярия, сыпной тиф, кожный лейшманиоз), для других - слизистые оболочки дыхательных путей (грипп, корь, краснуха), пищеварительного тракта (дизентерия, брюшной тиф) или половых органов (гонорея, сифилис). Однако при некоторых инфекционных болезнях возбудитель может проникать в организм различными путями, что сказывается и на клинической картине (дифтерия: зева и раневая; гума: кожно-бубонная и легочная формы; туляремия: бубонная, глазо-бубонная, ангинозно-бубонная, кишечная, легочная и генерализованная формы).
К этой классификации близка систематизация инфекций по клинико-анатомическому принципу с делением на инфекции общего и местного синдрома или на:
- генерализованные инфекции;
- инфекции с преобладающей локализацией процесса в определенных органах и системах, но с выраженными общими реакциями;
- местные (топические) инфекции без выраженной общей реакции.
Другим вариантом такой классификации является деление инфекций в зависимости от тропности (аффинитета) возбудителя к определенным системам, тканям и даже клеткам. Так, например, возбудитель гриппа тропен главным образом к эпителию дыхательных путей, эпидемического паротита — к железистой ткани, бешенства — к нервным клеткам аммонова рога, оспы — к клеткам эктодермального происхождения (кожи и слизистых оболочек), дизентерии — к энтероцитам, сыпного тифа — к эндотелиоцитам и т. д.
По биологигескому принципу инфекции могут подразделяться на антропонозы (полиомиелит, менингококковая инфекция, вирусный гепатит и др.) и зоонозы (бешенство, бруцеллез, лептоспироз, сибирская язва, туляремия, ящур и др.), выделяют также природно-огаговые инфекции (клещевой энцефалит, ГЛПС) и инвазии (протозойные болезни — малярия, амебиаз, лейшманиозы и др.; гельминтозы).
Клинически инфекционные болезни характеризуются по проявлениям (манифестные и инаппарантные), по тяжести (легкие, средней тяжести, тяжелые и крайне тяжелые), по клиническим формам (например, менингококковая инфекция может проявляться в виде назофарингита, менингита, менин-гоэнцефалита, менингококцемии), по течению (типичные и атипичные; циклические и ациклические; молниеносные, или фулминантные; острые, подострые, или затяжные; и хронические).
Инаппарантные, или субклинические (менее удачное название), формы инфекционных болезней протекают бессимптомно, хотя в организме человека наблюдаются иммунологические, а также функциональные и морфологические изменения, типичные для соответствующего заболевания. Выраженные в малой степени, они не приводят к манифестации патологического процесса, и внешне человек остается здоровым. Инаппарантные формы весьма характерны для некоторых инфекций (брюшной тиф, сальмонеллезы, дизентерия, вирусный гепатит В и др.) и, напротив, несвойственны для других (натуральная оспа, скарлатина, рожа и др.). Инаппарантные формы могут протекать остро (вирусный гепатит А) и хронически (бруцеллез). Особым вариантом хронического инаппарантного процесса является латентная форма инфекции. При этом возбудитель находится в дефектной форме (вирус в виде дефектных субвирусных интерферирующих частиц, бактерии — в виде L-форм, сферопластов) и поддерживает свою жизнедеятельность за счет внутриклеточного паразитизма, не выделяясь во внешнюю среду. Под влиянием некоторых факторов (интеркуррентные болезни, травмы, стресс и др.) латентная инфекция может трансформироваться в острую манифестную с восстановлением обычных свойств возбудителя (герпетическая инфекция).
Своеобразной формой взаимодействия вирусов и организма человека является медленная инфекция. Она отличается тем, что, несмотря на раз-питие патологического процесса, как правило, в одном органе или в одной тканевой системе (чаще в нервной) наблюдается многомесячный или даже многолетний инкубационный период, после которого медленно, но неуклонно развиваются симптомы заболевания, всегда заканчивающегося летально |3уев В. Л., 1988]. К медленным инфекциям человека в настоящее время относят заболевания, вызываемые прионами (инфекционными безнуклеиновыми белками),- болезнь Куру, болезнь Крейтцфельда-Якоба, синдром Герстманна—Шреуслера, амиотрофический лейкоспонгиоз, а также вирионами — подострый коревой склерозирующий панэнцефалит, подострый послекоревой лей-коэнцефалит, прогрессирующая врожденная краснуха и др. Число медленных инфекций, открываемых учеными, все время возрастает и в настоящее время превышает 30.
Одной из наиболее распространенных и часто цитируемых является классификация Л. В. Громашевского, построенная преимущественно по принципу учета механизма передачи инфекции. Она предусматривает деление всех инфекций на пять групп: 1) кишечные; 2) дыхательных путей; 3) «кровяные»; 4) наружных покровов; 5) с различными механизмами передачи. При этом, например, в группу кишечных инфекций попадают дизентерия и гельминтозы, ботулизм и отравления стафилококковым энтеротоксином, амебиаз, трихинеллез и даже бруцеллез, лептоспироз, пситтакоз; в группу «кровяных» (трансмиссивных) — малярия, риккетсиозы и туляремия. Очевидно несовершенство подобной классификации с позиции врача-инфекциониста, поскольку совершенно разные по возбудителю (вирусы, бактерии, простейшие, грибы, гельминты) и по патогенезу заболевания (малярия, туляремия) попадают в одну группу.
В этой связи более логичной представляется классификация, построенная по этиологическому принципу. Она предусматривает выделение бактериозов (бактериальные инфекции), отравлений бактериальными токсинами, вирусных болезней, риккетсиозов, хламидиозов, микоплазмозов, протозойных болезней, микозов и гельминтозов. В каждой из этих групп болезни могут объединяться по патогенетическому принципу, по механизму передачи или по тропности возбудителя. В настоящем учебнике сведения об инфекционных заболеваниях изложены в соответствии с этиологической классификацией.
ПРИНЦИПЫ ДИАГНОСТИКИ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
В диагностике инфекционных болезней используются все принципы, методы и приемы, применяемые в клинике внутренних болезней (анамнез, клинические методы обследования больного, лабораторные, инструментальные и специальные методики). Однако, кроме того, инфекционисты применяют ряд методик, используемых только для диагностики инфекционных заболеваний.
К ним относятся, во-первых, различные способы обнаружения или выделения возбудителей инфекции, а также выявления специфических признаков ответной реакции организма на возбудителя (бактериологические, вирусологические, паразитологические, серологические, иммунологические исследования, биологические и кожные аллергические пробы, методы ДНК-зондов, полимеразная цепная реакция и др.).
Во-вторых, диагностика инфекционной болезни требует особого клинико-эпидемиологического метода. Помимо знаний о санитарно-эпидемическом состоянии и общей ситуации по инфекционной заболеваемости в районе, врач обязан использовать в работе с больными методику сбора эпидемиологического анамнеза. Эпидемиологический анамнез предполагает получение при опросе больного сведений о возможном источнике болезни и путях передачи инфекции, о перенесенных инфекционных болезнях и профилактических прививках. В совокупности с клиническими показателями эпидемиологический анамнез может сыграть большую диагностическую роль при эпидемической вспышке, в то же время его диагностическая ценность при спорадических (единичных) заболеваниях значительно ниже.
В целом, под диагностикой инфекционного заболевания следует понимать постановку конкретного диагноза на основании анализа комплекса данных, полученных различными методами. При этом наиболее информативными и важными являются результаты клинического обследования больного. Они дают возможность поставить предварительный диагноз и на основании этого начать лечение и проведение профилактических мероприятий. Предварительный диагноз позволяет существенно сузить круг лабораторных исследований, необходимых для уточнения диагноза. Диагноз инфекционной болезни должен быть развернутым и индивидуальным. В нем учитывается как нозологическая, так и клиническая форма заболевания (включая состояние больного), период болезни, характер течения, наличие осложнений и сопутствующих заболеваний. Очевидно, что ранняя диагностика инфекционного заболевания имеет значение не только для заболевшего человека (рано начатое лечение позволяет купировать заболевание, предупредить развитие осложнений и тем самым уменьшить трудопотери), но и для коллектива, так как позволяет своевременно начать проведение профилактических и противоэпидемических мер. Поздняя диагностика (поздняя изоляция и госпитализация) может, наоборот, способствовать возникновению вспышки инфекционных болезней, особенно в организованных коллективах.
По определению Н. И. Рагозы, под ранней диагностикой понимается диагностика в начальном периоде инфекционного заболевания, то есть до формирования полной клинической картины болезни с ее типичными проявлениями. Длительность начального периода при разных инфекционных болезнях существенно различается. При брюшном тифе он продолжается около недели (до появления характерных розеол и гепато-лиенального синдрома), а при скарлатине — всего около 12—24 ч (до появления типичной экзантемы). Возможности диагностики в периоде разгара заболевания значительно увеличиваются.
При инфекционных заболеваниях в различной степени поражаются все органы и системы организма человека, поэтому только тщательное и систематическое обследование больного, внимательное отношение к любому признаку, кажущемуся на первый взгляд мелким, второстепенным, позволяет составить полное представление о клинической картине болезни. С другой стороны, инфекционный процесс постоянно развивается, непрерывно меняется клиническая картина, отражая закономерности течения болезни. В этой связи, все обнаруженные симптомы (субъективные и объективные) необходимо рассматривать в динамике — сроки и последовательность появления и исчезновения, характер изменений и т. д.
Для диагностики большое значение имеет правильный расспрос больного. Вначале выясняются жалобы больного на момент его опроса, которые по сути своей являются субъективным проявлением болезни. При первичном осмотре целесообразно предоставить больному возможность их произвольного изложения. Затем активным опросом по органам и системам необходимо выявить основные и второстепенные признаки заболевания, уточняя их по времени, интенсивности, продолжительности, локализации и т. п. Например, беспокоит ли головная боль (локализация, интенсивность); имеются ли нарушения аппетита и расстройство сна (бессонница, кошмарные сны); мышечная слабость, тошнота и рвота (когда появились, как часто, объем и характер рвотных масс); есть ли насморк (чихание, выделения из носа); были ли носовые кровотечения; отмечаются ли боли в горле при глотании (справа, слева, с обеих сторон, сильные или слабые), в ушах (в каком положении, при глотании, открывании рта), в груди (в покое, при движениях, при дыхании), в животе (локализация, постоянные или приступообразные, уменьшаются после рвоты или дефекации), в суставах (в каком, в покое или при движениях, опухают ли суставы), боли другой локализации (например, в подвздошной или паховой области, в икроножных мышцах). При характеристике жалоб больного необходимо уточнять их, обращая внимание на особенности, присущие тому или иному инфекционному заболеванию. Так, при большинстве инфекционных болезней, протекающих с лихорадкой, больные жалуются на мышечные боли, но при лептоспирозе они локализуются преимущественно в икроножных мышцах и выражены настолько резко, что больной из-за них с трудом может передвигаться. Также часто больные жалуются на головную боль, но при брюшном тифе она выражена умеренно, при сыпном — сильно, а при менингококковом менингите — очень сильно.
При наличии болей подробно выясняются другие ощущения со стороны соответствующих органов, при отсутствии их опрос продолжается по системам (кровообращения, дыхания, пищеварения, мочевыделения), в частности, выясняются особенности физиологических отправлений: запор или понос (число дефекаций, тенезмы или ложные позывы, характер и объем испражнений, патологические примеси — слизь, гной, кровь, глисты), мочевыделение (свободное или затрудненное, дизурические явления), цвет мочи (светло-желтая, темная, в виде «мясных помоев»).
Анамнез болезни предполагает детальное восстановление всего хода заболевания от начальных проявлений до состояния больного в момент поступления (обследования). Важно установить особенности начала болезни (острое, подострое или постепенное). При многих инфекционных заболеваниях начало острое с бурным развитием основных клинических симптомов. При таких инфекциях начальный период исчисляется часами (грипп, менингококковый менингит, отравление стафилококковым токсином, ботулизм и др.). В этих случаях, обычно, больные могут указать даже час начала болезни. Некоторые инфекции с острым началом характеризуются молниеносным течением с возможным летальным исходом в течение суток (грипп, менингококкцемия, холера, ботулизм, тропическая малярия у неиммунных лиц и др.).
О подостром начальном периоде можно говорить в случаях, когда типичные симптомы или синдромы болезни проявляются в течение 1—3 сут. Если же начало заболевания растягивается от 4 до 7 и более сут., это свидетельствует о постепенном его развитии.
Поэтому отсчет времени развития инфекционного заболевания в случаях «строго начала, молниеносного течения проводится в часах. Динамика течения болезни в других случаях отмечается по дням болезни.
Важно уточнить первые симптомы болезни, характер температурной кривой, сроки появления и исчезновения отдельных симптомов и синдромов (экзантемы и другие изменения кожи и слизистых оболочек, поражения опорно-двигательного аппарата, верхних дыхательных путей, зева, желудочно-кишечного тракта, нервной системы и пр.). Следует выяснить проводившееся ранее лечение больного, уточнить, какие препараты он принимал, так как многие из них (антибиотики, химиопрепараты и др.) могут изменить клиническое течение болезни, обусловить токсико-аллергические дерматозы и др. Результаты клинических, инструментальных, лабораторных и других исследований, выполненных ранее, также должны быть отражены в анамнезе заболевания. Выяснение анамнеза болезни должно быть вдумчивым, всесторонним, с активным участием самого больного и учетом его состояния, психологических особенностей, характера, интеллекта и воспитания.
Эпидемиологический анамнез является неотъемлемой частью истории болезни инфекционного больного. Он всегда должен быть конкретизирован, исходя из предполагаемого заболевания у пациента (продолжительность инкубационного периода, особенности эпидемиологии той или иной инфекции). Иногда в анамнезе содержатся данные, указывающие на источник инфекции, например контакт с больным гриппом во время его эпидемии, присасывание клеща при клещевом энцефалите или клещевом боррелиозе, контакт с больным (корью, ветряной оспой, краснухой, эпидемическим паротитом) в сроки, соответствующие длительности инкубационного периода того или иного заболевания. Большое значение имеют сведения о пребывании в эндемичной местности (малярия, туляремия, лептоспироз, клещевой сыпной тиф Средней Азии) и указания на эпизоды, когда заражение могло быть весьма вероятным, например купание в пресноводных водоемах (лептоспироз), укусы комаров (малярия), бездомных собак (бешенство), повреждение кожи с попаданием в рану земли (столбняк) и др. В некоторых случаях удается выявить лишь косвенные данные, говорящие о возможности инфицирования (эпидемические предпосылки). К ним можно отнести, например, наличие педикулеза (сыпной тиф), обилие мышевидных грызунов (туляремия, геморрагическая лихорадка, псевдотуберкулез), употребление сырого овечьего молока или брынзы домашнего приготовления (бруцеллез), козьего молока (клещевой вирусный энцефалит), использование продуктов домашнего консервирования (ботулизм), сырых яиц и неправильно хранившихся готовых мясных продуктов (сальмонеллез), кремовых пирожных и киселей (стафилококковая инфекция), сырых салатов из свежих овощей (иерсиниоз) и др. При уточнении эпиданамнеза необходимо иметь в виду группу инфекций, при которых передача возбудителей
происходит через кровь без участия кровососущих насекомых. Это вирусные гепатиты (В, С, D, G), ВИЧ-инфекция, хламидиозы, цитомегаловирусные, герпетические инфекции и др. Они могут передаваться естественным (половой, трансплацентарный, перинатальный) и искусственным путем (переливание крови, операции, косметические процедуры, нанесение татуировок, совместное пользование бритвой, полотенцем, зубной щеткой и др.). Заражение с использованием нестерильных шприцев особенно типично для наркоманов. Половой путь передачи характерен в среде гомосексуалистов, при частых и неразборчивых сменах половых партнеров.
При оценке анамнеза жизни, помимо общих данных, необходимо учитывать перенесенные инфекционные болезни, так как некоторые их них оставляют после себя длительный иммунитет и повторные заболевания практически не встречаются (корь, краснуха, эпидемический паротит, ветряная оспа) или протекают в атипичной форме. Необходимо уточнить, какие прививки получал больной, так как у привитых заболевание также чаще протекает в атипичной форме (корь, дифтерия). Важным может оказаться аллергологический анамнез. Так, некоторые болезни (кишечный иерсиниоз, псевдотуберкулез, трихинеллез и некоторые другие глистные инвазии) протекают иногда с выраженным аллергическим компонентом, а очаговые инфекции (одонтогенная, тонзиллогенная) способствуют аллергизации организма.
Объективное обследование больного всегда проводится по определенной схеме: общее состояние больного, выраженность интоксикации и лихорадки, кожа и слизистые оболочки, лимфатические узлы, опорно-двигательный аппарат, сердечно-сосудистая система, органы дыхания, пищеварительная система, печень и селезенка, мочевая система, нервная система и железы внутренней секреции. Эта схема помогает не упустить что-либо как при обследовании больного, так и при изложении полученных данных в истории болезни, и является общепринятой.
При оценке общего состояния отмечают особенности телосложения, состояние питания, физическое развитие, определяют тяжесть состояния больного на основании, прежде всего, лихорадки и симптомов общей интоксикации.
Клинические проявления общей интоксикации являются характерными для большинства инфекционных болезней и отличаются многообразием. Среди них — головная боль, слабость, адинамия, общая разбитость, ломящие боли во всем теле, боли в определенных мышечных группах, артралгия, снижение аппетита, нарушение сна, иногда тошнота и рвота. К симптомам интоксикации относятся и различные нарушения психики — возбуждение, угнетение, расстройства сознания. При возбуждении больной многословен: детально, торопясь, рассказывает о своих ощущениях (сыпной тиф); при угнетении больной, наоборот, малоподвижен, вял, неразговорчив, на вопросы отвечает односложно, спустя некоторое время после заданного вопроса (брюшной тиф).
Различают три основные степени нарушения сознания: сомноленция, сопор, кома. Сомноленция (оглушенность, заторможенность) — вид «дремлющего» или полусонного человека, внешние раздражители воспринимаются с задержкой, с трудом, больной как бы пробуждается в ответ на обращение к нему. Сопор — сознание утрачено не полностью, сохранены реакции на сильные раздражители (окрик, щипок, укол). Кома — полная потеря сознания, реакции на внешние раздражители отсутствуют, возможны периодические сокращения мускулатуры (гримасы, движения пальцев), непроизвольные дефекация и мочеиспускание. Обычно эти нарушения сознания развиваются последовательно (сомноленция сменяется сопором, а затем комой).
Лихорадка является наиболее частым проявлением инфекционного процесса. Она является не только признаком общей интоксикации, но и относится к важнейшим защитным реакциям. Например, при повышенной температуре тела репродукция многих вирусов резко сокращается (в 50 раз и более). Лихорадка стимулирует обмен веществ, повышает фагоцитарную активность лейкоцитов. В основе развития лихорадки лежит изменение нейрогуморальной регуляции за счет повышения теплообразования (главным образом в печени и в мышцах) и уменьшения теплоотдачи. Лихорадка возникает в результате воздействия различных продуктов жизнедеятельности возбудителя — токсинов, антигенов, аллергенов (пирогены), а также под влиянием продуктов распада тканей и веществ, образующихся в лейкоцитах (лейкоцитарные пирогены).
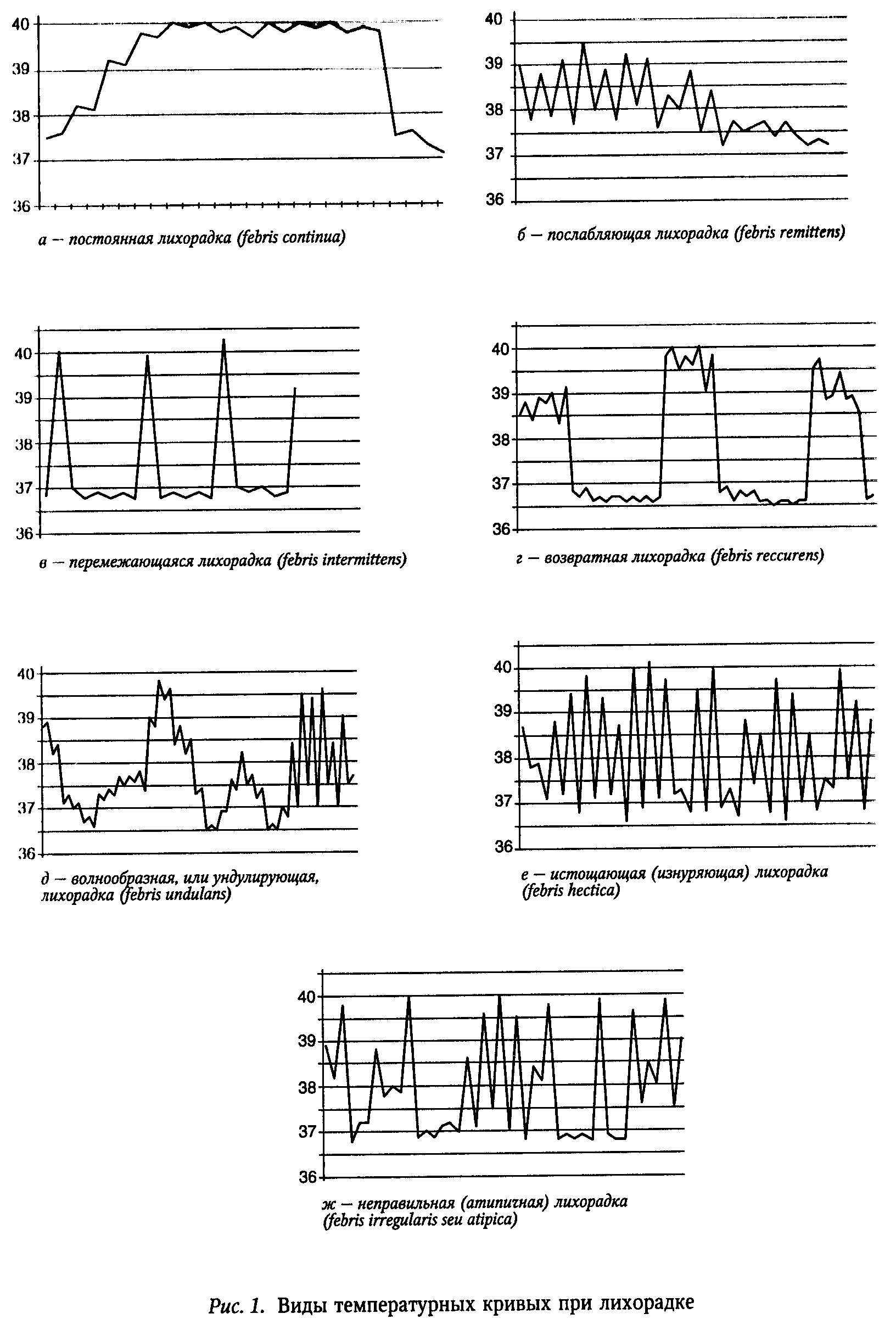
Лихорадка различается по длительности, степени повышения температуры тела и по характеру температурной кривой (рис. 1). По длительности лихорадка может быть острая (до 2 нед.), подострая (до 6 нед.) и хроническая (свыше 6 нед.). По выраженности повышения температуры тела различают субфебрилитет (до 38° С) и собственно лихорадку, которая может быть у м е р е н н о й (до 39° С) и в ы с о к о й (до 41° С) и гиперпиретичес к о й (свыше 41° С). Для диагностики большое значение имеет тип температурной кривой. Различают несколько основных типов температурных кривых:
1. Постоянная лихорадка (febris continua) — температура тела высокая, суточные колебания не превышают 1° С. Наблюдается при брюшном тифе, паратифах, лихорадке Ку, сыпном тифе, псевдотуберкулезе и др. (рис. 1, а).
2. Послабляющая лихорадка (febris remittens) — суточные колебания составляют 1—2° С, при снижении температура тела до нормы не доходит. Характерна для орнитоза, клещевого риккетсиоза, геморрагических лихорадок, вирусных энцефалитов и др. (рис. 1, б).
3. Перемежающаяся лихорадка (febris intermittens) — в пределах суток температура тела с высоких значений опускается до нормы и ниже, колебания — до 3—4° С. Наблюдается при малярии и клещевом возвратном тифе (рис. 1, в).
4. Возвратная лихорадка (febris recurrens) — правильное чередование высоколихорадочных и безлихорадочных (апирексия) периодов длительностью до 2-7 сут. Характерна для вшивого возвратного тифа, содоку (болезнь укуса крыс) (рис. 1, г).
5. Волнообразная, или ундулирующая, лихорадка (febris undulans) — постепенное нарастание температуры тела до высоких значений и затем постепенное ее снижение до субфебрильной, а иногда и нормальной; через 2—3 нед. цикл повторяется. Наблюдается как при инфекционных (бруцеллез, висцеральный лейшманиоз), так и неинфекционных заболеваниях (лимфогранулематоз) (рис. 1, д).
6. Истощающая (изнуряющая) лихорадка (febris hectica) — длительное повышение температуры тела с очень большими суточными подъемами (3—5° С) и снижениями до (суб)нормальной температуры (сепсис, генерализованные вирусные инфекции и др.) (рис. 1, е).
7. Неправильная (атипигная) лихорадка (febris irregularis seu atipica) — суточный ритм нарушен, имеются повышения температуры по утрам и спады к вечеру (febris inversa), либо два или три подъема и спуска, либо вообще незакономерные колебания температуры в течение суток. Возможна при сепсисе и др. (рис. 1,ж).
Помимо приведенных классических типов температурных кривых, профессор ВМедА А. П. Казанцев (1991) предложил выделять еще два: острую волнообразную и рецидивирующую лихорадку.
Острая волнообразная лихорадка (febris undulans acuta) — в от-личие от ундулирующеи характеризуется относительно кратковременными волнами (3—5 сут.) и отсутствием ремиссии между волнами; обычно температурная кривая представляет собой ряд затухающих волн, то есть каждая последующая волна менее выражена по высоте и длительности, чем предыдущая (брюшной тиф, орнитоз, мононуклеоз и др.); когда последующая волна обусловлена присоединением осложнения, наблюдаются обратные соотношения, то есть вторая волна более выражена, чем первая (эпидемический паротит, грипп и др.).
Рецидивирующая лихорадка (febris recidiva) — в отличие от возвратной лихорадки (правильное чередование волн лихорадки и апирексии) характеризуется рецидивом (обычно одним) лихорадки, который развивается в различные сроки (от 2 сут. до месяца и более) после окончания первой температурной волны (лептоспироз, псевдотуберкулез и др.). Рецидивы развиваются у части больных (10—20%). В связи с этим если рецидив имеет важное диагностическое значение, то отсутствие его вовсе не исключает возможности перечисленных болезней.
Следует отметить, что при раннем применении этиотропных средств (антибиотиков, антипаразитарных препаратов и др.) температурная кривая существенно изменяется, что необходимо учитывать при ее диагностической оценке.
Изменения кожи и слизистых оболочек наблюдаются при многих инфекционных болезнях и имеют большое дифференциально-диагностическое значение. Сыпь на коже называется экзантемой, а на слизистых оболочках — энантемой.
Сыпь (эффлоресценция) — это очаговая реакция кожи или слизистой оболочки на действие возбудителей или продуктов их жизнедеятельности (токсинов, аллергенов, антигенов); могут иметь значение образующиеся при инфекции гистаминоподобные вещества (аллергические сыпи), нарушения свертываемости крови (микротромбозы в прекапиллярах) и др. В основе этой реакции чаще всего лежит первичное поражение сосудов кожи и слизистых оболочек (гиперемия) с последующим развитием воспаления (инфильтрат, гранулема, некроз). Как правило, сыпь является отражением циркуляции возбудителя в крови.
Экзантемы делятся на первичные и вторичные. К первичным относятся розеола, пятно, эритема, геморрагии, папула, бугорок, пузырек, пустула, волдырь, пузырь и другие; ко вторичным — чешуйка, пигментация, язва, рубец.
Розеола — пятнышко от бледно-розового до пурпурного цвета размером до 5 мм; при надавливании или растягивании кожи (витропрессии) исчезает. Характерна для тифо-паратифозных заболеваний, брюшного тифа.
Пятно отличается от розеолы величиной (от 5 до 20 мм); в зависимости от размеров элементов различают мелкопятнистую (5—10 мм) и крупнопятнистую сыпь (более 10 мм); характерна для кори, краснухи, псевдотуберкулеза.
Эритема — обширные участки гиперемированной кожи, образовавшиеся при слиянии крупных пятен (корь, псевдотуберкулез, рожа, клещевые иксодовые боррелиозы).
Геморрагии — кровоизлияния в кожу различной величины от точечных (петехии) до более крупных (пурпура — от 2 до 5 мм; экхимоз — более 5 мм); характерны для геморрагических лихорадок, лептоспироза, менингококковой инфекции («звездчатая сыпь»), сыпного тифа (розеолезно-петехиальная сыпь).
Папула — мягкий плоский узелок (поверхностный инфильтрат), слегка возвышающийся над кожей, размером чаще от 3 до 5 мм (может быть чуть больше); часто сочетается с розеолой — розеолезно-папулезная сыпь (брюшной тиф и паратифы) или с пятном — пятнисто-папулезная сыпь (корь).
Бугорок (tuberculum) отличается от папулы наличием плотного образования в коже (узел, инфильтрат в глубоких слоях дермы), размером от 1 до 5 см, часто изъязвляется, оставляя рубец (кожный лейшманиоз).
Пузырек (vesicula) — ограниченная полость размером от 1 до 5 мм, заполненная прозрачной серозной или кровянистой жидкостью; часто превращается в пустулу (содержимое пузырька мутнеет — нагноение); может засыхать (корочка) или вскрываться (эрозия). Пузырьки после себя следа не оставляют; после пустул могут остаться рубчики. Наблюдаются при натуральной оспе.
Волдырь (urtica) — плотное, возвышающееся над кожей образование розового или белого цвета с красной каемкой; величиной от 5 мм до нескольких сантиметров; исчезает быстро и бесследно, поскольку представляет собой острый ограниченный отек кожи. Уртикарная сыпь характерна для сывороточной болезни.
Пузырь — полостное образование диаметром от 5 до 10 мм и более с серозным или серозно-геморрагическим содержимым. Наблюдается при рожистом воспалении кожи.
Из вторичных экзантем следует указать на шелушение, которое появляется при некоторых заболеваниях на месте сыпи. Различают отрубевидное (мельчайшие чешуйки), пластингатое (чешуйки размером 2—5 мм) и листовидное шелушение (чешуйки больше 5 мм). Листовидное шелушение наблюдается на ладонях и подошвах при скарлатине, псевдотуберкулезе.
Для дифференциальной диагностики важно не только определить характер экзантемы (ее отдельных элементов), но и установить время появления сыпи (день болезни), последовательность (этапность высыпания), преимущественную локализацию, количество элементов и динамику сыпи.
Помимо инфекционных экзантем на коже могут возникать и другие виды первичных поражений: очаговый некроз на месте присасывания клеща — переносчика клещевого риккетсиоза (первичный аффект), характерные язвы при кожных формах туляремии, лейшманиоза, содоку; сибиреязвенный карбункул; сапные абсцессы и другие.
Энантемы обнаруживаются на слизистой оболочке глаза и ротоглотки. Так, например, к ним относятся мелкие кровоизлияния (соответственно симптомы Киари-Авцына и Розенберга при сыпном тифе); мельчайшие очажки некроза эпителия слизистой оболочки щек (пятна Вельского—Филатова—Коплика при кори), образование везикул и затем эрозий на слизистой оболочке ротоглотки (при натуральной оспе, герпангине, ящуре). Важное диагностическое значение имеет состояние конъюнктивы глаз: гиперемия конъюнктив и инъекция сосудов склер (грипп, риккетсиозы, геморрагические лихорадки, корь); инъекция эписклеральных сосудов в виде треугольника с основанием к роговой оболочке (симптом Пика при лихорадке паппатачи). Резкий отек век с образованием на конъюнктиве фибринозных налетов (дифтерия глаза, пленчатый аденовирусный конъюнктивит). Для ряда инфекционных болезней диагностическое значение имеет состояние зева и небных миндалин (стрептококковая ангина, скарлатина, дифтерия, инфекционный мононуклеоз, ангина Симановского—Венсана и другие), поэтому фарингоскопия является обязательным компонентом при обследовании больного.
При осмотре небных миндалин отмечаются размеры, гиперемия, отечность, наличие фолликулов, гной в лакунах, фибринозные налеты, очаговые некрозы, рубцовые изменения, спаянность с передними дужками, казеозное содержимое в лакунах и т. п. Обращается внимание на распространение налетов за пределы миндалин (дифтерия). Собственно воспаление миндалин обозначается термином «тонзиллит», который как сидром характерен для многих инфекционных заболеваний (ангина, скарлатина, туляремия и др.).
При многих инфекционных болезнях отмечается поражение лимфатических узлов. Большое диагностическое значение имеют их размеры, консистенция, подвижность, болезненность, локализация по отношению к возможным входным воротам инфекции. Для одних заболеваний характерно увеличение отдельных лимфатических узлов (специфический лимфаденит), для других — множественное их поражение (системный полиаденит или полилимфаденопатия). Нередко наблюдается изменение ближайших к месту внедрения инфекции периферических лимфатических узлов (содоку, доброкачественный лимфоретикулез). Значительное увеличение отдельных лимфатических узлов носит название бубона (чума, туляремия). При обследовании таких больных отмечается локализация бубона (при чуме чаще бедренные и паховые, при туляремии — подмышечные и шейные), болезненность (резко болезненные при чуме, малоболезненные — при туляремии), подвижность (отсутствие подвижности связано с развитием периаденита и характерно для чумы), сроки нагноения бубона (при чуме — через неделю, при туляремии — через 3 нед.). Множественное поражение лимфоузлов характерно для бруцеллеза (микропо-лиаденит), токсоплазмоза, инфекционного мононуклеоза, ВИЧ-инфекции, листериоза (полилимфаденопатия). В некоторых случаях больше поражаются определенные группы лимфатических узлов, например заднешейные и затылочные при краснухе. Всегда следует учитывать возможность вторичного лимфаденита (регионарный углочелюстной при ангине, скарлатине, дифтерии). Своеобразным вариантом регионарного лимфаденита является мезаденит, который наблюдается при ряде инфекций с алиментарным путем инфицирования (брюшной тиф, паратифы, псевдотуберкулез, токсоплазмоз), а также поражение паратрахеальных и трахеобронхиальных лимфатических узлов при аэрогенном инфицировании (лихорадка Ку). Изолированное увеличение паховых лимфатических узлов типично для сифилиса. Необходимо иметь в виду, что распространенная лимфаденопатия встречается и при тяжелых заболеваниях неинфекционной природы (лейкозы, лимфогранулематоз, лимфосаркома и др.). Состояние опорно-двигательной системы имеет определенное значение для диагностики инфекционных болезней. Чаще наблюдается поражение мышц в виде миалгий (обусловлены синдромом общей интоксикации) или миозитов (характерны для лептоспироза, бруцеллеза, трихинеллеза). Локализация миозитов может быть различной. При лептоспирозе особенно часто поражаются
икроножные мышцы, а при энтеровирусной эпидемической миалгий — мышцы живота. При длительных миозитах в мышцах могут образовываться кальцификаты (токсоплазмоз, трихинеллез). Реже поражаются суставы, причем артриты могут рассматриваться как проявления инфекции (бруцеллез) и как осложнения (сальмонеллез, краснуха и др.).
Нарушения деятельности сердечно-сосудистой системы сходны при многих инфекционных болезнях и важны, в основном, для оценки тяжести и прогноза заболевания, однако имеют некоторое диагностическое значение. Так, например, большинству инфекций свойственна тахикардия (ангина, скарлатина, сальмонеллез, сыпной тиф, сибирская язва и т. д.). В то же время, при некоторых инфекционных заболеваниях учащение пульса не соответствует высоте лихорадки, как бы отстает от нее (напомним, что на каждый 1° С повышения температуры тела число сердечных сокращений увеличивается на 10). Это явление называется относительной брадикардией (брюшной тиф, паратифы, грипп, орнитоз, менингит). Для отдельных инфекций характерна абсолютная брадикардия (вирусные гепатиты, ботулизм); она наблюдается также у реконвалесцентов после инфекционных болезней. Миокардиты могут возникать с первых дней болезни (дифтерия) или в периоде реконвалесценции (орнитоз); иногда отмечается выраженная ломкость сосудов (скарлатина, корь).
Поражение органов дыхания наблюдается очень часто при различных инфекционных заболеваниях. Иногда преобладают изменения дыхательных путей; выделена даже целая группа острых респираторных заболеваний. В зависимости от этиологии могут преобладать поражения того или иного отдела респираторного тракта. На первый план могут выступать симптомы ринита (риновирусные заболевания), ринофарингита (аденовирусные болезни), ларингиты (парагрипп), трахеита (грипп), бронхита (респираторно-синтициаль-ная инфекция). Часто поражаются легкие (орнитоз, микоплазмоз, лихорадка Ку), иногда в виде тяжелой геморрагической пневмонии (легочные формы чумы и сибирской язвы). Могут быть поражения органов дыхания за счет паралича дыхательных мышц (ботулизм, полиомиелит). Наконец, пневмонии являются одним из наиболее частых осложнений при многих инфекционных болезнях (грипп, корь, брюшной тиф).
Поражение желудочно-кишечного тракта характерно для многих инфекционных болезней. Могут наблюдаться симптомы гастрита (отравление стафилококковым токсином), гастродуоденита (сальмонеллез), энтерита (холера), так называемый терминальный илеит (брюшной тиф, паратифы, псевдотуберкулез), энтероколит (эшерихиоз), колит (амебиаз, балантидиаз), дистальный колит (дизентерия). Вздутие живота (метеоризм), болезненность и громкое урчание при пальпации правой подвздошной области свойственны брюшному тифу (симптомы Падалки и Трусевича). Сюда же можно отнести характерные изменения языка: отечный, утолщенный с отпечатками зубов, покрытый грязно-бурым налетом — при брюшном тифе; ярко-красный с резко увеличенными сосочками — при скарлатине и псевдотуберкулезе («малиновый язык»); отечный, покрытый густым белым («меловым») налетом — при чуме.
Большое значение придается изменениям печени и селезенки. Увеличение этих паренхиматозных органов свидетельствует, как правило, о гематогенном распространении возбудителя и наблюдается при многих инфекционных болезнях. Небольшое увеличение печени и особенно селезенки можно определить перкуторно (печени — путем исследования по Курлову, селезенки — в положении больного на правом боку по Н. И. Рагозе). Следует обращать внимание на степень увеличения и плотность органов (значительное увеличение и плотность селезенки наблюдается при малярии, возвратном тифе, висцеральном лейшманиозе; мягкая селезенка — при сепсисе), а также на их болезненность (при вирусном гепатите).
При некоторых заболеваниях возникают характерные изменения в мочеполовых органах в виде поражения почек (лептоспироз, геморрагическая лихорадка с почечным синдромом), мочевого пузыря (шистосомоз). В качестве осложнений возникают орхиты (эпидемический паротит), самопроизвольные выкидыши (бруцеллез, токсоплазмоз).
Поражение центральной нервной системы может заключаться не только в симптомах общей интоксикации. Возможны серозный (эпидемический паротит, лептоспироз, орнитоз, энтеровирусные инфекции) или гнойный (менингококковая, пневмококковая, стафилококковая и стрептококковая инфекции, листериоз) менингиты, а также энцефалиты (первичные энцефалиты, корь, краснуха), миелит и поражение периферических нервов (бруцеллез), токсические параличи (ботулизм, дифтерия). Могут быть различные поражения глаз в виде иридоциклитов (лептоспироз, возвратные лихорадки), хориоретинитов (бруцеллез, токсоплазмоз), увеита (токсоплазмоз, менингококковая инфекция).
После детального сбора информации в процессе расспроса и осмотра больного необходимо проанализировать полученные данные. При этом следует стремиться к объединению отдельных симптомов в синдромы. Если симптом — это любой признак болезни, доступный определению независимо от метода, который для этого применялся, то синдром — это совокупность симптомов, объединенных общим патогенезом (интоксикационный, менингеальный, гепатолиенальный, колитический и т. д.). Поставить правильный диагноз на основании одного симптома удается крайне редко, лишь в том случае, когда этот симптом является патогномоничным, т. е. присущим только данной болезни и никакой другой. К сожалению, таких симптомов очень мало. Среди них нужно назвать пятна Вельского—Филатова—Коплика при кори, судорожный кашель с репризами при коклюше, опистотонус при столбняке, «водобоязнь» при бешенстве и некоторые другие.
При типичном течении инфекционного заболевания и наличии патогномоничных симптомов можно сразу установить нозологический диагноз.
Патогномонигные симптомы встречаются при следующих инфекционных заболеваниях:
- при кори — пятна Вельского—Филатова—Коплика;
- при менингококкцемии — звездчатые геморрагически-некротические высыпания с уплотнениями в центре;
- при натуральной оспе — появление в начальном периоде кореподобной или скарлатиноподобной транзиторной «раш-сыпи» своеобразной локализации;
- при герпетической инфекции — появление на коже мелких пузырьков, тесно примыкающих друг к другу, с локальным жжением и зудом;
- при герпангине энтеровирусной природы — появление мелких, не сливающихся пузырьков на слизистой оболочке задней стенки глотки и нёбных дужках;
— при лихорадке паппатачи — симптом Пика в виде выраженной инъекции склеральных сосудов в виде треугольников с основанием у наружного края глаза и верхушкой, обращенной к роговице;
— при столбняке — опистотонус;
— при бешенстве — пароксизмы гидрофобии;
— при коклюше — приступы судорожного кашля.
При отсутствии патогномоничных признаков в клинической картине руководствуются многочисленными опорными диагностигескими симптомами и синдромами инфекционных болезней [Соринсон С. Н., 1993]:
— при сыпном тифе — багрово-фиолетовые пятнышки на переходной складке конъюнктив (пятна Киари—Авцына) и точечные кровоизлияния у основания язычка (экзантема Розенберга);
— при брюшном тифе — скудные мономорфные розеолезные высыпания;
— при псевдотуберкулезе — симптомы «перчаток» и «носков» (гиперемия кистей и стоп);
— при скарлатине — обильная точечная сыпь на гиперемированном фоне;
— при тяжелых формах геморрагической лихорадки с почечным синдромом — кровоизлияния в конъюнктиву глаза;
— при гриппе — мелкая зернистость слизистой оболочки зева;
— при стрептококковой ангине — переднешейный углочелюстной лимфаденит при отсутствии полилимфаденопатии;
— при инфекционном мононуклеозе — полилимфаденопатия;
— при дизентерии — стул в виде «ректального плевка» (небольшой объем слизи, иногда с примесью крови);
— при сальмонеллезе — жидкий стул с зеленью;
— при холере — стул типа «рисового отвара»;
— при кишечном амебиазе — стул типа «малинового желе».
Оценка диагностического значения опорных признаков требует учета сроков их появления при разных инфекциях.
Выделение синдромов болезни имеет не только диагностическое, но и терапевтическое значение. Так, выделение синдромов неотложных (критических) состояний: инфекционно-токсический шок, инфекционно-токсическая энцефалопатия, острая печеночная недостаточность, острое обезвоживание организма и т. д. позволяют еще до установления нозологического диагноза начать осуществление неотложной помощи и интенсивной терапии, спасающих жизнь больному.
Как это ни парадоксально, но количество синдромов существенно меньше числа известных инфекционных болезней. Поэтому одни и те же синдромы могут быть представлены в клинической картине самых разных инфекций. В этой связи существует понятие о симптомокомплексе (синдромокомплексе). Симптомокомплекс — это сочетание патогенетически взаимосвязанных синдромов и симптомов, которое встречается при данной нозологической форме в абсолютном большинстве случаев (Шувалова Е. П.). Несмотря на высокую специфичность, симптомокомплекс конкретной болезни может быть различным в разные периоды заболевания. Например, при вирусном гепатите симптомокомплекс начального периода представляет собой сочетание интоксикации, диспепсического, артралгического и некоторых других синдромов, а в желтушном периоде главные проявления болезни обнаруживаются в форме симптомокомплекса, включающего синдром желтухи, гепатолиенальный. иногда синдром холестаза и т. д. Именно поэтому главными кирпичиками, из которых строится здание нозологического диагноза инфекционной болезни, являются клинико-патогенетические синдромы. Выделение их способствует систематизации клинического мышления, так как позволяет объяснить большое количество самых разнообразных симптомов, выявляемых у инфекционных больных, на основе единого принципа — общего патогенеза болезни. На основании анализа и сопоставления отдельных синдромов и симптомов, обнаруженных у больного, с аналогичными синдромами и симптомами, характерными для других, сходных по клинической картине болезней (дифференциальная диагностика), устанавливается нозологический диагноз болезни (Матковский В. С, Казанцев А. П.). Анализ клинических признаков проводится с обязательным учетом тяжести, периода и клинической формы болезни. Диагностика осуществляется на основании совокупности всех данных клинического обследования больного (включая данные анамнеза, в том числе эпидемиологического), а также результатов лабораторных и инструментальных методов исследования.
Из лабораторных методов исследования используется, прежде всего, анализ периферической крови. При некоторых болезнях развивается выраженная анемия (малярия, лейшманиоз, сепсис); может быть, наоборот, увеличение количества гемоглобина и числа эритроцитов за счет сгущения крови (холера, сальмонеллез). Для ряда бактериальных инфекционных болезней характерен лейкоцитоз (ангина, менингококковая инфекция, лептоспироз); большинство вирусных болезней протекает с лейкопенией (грипп, корь, вирусный гепатит). Могут быть характерные изменения лейкоцитарной формулы, например нейтропения и увеличение числа одноядерных элементов (инфекционный мононуклеоз), увеличение числа эозинофилов (псевдотуберкулез, трихинеллез) или плазматических клеток (краснуха).
Для диагностики используются также данные различных биохимических методов исследования. Например, для висцерального лейшманиоза характерна выраженная диспротеинемия. Иногда выявляется повышение активности сывороточных аминотрансфераз (вирусный гепатит, желтая лихорадка, дифтерийный миокардит), увеличение содержания билирубина (вирусный гепатит, лептоспироз, малярия), остаточного азота (геморрагическая лихорадка с почечным синдромом, лептоспироз), диастазы крови и мочи (эпидемический паротит).
Помимо этих и других неспецифических исследований в инфекционной клинике широко используются специфические лабораторные анализы: обнаружение, выделение и идентификация возбудителей, токсинов, антигенов, биологические пробы, серологические реакции, аллергические пробы и некоторые другие.
Возбудителей болезни можно обнаружить при некоторых болезнях простой микроскопией окрашенных или нативных препаратов (плазмодии малярии, лейшмании, амебы, балантидии, лямблии, спирохеты возвратного тифа). Для обнаружения возбудителей широко используется иммунофлюоресцентный метод. С помощью этого метода можно обнаружить вирус гриппа и возбудителей других ОРЗ в слизи из ротоглотки; вирусы оспы в материале, взятом из везикул и пустул; возбудителей сибирской язвы в материале из кожных поражений; косвенно судить о наличии боррелий в организме больного при клещевом иксодовом боррелиозе по непрямой реакции иммунофлюоресценции. Для экспресс-диагностики используются реакции коагглютинации, латекс-агглютинации, агрегатагглютинации (АГА), РИГА с иммуноглобулиновыми диагностикумами. Иногда приходится предварительно «подращивать» возбудителей в питательных средах (сальмонеллы, микоплазмы) или культурах тканей (вирусы). Метод ценен тем, что позволяет значительно сократить сроки проведения исследования. В ряде случаев используют обнаружение токсинов в крови (ботулотоксин, дифтерийный токсин), в содержимом желудка или остатках пищи (ботулотоксин, энтеротоксин стафилококка). Диагностическое значение может иметь обнаружение антигенов, например антигена сибиреязвенной палочки и материале из кожных поражений больного или HBsAg («австралийский антиген») в сыворотке крови больных вирусным гепатитом В. В последние годы появились новые высокоинформативные методы обнаружения возбудителей и их антигенов — это метод ДНК-зондов, полимеразная цепная реакция (ПЦР), позволяющая идентифицировать ничтожно малое количество патогена (десятки в пробе) за счет копирования его in vitro (вирусные гепатиты В, С; ВИЧ-инфекция и любые другие инфекционные заболевания, для которых имеются праймеры). Эти методы позволяют производить не только качественную, но и количественную оценку возбудителя (например, определять так называемую вирусную нагрузку — количество РНК вирусов в крови при ВИЧ-инфекции и гепатите С). Это имеет значение не только для диагностики, но и для оценки эффективности проводимой терапии. Внедряются методы генотипирования возбудителя (в первую очередь вирусов). В диагностике получил распространение высокоспецифичный метод использования моноклональных антител.
Широко используется классический бактериологический метод выделения и идентификации возбудителя в различных материалах, взятых от больного (кровь, спинномозговая жидкость, пунктаты и биоптаты органов, рвотные массы, отделяемое из язв, смывы со слизистых оболочек и др.). Для посева используются различные питательные среды (выделение бактерий, микоплазм) или культуры тканей (выделение вирусов, хламидий, риккетсий). Следует учитывать, что выделить возбудителя удается далеко не у всех больных, поэтому отрицательный результат не исключает возможности предполагаемой инфекционной болезни. Иногда выделение возбудителя является бесспорным подтверждением диагноза (менингококк из спинномозговой жидкости, брюшнотифозная палочка из крови), в других случаях это может быть и бактерионосительство (брюшнотифозная палочка в испражнениях). Для выделения возбудителей может использоваться биологическая проба на животных. Используется реакция нейтрализации в опытах на животных (энтеровирусные болезни, ботулизм) или на культурах тканей (оспа). Иногда при заражении животных выявляются специфические поражения (скротальный феномен у морских свинок при сапе). Для бактериологических исследований важно взятие материала до начала этиотропной терапии.
Серологические методы исследования не утратили своего значения в диагностике инфекционных болезней. Напротив, именно они являются строго специфичными. Помимо классических реакций агглютинации (РА), связывания комплемента (РСК), непрямой гемагглютинации (РИГА), реакции задержки или торможения гемагглютинации (РЗГА или РТГА), преципитации, нейтрализации, применяются высокочувствительные радиоиммунный (РИА) и иммуноферментный (ИФА) анализ, метод иммунного блоттинга (ИБ), позволяющий, например, выявлять антитела даже к отдельным белкам ретровирусов (при ВИЧ-инфекции). Однако при оценке всех серологических реакций надо учитывать ряд обстоятельств. Прежде всего, антитела появляются при острых инфекциях лишь с 5—7-го дня болезни и для ранней диагностики эти методы непригодны.
В результате широкого распространения некоторых инфекций антитела к их возбудителям часто выявляются у здоровых лиц (грипп, аденовирусные заболевания, парагрипп, микоплазмоз, корь, эпидемический паротит и др.). В этих случаях диагностическое значение может иметь только нарастание титра антител (в 4 раза и более) в ходе болезни. Для этой цели берут парные сыворотки (первая — до 5—7-го дня болезни, вторая — спустя 10—14 дней). В случае выделения от больного возбудителя для доказательства его этиологической роли не следует забывать о возможности постановки реакции агглютинации с аутокультурой. Значительно меньшее диагностическое значение имеют неспецифические серологические методы (например, реакция гетероагглютинации при инфекционном мононуклеозе или холодовая агглютинация при микоплазмозе).
Аллергические пробы применяют в диагностике тех инфекций, при которых наступает значительная аллергическая перестройка организма (бруцеллез, токсоплазмоз, туляремия, туберкулез). Проба очень проста — внутрикожно вводят 0,1 мл специфического аллергена и через 24 и 48 ч учитывают результаты реакции. Она характеризуется местными изменениями в виде гиперемии и инфильтрации кожи (обычно до 1 см и более), регионарным лимфаденитом и общей реакцией (повышение температуры тела). Положительной проба становится не ранее 5-7-го дня болезни.
Значительное место в диагностике инфекционных заболеваний занимают современные инструментальные методы исследования (эндоскопические, радиоизотопные, ультразвуковые, гистологические в сочетании с биопсией различных органов и тканей, рентгенологические — компьютерная томография, магниторезонансная томография и др.).
ПРИНЦИПЫ ТЕРАПИИ ИНФЕКЦИОННЫХ БОЛЬНЫХ
Общими принципами терапии инфекционных больных являются раннее начало лечения, его индивидуализированность и комплексность.
Принцип как можно более раннего начала лечения не требует пояснения. Однако следует заметить, что даже при отсутствии точного диагноза лечение должно немедленно начинаться, исходя из наиболее вероятной диагностической гипотезы. При острых инфекциях это в ряде случаев определяет прогноз жизни или смерти больного, а у оставшихся в живых — степень и сроки выздоровления, а также вероятность развития затяжных и хронических форм болезни.
Принцип индивидуализированности терапии предполагает необходимость в каждом конкретном случае стремиться к назначению лечения, соответствующего возможно более полному индивидуальному диагнозу. Целесообразно, чтобы такой индивидуальный диагноз включал в себя как нозологический (этиология и клиническая форма), так и патогенетический диагноз (патогенез и тяжесть состояния больного с учетом физиологических особенностей его организма, периода болезни, возможных осложнений и сопутствующих заболеваний). К сожалению, нередко врачи вынуждены ограничиваться синдромальным диагнозом. Эта вынужденная мера обусловлена в значительной степени несовершенством лабораторной и, прежде всего, микробиологической базы.
Принцип комплексности терапии является ведущим. В соответствии с ним рациональное лечение инфекционных больных предполагает влияние на все составляющие инфекционного процесса, а конкретными направлениями терапии должны быть одновременные воздействия на возбудителя болезни и его токсины, на реактивность макроорганизма (повышение защитных сил), и на отдельные звенья патогенеза.
Разделение лечебных мероприятий на этиотропную, патогенетическую и симптоматическую терапию имеет условный характер, ибо терапия больного является единой, где все виды лечения тесно переплетаются. Нельзя противопоставлять этиотропную и патогенетическую терапию. Так, воздействие на возбудителя и его токсины, что ранее определялось как этиотропная терапия, включавшая, главным образом, антибактериальное, противовирусное и антипаразитарное лечение, в настоящее время следует рассматривать значительно шире. Например, ряд методов эфферентной терапии с полным основанием можно относить к этому направлению лечения, поскольку оно предусматривает связывание и удаление не только микробных токсинов, но и самих бактерий и вирусов. Аналогично иммунотерапия в ряде случаев может и должна рассматриваться в этом же аспекте, например, использование специфических сывороток и иммуноглобулинов при некоторых экзотоксических инфекционных заболеваниях - дифтерия, ботулизм и др.
Комплексность терапии не означает, что нужно применять как можно большее число препаратов. Для лечения каждого конкретного больного выбирают только необходимые лекарственные средства и лечебные процедуры. Полипрагмазия (множественные медикаменты) не менее вредна, чем примитивное представление о том, что при лечении инфекционных больных можно ограничиться только назначением антибиотиков.
