- •Фогель ф., Мотульски а. Генетика человека: в 3-х т. Т. 1: Пер. С англ. – м.: Мир, 1989. – 312 с.
- •Ф. Фогель, а.Мотульски генетика человека
- •Фогель ф., Мотульски а. Генетика человека: в 3-х т. Т. 1: Пер. С англ. – м.: Мир, 1989. – 312 с.
- •Предисловие редакторов перевода
- •Предисловие ко второму изданию
- •Предисловие к первому изданию
- •Введение
- •1. История генетики человека
- •1.1. Греки
- •1.2. Ученые до Менделя и Гальтона
- •1.3. Работа Гальтона «Наследование таланта и характера» [248]
- •1.4. Работа Грегора Менделя [266]
- •1.5. Прикладные исследования применительно к человеку: «врожденные ошибки метаболизма» по Гэрроду
- •1.6. Видимые носители генетической информации: первые исследования хромосом
- •1.7. Первые достижения в области генетики человека
- •1.7.1. Группы крови аво
- •1.7.2. Закон Харди-Вайнберга
- •1.7.3. Достижения генетики человека в период 1910-1930 гг.
- •1.8. Генетика человека, евгеника и политика
- •1.8.1. Великобритания и сша [236; 246; 256; 263; 283]
- •1.8.2. Германия [250; 236а]
- •1.8.3. Советский Союз [246, 250]
- •1.8.4. Генетика поведения человека
- •1.9. Развитие медицинской генетики (с 50-х гг. По настоящее время)
- •1.9.1. Генетическая эпидемиология
- •1.9.2. Биохимические методы
- •1.9.3. Индивидуальные биохимические различия
- •1.9.4. Цитогенетика, генетика соматических клеток, пренатальная диагностика
- •1.9.5. Методы исследования днк в медицинской генетике
- •1.9.6. Нерешенные проблемы
- •2. Хромосомы человека
- •2.1. Цитогенетика человека – запоздалое, но счастливое рождение
- •2.1.1. История развития цитогенетики человека
- •2.1.2. Нормальный кариотип человека в митозе и мейозе
- •2.1.2.1. Митоз
- •2.1.2.2. Приготовление и окрашивание препаратов метафазных хромосом [201; 88; 406]
- •2.1.2.3. Нормальный кариотип человека в метафазе митоза
- •2.1.2.4. Мейоз
- •2.2. Хромосомные заболевания человека
- •2.2.1. Синдромы, связанные с аномалиями числа хромосом
- •2.2.2. Синдромы, связанные со структурными аномалиями аутосом
- •2.2.2.1. Кариотипы u клинические синдромы
- •2.2.2.2. Сегрегация и пренатальная селекция транслокаций: методологические аспекты
- •2.2.3. Половые хромосомы
- •2.2.3.1. Первые наблюдения
- •2.2.3.3. Дозовая компенсация х-хромосомы млекопитающих [357]
- •2.2.4. Хромосомные аберрации и спонтанные аборты [413]
- •2.3. Организация генетического материала в хромосомах человека
- •2.3.1. Структура хроматина
- •2.3.1.1. Уникальная и повторяющаяся днк
- •2.3.1.2. Гетерохроматин
- •2.3.1.3. Нуклеосомная структура хроматина [1172; 427]
- •2.3.1.4. Интеграция хроматиновых волокон в хромосомную структуру
- •2.3.1.5. Интегральная модель структуры хромосомы
- •2.3.2. Генетический код
- •2.3.3. Тонкая структура генов человека: «Новая генетика»
- •2.3.3.1. Анализ гена человека
- •2.3.3.2. Рестрикционные эндонуклеазы
- •2.3.3.3. Гибридизация нуклеиновых кислот
- •2.3.3.4. Секвенирование днк [117; 122; 381]
- •2.3.3.5. Сортировка хромосом при помощи цитофлуорометрии
- •2.3.3.6. Анализ β-глобинового гена и обобщение опыта исследования одного гена.
- •2.3.3.7. Структура гена фактора VIII (антигемофилический фактор)
- •2.3.3.8. Семейства генов
- •2.3.3.9. Полиморфизм сайтов рестрикции [548; 507; 505]
- •2.3.4. Динамичность генома
- •2.3.5. Геном митохондрий
- •2.3.6. Новая генетика и концепция гена
- •3. Формальная генетика человека
- •3.1. Менделевские типы наследования и их приложение к человеку
- •3.1.1. Кодоминантный тип наследования
- •3.1.2. Аутосомно-доминантиый тип наследования
- •3.1.3. Аутосомно-рецессивный тип наследования
- •3.1.5. Родословные, не соответствующие простым типам наследования
- •3.1.6. «Летальные факторы» [696]
- •3.1.7. Гены-модификаторы
- •3.1.8. Количество известных заболеваний человека с простым типом наследования
- •3.2. Закон Харди—Вайнберга и его приложения
- •3.2.1. Формулировка и вывод закона
- •3.2.2. Соотношения Харди—Вайнберга доказывают генетическую основу групп крови системы аво
- •3.2.3 Генные частоты
- •3.3 Статистические методы формальной генетики: анализ сегрегационных отношений
- •3.3.1. Сегрегационные отношения как вероятности
- •3.3.2. Простые вероятностные проблемы в генетике человека
- •3.3.3. Тестирование сегрегационных отношений в отсутствие смещений, связанных с регистрацией: ко доминантное наследование
- •3.3.4. Тестирование сегрегационных отношений: редкие признаки
- •3.3.5. Дискриминация клиникогенетических вариантов: генетическая гетерогенность
- •3.3.6. Заболевания со сложным типом наследования
- •3.4. Сцепление: локализация генов на хромосомах
- •3.4.1. Классические подходы в экспериментальной генетике: эксперименты по скрещиванию и гигантские хромосомы
- •3.4.3. Анализ сцепления у человека: гибридизация клеток и днк-технология
- •3.5. Тесно сцепленные и функционально родственные гены
- •3.5.1. Некоторые примеры из экспериментальной генетики
- •3.5.2. Некоторые особенности генетической карты человека
- •3.5.3. Почему существуют кластеры генов?
- •3.5.4. Группы крови: Rh-комплекс, неравновесие по сцеплению
- •3.5.5. Главный комплекс гистосовместимости (мнс) [193; 188]
- •3.5.6. Генетическая детерминация мимикрии у бабочек
- •3.5.7. Гены х-хромосомы человека, имеющие родственные функции
- •3.5.8. Неравный кроссинговер
- •3.6. Условия и ограничения генетического анализа у человека: мультифакториальное наследование
- •3.6.1. Уровни генетического анализа
- •3.6.1.1. Генный уровень
- •3.6.1.2. Анализ продукта гена: биохимический уровень
- •3.6.1.3. Качественный феногенетический анализ: простые типы наследования
- •3.6.1.4. Генетический анализ на уровне количественного фенотипа – биометрический уровень
- •3.6.1.5. Концепция наследуемости
- •3.6.1.6. Один пример: рост
- •3.6.1.7. Количественная генетика; концепции Менделя и Гальтона
- •3.6.2. Мультифакториальное наследование в комбинации с пороговым эффектом
- •3.6.2.1. Описание модели: эксперименты на животных
- •3.6.2.2. Простая теоретическая модель
- •3.6.2.3. Как нужно использовать модель для анализа данных [925]?
- •3.6.2.4. Какой вывод следует сделать, если статистический анализ не дает четкого ответа?
- •3.6.2.5. Индуцированные радиацией доминантные мутации у мыши: мутации главных генов, не выявленные у человека
- •3.6.2.6. Идентификация элементарных клинико-генетических вариантов моногенного наследования с использованием дополнительных фенотипических критериев
- •3.6.2.7. Как анализировать мулыпифакториальный признак, если отдельные формы с простыми типами наследования выделить нельзя?
- •3.7. Генетический полиморфизм и патология
- •3.7.1. Новая стратегия исследований
- •3.7.2. Ассоциация заболеваний с группами крови
- •3.7.2.1. Система аво
- •3.7.2.2. Kell-система
- •3.7.3. Система hla и заболевания [888, 207а]
- •3.7.4. Полиморфизм α1-антитрипсина и патология [749, 653]
- •3.8. Концепция: природа - воспитание. Близнецовый метод
- •3.8.1. Исторические замечания
- •3.8.2. Исходная концепция
- •3.8.3. Биология близнецовости
- •3.8.4. Ограничения близнецового метода
- •3.8.5. Диагностика зиготности
- •3.8.6. Применение близнецового метода для анализа альтернативных признаков
- •3.8.7. Пример: проказа в Индии
- •3.8.8. Близнецовые исследования других широко распространенных заболеваний
- •3.8.9. Близнецовый метод в изучении признаков с непрерывным распределением
- •3.8.10. Значения оценок наследуемости: данные по росту
- •3.8.11. Метод близнецовых семей [768; 732]
- •3.8.12. Метод контроля по партнеру [680]
- •3.8.13. Вклад генетики человека в теорию болезней [923]
- •3.8.14. Современное представление о генетике широко распространенных болезней [808, 810]
- •3.8.14.1. Биологические и патофизиологические подходы к генетической этиологии широко распространенных заболеваний
- •3.8.14.2. Генетика ишемической болезни сердца (ибс) [847; 827; 570]
- •Ассоциации ишемической болезни сердца с генетическими маркерами [570, 801]
- •Оглавление
- •Электронное оглавление
- •1. История генетики человека 20
- •2. Хромосомы человека 35
- •3. Формальная генетика человека 151
3.5.8. Неравный кроссинговер
Открытие неравного кроссинговера. В первые годы работы с дрозофилой некоторые авторы обратили внимание на то, что мутация Bar (Х-сцепленный доминантный признак) иногда ревертировала к нормальному фенотипу. Гомозиготы по этому аллелю давали потомство, несущее новый аллель, позже названный «двойной Bar», с еще более выраженным эффектом. Стертевант (1925) [904] показал, что такое необычное поведение было следствием не точковых мутаций, а неравного кроссинговера, приводящего к появлению хромосомы с двумя локусами Bar (двойной Bar) и одновременно хромосомы вовсе без этого локуса. Когда методика работы с гигантскими хромосомами слюнных желез дрозофилы позволила визуально проверять генетические гипотезы, Бриджесу (1936) [588] удалось показать, что простая доминантная мутация Bar была вызвана дупликацией хромосомного диска. Реверсия соответствует недушшцированному состоянию, тогда как двойной Bar вызывается трипликацией этого диска. Как реверсия, так и трипликация порождаются одним-единственным событием неравного кроссинговера. Тем не менее Бриджес не сформулировал четко причину этого события, по его мнению, она заключается в ошибочном спаривании «структурно-гомологичных», а не «позиционно-гомологичных» хромосомных сайтов (рис. 3.43, 2.97).
Неравный кроссинговер в генетике человека. Гаптоглобин- транспортный белок для гемоглобина, содержащийся в сыворотке крови [584а]. Наиболее распространенные в популяции аллели обозначаются HP1F, HP1S и HP2. В 1962 г. было обнаружено [884], что аллель HP2, судя по первичной структуре соответствующей полипептидной цепи, почти вдвое длиннее каждого из двух аллелей HP1F и HP1S. В НР2-цепи аминокислотная последовательность НР1цепи повторяется почти полностью. Авторы сделали вывод о том, что аллель HP2 возник в результате генной дупликации. Кроме того, они предсказали, что существует относительно высокая вероятность
|
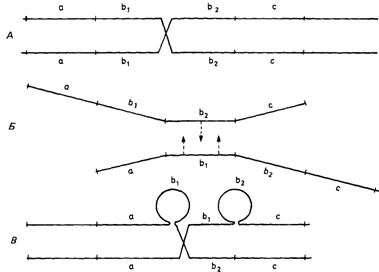
Рис. 3.43. Принцип неравного кроссинговера. А. Нормальное спаривание и кроссинговер. Предполагается, что два гена b1 и b2 имеют одинаковые последовательности ДНК. Б. Гены b1 и b2 спариваются. Это ведет к сдвигу двух гомологичных хромосом относительно друг друга. В. Такое спаривание возможно при образовании двух петель на одной из хромосом. |
228 3. Формальная генетика человека
|
Рис. 3.44. Неравный кроссинговер между генами, гомологичными по структуре, но негомологичными по положению. А. Неравный кроссинговер всегда будет приводить к одному кроссоверу с дупликацией гена b (b1b или bb2) и одному кроссоверу только с одним геном. Б. Формирование тандемно-полиаллельной последовательности становится возможным, если первичная дупликация гомозиготна. В этом случае возможно образование участка хромосомы с тремя аллелями [748]. |
повторного неравного кроссинговера между НР2-аллелями, что должно привести к появлению, с одной стороны, аллеля, подобного HP1, а с другой – аллеля, содержащего почти утроенную генетическую информацию. Последующие кроссинговеры между такими аллелями могут привести к образованию еще более протяженных генов и, следовательно, к полиморфизму в популяции по длине аллелей.
Имеется существенное различие между первым уникальным событием, в результате которого образуется ген почти вдвое длиннее обычного (например, HP2) из единичного гена HP1, и неравным, но гомологичным кроссинговером, который становится возможным, как только в популяции появится дуплицированный аллель [748].
Первое событие. Пусть имеется пара гомологичных хромосом, причем оба партнера содержат протяженные идентичные нуклеотидные последовательности. В норме эти партнеры спариваются в мейозе, и неравный кроссинговер не может произойти. Чтобы вызвать ошибочное спаривание и тем самым неравный кроссинговер, необходима исходная дупликация по крайней мере одного гена. В цитогенетике известны механизмы такой дупликации, простейший из которых - два разрыва в немного смещенных (один относительно другого) сайтах в конъюгирующих гомологичных хроматидах во время мейоза и последующее перекрестное воссоединение. Другой механизм – это ошибочное спаривание вследствие гомологии коротких нуклеотидных последовательностей в негомологичных положениях. По современным представлениям структура последовательностей ДНК между транскрибируемыми участками генов (разд. 2.3) допускает много разных возмож-
3. Формальная генетика человека 229
ностей для такого ошибочного спаривания. Если сайты разрыва отстоят только на длину одного структурного гена, то результатом этого события будут четыре гаметы: две, вовсе не содержащие данный ген, и две другие, содержащие его в дуплицированном виде (рис. 3.44). Гаметы, содержащие делецию, с высокой вероятностью могут утратиться вследствие гибели эмбриона. С другой стороны, гамета с дупликацией приведет к появлению диплоидного индивида, у которого в мейозе возможно ошибочное спаривание гомологичных цистронов и, следовательно, неравный кроссинговер.
Последствия неравного кроссинговера. Последствия показаны на рис. 3.44. Пока дупликация остается гетерозиготной, все гаметы будут содержать либо одну, либо две копии дуплицированного гена. Однако, когда дупликация становится гомозиготной, возникают другие типы гамет. В результате неравного кроссинговера могут образоваться, с одной стороны, гаметы с единственной копией, а с другой - гаметы, содержащие три, а в последующих поколениях и большее число копий данного гена (рис. 3.44, 3.45). Если вероятность неравного кроссинговера не слишком мала, то довольно быстро создается высокая изменчивость по числу гомологичных хромосомных сегментов, которые, оставаясь сходными по первичной структуре, различаются по положению. Если отбор благоприятствует определенному числу таких хромосомных сегментов, то вскоре это число станет наиболее распространенным. Затухание отбора приведет к увеличению изменчивости в обоих направлениях. Постепенно увеличится доля идивидов как с очень высоким, так и с небольшим числом таких генов [748]. Другой генетический механизм, сходный в некоторых аспектах с неравным кроссинговером, - это генная конверсия, в результате которой образуются нереципрокные продукты (разд. 2.3, рис. 2.97).
Возможное значение в генетике человека. Как уже упоминалось, гаптоглобиновый аллель HP2 представляет собой почти полностью дуплицированный HP1-аллель. В этом случае неравный кроссинговер, как ожидается, приводит иногда к появлению аллелей, содержащих утроенную информацию. Такие аллели на самом деле иногда наблюдались. Они известны как аллели типа Джонсона [883].
Другим примером могут служить тесно сцепленные глобиновые β- и δ-цистроны (разд. 4.3). В этом случае неравный кроссинговер может породить мутанты типа Лепоре (рис. 4.51), а также Х-сцешгенные гены цветоощущения [825а]. Кроме того, имеется много примеров умеренно и высокоповторяющихся последовательностей ДНК, внутри которых возможен неравный кроссинговер. Гены рибосомных РНК, локализованные внутри районов ядрышкового организатора, имеют около 300-400 идентичных копий с заметной вариацией. На первый взгляд такая ситуация обеспечивает наилучшие условия для неравного кроссинговера. Однако эти гены локализованы близко к центромере акроцентрических хромосом, где кроссинговер вряд ли происходит.
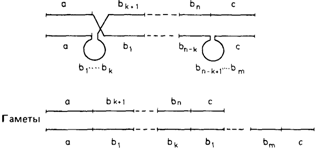
Рис. 3.45. Последствия неравного кроссинговера. В последовательных поколениях могут формироваться хромосомы с неограниченным (теоретически) числом тандемно расположенных аллелей. Неравный кроссинговер между любыми из них может привести к еще более длинным (или более коротким) гаплотипам. b1 ... bk ... bn относятся к гомологичным генам. |
|
230 3. Формальная генетика человека
Остаются нерешенными вопросы, может ли вообще происходить кроссинговер в дистальных районах акроцентрических хромосом и не является ли акроцентрическая локализация защитным механизмом против отклонения от оптимального количества рРНК-генов за счет неравного кроссинговера? Гены, кодирующие иммуноглобулины (разд. 4.4), также являются повторяющимися последовательностями ДНК. Чем больше мы узнаем о функциональном значении повторяющихся последовательностей ДНК, тем лучше будем понимать роль неравного кроссинговера.
Внутрихромосомный неравный кроссинговер. У структурно-гомологичных (но не позиционно-гомологичных) генов, таких, как найденные в мультигенных семействах (разд. 2.3.3.8), неравный кроссинговер происходит не только между гомологичными хромосомами, но также между сестринскими хроматидами (внутрихромосомный неравный кроссинговер). Теоретические рассуждения показывают, что этот процесс мог сыграть определенную роль в молекулярной эволюции [1941].