
- •1. Зміст дисципліни
- •2. Загальна характеристика металів та розвиток науки про них
- •Розділ 1.1 виробництво чавуну
- •1.1.1. Вогнетривкі матеріали
- •1.1.3. Залізні та марганцеві руди
- •1.1.4. Флюси
- •1.1.5. Підготовка залізних руд до плавлення
- •1.1.6. Будова доменної печі та її допоміжних агрегатів
- •1.1.7. Доменний процес
- •1.1.8. Продукти доменного виробництва
- •1.1.9.Техніко-економічні показники виробництва чавуну
- •1.2.1. Суть процесу
- •1.2.3. Виробництво сталі в кисневих конвертерах
- •1.2.4. Техніко-економічні показники виробництва сталі в кисневих конвертерах
- •1.2.5. Виробництво сталі в електропечах
- •Розділ 1.3 розливання сталі
- •1.3.1. Розливання сталі у виливниці
- •1.3.2. Будова сталевого зливка
- •1.3.3. Безперервне розливання сталі
- •1.3.4. Рафінування сталі поза межами виплавлювального агрегату
- •1.4.1. Руди алюмінію
- •1.4.2. Виробництво глинозему
- •1.4.3. Електроліз глинозему
- •1.4.4. Рафінування алюмінію
- •Розділ 1.5 металургія міді
- •1.5.1. Руди міді
- •1.5.2. Збагачення мідних руд
- •1.5.3. Випалювання мідних руд
- •1.5.4. Отримання мідного штейну
- •1.5.5. Отримання чорнової міді
- •1.5.6. Вогняне рафінування чорнової міді
- •1.5.7. Електролітичне рафінування міді
- •Розділ 1.6 виробництво титану
- •1.6.1. Руди титану
- •1.6.2. Отримання титанового шлаку
- •1.6.3. Отримання чотирихлористого титану
- •1.6.4. Відновлення титану
- •1.6.5. Отримання зливків титану
- •Матеріалознавство
- •2.1.1. Класифікація металів
- •2.1.2. Електронна будова атома та періодична система елементів
- •2.1.3. Типи міжатомних зв'язків у твердих тілах
- •2.1.4. Кристалічна будова металів
- •2.1.5. Дефекти кристалічної будови
- •2.1.5.1. Точкові дефекти
- •2.1.5.2. Лінійні дефекти
- •2.1.5.3. Поверхневі дефекти
- •2.1.5.4. Об'ємні дефекти
- •Розділ 2.2 кристалізація металів
- •2.2.1. Енергетичні умови процесу кристалізації
- •2.2.2. Механізм кристалізації
- •2.2.3. Кінетика кристалізації
- •2.2.4. Поліморфні перетворення
- •Розділ 2.3
- •2.3.1. Поняття про напруження
- •2.3.2. Пружна і пластична деформації металів
- •2.3.3. Наклеп
- •2.3.4. Відмова
- •2.3.5. Рекристалізація
- •2.3.6. Механічні властивості металів
- •2.3.6.2. Пластичність
- •2.3.6.3. Твердість
- •2.3.6.4. Ударна в'язкість
- •2.4.1. Сплави
- •2.4.2. Поняття про діаграми стану
- •2.4.3. Правило фаз
- •2.4.4. Діаграма стану сплавів, компоненти яких утворюють необмежені тверді розчини
- •2.4.5. Правило відрізків
- •2.4.6. Діаграма стану сплавів, компоненти яких утворюють обмежені тверді розчини та евтектику
- •2А.7. Діаграма стану сплавів з перитектичним перетворенням
- •2.4.8. Діаграма стану сплавів з утворенням хімічної сполуки
- •2.4.9. Про зв'язок властивостей сплаву з типом діаграми
- •Розділ 2.5 залізовуглецеві сплави
- •2.5.1. Компоненти залізовуглецевих сплавів
- •2.5.2. Фази системи залізо-вуглець
- •2.5.3. Діаграма стану залізо-вуглець
- •Розділ 2.6 вуглецеві сталі
- •2.6.1. Вплив вуглецю
- •2.6.2. Вплив постійних домішок на властивості сталі
- •2.6.3. Класифікація вуглецевих сталей
- •2.6.3.1. Сталі звичайної якості
- •Розділ 2.7 чавуни
- •2.7.1. Білі чавуни
- •2.7.2. Графітизація чавунів
- •2.7.3. Діаграма стану залізо-графіт
- •2.7.4. Вплив домішок і швидкості охолодження на структуру та властивості чавунів
- •2.7.5. Чавуни з пластинчастим графітом (сірі чавуни)
1.4.1. Руди алюмінію
У чистому вигляді алюміній у природі не існує через свою високу хімічну активність. Сполуки алюмінію входять до складу близько 250 мінералів. До найпоширеніших руд алюмінію належать боксити, нефеліни, алуніти й каоліни.
Боксити — найважливіші із руд алюмінію. За зовнішнім виглядом боксити — це глиноподібна, часто кам'яниста порода від білого до темно-червоного кольору. Свою назву боксити отримали від французького міста Бо, де є їх великі поклади. У бокситах алюміній перебуває у вигляді глинозему А1203, гідроксидів А1(ОН)3 і АЮ(ОН) та каолініту Al2Cy2Si02 -2H20. До складу бокситів входить ЗО... 70 % глинозему (в перерахунку з гідроксидів). Якість бокситів прямо пропорційно залежить від вмісту кремнезему.
Промислове значення мають алуніти K2SCyAl2(S()4)3-4Al(OH)3 і нефеліни (К, Na)20 Al2Cy Si02. Нефеліни є побічним продуктом у виробництві мінеральних добрив, наприклад апатитів.
Виробництво алюмінію має три основні стадії: отримання глинозему з руди, електроліз глинозему та рафінування алюмінію.
1.4.2. Виробництво глинозему
Найпоширеніший лужний спосіб виробництва глинозему, який складається з таких операцій:
Подрібнення руди (переважно бокситу) на дробарках з подальшим мокрим меленням у кульових млинах.
Вилуговування бокситу у водяному розчині лугу NaOH в автоклавах при температурі 230...250 °С, під тиском 2,5... 5,0 МПа з метою отримання алюмінату натрію. Для нагрівання використовують водяну пару. В автоклаві відбуваються такі реакції:
2А1(ОН)3 + 2NaOH = Na20 -А1203 + 4Н20, (1.4.1)
2А10(ОН) + 2NaOH = Na20 -A1208 + 2Н20. (1.4.2)
Утворений під час реакцій алюмінат натрію Na,0 A1203 добре розчиняється у воді й переходить у розчин, а нерозчинні в
 лузі
оксиди заліза й титану випадають в осад.
Кремнезем Si02,
що
входить до складу бокситу, також
розчиняється лугом з утворенням
силікату натрію Na2Si03,
який реагує з алюмінатом натрію й
водою, утворюючи Na20
-Al203-2Si02-
лН20,
що теж випадає в осад. Тому зі
збільшенням Si02
в
бокситі зменшується частка глинозему,
що потрапляє в розчин.
лузі
оксиди заліза й титану випадають в осад.
Кремнезем Si02,
що
входить до складу бокситу, також
розчиняється лугом з утворенням
силікату натрію Na2Si03,
який реагує з алюмінатом натрію й
водою, утворюючи Na20
-Al203-2Si02-
лН20,
що теж випадає в осад. Тому зі
збільшенням Si02
в
бокситі зменшується частка глинозему,
що потрапляє в розчин.
Відокремлення від осаду водяного розчину алюмінату натрію шляхом відстоювання й подальшого фільтрування.
Розкладання (викручування) пересиченого водяного розчину алюмінату натрію в спеціальних апаратах, в яких під час повільного перемішування виділяється кристалічний А1(ОН)3:
Na20 А1203 + 4Н20 = 2NaOH + 2А1(ОН)3. (1.4.3)
Під час розкладання, яке триває 75...90 год, в осад випадає гідроксид алюмінію А1(ОН)3.
Вилучення з розчину кристалів А1(ОН)3 в гідроциклонах і вакуум-фільтрах.
Зневоднювання гідроксиду алюмінію в обертальних печах і поступове його нагрівання до температури 1200 °С, щоб отримати А1203:
2А1(ОН)3 = А1203 + ЗН20. (1-4.4)
1.4.3. Електроліз глинозему
Для виробництва алюмінію використовують глинозем, кріоліт і вугільні аноди. Ванна для електролізу глинозему складається зі сталевого кожуха 2 (рис. 1.4.2), викладеного футерів-кою 11 із шамотної цегли, вугільних стін 3, вугільного поду /, до якого підведені катодні шини 12. Бічні вугільні стіни разом з подом утворюють ванну глибиною 400...600 мм. У ванні перебувають глинозем, кріоліт і рідкий алюміній. Розташований угорі анод 6 являє собою напіврідку масу 7 в алюмінієвому кожусі 10, яка складається з меленого коксу або вугілля та кам'яновугільної смоли. Ця маса, починаючи знизу, поступово спікається та коксується. До штирів 9 анода підведені шини 8.
Ванну завантажують глиноземом А1203у кількості 8... 10 % і кріолітом 3NaF "A1F3. Робоча напруга на затискачах ванни 4,0...
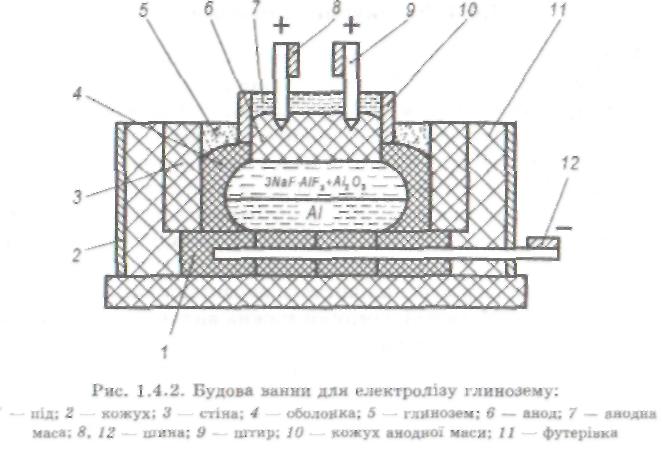
4,5 В. Електричний струм нагріває електроліт до 950...970 °С, розплавляє його та підтримує електроліз. На боках ванни та верхній її частині утворюється тверда оболонка 4 з електроліту, яка зменшує тепловіддачу та його випаровування. Виділений алюміній внаслідок більшої густини порівняно з електролітом збирається на дні ванни. Коли кількість глинозему зменшується до 1,2 %, напруга підвищується від 5 до ЗО В (анодний ефект). Завантаження нової порції глинозему 5 призупиняє це явище.
Під час електролізу глинозем дисоціює за такою спрощеною схемою:
А1203 - 2А1+++ + ЗО"". (1.4.5)
Катіон Алюмінію АГ+І розряджається на катоді, а аніон Оксигену О™ — на аноді. Оксиген оксидує Карбон анода до CO і С02. Під час оксидації анод поступово опускається у ванну.
Для виробництва 1 т алюмінію витрачається близько 18 МВт год електроенергії й до 0,7 т анодної маси. Рідкий алюміній кожних 3...4 доби вибирають сифоном. Він містить домішки металів (Fe, Si, Zn і ін.), гази (02, Н2, CO і С02) та неметалеві вкраплення (А1003, С), через що такий алюміній рафінують.
