
- •Введение
- •Часть I Материаловедение
- •1. Строение и свойства материалов
- •1.1. Классификация материалов
- •Плазма газ жидкость твердое тело
- •1.2. Кристаллическое строение материалов
- •1.3. Дефекты кристаллического строения
- •1.3.1. Точечные дефекты
- •1.3.2. Линейные дефекты
- •1.3.3. Поверхностные и объемные дефекты
- •2. Крсталлизация металлов и сплавов
- •2.1. Межатомное взаимодействие
- •2.2. Гомогенная и гетерогенная кристаллизация
- •2.3. Строение металлического слитка
- •2.4. Аморфные металлические сплавы
- •3. Деформация и разрушение металлов
- •3.1. Упругая и пластическая деформация
- •3.2 Деформация моно- и поликристаллов
- •3.3. Влияние нагрева на структуру деформированного металла
- •3.4. Свойства материалов и методы их испытаний
- •4. Основы теории двойных сплавов
- •4.1. Строение сплавов
- •4.2. Диаграммы состояния двойных сплавов
- •5. Железоуглеродистые сплавы
- •5.1. Компоненты и фазы
- •5.2. Превращения в сплавах системы железо–цементит
- •5.2.1. Первичная кристаллизация сталей
- •5.2.2. Вторичная кристаллизация сталей
- •5.2.3. Влияние углерода и постоянных примесей на свойства стали
- •5.2.4. Кристаллизация белых чугунов
- •5.3. Превращения в сплавах системы железо–графит
- •6. Основы термической обработки сталей
- •6.1. Основные превращения в стали
- •6.2. Отжиг стали
- •6.3. Закалка и отпуск
- •7. Поверхностное упрочнение деталей
- •7.1. Упрочнение методом пластической деформации
- •7.2. Упрочнение методом поверхностной закалки
- •7.3. Химико-термическая обработка
- •8. Легированные стали
- •8.1. Маркировка легированных сталей
- •8.2. Классификация легированных сталей
- •8.2.1. Конструкционные стали
- •8.2.2. Инструментальные стали
- •8.2.3. Стали и сплавы с особыми свойствами
- •9. Цветные металлы и сплавы
- •9.1. Титан и его сплавы
- •9.2 Алюминий и его сплавы
- •9.3. Магний и его сплавы
- •9.4. Медь и ее сплавы
- •9.5. Другие цветные металлы и сплавы
- •10. Неметаллические и композиционные материалы
- •10.1. Полимеры
- •10.2. Пластмассы
- •10.3. Композиционные материалы
- •10.3. Керамические материалы
- •Часть 2 Технология конструкционных материалов
- •11. Металлургическое производство
- •11.1. Основные сведения о производстве чугуна
- •11.2. Производство стали
- •11.3. Разливка стали
- •12. Литейное производство
- •12.1. Литейные свойства сплавов
- •12.2. Литье в песчано-глинистые формы
- •12.3. Плавильные печи
- •12.4. Специальные способы литья
- •12.5. Сплавы для изготовления отливок
- •13. Обработка металлов давлением
- •13.1. Прокатка
- •13.2. Волочение и прессование
- •13.3. Ковка
- •13.4. Штамповка
- •14. Обработка металлов резанием
- •14.1. Основы резания металлов
- •14.2. Обработка на токарных станках
- •14.3. Обработка на сверлильных станках
- •14.4. Обработка на фрезерных станках
- •14.5. Обработка на строгальных и долбежных станках
- •14.6. Обработка на шлифовальных и отделочных станках
- •14.7. Точность и качество поверхности при обработке
- •15. Сварка, резка и пайка
- •15.1. Сварка металлов плавлением
- •15.2. Сварка металлов давлением
- •15.3. Термическая резка металлов
- •Области применения способов термической резки
- •15.4. Пайка металлов
- •16. Электрофизические и электрохимические способы обработки материалов
- •16.1. Электрофизические способы
- •16.2. Электрохимические способы
- •17. Основы рационального выбора материалов
- •17.1. Выбор материала
- •17.2. Основные направления экономии материалов
- •Литература
- •Оглавление
- •Евгений Петрович Чинков
- •Андрей Геннадьевич Багинский
- •Материаловедение и технология
- •Конструкционных материалов
- •Подписано к печати.
1.3. Дефекты кристаллического строения
Нарушения идеальной трансляционной симметрии кристалла называются структурными дефектами (от лат. defectus – недостаток, изъян). Дефекты оказывают существенное влияние на многие свойства твердых тел. Модель идеальной (совершенной) структуры кристалла позволяет объяснить упругие и оптические свойства, электро- и теплопроводность, которые обусловлены коллективным взаимодействием электронов с полем, создаваемым ионами. Модель неидеальной (дефектной) структуры привлекается для объяснения упрочнения материалов, структурных изменений при термической обработке и др.
К динамическим дефектам структуры относят искажения кристаллической решетки, вызванные тепловыми колебаниями или колебаниями атомов в поле проходящей через кристалл электромагнитной волны. Статические дефекты делятся на собственные и несобственные (примесные). За основу классификации дефектов приняты размеры и протяженность областей нарушения.
1.3.1. Точечные дефекты
1. Собственные дефекты. Нарушения структуры локализованы в отдельных точках кристалла, их размеры в трех измерениях не превышают одного или нескольких параметров решетки. К ним относят: вакансии – отсутствие атомов в узлах решетки; междоузельные атомы основного вещества, комплексы точечных дефектов, антиструктурные дефекты. Точечные дефекты могут быть электрически активными и неактивными. Для них должно выполняться условие аддитивности: пространственная изолированность и не взаимодействие друг с другом.
В акансия
–
отсутствие атома (иона, молекулы) в узле
решетки. Вакансию,
возникающую за счет ухода атома из узла
на какую-либо границу внутри кристалла,
называют дефектом
по Шоттки.
В кристаллах переходных металлов с
валентными d-электронами
(Ti,
V,
Cr,
Mn,
Fe,
Co,
Ni,
Cu)
ими являются одиночные
вакансии. К
ним также
относятся: пары
Шоттки
–
катионная
и анионная вакансии, например, в кристалле
NaCl;
трио
Шоттки
–
катионная
и две анионные вакансии в кристалле
CaF2.
Парный
дефект (вакансия + междоузельный атом),
возникающий за счет перехода атома из
узла решетки в междоузлие, называют
дефектом
Френкеля
(рис. 1.11).
акансия
–
отсутствие атома (иона, молекулы) в узле
решетки. Вакансию,
возникающую за счет ухода атома из узла
на какую-либо границу внутри кристалла,
называют дефектом
по Шоттки.
В кристаллах переходных металлов с
валентными d-электронами
(Ti,
V,
Cr,
Mn,
Fe,
Co,
Ni,
Cu)
ими являются одиночные
вакансии. К
ним также
относятся: пары
Шоттки
–
катионная
и анионная вакансии, например, в кристалле
NaCl;
трио
Шоттки
–
катионная
и две анионные вакансии в кристалле
CaF2.
Парный
дефект (вакансия + междоузельный атом),
возникающий за счет перехода атома из
узла решетки в междоузлие, называют
дефектом
Френкеля
(рис. 1.11).
Дефекты по Шоттки в основном образуются в плотноупакованных структурах. В общем случае в кристалле имеются дефекты по Шоттки и Френкелю. Преобладают те, на образование которых требуется меньшая энергия на разрыв связей при образовании дефекта и искажение решетки вокруг него – смещение атомов из равновесных положений.
В химических соединениях (например, полупроводниках), когда размеры и электроотрицательности атомов А и В близки, обмен местами атомов приводит к появлению антиструктурных дефектов. В ионных соединениях эти дефекты не встречаются.
Если
кристалл представить в виде упругой
сплошной среды, то деформации
вокруг дефекта убывают пропорционально
![]() ,
где r
–
расстояние от дефекта. Однако имеет
место анизотропия смещений атомов.
Ближайшие соседи смещаются в сторону
вакансии, вторые – от вакансии, третьи
– к вакансии (рис. 1.12). Вокруг
междоузельного атома ближайшие атомы
смещены по направлению от него, вторые
соседи –
к нему. Упругое поле, созданное точечным
дефектом, охватывает несколько постоянных
решетки, кулоновское поле –
десятки
постоянных.
,
где r
–
расстояние от дефекта. Однако имеет
место анизотропия смещений атомов.
Ближайшие соседи смещаются в сторону
вакансии, вторые – от вакансии, третьи
– к вакансии (рис. 1.12). Вокруг
междоузельного атома ближайшие атомы
смещены по направлению от него, вторые
соседи –
к нему. Упругое поле, созданное точечным
дефектом, охватывает несколько постоянных
решетки, кулоновское поле –
десятки
постоянных.
О бъединение
точечных дефектов энергетически выгодно,
так как уменьшается число оборванных
связей. Вероятность объединения тем
выше, чем выше концентрация одиночных
дефектов (больше вероятность встречи).
Свойства сложных и простых дефектов
отличаются. Вакансии могут объединяться
в дивакансии, тривакансии и т. д. Скопления
вакансий образуют поры, пустоты.
Междоузельные атомы объединяются в
гантель или линейную конфигурацию
(статический
краудион),
собираются в пластины.
бъединение
точечных дефектов энергетически выгодно,
так как уменьшается число оборванных
связей. Вероятность объединения тем
выше, чем выше концентрация одиночных
дефектов (больше вероятность встречи).
Свойства сложных и простых дефектов
отличаются. Вакансии могут объединяться
в дивакансии, тривакансии и т. д. Скопления
вакансий образуют поры, пустоты.
Междоузельные атомы объединяются в
гантель или линейную конфигурацию
(статический
краудион),
собираются в пластины.
Механизмы образования точечных дефектов. Дефекты образуются: в процессе выращивания кристалла при неравновесных условиях, при нагревании, при облучении радиацией, при пластической деформации или термической обработке.
Образование дефектов при пластической деформации. При смещении атома из положения равновесия в ближайшее междоузлие в металле образуется пара Френкеля (рис. 1.13,а). При снятии нагрузки такая близкорасположенная пара дефектов окажется неустойчивой. На положительно заряженный междоузельный атом будут действовать кулоновские силы: притяжения со стороны отрицательно заряженной вакансии, отталкивания – со стороны ближайшего окружения.
Н аиболее
вероятный механизм образования точечных
дефектов –
распространение динамического
краудиона.
Атомы из зоны приложения нагрузки
удаляются «разбегающимися» краудионами
(рис. 1.13,б).
В результате на некотором расстоянии
создается повышенная концентрация
междоузельных атомов (рис. 1.13,в).
Краудионы двигаются вдоль плотноупакованных
направлений в кристалле и эффективно
рассеиваются на незначительных смещениях
атомов из узлов кристаллической решетки.
аиболее
вероятный механизм образования точечных
дефектов –
распространение динамического
краудиона.
Атомы из зоны приложения нагрузки
удаляются «разбегающимися» краудионами
(рис. 1.13,б).
В результате на некотором расстоянии
создается повышенная концентрация
междоузельных атомов (рис. 1.13,в).
Краудионы двигаются вдоль плотноупакованных
направлений в кристалле и эффективно
рассеиваются на незначительных смещениях
атомов из узлов кристаллической решетки.
Тепловые дефекты. С повышением температуры Т концентрация точечных дефектов возрастает. Прирост энтропии S вследствие увеличения беспорядка в расположении атомов компенсирует рост внутренней энергии U. Свободная энергия F = U – T S минимальна, кристалл остается в состоянии термодинамического равновесия.
Вероятность образования дефектов по Шоттки зависит от температуры в соответствии с законом Больцмана:
![]() ,
,
где N – число атомов в единице объема кристалла; n – число дефектов; ЕА – энергия образования дефекта; k – постоянная Больцмана.
Число атомов в 1 см3 кристалла:
![]() ,
,
где NА – число Авогадро; – плотность; М – молекулярная масса.
Для кристаллов меди N = 8,4 1022, энергия образования вакансии около 1 эВ, междоузельного атома – 2,5 эВ. При температуре, близкой к температуре плавления (1000 K), относительная доля вакансий P ~ 10–5, т. е. на каждые 105 атомов меди приходится одна вакансия, среднее расстояние между вакансиями составляет несколько параметров решетки.
Концентрация дефектов по Френкелю также находится в соответствии с законом Больцмана:
![]() ,
,
где ЕА – энергия, необходимая для удаления атома на поверхность кристалла, а затем его перемещения с поверхности в междоузлие; N1 и N2 – число атомов и междоузлий в единице объема. При понижении температуры концентрация дефектов убывает экспоненциально и оказывается очень малой при температурах ниже комнатной. Если кристалл нагреть и быстро охладить (закалить), то концентрация дефектов будет соответствовать высокой температуре. В реальных условиях концентрация точечных дефектов превышает равновесную концентрацию.
Радиационные дефекты, в отличие от тепловых, являются термодинамически неравновесными. Воздействие радиации на кристалл сопровождается разными явлениями, из которых выделим основные.
1. Возбуждение и ионизация атомов (ионов). В кристалле создается неравновесное распределение зарядов. Время перехода к равновесному распределению зарядов:
![]() ,
,
где ε – диэлектрическая проницаемость, σ – проводимость материала. В металлах время мало (τ ~ 10-19 с), ионные кристаллы находятся в ионизованном состоянии после облучения длительное время.
2. Смещение атомов из положений равновесия. Пороговый механизм образования дефектов – энергия радиации (налетающей частицы, кванта электромагнитного излучения) непосредственно передается атому в узле решетке. Допороговый – первичный процесс ионизации приводит к смещению возбужденного атома из положения равновесия.
3. Ядерные превращения – распад радиоактивных атомов и появление примесных дефектов.
4. Тепловые клинья. Движущаяся высокоэнергетическая частица передает большую часть энергии ближайшим атомам. В узкой области вдоль пути пробега частицы вещество сильно нагревается (до 1000 °С) и очень быстро охлаждается.
Радиационные повреждения вызывают повышение твердости, скалывающего напряжения, прочности (радиационное упрочнение), изменение коэффициента диффузии и др. Первоначальные свойства облученного кристалла восстанавливаются в результате отжига.
Д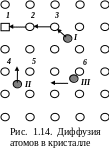 иффузия
атомов в кристалле. При
образовании дефектов в кристалле,
например, пары Френкеля (рис. 1.14),
увеличивается свободная энергия. Энергия
неадиабатической системы стремится к
минимуму. Междоузельный атом (заштрихован)
должен занять положение вакансии.
Перемещение атомов на расстояния больше
периода решетки носит общее название
– диффузия.
Атомы, находящиеся в узлах кристаллической
решетки, непрерывно колеблются около
положения равновесия. Для перескока
атома необходима энергия, которая
значительно больше средней энергии
теплового движения (
kT).
Эта
энергия связана главным образом с силами
отталкивания, которые увеличиваются
при сближении атомов. Вероятность
перескока мала, от
температуры зависит в соответствии с
законом Больцмана.
иффузия
атомов в кристалле. При
образовании дефектов в кристалле,
например, пары Френкеля (рис. 1.14),
увеличивается свободная энергия. Энергия
неадиабатической системы стремится к
минимуму. Междоузельный атом (заштрихован)
должен занять положение вакансии.
Перемещение атомов на расстояния больше
периода решетки носит общее название
– диффузия.
Атомы, находящиеся в узлах кристаллической
решетки, непрерывно колеблются около
положения равновесия. Для перескока
атома необходима энергия, которая
значительно больше средней энергии
теплового движения (
kT).
Эта
энергия связана главным образом с силами
отталкивания, которые увеличиваются
при сближении атомов. Вероятность
перескока мала, от
температуры зависит в соответствии с
законом Больцмана.
Существуют разные механизмы диффузии: вакансионный, междоузельный, диссипативный и др.
Наиболее вероятным является вакансионный механизм, при котором вакансия 1 занимается расположенным рядом атомом 2 (рис. 1.14). Т. е., вакансия последовательно перемещается (из положения 1 в положение 2, а затем в положение 3) до тех пор, пока междоузельный атом I не займет рядом образовавшуюся вакансию.
При междоузельном механизме наблюдается перескок атома из одного междоузлия в соседнее. Данный механизм требует больших энергетических затрат, чем вакансионный. Атомы 4 и 5 (рис. 1.14) совершают относительно положения равновесия как симметричные (как целое), так и несимметричные колебания. Чтобы вернуться в положение вакансии, междоузельный атом II должен «протиснуться» между этими атомами – эффект колебательного «узкого горла». Такой механизм характерен для диффузии атомов с малым радиусом: например, углерода, азота, водорода в железоуглеродистых сплавах.
Диссоциативный механизм. Чтобы вернуть междоузельный атом III в положение вакансии необходимо сначала затратить энергию на разрыв его химической связи с узельным атомом 6.
Общим для всех случаев диффузии является экспоненциальная зависимость от температуры. Следовательно, значительную роль диффузия играет только при высоких температурах, сопоставимых с температурой плавления вещества. Например, в альфа-железе при температуре 1500 °С частота перескоков атома углерода составляет 1011 раз в секунду, при комнатной температуре – 1 раз за десятки секунд. Защитное никелевое или хромовое покрытие практически не "впитывается" в железо при комнатной температуре, но при нагреве выше 1000 °С процесс значительно ускоряется. Кратковременный высокотемпературный нагрев широко используется для легирования полупроводников.
2. Примесные дефекты – атомы (ионы) примеси, которые замещают атомы основы в узле решетки, или располагаются в междоузельном пространстве (пустотах). Атомы основы образуют собственную кристаллическую решетку, примесь присутствуют в виде отдельных атомов и собственной решетки не имеет. Растворимость уменьшается:
1) если элементы имеют разный тип связывающих орбиталей;
2) с увеличением разницы валентностей элементов;
3) с увеличением разницы размеров атомов основы и примеси;
4) если элементы имеют разные кристаллические решетки;
5) если образуется промежуточная фаза.
Твердые растворы внедрения (рис. 1.15,а) образуются, когда атомы (ионы) примеси внедряются в междоузельные позиции решетки основного элемента. Растворимость ограничена размерами пустот. Растворы внедрения образуются при сплавлении металлов с неметаллами, имеющими малый атомный (ионный) радиус (C, N, B, H). Размеры атомов и межатомных промежутков не совпадают. Это вызывает искажение решетки и возникновение механических напряжений. Период кристаллической решетки твердого раствора внедрения всегда изменяется. Предельная концентрация растворов – не более 2–2,5 %.
Т вердые
растворы замещения
(рис. 1.15,б)
образуются в том случае, когда размеры
атомов (ионов) компонентов отличаются
не более чем на 15 %. Атомы примеси замещают
атомы основного элемента в узлах
кристаллической решетки. Упорядоченные
твердые растворы можно рассматривать
как промежуточные фазы между твердыми
растворами и химическими соединениями.
Если замещение осуществляется в
случайных
местах, то растворы называют
неупорядоченными.
вердые
растворы замещения
(рис. 1.15,б)
образуются в том случае, когда размеры
атомов (ионов) компонентов отличаются
не более чем на 15 %. Атомы примеси замещают
атомы основного элемента в узлах
кристаллической решетки. Упорядоченные
твердые растворы можно рассматривать
как промежуточные фазы между твердыми
растворами и химическими соединениями.
Если замещение осуществляется в
случайных
местах, то растворы называют
неупорядоченными.
Если размеры атомов примеси больше размеров атомов основы, то решетка растягивается, если меньше – сжимается. В первом приближении изменение параметров решетки пропорционально концентрации примеси и определяет изменение механических свойств твердых растворов замещения. Уменьшение параметра решетки ведет к большему упрочнению, чем увеличение. Твердые растворы замещения бывают ограниченными и неограниченными. Компоненты должны иметь близкие атомные радиусы и одинаковый тип решетки. Неограниченная растворимость в твердом состоянии наблюдается в сплавах: Cu–Ni, Cu–Au, Si–Ge.
Твердые растворы вычитания образуются в химических соединениях компонентов, в которых узлы кристаллической решетки не заняты полностью – часть атомов как бы вычтена из кристаллической решетки, и образуются вакансии. Появление вакансий связано, как правило, с присутствием ионов переменной валентности (Fe, Mn). С увеличением количества вакансий период кристаллической решетки уменьшается. Например, в вюстите FeO с увеличением содержания кислорода, т. е. с уменьшением количества ионов железа в своей подрешетке, период кристаллической решетки уменьшается.
