
- •Предисловие
- •Введение
- •1 Предмет курса "поверхностные явления
- •2 Классификация поверхностных явлений
- •3 Дисперсность, удельная поверхность
- •4 Классификация дисперсных систем
- •4.1 Классификация дисперсных систем по размерам частиц дисперсной фазы
- •4. 2 Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •4.3 Классификация по интенсивности взаимодействия дисперсной фазы и дисперсионной среды
- •4.4 Классификация по интенсивности взаимодействия
- •5 Поверхностные явления на границе раздела фаз
- •5.1 Поверхностная энергия, поверхностное натяжение
- •5.2 Термодинамика поверхности раздела фаз
- •5.3 Пути понижения энергии Гиббса на границе раздела фаз
- •5.4 Когезия. Работа когезии
- •5.5 Адгезия, работа адгезии, термодинамические основы адгезии
- •5.6 Смачивание, краевой угол смачивания, теплота смачивания, гидрофилизация и гидрофобизация поверхностей.
- •5.7 Растекание, критерий растекания, поверхностные пленки, двумерный газ
- •5.8 Адсорбция
- •5.8.1 Общие положения, классификация изотерм адсорбции
- •5.8.2 Фундаментальное термодинамическое уравнение адсорбции Гиббса
- •5.8.3 Адсорбция газов и паров на поверхности твердых тел
- •5.8.4 Уравнение адсорбции Фрейндлиха. Его анализ и решение
- •5.8.5 Мономолекулярная теория (теория Ленгмюра)
- •5.8.6 Полимолекулярная теория (теория Поляни)
- •5.8.7 Теория полимолекулярной адсорбции бэт
- •Пористые адсорбенты, классификация пористых тел по Дубинину
- •5.8.10 Влияние природы и структуры адсорбента, природы и свойств газов и паров на адсорбцию. Адсорбция из смеси газов.
- •5.9 Адсорбция из раствора на границе с газом
- •5.8.10.1. Молекулярная адсорбция
- •5.8.11.2. Ионная адсорбция (адсорбция электролитов)
- •5.8.12 Ионобменная адсорбция
5.8.10.1. Молекулярная адсорбция
Адсорбция из раствора на твердом теле является практически наиболее распространенной, так как является основным методом разделения смесей и очистки производственных растворов от смесей.
Адсорбция осложняется тем, что адсорбируются на поверхности твердого тела два конкурирующих вещества : растворитель и растворенное вещество.
При молекулярной адсорбции величина адсорбции может быть определена по уравнению:
A = (co-c) q/m, (V.41)
где co, c - начальная и равновесная концентрации растворенного вещества;
m - масса адсорбента;
q - добьем раствора.
Изотерма молекулярной адсорбции описывается уравнением Ленгмюра в виде
A = А maxКС/(1+КС); (V.42)
уравнением Фрейндлиха
А = kC1/n ; (V.43)
уравнением Гиббса в виде
![]() .
.
При
молекулярной адсорбции из растворов
наблюдается эффект отрицательной
адсорбции
(рис. V.32)
А
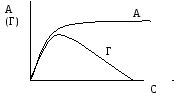
Рисунок V.32 - Отрицательная молекулярная адсорбция из раствора
Это явление связано с тем, что различают величину адсорбции Г как
избыток компонента в адсорбционном пространстве и А как полное содержание компонента в адсорбционном пространстве:
А = Г + С1 Vo .
Изотерма адсорбции отражает изменение полного содержания компонента в адсорбционном пространстве. По мере повышения концентрации раствора увеличивается слагаемое С1 Vo и уменьшается избыток компонента в адсорбционном пространстве по сравнению с раствором.
1.1. Влияние различных факторов на молекулярную адсорбцию
1.1.1. Влияние свойств среды
а) чем больше поверхностное натяжение растворителя, тем меньше его способность к адсорбции, следовательно, тем лучше будет идти адсорбция растворенного вещества. Поэтому адсорбция на неполярном теле лучше идет из водных растворов, чем из органических;
б) теплота смачивания растворителем твердого тела показывает интенсивность взаимодействия растворителя с адсорбентом. Чем выше теплота адсорбции, тем большую конкурентную способность оказывает растворитель растворенному веществу;
в) чем лучше вещество растворяется в данной среде, тем хуже идет в этой среде его адсорбция, что объясняется усилением межмолекулярного взаимодействия среды и растворенного вещества.
1.1.2. Влияние свойств адсорбента
а) неполярные адсорбенты хорошо адсорбируют неполярные адсорбтивы и наоборот;
б) чем больше пористость адсорбента, тем большее количество адсорбтива он способен адсорбировать, если величина пор не меньше размера молекул адсорбтива.
1.1.3. Влияние свойств адсорбтива.
Однозначно выяснить влияние свойств адсорбтива на величину адсорбции крайне трудно. В качественном отношении для выбора адсорбента можно ориентироваться эмпирическим правилом уравнивания полярностей Ребиндера: вещество С будет адсорбироваться на границе раздела фаз А и В, если оно своим появлением там уравнивает разность полярностей этих фаз. Под полярностью понимается любое физико-химическое свойство, например, диэлектрическая проницаемость , поверхностное натяжение . Вещество будет адсорбироваться на поверхности раздела фаз А и В лишь тогда, когда выполняется одно из неравенств:
А < C < B ; A > C > B ; A < C < B ; A > C > B .
Из анализа правила Ребиндера следует, что:
а) чем больше разность полярностей твердого адсорбента и растворителя, тем лучше будет адсорбироваться растворенное вещество;
б) чем больше разность полярностей между растворенным веществом и раствором, тем лучше оно адсорбируется;
в) дифильные молекулы адсорбтива должны на границе фаз ориентироваться полярной частью к полярной фазе, неполярной частью - к неполярной фазе;
г) полярные адсорбенты должны лучше адсорбировать ПАВ из неполярных жидкостей и наоборот.
При оценке адсорбируемости используют правило Траубе.
Для жирных кислот и алифатических спиртов при адсорбции на неполярном адсорбенте ( активированный уголь) адсорбируемость увеличивается с увеличением числа групп –СН2- в молекуле.
На гидрофильных адсорбентах (силикагели) из неполярных растворителей величина предельной адсорбции с ростом молекулярной массы уменьшается.
