
- •1.Физиологическая роль углеводов
- •2. Пищевые источники и потребность организма в углеводах. Переваривание углеводов в желудочно-кишечном тракте. Судьба всосавшихся моносахаридов.
- •4. Гликоген как резервный полисахарид. Глюкостатическая функция печени.
- •5. Глюкоза в крови. Регуляция уровня глюкозы в крови. Роль адреналина, глюкагона, инсулина, тиреоидных гормонов.
- •7) Клиническое значение определения концентрации глюкозы в моче
- •8) Изучение углеводного обмена методом однократной сахарной нагрузки.
- •10) Механизм внутриклеточного окисления глюкозы. Дихотомическое анаэробное окисление углеводов (гликолиз).
- •Суммарное уравнение анаэробного гликолиза.
- •11)Гомеостаз молочной кислоты
- •2. Продукция лактата
- •3. Утилизация лактата
- •4. Молочнокислый ацидоз
- •12) Энергетический эффект распада углеводов и триглицеридов
- •14) Гликолиз
- •21. Регуляция содержания глюкозы в крови в абсорбтивном и постабсорбтивном периодах, при длительном голодании, в период голодания и в период покоя.
- •22.Апотомический путь окисления глюкозы(пентозофосфатный шунт).Окислительный этап.Неокислительный этап.Биологическое значение процесса
- •23. Дефект глюкозо-6-фосфат дегидрогеназы в эритроцитах
- •24.Метаболизм фруктозы.Нарушение метаболизма.Недостаточность фруктокиназы.
- •25.Метаболизм галактозы.Нарушение метаболизма галактозы(дефекты галактокиназы, галактазо-1-фосфатуридилтрансферазы)
- •32. Эйкозаноиды (простагландины, простациклины, тромбоксаны, лейкотриены), био роль, представители.
- •1. Структура и номенклатура простагландинов и тромбоксанов
- •2. Циклооксигеназный путь: синтез простагландинов и тромбоксанов
- •33. Фосфатиды-глицериды. Классификация, структура, био роль.
- •34. Фосфатиды-неглицериды. Классификация, сфингозин-фосфатиды. Био роль.
- •35. Переваривание экзогенных липидов в жкт. Липолитические ферменты: желудочная липаза, панкреатическая липаза, фосфофолипазы, особенности их каталитической активности.
- •41) Сущность b-окисления, химизм реакций, характеристика ферментов.
- •42) Общий энергетический эффект полного окисления. Взаимосвязь окисления жк с процессами тканевого дыхания.
- •43) Особенности окисления ненасыщенных жк. Энергетический эффект окисления.
- •44) Цикл Рэндла.
- •45) Катаболизм фосфолипидов – глицеридов.
- •Вопрос 54
- •Кетонурия
- •51.Представление о биосинтезе холестерина (хс). Роль оксиметилглутарил-КоА-редуктазы в биосинтезе хс. Регуляция процесса биосинтеза хс.
- •53. Кетогенез: химизм реакции. Кетоновые тела (ацетоуксусная кислота, β-оксимасляная кислота, ацетон) и их биологическая роль. Кетолиз (окисление кетоновых тел в тканях).
- •Вопрос 55,56 транспорт жиров из кишечника хиломикронами
- •60)Классификация липопротеинемии по Фридрексону( у кого есть скинте)
- •Вопрос 61 биологические мембраны
- •I. Роль мембран в метаболизме и их разнообразие
- •1. Структура и свойства липидов мембран
- •2. Трансмембранная асимметрия липидов
- •3. Жидкостностъ мембран
- •4. Функции мембранных липидов
35. Переваривание экзогенных липидов в жкт. Липолитические ферменты: желудочная липаза, панкреатическая липаза, фосфофолипазы, особенности их каталитической активности.
Б. Гормоны, активирующие переваривание жиров
При поступлении пищи в желудок, а затем в кишечник клетки слизистой оболочки тонкого кишечника начинают секретировать в кровь пептидный гормон холецистокинин (панкреозимин). Этот гормон действует на жёлчный пузырь, стимулируя его сокращение, и на экзокринные клетки поджелудочной железы, стимулируя секрецию пищеварительных ферментов, в том числе панкреатической липазы. Другие клетки слизистой оболочки тонкого кишечника в ответ на поступление из желудка кислого содержимого выделяют гормон секретин. Секретин - гормон пептидной природы, стимулирующий секрецию бикарбоната (НСО3-) в сок поджелудочной железы.
В. Переваривание жиров панкреатической липазой
Переваривание жиров - гидролиз жиров панкреатической липазой. Оптимальное значение рН для панкреатической липазы ≈8 достигается путём нейтрализации кислого содержимого, поступающего из желудка, бикарбонатом, выделяющимся в составе сока поджелудочной железы:
Н+ + НСО3- → Н2СО3 → Н2О + СО2 ↑.
Выделяющийся углекислый газ способствует дополнительному перемешиванию содержимого тонкой кишки.
Панкреатическая липаза выделяется в полость тонкой кишки из поджелудочной железы вместе с белком колипазой. Колипаза попадает в полость кишечника в неактивном виде и частичным протеолизом под действием трипсина превращается в активную форму. Колипаза своим гидрофобным доменом связывается с поверхностью мицеллы эмульгированного жира. Другая часть молекулы способствует формированию такой конформации панкреатической липазы, при которой активный центр фермента максимально приближен к своим субстратам - молекулам жиров (рис. 8-12), поэтому скорость реакции гидролиза жира резко возрастает.
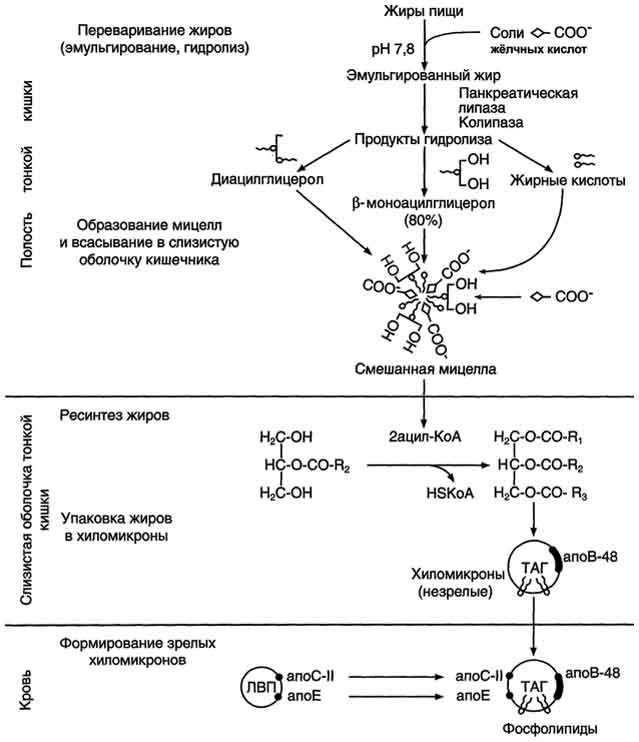
Рис. 8-11. Этапы поступления экзогенных жиров в организм.

Рис. 8-12. Расположение панкреатической липазы и колипазы на границе раздела фаз вода/жир.
Панкреатическая липаза гидролизует жиры преимущественно в положениях 1 и 3 (рис. 8-13), поэтому основными продуктами гидролиза являются свободные жирные кислоты и 2-моноацилглицеролы (β-моноацилглицеролы).
Молекулы 2-моноацилглицеролов также обладают детергентными свойствами и способствуют эмульгированию жира.
Г. Переваривание других липидов
Кроме жиров, с пищей поступают фосфолипиды, эфиры холестерола, однако количество этих липйдов в составе пищи значительно меньше, чем жиров (≈10%).
Переваривание глицерофосфолипидов
В переваривании глицерофосфолипидов участвуют несколько ферментов, синтезирующихся в поджелудочной железе. Фосфолипаза А2 гидролизует сложноэфирную связь у второго атома углерода глицерола, превращая глицерофосфолипиды в соответствующие лизофосфолипиды. На рисунке 8-14 представлен пример гидролиза фосфатидилхолинов при переваривании.

Рис. 8-13. Гидролиз триацилглицеролов панкреатической липазой.

Рис. 8-14. Переваривание фосфатидилхолинов.
Фосфолипаза A2 секретируется в кишечник в виде профермента и активируется уже в полости кишечника путём частичного протеолиза. Для проявления активности фосфолипазы A2 необходимы ионы кальция.
Жирная кислота в положении 1 отщепляется под действием лизофосфолипазы, а глицерофосфохолин гидролизуется далее до глицерола, холина и фосфорной кислоты, которые всасываются. Лизофосфолипиды - эффективные эмульгаторы жира, ускоряющие его переваривание.
Переваривание эфиров холестерола
В составе пищи холестерол находится в основном в виде эфиров. Гидролиз эфиров холестерола происходит под действием холестеролэстеразы - фермента, который также синтезируется в поджелудочной железе и секретируется в кишечник (рис. 8-15). Продукты гидролиза (холестерол и жирные кислоты) всасываются в составе смешанных мицелл.
Д. Переваривание жира у грудных детей
У грудных детей и детей младшего возраста основной пищей служит молоко. Молоко содержит жиры, в состав которых входят в основном жирные кислоты с короткой и средней длиной алифатических цепей (4-12 атомов углерода). Жиры в составе молока находятся уже в эмульгированном, смешанном с водой виде, поэтому они сразу же доступны для гидролиза ферментами. На жиры молока в желудке детей действует липаза, которая синтезируется в железах языка (липаза языка). Кроме того, в желудке детей грудного и младшего возраста вырабатывается желудочная липаза, которая активна при нейтральном значении рН, характерном для желудочного сока детей, и не активна у взрослых (рН желудочного сока -∼1,5). Эта липаза гидролизует жиры, отщепляя, в основном, жирные кислоты у третьего атома углерода глицерола. Далее гидролиз жиров молока продолжается в кишечнике под действием панкреатической липазы. Жирные кислоты с короткой цепью, как водорастворимые, всасываются частично уже в желудке. Остальные жирные кислоты всасываются в тонком кишечнике. Для детей грудного возраста основным источником энергии являются жиры, в то время как у взрослых людей при нормальном питании основным источником энергии служит глюкоза.

Рис. 8-15. Гидролиз эфиров холестерола в тонкой кишке.
Вследствие этого нарушение переваривания и всасывания жиров у детей более опасно, чем у взрослых.
Переваривание липидов в желудочно-кишечном тракте - это часть метаболизма липидов, совокупность управляемых процессов, осуществляемых в системе пищеварения, которые представляют собой химическую переработку липидов, поступающих в организм с пищей, для последующего их всасывания в кровь и в лимфу.
Пищевые вещества содержат крупномолекулярные белки, углеводы и липиды, которые не способны к всасыванию в кровь и лимфу из-за больших размеров своих молекул. Химическая переработка пищи в желудочно-кишечном тракте представляет собой последовательное ступенчатое ферментативное гидролитическое расщепление крупномолекулярных белков, углеводов и липидов до простых веществ, способных к всасыванию. Ферменты, катализирующие эти реакции гидролиза называют гидролазами.



Панкреатическая фосфолипаза — фосфолипаза класса А2 (КФ 3.1.1.4), липолитический фермент, разлагающий жиры пищи (триглицериды). Секретируется в виде профермента поджелудочной железы профосфолипазы, который активируется в тонкой кишке трипсином (Саблин О.А. и др.). Оптимальная кислотность для каталитической активности панкреатической фосфолипазы 7,5–9,0 рН. «Работает» как фермент в присутствии Ca2+ (являющимся коферментом для фосфолипазы).
При воздействии фосфолипазы на лецитин желчи образуется лизолецитин.
Инициальное переваривание пищевого жира в желудке является предварительным условием для опитимального липолиза в кишечнике. Эта функция обеспечивается липазой желудка. этот энзим имеет низкий оптимум рН, устойчив к кислой среде желудка и к действию желудочных протеаз и не нуждается в желчных солях или кофакторах для триглицеридного гидролиза. Свободные жирные кислоты и моноглицериды возникающие в результате липолиза в желудке усиливают последующий гидролиз триглицеридов панкреатическими липазами. Значение желудочной липазы увеличивается в контексте перинатальной физиологии и патологичских условий, когда секреция гастрической липазы может компенсировать до некоторой степени подавленную панкреатическую активность.
Панкреатическая липаза
Панкреатическая липаза синтезируется в поджелудочной железе и в составе панкреатического сока попадает в двенадцатиперстную кишку.
Липаза имеет гидрофильную и гидрофобную части и действует только на поверхности раздела вода-жир. Панкреатическая липаза катализирует в полости тонкой кишки разложение жиров пищи (триглицеридов) на глицерин и высшие жирные кислоты, образуя сначала 1.2 и 2.3-диглицериды, а затем 2-моноглицериды. На одну молекулу триглицерида освобождается две молекулы жирных кислот. Этот процесс происходит в полости тонкой кишки посредством полостного пищеварения. Гидролиз 2-моноглицерида идет очень медленно под воздействием моноглицеридлипазы. При этом образуются глицерин и жирная кислота.
Роль желчи
1. Наряду с панкреатическим соком нейтрализация кислого химуса, поступающего из желудка. При этом карбонаты взаимодействуют с НСl, выделяется углекислый газ и происходит разрыхление химуса, что облегчает переваривание.
2. Усиливает перистальтику кишечника.
3. Обеспечивает переваривание жиров:
эмульгирование для последующего воздействия липазой, необходима комбинация [желчные кислоты+жирные кислоты+моноацилглицеролы],
уменьшает поверхностное натяжение, что препятствует сливанию капель жира,
образование мицелл, способных всасываться.
4. Благодаря п.п.1 и 2 обеспечивает всасывание жирорастворимых витаминов (витамин A, витамин D, витамин K, витамин E).
5. Экскреция избытка ХС, желчных пигментов, креатинина, металлов Zn, Cu, Hg, лекарств. Для холестерина желчь – единственный путь выведения, с ней может выводиться 1-2 г/сут.
Желчные кислоты
Монокарбоновые оксикислоты, относящиеся к классу стероидов . Твердые оптически активные вещества, плохо растворимые в воде. Вырабатываются печенью из холестерина , содержат (у млекопатиющих) 24 атома углерода. У различных животных структура доминирующих желчных кислот видоспецифична. В организме желчные кислоты обычно образуют конъюгаты с глицином ( гликолевая кислота ) или таурином ( таурохолевая кислота ).
Синтез таковых(схема)
П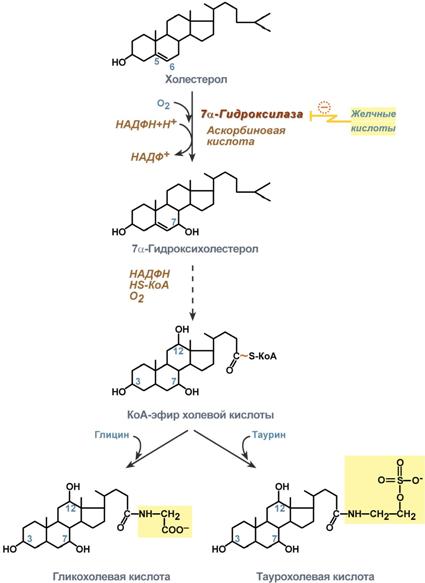 ричины
образования камней
ричины
образования камней
В случае нарушения количественного соотношения компонентов желчи в организме происходит формирование твердых образований (хлопьев), которые с течением заболевания разрастаются и сливаются в камни. Наиболее часто встречается холелитиаз при нарушенном обмене холестерина (избыточном его содержании в желчи). Перенасыщенная холестерином желчь называется литогенной.
Избыток холестерина образуется вследствие следующих факторов:
при ожирении и употреблении большого количества холестеринсодержащих продуктов;
при снижении количества желчных кислот, поступающих в желчь (пониженная секреция при эстрогении, депонирование в желчном пузыре, функциональная недостаточность гепатоцитов);
при снижении количества фосфолипидов, которые подобно желчным кислотам не дают холестерину и билирубину переходить в твердое состояние и оседать;
при застойных явлениях в системе циркуляции желчи (сгущение желчи вследствие всасывания в желчном пузыре воды и желчных кислот).

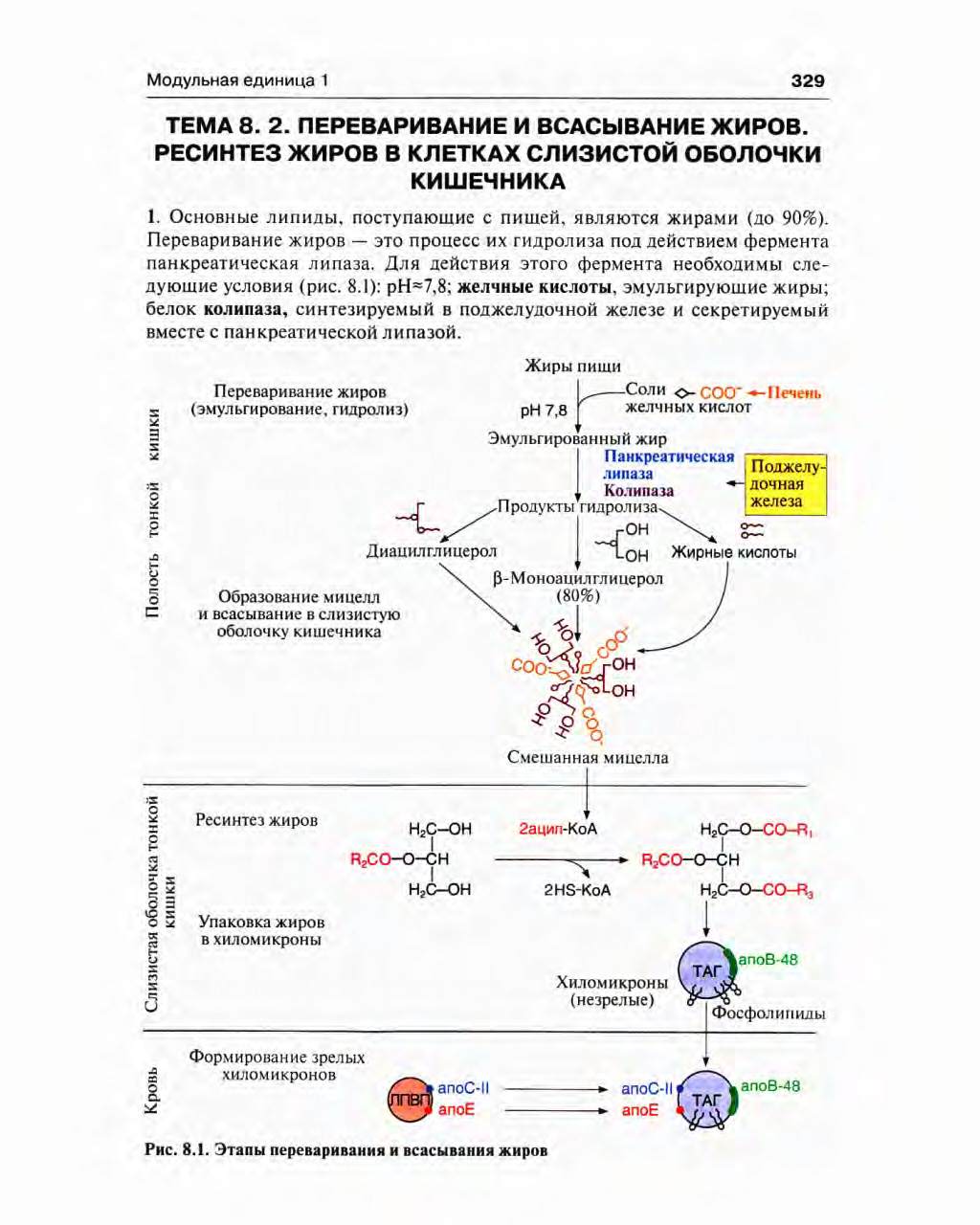
А потом будет идти тот рисунок который сверху.
Жиры хранятся до момента их использования. Катаболизм жира идет в три этапа.
Гидролиз жира до глицерина и жирных кислот (липолиз).
Превращение глицерина (вступает в ГБФ-путь) и жирных кислот (подвергаются -окислению) в ацетил-КоА.
Общий путь - цикл трикарбоновых кислот.
Процесс липолиза известен как мобилизация жира. Мобилизация жира - это реакция гидролиза жира до глицерина и жирных кислот.
Это ферментативный процесс. Осуществляют его два фермента:
липаза жировой ткани;
моноглицеридлипаза.
Ключевым ферментом является липаза жировой ткани. Она регулируется гормонами, поэтому часто ее называют гормончувствительная липаза. Это небольшой белок (мол. масса 82-88 кДа) находится в жировых клетках. Существует в двух формах: фосфорилированной - активной и дефосфорилированной - неактивной. Фосфорилирование липазы происходит под действием протеинкиназы А. Липаза жировой ткани - является цАМФ-зависимым ферментом. Гормоны, увеличивающие концентрацию цАМФ, усиливают липолиз.
Все гормоны, влияющие на мобилизацию жира, можно разделить на 2 группы.
Гормоны прямого действия (адреналин, соматотропный гормон гипофиза, инсулин).
Гормоны косвенного действия (глюкокортикостероиды, половые гормоны, лептин).
Адреналин.
Мембраны адипоцитов содержат адренорецепторы двух типов (и). Взаимодействие адреналина с рецепторами обоих типов вызывает изменение концентрации цАМФ. Однако, это влияние разнонаправленное.
адренорецептор связан с ингибирующим G-белком (Gi), свызывающим понижение активности аденилатциклазы. Это приводит к уменьшению концентрации цАМФ, и, в конечном счете, торможению липолиза.
адренорецептор связан со стимулирующим G-белком (Gs) - эффектом будет стимуляция липолиза. Соотношение - и -адренорецепторов зависит от индивидуальных особенностей организма. Это касается как организма в целом, так и распределения этих рецепторов в разных частях тела - поэтому в процессе липолиза разные части тела у разных людей "худеют" неодинаково. Однако в целом у человека преобладают -адренорецепторы, поэтому суммарное действие адреналина приводит к активации липолиза.
Соматотропный гормон - стимулирует липолиз, воздействуя через аденилатциклазную систему.
Действие инсулина связано с повышением активности внутриклеточной фосфодиэстеразы, что приводит к снижению концентрации цАМФ и угнетению липолиза. Таким образом, инсулин усиливает синтез жира и уменьшает скорость его мобилизации.
Глюкокортикостероиды: рецепторы к этим гормонам присутствуют в адипоцитах и содержат в своем составе белки теплового шока. После взаимодействия гормона с рецептором белки теплового шока отделяются, а сам комплекс транспортируется в ядро клетки, где влияет на синтез белков адипоцита. Конкретные механизмы влияния не до конца выяснены и находятся в стадии изучения. В итоге глюкокортикостероиды оказывают двоякое действие: на фоне мышечной работы они стимулируют липолиз, а в состоянии покоя - ингибируют его. Установлено, что при развитии опухоли коры надпочечников или при введении высоких доз препаратов глюкокортикостероидов, наблюдается рост жировых запасов на лице и в верхней части туловища (синдром Иценко-Кушинга).
Половые гормоны: точный механизм их воздействия на жировой обмен пока не выяснен, но известно, что действуют эти гормонов связано со стимуляцией синтеза определенных белков. Действие половых гормонов однонаправленное: стимуляция распада жира. Ярким примером является действие тестостерона. Кастрация приводит к увеличению запасов жира.
Лептин (от лат. Leptos - тонкий, худой). По химической природе - полипептид, синтезируется в адипоцитах. Лептин - гормон жировой ткани (поэтому жировую ткань можно отнести к эндокринным). Рецепторы к лептину расположены в гипоталамусе и в тканях репродуктивной системы. Лептин снижает выработку нейропептида Y, который вызывает повышение аппетита и усиливает синтез жира (точные механизмы воздействия пока неясны). Лептин также стимулирует выработку разобщающих белков бурого жира. Суммарный эффект лептина: снижение аппетита и усиление липолиза. Концентрация лептина в крови пропорциональна количеству жировых клеток. Поэтому, можно считать, что лептин передает в головной мозг информацию о количестве жира в организме. Лептин также усиливает репродуктивную функцию человека. В настоящее время ведутся работы над созданием рекомбинантного лептина для лечения ожирения.
Продукты липолиза - глицерин и жирные кислоты выходят из жировой клетки, попадают в кровь и поступают в клетки других тканей. Глицерин как вещество гидрофильное растворяется в плазме крови. Жирные кислоты - гидрофобные вещества. Поэтому для транспорта в кровяном русле для них необходимы переносчики. Транспорт жирных кислот обеспечивают белки плазмы крови альбумины, образующие с ними комплексы. Такие комплексы образуются путем формирования слабых типов связей: гидрофобного взаимодействия радикалов жирных кислот и ионных связей СООН-групп жирных кислот с радикалами лизина молекулы альбумина. Следовательно, жирные кислоты в составе комплекса являются химически свободными. Жирные кислоты, находящиеся в комплексе с альбуминами, обозначаются термином неэстерифицированные жирные кислоты (НЭЖК). Уровень НЭЖК в крови - показатель степени мобилизации жира: чем больше в плазме крови НЭЖК, тем интенсивнее идет липолиз.
Липолиз происходит в ходе мышечной работы и при голодании, что сопоровождается повышением концентрации НЭЖК в крови. Глицерин и жирные кислоты в этой ситуации выступают как источники энергии.
Пути метаболизма глицерина.
Глицерин может быть повторно использован для синтеза жира или других липидов.
Глицерин может вступить в обмен углеводов.
В любом случае в первую очередь происходит активация глицерина.
Она похожа на активацию углеводов.
Распад глицерина по пути к углеводам.
Если глицерин распадается по пути к углеводам, то происходит дегидрирование.
Митохондриальная фосфоглицериндегидрогеназа содержит в качестве небелковой части ФАД, а цитоплазматическая - НАД. В митохондриях отщепляемый водород переносится по укороченной цепи митохондриального окисления, и образуется 2 молекулы АТФ (фосфоглицерин (ФГА) - субстрат укороченной цепи).
Для фосфоглицеринового альдегида существует два варианта дальнейших превращений.
ФГА может окисляться в ГБФ-пути до СО2 и Н2О с образованием 21 молекулы АТФ.
ФГА может вступить в реакции гликонеогенеза с образованием углеводов - глюкозы или гликогена.
Пути использования жирных кислот. Жирные кислоты могут вступать в реакции только после активации. Активация жирных кислот принципиально отличается от активации углеводов.
Реакция начинается с переноса от АТФ не фосфата, а АМФ, с образованием промежуточного продукта - ациладенилата. Затем с участием HS-KoA отщепляется АМФ, и образуется активная форма любой жирной кислоты - АЦИЛ-КоА.
Образовавшийся АМФ не может превратиться в АТФ. Поэтому протекает еще одна реакция, и тоже - с затратой АТФ: АМФ + АТФ ---> 2 АДФ.
Как видно, распад 1 АТФ до АМФ энергетически равен распаду 2-х АТФ до 2-х АДФ. Поэтому затраты энергии на активацию жирной кислоты составляют 2 АТФ на одну молекулу жирной кислоты.
Для активной жирной кислоты, как и для глицерина, возможны два пути метаболических превращений.
Синтез жира или других липидов.
Катаболизм до Ацетил-КоА. Этот процесс называют бета-окисление жирных кислот.
С уммарный
энергетический эффект окисления одной
молекулы глицерина равен 22 АТФ.
уммарный
энергетический эффект окисления одной
молекулы глицерина равен 22 АТФ.
О кисление
высших жирных кислот.
кисление
высших жирных кислот.
Источники ВЖК:
- липиды жировой ткани
- липопротеины
-триацилглицерины
-фосфолипиды клеточных биомембран
Окисление ВЖК происходят в митохондриях клеток, и называется бетта окислением. Доставка их к тканям и органам происходит при участии альбумина, а транспорт из цитоплазмы в митохондрии при участии карнитина.
Процесс бета-окисления ВЖК складывается из следующих этапов:
-активация ВЖК на наружной поверхности мембраны митохондрий при участии АТФ, конзима А и ионов магния с образованием активной формы ВЖК (ацил - КоА).
-транспорт жирных кислот внутрь митохондрий возможен при присоединении активной формы жирной кислоты к карантину, находящемуся на наружной поверхности внутренней мембраны митохондрий. Образуется ацил-карнитин, обладающий способностью проходить через мембрану. На внутренней поверхности комплекс распадается и карнитин возвращается на наружную поверхность мембраны.
-внутримитохондриальное окисление жирных кислот состоит из последовательных ферментативных реакций. В результате одного завершенного цикла окисления происходит отщепление от жирой кислоты одной молекулы ацетил-КоА, т.е. укорочение жирнокислотной цепи на два углеродных атома.Приэтом в результате двух дегидрогеназных реакций восстанавливается ФАД до ФАДН2 и НАД+ до НАДН2.
