
- •Начала квантовой химии и строение молекул
- •Решаемые задачи:
- •Модель Томсона (1904 г.)
- •Взаимное расположение электронов в атоме
- •Х. Гейгер и е. Марсден (1906-1909 г.)
- •Планетарная модель атома:
- •Серия Бальмера в спектре атома водорода (снизу указаны длины волн соответствующих линий в нм).
- •II. Способность атома поглощать и испускать излучение подчиняется закону, по которому излучение, связанное с переходом, должно быть монохроматическим и иметь частоту ν, определяемую соотношением
- •Зависимость силы анодного тока в цепи от ускоряющей разности потенциалов eVа.
- •Некоторые допустимые решения волнового уравнения для одномерных колебаний натянутой струны.
- •УравнениеШредингера
- •Решение уравнения Шредингера для простейших модельных систем
- •Квантовое число m может принимать значения
- •Спиновые квантовые числа некоторых элементарных частиц и атомных ядер.
- •Физический смысл квантовых чисел электрона
- •1. Размеры орбитали.
- •2. Энергию электронов, находящихся на орбитали.
- •Радиальное распределение для орбиталей атома водорода.
- •Теория и методы описания химической связи и строения молекул Метод валентных связей
- •В молекуле н2.
- •Зависимость полной энергии молекулы водорода от межъядерного расстояния
- •Результаты теоретических и экспериментальных определений энергии и длины связи в молекуле н2
- •Основные принципы метода
- •1. Перекрывающиеся ао должны иметь близкие энергии.
- •2. Взаимодействующие ао должны перекрываться в значительной области пространства.
- •3. Ао должны обладать одинаковыми свойствами симметрии относительно оси связи в молекуле.
- •Изменение значений scc в зависимости от межатомного расстояния с─с
- •Водородоподобные.
- •Слетеровские функции (sto).
- •Гауссовские функции (gto). Наименьшие базисные наборы, обеспечивающие описание
- •Число кулоновскихинтеграллов для молекуле пропана, возникающих в различных методах расчета.
- •Сравнительная характеристика полуэмпирических методов.
- •Indo – Intermediate Neglect of Differential Overlap – частичное пренебрежение дифференциальным перекрыванием.
- •Симметрия молекулярных систем Элементы и операции симметрии
- •Оси и плоскости симметрии куба
- •Плоскости симметрии на примере комплексного иона [CuF4]─.
- •1. Правило соответствия
- •2. Правило ассоциативности группового умножения
- •Квантово-химическое описание реакций Квантовая теория химических реакций Понятие о поверхностях потенциальной энергии.
- •Симметрия и относительная энергия мо бутадиена (а) и этилена (б).
- •Схемы строения переходных комплексов для реакции димеризации этилена и взаимодействия этилена с бутадиеном.
- •Симметрия переходного состояния реакции взаимодействия этилена с бутадиеном
Начала квантовой химии и строение молекул
«Все должно быть изложено так просто, как только возможно, но не проще».
А. Эйнштейн.
Квантовая химия – раздел теоретической химии, в котором строение, свойства и взаимодействия веществ исследуются на основе представлений квантовой механики и экспериментально установленных закономерностей.
Решаемые задачи:
- изучение биологических и биологически активных веществ, исследование структуры высокоперспективных материалов, например высокотемпературных сверхпроводников, углеродных нанотрубок, фуллеренов;
- изучение супрамолекулярных систем - сложных образований, являющихся результатом ассоциации нескольких химических частиц, связанных вместе межмолекулярными взаимодействиями.
- исследование комплексных соединений, динамических свойств атомов и ионов в различных кристаллических и молекулярных структурах, и др.
Результаты квантово-химических исследований необходимо подтверждать ключевыми экспериментами.
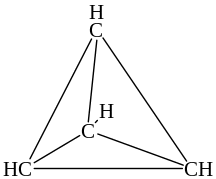
Тетраэдран
Нобелевскими премиями были награждены:
Л. Полинг за теорию гибридизации
Р. Хоффманн и К. Фукуи за развитие квантово-химической теории механизмов реакций
Р. Керл, Х. Крото и Р. Смолли за обнаружение по УФ спектрам межзвездного газа нанотрубок и последующий их синтез
А.А. Бочвар и Е.Г. Гальперн теоретически предсказали фуллерены и рассчитали их электронную структуру
М.Ю. Корнилов предсказал нанотрубки, которые позднее были открыты.
Открытие сложного строения атома
М. Фарадей установил, что электрические заряды, как и материя, имеют дискретный характер и существует некий минимальный заряд.
Эксперименты с газоразрядными трубками показали, что в состав атомов должны входить отрицательно заряженные частицы, которые впоследствии были названы электронами.
Схема опыта У. Крукса
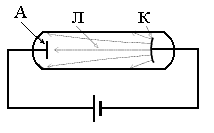
A - анод, K - катод, Л - катодный луч
Модель Томсона (1904 г.)
Положительный заряд равномерно распределен по всему объему атома. Отрицательньно заряженные электроны, образуя правильные конфигурации, закономерно вкраплены в эту положительную сферу. Их суммарный заряд равен положительному заряду сферы. Число и расположение электронов зависит от природы атома. Электроны находятся в равновесных положениях и при возбуждении могут колебаться около них, излучая в пространство электромагнитные волны.
Взаимное расположение электронов в атоме
|
Число электронов в кольце |
||||||||||
Кольцо 1 |
5 |
6 |
7 |
8 |
8 |
8 |
9 |
10 |
10 |
10 |
11 |
Кольцо 2 |
1 |
1 |
1 |
1 |
2 |
3 |
3 |
3 |
4 |
5 |
5 |
