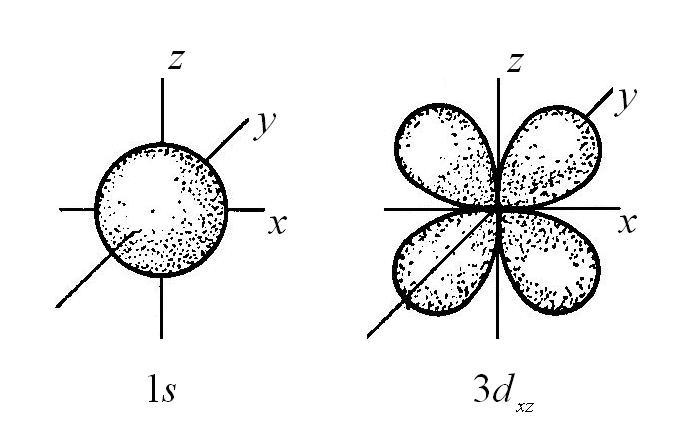- •Начала квантовой химии и строение молекул
- •Решаемые задачи:
- •Модель Томсона (1904 г.)
- •Взаимное расположение электронов в атоме
- •Х. Гейгер и е. Марсден (1906-1909 г.)
- •Планетарная модель атома:
- •Серия Бальмера в спектре атома водорода (снизу указаны длины волн соответствующих линий в нм).
- •II. Способность атома поглощать и испускать излучение подчиняется закону, по которому излучение, связанное с переходом, должно быть монохроматическим и иметь частоту ν, определяемую соотношением
- •Зависимость силы анодного тока в цепи от ускоряющей разности потенциалов eVа.
- •Некоторые допустимые решения волнового уравнения для одномерных колебаний натянутой струны.
- •УравнениеШредингера
- •Решение уравнения Шредингера для простейших модельных систем
- •Квантовое число m может принимать значения
- •Спиновые квантовые числа некоторых элементарных частиц и атомных ядер.
- •Физический смысл квантовых чисел электрона
- •1. Размеры орбитали.
- •2. Энергию электронов, находящихся на орбитали.
- •Радиальное распределение для орбиталей атома водорода.
- •Теория и методы описания химической связи и строения молекул Метод валентных связей
- •В молекуле н2.
- •Зависимость полной энергии молекулы водорода от межъядерного расстояния
- •Результаты теоретических и экспериментальных определений энергии и длины связи в молекуле н2
- •Основные принципы метода
- •1. Перекрывающиеся ао должны иметь близкие энергии.
- •2. Взаимодействующие ао должны перекрываться в значительной области пространства.
- •3. Ао должны обладать одинаковыми свойствами симметрии относительно оси связи в молекуле.
- •Изменение значений scc в зависимости от межатомного расстояния с─с
- •Водородоподобные.
- •Слетеровские функции (sto).
- •Гауссовские функции (gto). Наименьшие базисные наборы, обеспечивающие описание
- •Число кулоновскихинтеграллов для молекуле пропана, возникающих в различных методах расчета.
- •Сравнительная характеристика полуэмпирических методов.
- •Indo – Intermediate Neglect of Differential Overlap – частичное пренебрежение дифференциальным перекрыванием.
- •Симметрия молекулярных систем Элементы и операции симметрии
- •Оси и плоскости симметрии куба
- •Плоскости симметрии на примере комплексного иона [CuF4]─.
- •1. Правило соответствия
- •2. Правило ассоциативности группового умножения
- •Квантово-химическое описание реакций Квантовая теория химических реакций Понятие о поверхностях потенциальной энергии.
- •Симметрия и относительная энергия мо бутадиена (а) и этилена (б).
- •Схемы строения переходных комплексов для реакции димеризации этилена и взаимодействия этилена с бутадиеном.
- •Симметрия переходного состояния реакции взаимодействия этилена с бутадиеном
Радиальное распределение для орбиталей атома водорода.
Нормированные действительные угловые волновые функции
Орбиталь |
Ylm |
Орбиталь |
Ylm |
s |
|
dyz |
|
pz |
|
|
|
px |
|
|
|
py |
|
|
|
|
|
|
|
|
|
|
|
dxz |
|
|
|
dxy |
|
|
|
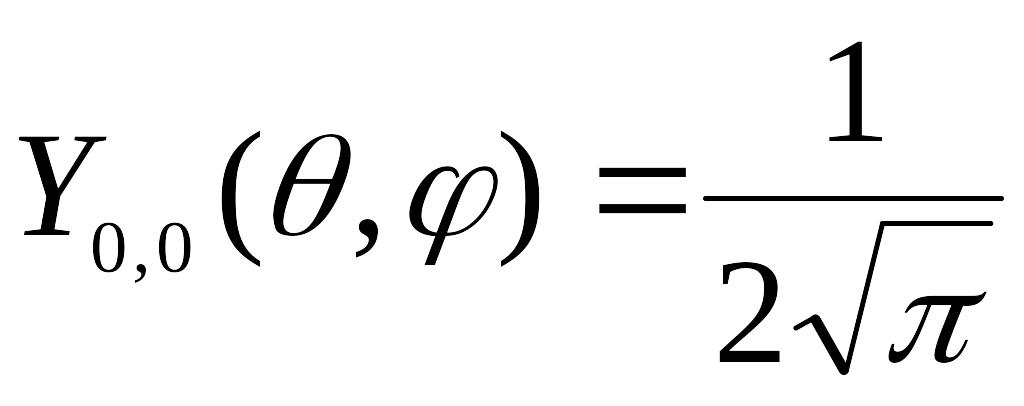
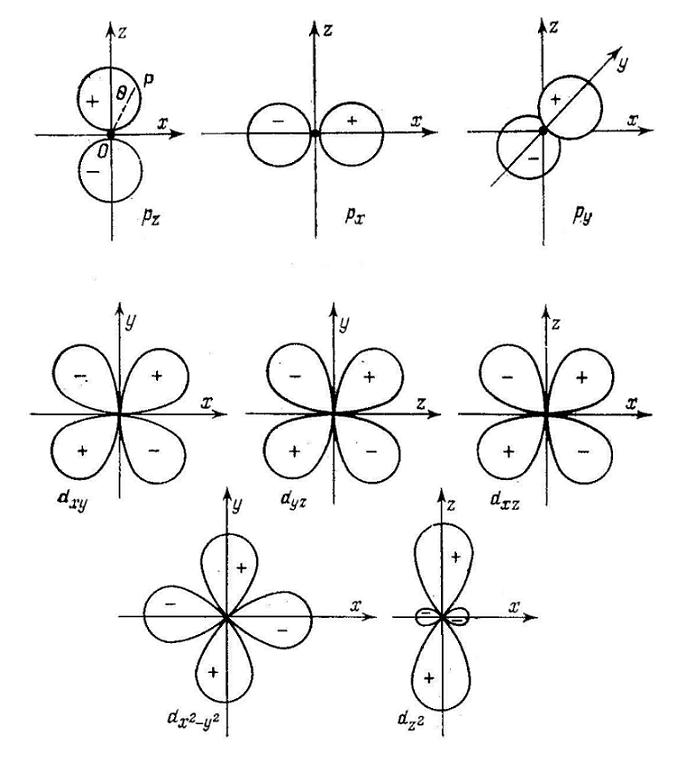
Орбитальные диаграммы для p и d орбиталей.
а |
б |
в |
|
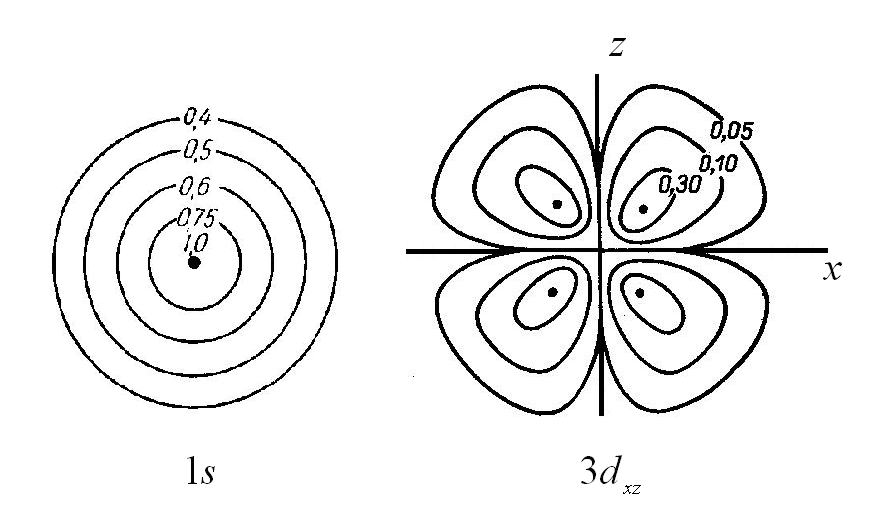
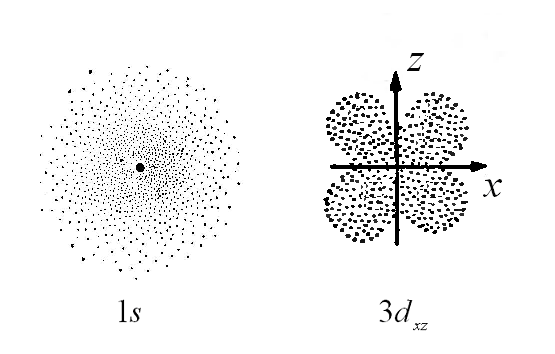
Различные способы изображения атомных орбиталей
на примере 1s и 3dxz – орбиталей
а – граничная поверхность, б – диаграммы электронной плотности, в – зарядовое облако
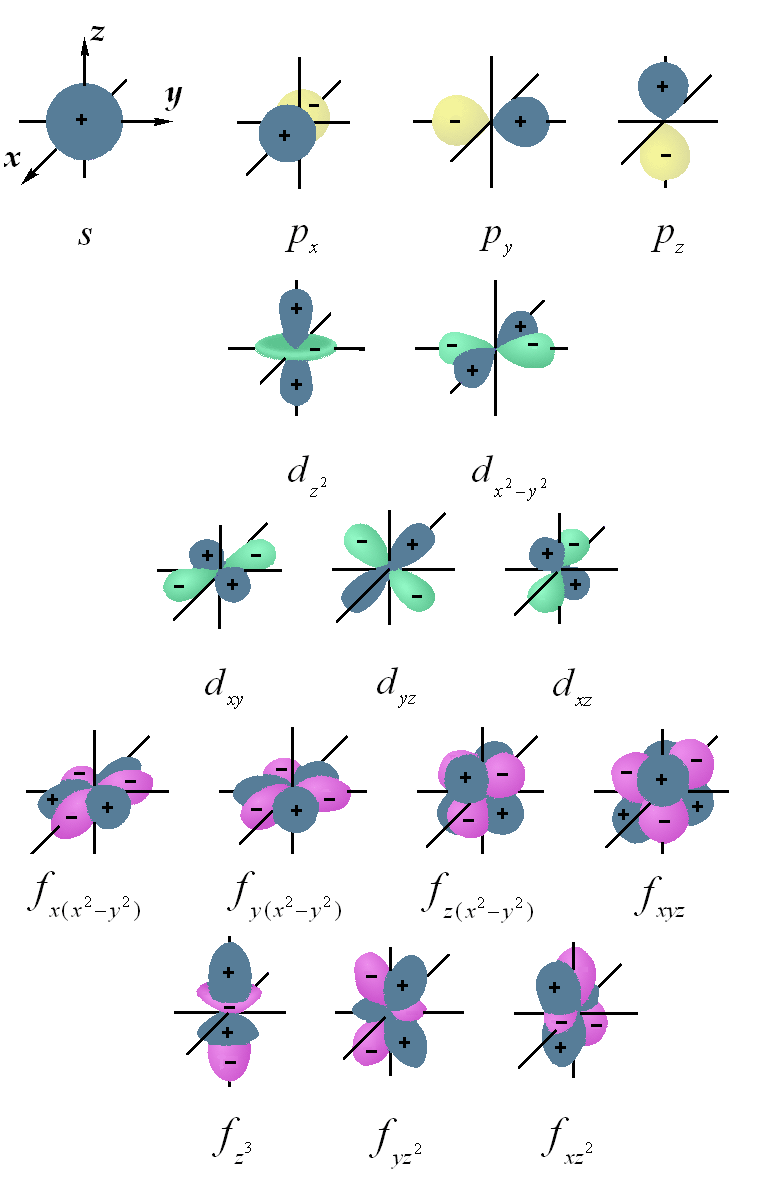
Форма атомных орбиталей s-, p-, d- и f- типа.
Строение многоэлектронных атомов
Методы решения волнового уравнение для многоэлектронных атомов
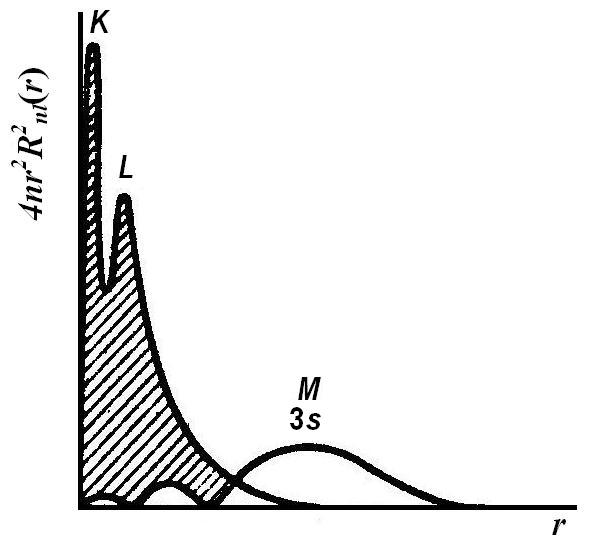
Радиальное распределение вероятности нахождения
электронов в атоме натрия
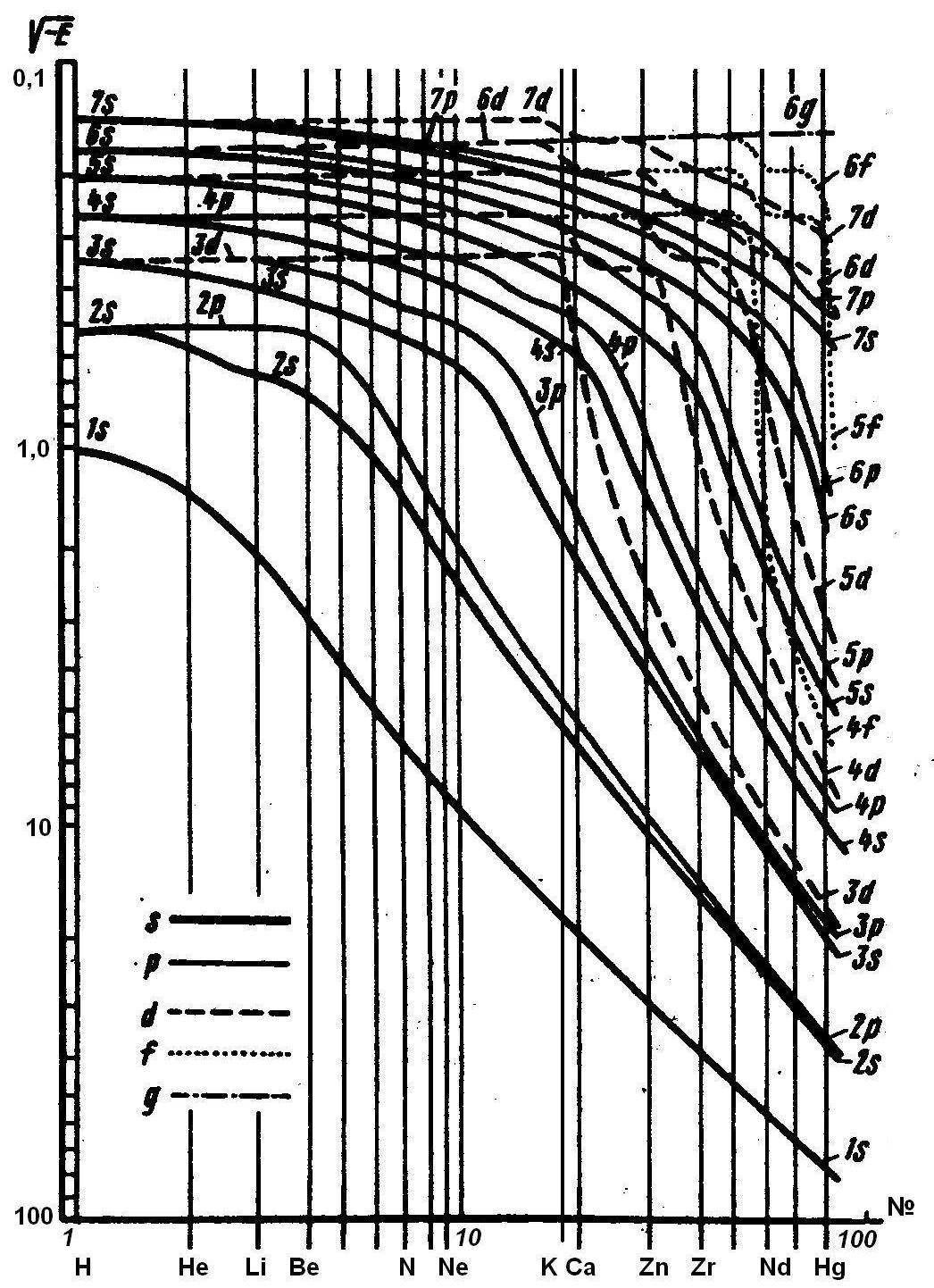
Зависимость энергии атомных орбиталей от порядкового
номера элемента.
Принцип Паули - в данном атоме или молекуле не может быть электронов, у которых бы все четыре квантовых числа совпадали; любая электронная, волновая функция должна, быть антисимметрична по отношению к перестановке любой пары электронов.
Правило Хунда - в пределах одного подуровня электроны распределяются по орбиталям таким образом, чтобы модуль суммы их спиновых квантовых чисел был максимальным.
Принцип минимума энергии - наиболее устойчивыми состояниями любой системы являются состояния с минимальным запасом энергии.
Энергия подуровней растет в ряду:
1s < 2s < 2р < 3s < 3р < 4s < 3d < 4р < 5s < 4d < 6p < 6s < 4f ≈ 5d<6p<7s<5f ≈ 6d < 7p...
1-е правило Клечковского − уровни и подуровни атомов заполняются электронами в порядке возрастания суммы главного и орбитального квантовых чисел (n + l).
2-е правило Клечковского − при одном и том же значении суммы (n + l) заполнение подуровней происходит в порядке возрастания главного квантового числа п.
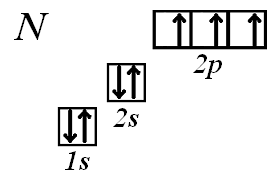
Электронная конфигурация (формула) атома − это условная запись распределения электронов по орбиталям в основном состоянии этого атома.
[Ne] ≡ 1s22s22p6; [Cl] ≡ 1s22s22p63s23p5 или [Ne] 3s23p5
1s2 2s 22px2py
Хром [Ar]3d54s1, медь [Ar]3d104s1, палладий [Kr]4d105s1,
ниобий [Kr]4d45s1, рутений [Kr]4d75s1, родий [Kr]4d85s1,
платина [Xe]4f145d85s1
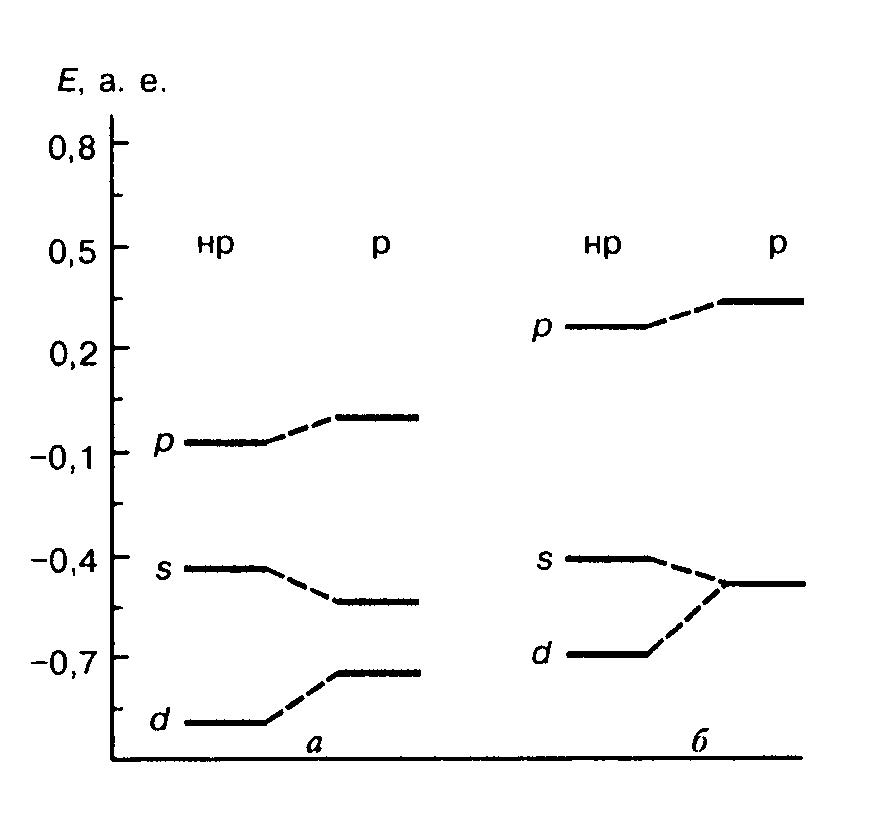
Энергетические уровни, в рассчитанные в релятивистском (р) и нерелятивистском (нр) приближениях:
а – атом ртути; б – кристаллическая фаза.
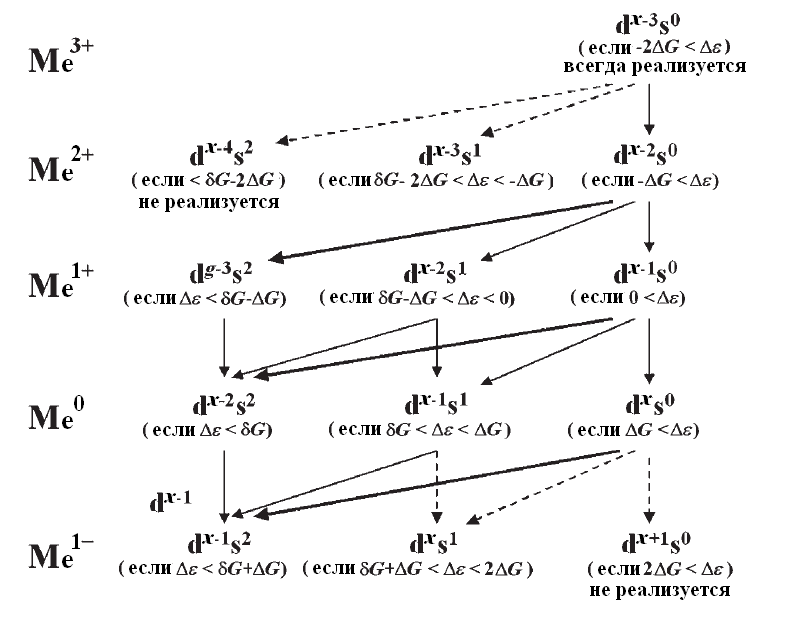
Возможные электронные конфигурации атомов и ионов переходных металлов и переходы между ними
V [Ar]3d34s2 → V+ [Ar]3d44s0
Ti [Ar]3d25s2 → Ti+ [Ar]3d25s1
Y [Ar]4d15s2 → Y+ [Ar]4d05s2
Δε = Es – Ed – разница в энергии между внешним s-АО и предвнешней d – АО
δG = Gds – Gss
ΔG = Gdd – Gds, где Gij – энергия взаимодействия между электронами, находящимися на АО i и j
Gss < Gds < Gdd
+