
методичка р-элементы
.pdf71
или дегидратацией азотной кислоты:
4НNO3 + Р4O10 = 2N2O5 + 4HPO3
Азотистая кислота, НNO2, — слабая кислота ((Ka = 5·10–4), существует только в раз-
бавленных растворах, легко разлагается:
3НNO2 = HNO3 + 2NO + H2O
Соли азотистой кислоты — нитриты — устойчивы. Кислота и ее соли проявляют окислительно-восстановительную двойственность с преобладанием восстановительных свойств:
5KNO2 + 2KМnО4 + 3Н2SO4 = 5KNO3 + 2МnSO4 + 3Н2O
Окислительные свойства нитритов проявляются при взаимодействии только с силь-
ными восстановителями:
NaNO2 + Zn + 5NaOH + 5H2O = NH3 + 3Na2[Zn(OH)4]
Азотная кислота, HNO3, — бесцветная жидкость. В промышленности азотную кис-
лоту получают каталитическим окислением аммиака:
Pt
4NH3 + 5O2  4NO + 6H2O
4NO + 6H2O
2NO + O2 = 2NO2
4NO2 + O2 + 2H2O = 4HNO3
В лаборатории азотную кислоту получают обработкой концентрированной серной кислотой безводного нитрата калия.
При нагревании азотная кислота разлагается:
4НNO3 = 4NO2 + О2 + 2Н2O
Обычно используют 65–68 % кислоту, ρ = 1,41 г/мл.
3.2.9. Взаимодействие азотной кислоты с металлами и неметаллами
Азотная кислота — сильный окислитель. В зависимости от концентрации кислоты и активности восстановителя НNO3 восстанавливается до NО2, NO, N2O и NН4NO3. Чем ак-
тивнее восстановитель и меньше концентрация кислоты, тем выше степень восстановле-
ния азота (см. табл. 3.1.).
72
Таблица 3.1. Окислительные свойства азотной кислоты разных концентраций при взаимодействии с металлами и неметаллами
|
Продукты восстановления азотной кислоты |
|||
Концентрация |
|
|
|
|
активные металлы |
неактивные |
|
||
азотной кислоты |
|
|||
металлы |
неметаллы |
|||
(φ° < 0) |
||||
|
||||
|
(φ° > 0) |
|
||
|
|
|
||
|
|
|
|
|
Концентрированная |
NO2 |
NO2 |
NO2 |
|
(w > 60%) |
||||
|
|
|
||
Средней |
|
|
|
|
концентрации |
NO |
NO |
NO |
|
(w = 25–30%) |
|
|
|
|
Разбавленная |
N2O, N2 |
не реагирует |
не реагирует |
|
(w = 10–15%) |
||||
|
|
|
||
Очень разбавленная |
NH4NO3 |
не реагирует |
не реагирует |
|
(w < 5%) |
||||
|
|
|
||
|
|
|
|
|
Сильные окислительные свойства проявляет «царская водка». «Царская водка» —
смесь концентрированных азотной и соляной кислот в объемном отношении 1:3.
Сильное окислительное действие «царской водки» обусловлено выделением атомар-
ного хлора:
НNO3 + 3НСl = 2Сl + NОСl + 2Н2O NOCl = NO + Cl
«Царская водка» растворяет такие малоактивные металлы, как платина и золото.
Например:
Аu + НNO3 +3НСl =АuСl3 + NO + 2Н2O
При избытке «царской водки» или соляной кислоты происходит образование ком-
плексных соединений золота:
АuСl3 + NOCl = NO[AuCl4]
АuСl3 + НСl = Н[AuCl4]
3.2.10. Термическое разложение солей азотной кислоты
73
Соли азотной кислоты — нитраты — термически нестойки и при нагревании разла-
гаются с выделением кислорода. Состав продуктов разложения определяется природой металла, входящего в соль. Нитраты щелочных металлов образуют нитриты:
2KNO3 = 2KNO2 + O2,
нитраты менее активных металлов — оксиды:
2Zn(NO3)2 = 2ZnO + 4NO2 + O2,
а нитраты благородных металлов — свободные металлы: 2АgNO3 = 2Аg + 2NO2 + O2
Окислительные свойства солей азотной кислоты можно подтвердить следующими реакциями:
а) окисление МnO2 в щелочной среде при сплавлении:
KNO3 + 2KОН + МnO2 = K2MnO4 + KNO2 + Н2O
б) восстановление в щелочном растворе активными металлами (Аl, Zn) нитратов до аммиака:
3KNO3 + 8Аl + 5KОН + 18Н2O = 8K[Al(ОН)4] + 3NH3
3.3. ЛАБОРАТОРНАЯ РАБОТА «АЗОТ И ЕГО СОЕДИНЕНИЯ»
Опыт 1. Получение азота
Собрать прибор для получения газа (см. рис. 3.3.1). В пробирку налить по 2–3 мл насыщенных растворов хлорида аммония и нитрита натрия. Смесь нагреть. Полученный газ собрать в пробирку и поместить в нее тлеющую лучину. Поддерживает ли газ горение?
Написать уравнение реакции получения азота.
NH4Cl + NaNO2 нагрев

74
2 |
3 |
|
1
4
Рис. 3.3.1. Прибор для получения газов, нерастворимых в воде: 1 – пробирка с реак-
ционной смесью; 2 – газоотводная трубка; 3 – пробирка с водой; 4 – стакан с водой
Опыт 2. Получение аммиака
В фарфоровый тигель поместить по 2–3 микрошпателя сульфата аммония и гидрок-
сида кальция. Смесь тщательно перемешать стеклянной палочкой, отметить запах аммиа-
ка. Смесь перенести в пробирку, закрыть пробкой с газоотводной трубкой и нагреть на слабом пламени спиртовка. К отверстию газоотводной трубки поднести влажную красную лакмусовую бумагу и отметить изменение ее цвета, затем поднести стеклянную палочку,
смоченную концентрированным раствором соляной кислоты. Написать уравнения реак-
ций получения аммиака и взаимодействия его с хлоридом водорода. (NH4)2SO4 + Ca(OH)2 →
NH3 + HCl →
Опыт 3. Свойства аммиака
3.1. Растворение аммиака в воде. В пробирке с газоотводной трубкой получить аммиак (см. опыт 2). Конец газоотводной трубки опустить в пробирку, наполненной водой с несколькими каплями раствора фенолфталеина (рис. 3.3.2). Несмотря на то, что аммиак непрерывно поступает в трубку, пробулькивания газа через жидкость не наблюдается. О
чем это свидетельствует? Как изменяется окраска жидкости в трубке Пелиго? Почему?

75
2

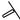 3 1
3 1 
Рис. 3.3.2. Прибор для получения водного раствора аммиака: 1 – пробирка со смесью сульфата аммония и гидроксида кальция; 2 – газоотводная трубка; 3 – пробирка с водой, содержащей фенолфталеин
Какое равновесие устанавливается в водном растворе аммиака? Как сместится это равновесие при добавлении к водному раствору аммиака хлорида аммония, сульфата алюминия, а также при нагревании?
3.2. Каталитическое окисление аммиака кислородом воздуха (демонстрацион-
ный). В колбу вместимостью 2–3 л поместить 10–15 мл 25%-ного раствора аммиака. Кол-
бу слегка нагреть, чтобы она заполнилась газообразным аммиаком. Затем поместить в нее небольшими порциями нагретый в металлической ложке порошок оксида хрома(III).
Наблюдать огненный дождь из частиц оксида хрома(III), которые раскаляются из-за экзо-
термической реакции окисления аммиака на их поверхности. Написать уравнение реакции каталитического окисления аммиака до оксида азота(II).
NH3 + Cr2O3 нагрев
3.3. Восстановительные свойства аммиака. В одну пробирку поместить 2–3 капли бромной воды, в другую — столько же раствора перманганата калия (c = 0,5 моль/л). В
каждую из пробирок добавить по 3–4 капли 25%-ного раствора аммиака. Содержимое пробирок слегка подогреть до изменения окраски растворов. Написать уравнения соответ-
ствующих реакций, учитывая, что аммиак окисляется до свободного азота, а перманганат калия восстанавливается до оксида марганца(IV).
NH3·H2O + KMnO4 → NH3·H2O + Br2 →
Стехиометрические коэффициенты определить ионно-электронным методом.
76
Опыт 4. Свойства солей аммония
4.1. Гидролиз солей аммония. В две пробирки поместить по 4–6 капель дистилли-
рованной воды и по 1 капле нейтрального раствора лакмуса. В одну из пробирок добавить
1 микрошпатель кристаллов хлорида аммония, в другую — столько же нитрата аммония.
Содержимое пробирок перемешать стеклянной палочкой. Отметить изменение окраски лакмуса в каждой пробирке. Написать в молекулярной и ионной формме уравнения реак-
ций гидролиза NH4Cl и NH4NO3.
NH4Cl + H2O →
NH4NO3 + H2O →
4.2. Термическое разложение солей аммония. В пробирку поместить 3–4 мик-
рошпателя хлорида аммония и закрыть пробирку пробкой с газоотводной трубкой. Закре-
пить трубку в лапках штатива с небольшим наклоном. Затем нагреть соль на пламени спиртовки. К отверстию трубки поместить влажную лакмусовую бумагу. Отметить изме-
нение ее цвета. Какой газ выделяется? Аналогично провести опыт с сульфатом аммония.
Написать уравнения реакций термического разложения солей, учитывая, что при этом из сульфата аммония образуется гидросульфат аммония.
NH4Cl нагрев
(NH4)2SO4 нагрев
Опыт 5. Качественная реакция на ион аммония
В пробирку поместить 2–3 капли раствора хлорида аммония (c = 0,5 моль/л) и столь-
ко же капель раствора гидроксида натрия (калия) (c = 2 моль/л). Содержимое пробирки слегка нагреть. Отметить выделение аммиака по запаху и по изменению цвета влажной красной лакмусовой бумаги, поднесенной к отверстию пробирки. Написать уравнение ре-
акции в молекулярной и ионной форме. NH4Cl + NaOH →
Опыт 6. Окислительно-восстановительные свойства гидразина и гидроксиламина
Гидразин, N2H4, и гидроксиламин, NH2OH, удобнее брать в виде их солей — хлорида
(сульфата) гидразиния (либо N2H4·HCl, либо N2H4·2HCl) и хлорида (сульфата) гидрокси-
77
аммония NH2OH·HCl. В уравнениях реакций можно записывать эти соли в виде гидразина или гидроксиламина.
6.1. Взаимодействие гидразина и гидроксиламина с перманганатом калия в
кислой среде. В две пробирки поместить по 3–4 капли раствора перманганата калия (c = 0,5 моль/л) и 1–2 капли раствора серной кислоты (c = 1 моль/л). В одну из пробирок доба-
вить 1–2 кристалла хлорида (сульфата) гидразиния, а во вторую — 1–2 кристалла хлорида
(сульфата) гидроксиаммония. Отметить обесцвечивание растворов. Написать уравнения реакций, учитывая, что гидразин и гидроксиламин окисляются до азота, а перманганат-
ион переходит в ион Mn2+.
N2H4 + KMnO4 + H2SO4 → NH2OH + KMnO4 + H2SO4 →
Стехиометрические коэффициенты определить ионно-электронным методом.
6.2. Взаимодействие гидроксиламина с сульфатом железа(II) в кислой среде. В
пробирку поместить 1 микрошпатель соли Мора [в уравнении реакции следует писать сульфат железа(II)], 5–6 капель дистиллированной воды и перемешать стеклянной палоч-
кой до растворения осадка. Затем добавить 2–3 капли раствора серной кислоты (c = 1 моль/л) и 1–2 кристалла хлорида гидроксиаммония. Содержимое пробирки снова пере-
мешать стеклянной палочкой. Что наблюдается? В полученную смесь добавить 1 каплю раствора тиоцианата аммония (c = 0,5 моль/л). В какой цвет окрашивается раствор? О
присутствии какого иона это свидетельствует? Написать уравнение реакции, учитывая,
что гидроксиламин восстанавливается до иона аммония.
NH2OH + FeSO4 + H2SO4 →
Стехиометрические коэффициенты определить ионно-электронным методом.
Опыт 7. Получение оксидов азота и исследование их свойств
Все опыты с оксидами азота проводить в вытяжном шкафу!
7.1. Получение оксида азота(I). В сухую пробирку поместить 2–3 микрошпателя нитрата аммония и осторожно нагреть. Наблюдать плавление соли и затем ее разложе-
ние (не нагревать пробирку выше 250 °С, так как при большей температуре разложение может пойти со взрывом). Написать уравнение реакции термического разложения нит-
рата аммония.
NH4NO2 нагрев
78
7.2. Получение оксида азота(II). В пробирку внести 2–3 кусочка медной стружки и
2–4 капли раствора азотной кислоты (c = 2 моль/л). Пробирку закрыть пробкой с газоот-
водной трубкой, которую затем погрузить в кристаллизатор с водой. Другую пробирку наполнить водой и, закрыв отверстие, поместить в кристаллизатор с водой вверх дном.
Открыв пробирку под водой, следить за тем, чтобы в нее не проник воздух. Пробирку с медными стружками и кислотой слегка подогреть на пламени горелки. Когда начнется энергичное выделение газа, подвести конец газоотводной трубки к отверстию переверну-
той пробирки и собрать выделяющийся газ. Отметить цвет оксида азота(II). Вынуть про-
бирку из кристаллизатора, перевернуть вверх отверстием и внести в нее тлеющую лучину.
Поддерживает ли горение оксид азота(II)? Удалить лучину, поставить пробирку в штатив и наблюдать на белом фоне за изменением цвета газа. Написать уравнения реакций меди с азотной кислотой и окисления оксида азота(II) в оксид азота(IV).
Cu + HNO3(разб.) нагрев NO + O2 →
7.3. Получение оксида азота(IV). В пробирку поместить 2–3 кусочка медной струж-
ки и добавить 2–4 капли концентрированного раствора азотной кислоты. Пробирку за-
крыть пробкой с газоотводной трубкой и нагреть на пламени горелки. Затем конец газоот-
водной трубки опустить в сухую пробирку и собрать выделяющийся газ. Когда пробирка заполнится бурыми парами оксида азота(IV), вынуть газоотводную трубку и добавить 2–
3 мл дистиллированной воды. Закрыть пробирку пробкой и энергично встряхнуть. Что наблюдается? К полученному раствору добавить 1 каплю нейтрального раствора лакмуса.
В какой цвет окрашивается раствор? О чем это свидетельствует? Написать уравнение ре-
акции меди с концентрированной азотной кислотой и уравнение реакции оксида азота(IV)
с водой.
Cu + HNO3(конц.) нагрев
NO2 + H2O →
Опыт 8. Окислительно-восстановительные свойства солей азотистой кислоты
В пробирку поместить 2–3 капли раствора перманганата калия (c = 0,5 моль/л), в
другую пробирку — 2–3 капли раствора дихромата калия (c = 0,25 моль/л), в третью — столько же раствора йодида калия (c = 0,5 моль/л). Во все пробирки добавить по 2–3 капли раствора серной кислоты (c = 1 моль/л), а в пробирку с раствором йодида калия — еще 1

79
каплю раствора крахмала. Во все три пробирки добавить по 4–5 капель раствора нитрита калия (c = 0,5 моль/л). Отметить изменение окраски растворов в каждой пробирке. Напи-
сать уравнения реакций, учитывая, что при взаимодействии с йодидом калия нитрит калия восстанавливается до оксида азота(II).
KNO2 + KMnO4 + H2SO4 →
KNO2 + K2Cr2O7 + H2SO4 → KNO2 + KI + H2SO4 →
Стехиометрические коэффициенты определить ионно-электронным методом.
Опыт 9. Свойства азотной кислоты
9.1. Разложение азотной кислоты при нагревании. Поместить 4–5 капель концен-
трированного раствора азотной кислоты в пробирку, закрепить ее в лапке штатива и нагревать до кипения. Что наблюдается? Поднести к краю пробирки тлеющую лучину.
Что происходит? О чем это свидетельствует? Написать уравнение реакции термического разложения азотной кислоты.
HNO3 нагрев
9.2. Взаимодействие азотной кислоты с металлами1. В одну пробирку поместить 1
микрошпатель порошка цинка, в другую — кусочек стружки железа. Добавить в каждую пробирку по 3–4 капли раствора азотной кислоты (c = 2 моль/л). Наблюдать выделение газа. Написать уравнения реакций цинка и железа с разбавленной азотной кислотой, учи-
тывая, что с цинком восстановление азотной кислоты может идти до азота, а с железом — до оксида азота(II). Железо при этом окисляется до иона Fe3+. Как доказать образование иона Fe3+?
Zn + HNO3(разб.) →
Fe + HNO3 (разб.) →
Аналогично провести опыт с концентрированным раствором кислоты. Происходит ли взаимодействие железа с концентрированной азотной кислотой? Затем пробирку нагреть. Что происходит? Написать уравнения реакций, учитывая, что образуется ион
Fe3+.
Zn + HNO3(конц.) →
1 Взаимодействие разбавленной и концентрированной азотной кислоты с медью рассматривалось в опытах 7.2 и 7.3
80
Fe + HNO3 (конц.) нагрев
Опыт 10. Свойства солей азотной кислоты
10.1. Окислительные свойства нитратов. В две пробирки поместить по 6–8 капель раствора нитрата калия (c = 0,5 моль/л) и 4–5 капель концентрированного раствора гид-
роксида натрия. В одну пробирку поместить 1 микрошпатель порошка цинка, а в дру-
гую — алюминия и осторожно нагреть, не доводя растворы до кипения. Обнаружить вы-
деляющийся аммиак по запаху и с помощью лакмусовой бумаги. Написать уравнения ре-
акций, учитывая, что в щелочной среде цинк и алюминий образует комплексные ионы со-
ответственно [Zn(OH)4]2– и [Al(OH)6]3–. Zn + NaOH + H2O нагрев
Al + NaOH + H2O нагрев
Стехиометрические коэффициенты определить ионно-электронным методом.
10.2. Термическое разложение солей азотной кислоты. В три сухие пробирки вне-
сти по 1 микрошпателю соответственно нитрата свинца, нитрата серебра и нитрата калия.
Укрепить пробирки в лапках штатива в вертикальном положении и нагревать до разложе-
ния солей. Отметить выделение бурого газа в первых двух пробирках. Внести в каждую пробирку тлеющую лучину. Что наблюдается? О выделении какого газа это свидетель-
ствует? Написать уравнения реакций термического разложения солей, учитывая, что при разложении нитрата свинца образуется оксид свинца(II), а при разложении нитрата сереб-
ра образуется серебро.
Pb(NO3)2 нагрев
AgNO3 нагрев
KNO3 нагрев
10.3. Горение угля и серы в расплавленном нитрате калия (демонстрационный,
проводить в вытяжном шкафу!). В пробирку из термостойкого стекла поместить 4–6
микрошпателей нитрата калия и укрепить ее в лапке штатива в вертикальном положении над фарфоровой чашкой, наполненной песком. Нагреть пробирку до расплавления соли и выделения пузырьков газа. Осторожно внести пинцетом в расплав маленький кусочек уг-
ля и продолжать нагревание. Когда уголь загорится, бросить в пробирку маленький кусо-
чек серы. Наблюдать бурное протекание реакции (иногда может происходить плавление
