
- •Кафедра физической и коллоидной химии
- •Учебно-целевая программа раздела
- •Знания, умения, навыки, которые должен приобрести студент.
- •Занятие № 1. Сталагмометрическое определение поверхностного натяжения водных растворов поверхностно-активных веществ (пав) и расчет размеров их молекул. План-конспект теоретической самоподготовки
- •Поверхностное натяжение.
- •Поверхностно-активные вещества
- •Свойства поверхностно-активных веществ
- •Сталагмометрическое определение поверхностного натяжения водных растворов пав.
- •Вопросы для самопроверки
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Занятие № 2. Определение критической концентрации мицеллообразования поверхностно-активных веществ с использованием метода наибольшего давления пузырьков воздуха (по Ребиндеру).
- •2.1. Мицеллообразование. Критическая концентрация мицеллообразования.
- •2.2. Способы определения критической концентрации мицеллообразования. Свойства мицеллярных растворов.
- •Вопросы для самопроверки
- •Занятие № 3. Адсорбция. Изучение адсорбции поверхностно-активных веществ на твердых сорбентах. План-конспект теоретической самоподготовки
- •3.1. Когезия. Адгезия. Растекание. Смачивание.
- •Гидрофилизация гидрофобизация
- •3.2. Адсорбция. Виды адсорбции. Уравнения Ленгмюра и Фрейндлиха.
- •3.3. Особенности адсорбции на границе раздела фаз твердое тело – жидкость. Экспериментальное определение адсорбции.
- •3.4. Адсорбция ионов из водных растворов электролитов.
- •3.5. Хроматография. Хроматографические методы.
- •Вопросы для самопроверки
- •Рекомендуемая литература: Основная
- •Дополнительная
- •Содержание
- •Для записей
- •357532, Г. Пятигорск, пр. Калинина, 11.
Вопросы для самопроверки
Что называется мицеллообразованием?
Что такое мицелла ПАВ?
Что называется критической концентрацией мицеллообразования?
Как зависит форма мицелл от концентрации ПАВ?
На чем основаны способы определения ККМ?
Что такое солюбилизация?
Какие виды солюбилизации различают?
Где применяется солюбилизация?
Что такое высаливание, почему оно происходит, чем вызывается?
обратную солюбилизацию, при которой солюбилизируются нерастворимые в воде органические вещества;
Занятие № 3. Адсорбция. Изучение адсорбции поверхностно-активных веществ на твердых сорбентах. План-конспект теоретической самоподготовки
3.1. Когезия. Адгезия. Растекание. Смачивание.
Когезия – явление притяжения (сцепления) частиц вещества: атомов, молекул, ионов – внутри одной фазы.
Работа, связанная с преодолением сил когезии, т.е. направленная на разъединение гомогенной фазы (тела), называется работой когезии.
Адгезия – явление притяжения (сцепления) приведенных в контакт разнородных твердых или жидких тел. Прочность сцепления разнородных фаз при адгезии называется адгезионной прочностью. В фармацевтической технологии адгезионная прочность является одной из характеристик, описывающих свойства таких лекарственных форм, как пластыри, драже, таблетки и др.
При одновременном контакте трех разнородных фаз - твердого тела, жидкости и газа (чаще всего – воздуха) наблюдается явление смачивания твердой поверхности жидкостью.
Угол, образованный между твердой поверхностью и плоскостью, касательной к поверхности капли и проведенной через какую-либо точку контура смачивания называется краевым углом смачивания (О).
Линия пересечения трех поверхностей раздела называется контуром смачивания.
Величина О определяется равновесием сил поверхностного натяжения, действующих на каждую точку контура смачивания (рис. 10)
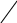 ж/г
ж/г

т/г т/ж
Рис. 10.
Это равновесие выражено уравнением Юнга:
т/г = т/ж + ж/г cos О, из которого можно получить выражение для cos О, являющегося количественной мерой смачивания:
![]()
В зависимости от природы контактирующих фаз возможны такие случаи:
полное смачивание (растекание), при котором жидкости растекаются по смачиваемой поверхности с образованием тончайшего практически плоского слоя. При этом краевой угол близок к нулю (например, растекание воды по поверхности кварца или бензина по воде);
полное несмачивание, при котором между жидкостью и твердым телом существует только механический контакт, и мелкие капли жидкости представляют собой почти идеальные шарики (например, капли ртути на поверхности большинства твердых тел) краевой угол при этом равен или близок к 180;
неполное (частичное) смачивание, при котором капля воды на поверхности принимает различную форму. Если величина краевого угла смачивания лежит между 0 и 90 - поверхность лиофильна (в случае воды – гидрофильна), если между 90 и 180- лиофобна (в случае воды - гидрофобна). Пример гидрофильной поверхности – капли воды на графите, О = 60, гидрофобной поверхности – капли воды на парафине О = 106.
Мерой лиофильности или лиофобности может служить также теплота смачивания – количество теплоты выделяющееся при смачивании.
Теплота смачивания более применима в случае определения лиофильности порошков, когда краевой угол измерить трудно или невозможно.
Характеристикой поверхности служит коэффициент гидрофильности (К) – отношение теплот смачивания поверхности водой и бензолом:
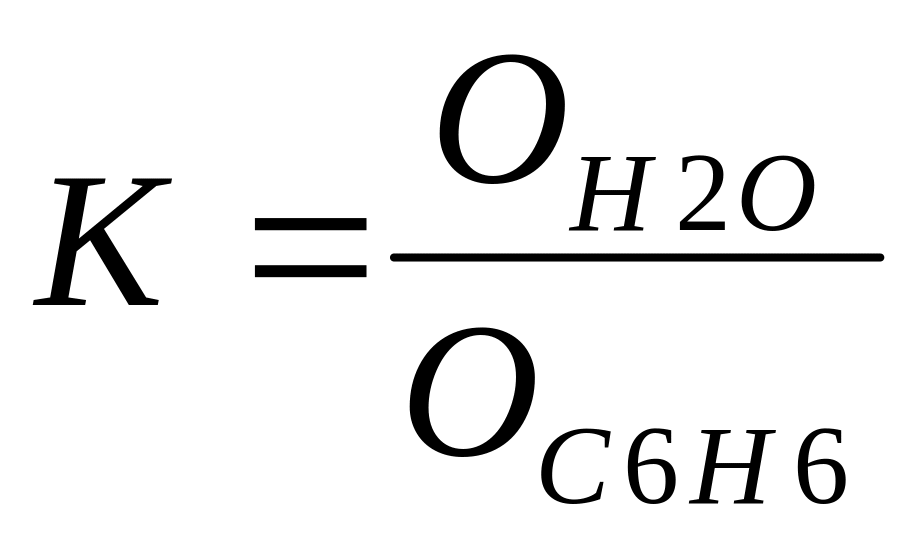 ,
для гидрофильных веществ К
1, для гидрофобных К
1.
,
для гидрофильных веществ К
1, для гидрофобных К
1.При адсорбции ПАВ на твердой поверхности возможно изменение ее лиофильности – инверсия смачивания. Инверсия смачивания является следствием определенной ориентации адсорбированных молекул ПАВ (рис. 11).

 / / / / / / / / /
/ / /_ / / / / / / / / / / /
/ / / / / / / / /
/ / /_ / / / / / / / / / / /
а) б)
