
- •1)Типы химических связей в органических соединениях
- •2)Характеристика соединений с поляризованной связью.
- •3)Виды изомерии в органических соединениях
- •4)Предельные углеводороды, их химические свойства.
- •5)Получение алканов.
- •6)Галогенопроизводные углеводородов
- •7)Алкены и их химические свойства.
- •8)Диеновые углеводороды. Особенности реакции присоединения в зависимости от положения двойных связей.
- •9)Алкины. Ацетилен и его химические свойства.
- •10)Получение непредельных углеводородов.
- •11)Качественные реакции на двойную, тройную связь.
- •12)Ароматические соединения. Бензол и его химические свойства
- •13)Гомологи бензола. Получения и свойства.
- •14)Особенности замещения в бензольном кольце. Правило ориентации второго заместителя
- •15)Механизм нитрования бензола.
- •16)Спирты одноатомные и многоатомные. Первичные, вторичные и третичные спирты. Получение спиртов.
- •17)Химические свойства спиртов.
- •18)Двухатомные и трёхатомные спирты.
- •19)Фенолы и их свойства.
- •20)Получение фенолов. Кислотные свойства фенолов
- •21)Альдегиды и их химические свойства.
- •22)Получение альдегидов.
- •23)Полимеризация и конденсация альдегидов.
- •24)Кетоны. Получение и химические свойства.
- •25)Общность и различие химических свойств альдегидов и кетонов.
- •26)Одноосновные карбоновые кислоты. Способы получения кислот.
- •27)Химические свойства одноосновных предельных кислот.
- •28)Непредельные кислоты и их химические свойства.
- •29)Дикарбоновые кислоты.
- •30)Цис - транс - изомерия.
- •31)Гидроксикислоты. Их химические свойства. Оптическая изомерия.
- •3 2)Кетокислоты. Кето — енольнаятаутометрия.
- •33)Высшие предельные и непредельные жирные кислоты. Понятие о незаменимых кислотах.
- •34)Получение простых эфиров и сложных эфиров.
- •35)Сложные эфиры. Реакции этерификации и гидролиза.
- •36)Строение триглицерида. Омыление жира. Гидрогенизация жира. Прогоркание жира. Мыла растворимые и нерастворимые.
- •37)Фосфолипиды Строение серинфосфатида, лецитина и кефалина.
- •38)Стерина и стериды. Химическая структура холестерола.
- •39)Использование магнийорганических соединений для получения различных органических соединений.
- •40)Пентозы. Строение рибозы, дезоксирибозы, ксилозы и арабинозы.
- •41)Гексозы. Строение глюкозы, галактозы, маннозы, фруктозы.
- •42)Циклическое строение моносахаридов.
- •43)Понятие об ассиметрическом атоме углерода. Зеркальная изомерия.
- •44)Восстанавливающие дисахариды.
- •45)Полисахариды. Схема строения крахмала и клетчатки.
- •46)Химические свойства моносахаров.
- •49)Моноаминодикарбоновые и диаминомонокарбоновые кислоты.
- •50)Циклические аминокислоты. Понятие о незаменимых аминокислотах.
- •51)Химические свойства аминокислот.
- •52)Строение белковой молекулы (первичная, вторичная, третичная, четвертичная структуры).
- •53)Ди - и трипептиды.
- •54)Пиримидиновые основания.
- •55)Пуриновые основания.
- •56)Нуклеозиды и нукпеотиды.
- •57)Пуриновые нуклеотиды.
- •58)Пиримидиновые нуклеотиды.
- •59)Схема строения рнк и днк.
- •60)Хромопротеиды. Структура гема.
19)Фенолы и их свойства.
Это производные ароматическихуглеводородов, у которых гидрок сильная группа связана непосредственнобензольным ядром.
![]()
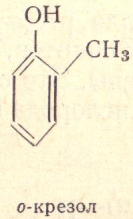
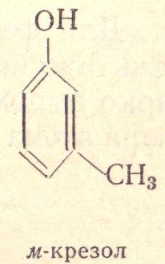
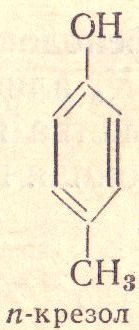
Хим. Св-ва 1.Кислотные свойства фенолов. 1)диссоциация с образованием ионов Н+,
C6H5OH С6Н5O- + H+ 2) щелочными металлами и щелочами стойкие феноляты 2C6H5OH + 2Na →2С6Н5ONa + H2; С6H5OH + NaOH →С6Н5ONa + H2O 3)с кисло тами, Феноляты C6H5ONa + HCl →С6Н5OH + NaCl 4) с ан- гидридами карбоновых кислот, Фенолы образуют сложные эфирыС6H5OH + CH3СOCl →С6H5-O-CO-CH3 + HCl
Фенилацетат 5) Фенолы образуют простые эфиры при взаимодействии с галогеналканамииспиртами. С6H5ONa + C2H5I →С6H5-O-C2H5(фенетол) + NaI; С6H5OH + CH3OH →С6H5-O-CH3 (анизол)+ H2O Окисление фенолов идет да же на воздухе,
Реакции замещения в бензольном ядре. 1)Взаимодействие фенолов с бром ной водой.Гидроксильная группа фенола ориентирует бром в орто- и параположения
2)Нитрование фенола идет в орто- и пара-положения
(2,4,6 тринитрофенол(пикриновая кислота))
3) Сульфирование
4) Взаимодействие с формальдегидом идет преимущественно по орто-положению и приводит к образованию фенолформальдегидных смол (бакелитов).
20)Получение фенолов. Кислотные свойства фенолов
Это производные ароматических углеводородов, у которых гидроксильная группа связана непосредственно бензольным ядром. Кислотные свойства фенолов. 1)диссоциация с образованием ионов Н+,
C6H5OH С6Н5O- + H+ 2) щелочными металлами и щелочами стойкие феноляты 2C6H5OH + 2Na →2С6Н5ONa + H2; С6H5OH + NaOH →С6Н5ONa + H2O 3)с кисло тами, Феноляты C6H5ONa + HCl →С6Н5OH + NaCl 4) с ан- гидридами карбоновых кислот, Фенолы образуют сложные эфирыС6H5OH + CH3СOCl →С6H5-O-CO-CH3 + HCl
Фенилацетат 5) Фенолы образуют простые эфиры при взаимодействии с галогеналканамииспиртами. С6H5ONa + C2H5I →С6H5-O-C2H5(фенетол) + NaI; С6H5OH + CH3OH →С6H5-O-CH3 (анизол)+ H2O
Получение: 1. Перегонкой каменноугольной смолы.
2. Синтез из бензола, через промежуточный продукт хлорбензол.
C6H6 + Cl2 →C6H5Cl + HCl C6H5Cl + 2NaOH →C6H5ONa + NaCl + H2O 3. Кумольныйметод одновременно получаются 2 ценных продукта - фенол и ацетонC6H6 + CH2=CH-CH3 C6H5-CH(CH3)2 (кумол)
4. Сплавление солей сульфо кислот со щелочами. Образую щийся фенолят натрия
разрушают кислотами.
C6H5-SO3Na + 2NaOH C6H5ONa + Na2SO3 + H2O
5. Гомологи фенола получают алкилированием фенола.
21)Альдегиды и их химические свойства.
К альдегидам и кетонам относят органические соединения, имеющие в своем составе карбо нильнуюгруппуС=О, соединен ную в альдегидах с одним углеводо родным радикалом, а в кетонах с двумя. Н-СОН формальдегид, муравьиный альльдегид, метаналь
СН3-СОН ацетальдегид, уксусный альдегид, этаналь
С2Н5-СОН пропионовый альдегид, пропаналь
С3Н7-СОН масляный альдегид, бутаналь
СН2=СН-СОН акролеин, пропеналь (ненасыщенный альдегид)
С6Н5-СОН бензальдегид (ароматический альдегид)
Хим. Св-ва.
РЕАКЦИИ ПРИСОЕДИНЕНИЯ
1. Гидрирование карбонильных соединений, как и алкенов, идет в присутствии ката-
лизаторов (Ni, Pt, Pd). Из альдегидов при восстановлении образуются первичныеспир-
ты, H-COH + H2 СH3OH;
2. Присоединение Н2О
R-COH+H2O=R-COHOHH (двухатомный спирт) 3. Взаимодействие сенильной кислотой R-COH+H-CN=R-COHCNH (оксинитрил)
4. Взаимодействие со спиртами R-COH+R1-OH=R-COR1OHH(полуацеталь) R-COH+R1-OH=(t* HCl)=R-COR1OR1H (ацеталь)
РЕАКЦИИ ЗАМЕЩЕНИЯ КАРБОНИЛЬНОЙ ГРУППЫ
CH3-COH+PO5=CH3-CClClH (1,1дихлорэтан)
РЕАКЦИИ ОБУСЛОВЛЕННЫЕ ЗАМЕЩЕНИЕМ В РАДИКАЛЕ
CH3-COH+Br2=Br-CH2-COH+HBR (бромуксусный альдегид)
Полимеризации. Это разновидность реакций присоединения по двойной связи..
1. Линейная полимеризация формальдегида c образованием полиформальдегида.
n(H-COH) (-CH2-O-)n
2. Циклическая полимеризация
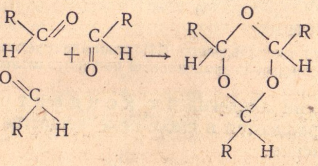 Поликонденсация —
процесс синтеза полимеров
из полифункциональных (чаще всего
бифункциональных) соединений, обычно
сопровождающийся выделением
низкомолекулярных побочных продуктов
(воды,
спиртов
и т. п.) при взаимодействии
функциональных групп 3. Реакции
поликонденсации с фенолом продуктом
конденсации фенола
с ,фенолформальдегидные
смолы.,4.
Конденсация с мочевиной (карбамидом)
приводит к образованию полимеровслужащих
основой карбамидных пластмасс.H-COH
+ NH2-CO-NH2
NH2-CO-NH-CH2OHNH2-CO-N=CH2
+ H2Oи
далее идет полимеризация по двойной
связи N=CH25.. Альдольная конденсация:
реакция ведет к удлинению углеводородного
радикала.CH3-COH
+ CH3-COHCH3-CHOH-CH2-COH
(альдегидоспирт,альдоль)
Поликонденсация —
процесс синтеза полимеров
из полифункциональных (чаще всего
бифункциональных) соединений, обычно
сопровождающийся выделением
низкомолекулярных побочных продуктов
(воды,
спиртов
и т. п.) при взаимодействии
функциональных групп 3. Реакции
поликонденсации с фенолом продуктом
конденсации фенола
с ,фенолформальдегидные
смолы.,4.
Конденсация с мочевиной (карбамидом)
приводит к образованию полимеровслужащих
основой карбамидных пластмасс.H-COH
+ NH2-CO-NH2
NH2-CO-NH-CH2OHNH2-CO-N=CH2
+ H2Oи
далее идет полимеризация по двойной
связи N=CH25.. Альдольная конденсация:
реакция ведет к удлинению углеводородного
радикала.CH3-COH
+ CH3-COHCH3-CHOH-CH2-COH
(альдегидоспирт,альдоль)
