
- •1)Типы химических связей в органических соединениях
- •2)Характеристика соединений с поляризованной связью.
- •3)Виды изомерии в органических соединениях
- •4)Предельные углеводороды, их химические свойства.
- •5)Получение алканов.
- •6)Галогенопроизводные углеводородов
- •7)Алкены и их химические свойства.
- •8)Диеновые углеводороды. Особенности реакции присоединения в зависимости от положения двойных связей.
- •9)Алкины. Ацетилен и его химические свойства.
- •10)Получение непредельных углеводородов.
- •11)Качественные реакции на двойную, тройную связь.
- •12)Ароматические соединения. Бензол и его химические свойства
- •13)Гомологи бензола. Получения и свойства.
- •14)Особенности замещения в бензольном кольце. Правило ориентации второго заместителя
- •15)Механизм нитрования бензола.
- •16)Спирты одноатомные и многоатомные. Первичные, вторичные и третичные спирты. Получение спиртов.
- •17)Химические свойства спиртов.
- •18)Двухатомные и трёхатомные спирты.
- •19)Фенолы и их свойства.
- •20)Получение фенолов. Кислотные свойства фенолов
- •21)Альдегиды и их химические свойства.
- •22)Получение альдегидов.
- •23)Полимеризация и конденсация альдегидов.
- •24)Кетоны. Получение и химические свойства.
- •25)Общность и различие химических свойств альдегидов и кетонов.
- •26)Одноосновные карбоновые кислоты. Способы получения кислот.
- •27)Химические свойства одноосновных предельных кислот.
- •28)Непредельные кислоты и их химические свойства.
- •29)Дикарбоновые кислоты.
- •30)Цис - транс - изомерия.
- •31)Гидроксикислоты. Их химические свойства. Оптическая изомерия.
- •3 2)Кетокислоты. Кето — енольнаятаутометрия.
- •33)Высшие предельные и непредельные жирные кислоты. Понятие о незаменимых кислотах.
- •34)Получение простых эфиров и сложных эфиров.
- •35)Сложные эфиры. Реакции этерификации и гидролиза.
- •36)Строение триглицерида. Омыление жира. Гидрогенизация жира. Прогоркание жира. Мыла растворимые и нерастворимые.
- •37)Фосфолипиды Строение серинфосфатида, лецитина и кефалина.
- •38)Стерина и стериды. Химическая структура холестерола.
- •39)Использование магнийорганических соединений для получения различных органических соединений.
- •40)Пентозы. Строение рибозы, дезоксирибозы, ксилозы и арабинозы.
- •41)Гексозы. Строение глюкозы, галактозы, маннозы, фруктозы.
- •42)Циклическое строение моносахаридов.
- •43)Понятие об ассиметрическом атоме углерода. Зеркальная изомерия.
- •44)Восстанавливающие дисахариды.
- •45)Полисахариды. Схема строения крахмала и клетчатки.
- •46)Химические свойства моносахаров.
- •49)Моноаминодикарбоновые и диаминомонокарбоновые кислоты.
- •50)Циклические аминокислоты. Понятие о незаменимых аминокислотах.
- •51)Химические свойства аминокислот.
- •52)Строение белковой молекулы (первичная, вторичная, третичная, четвертичная структуры).
- •53)Ди - и трипептиды.
- •54)Пиримидиновые основания.
- •55)Пуриновые основания.
- •56)Нуклеозиды и нукпеотиды.
- •57)Пуриновые нуклеотиды.
- •58)Пиримидиновые нуклеотиды.
- •59)Схема строения рнк и днк.
- •60)Хромопротеиды. Структура гема.
1)Типы химических связей в органических соединениях
1![]() )Ионная
связь : прочная химическая связь,
образующаяся между атомами с большой
разностью (>1,7 по шкале Полинга)
электроотрицательностей, при которой
общая электронная пара полностью
переходит к атому с большей
электроотрицательностью. Наиболее ярко
выражена в галогенидах щелочных металлов,
напр., в NaCl, KF. П-ер :
)Ионная
связь : прочная химическая связь,
образующаяся между атомами с большой
разностью (>1,7 по шкале Полинга)
электроотрицательностей, при которой
общая электронная пара полностью
переходит к атому с большей
электроотрицательностью. Наиболее ярко
выражена в галогенидах щелочных металлов,
напр., в NaCl, KF. П-ер :
2![]() )А.
Ковалентная связь -образована общей
для двух атомом парой электронов.Делится
на неполяную
–образована атома ми с одинако вой
электроотрицаемостью. Полярную
- образована атомами с различной эле
ктроотрицаемостью
)А.
Ковалентная связь -образована общей
для двух атомом парой электронов.Делится
на неполяную
–образована атома ми с одинако вой
электроотрицаемостью. Полярную
- образована атомами с различной эле
ктроотрицаемостью
2)Ковалентная : химическая связь, образованная перекрытием пары валентных электронных облаков. Обеспечивающие связь электронные облака называются общей электронной парой. Наиболее распространена в органической химии. Обладает высокой прочностью. П-ер :
3![]()
![]()
![]()
![]() )Донорно
– акцепторная связь : химическая связь
между двумя атомами или группой атомов,
осуществляемая за счет неподеленной
пары электронов одного атома (донора)
и свободной орбитали другого атома
(акцептора). П-ер :
)Донорно
– акцепторная связь : химическая связь
между двумя атомами или группой атомов,
осуществляемая за счет неподеленной
пары электронов одного атома (донора)
и свободной орбитали другого атома
(акцептора). П-ер :
4![]() )Водородная
:форма объединения между электроотрицательным
атомом и атомом водорода H, связанным
ковалентно с другим электроотрицательным
атомом. В качестве электроотрицательных
атомов могут выступать N, O или F, реже
Cl,Br,S.
Водородные связи могут быть межмолекулярными
или внутримолекулярными. П-ер :
)Водородная
:форма объединения между электроотрицательным
атомом и атомом водорода H, связанным
ковалентно с другим электроотрицательным
атомом. В качестве электроотрицательных
атомов могут выступать N, O или F, реже
Cl,Br,S.
Водородные связи могут быть межмолекулярными
или внутримолекулярными. П-ер :
2)Характеристика соединений с поляризованной связью.
Это молекулы включающие ковалентные полярные связи .Хар-ся наличием полюсов (наз-сяди полями. Чем выше разность электроотрицательных атомов тем более рекационно способна молекула.
3)Виды изомерии в органических соединениях
Изомерия-явление сущ-ияИзомеров.Изомер-вещ-ва имеющие одинаковый сост-в атомов, но различное в строе ние.
А)Структурная изомер-я 1)Изомерия углеродного скелета.
Различая во взаимном расположении атомов С.
2)Изомерия по положению кратной связи
(двойной).
3)Из положения функциональной группы Различия положения функциональной группы относительно углеродного скеле та.
В)Пространственная изомер-я
Связана с различным положением атомов или групп атомов относительно двойной связи.
4)Предельные углеводороды, их химические свойства.
Алканы (парафины) - это насыщенные (предельные) углеводороды с открытой цепью. Они имеют общую формулу СnН2n+2, В алканах атомы углерода связаны между собой только простыми (одинарными) связями, а остальные валентностиуглерода насыщены атомами водорода. Характерный суффикс для насыщенных углеводородов-ан.,
СН4 - метан; С2Н6 - этан; С3Н8 - пропан
С4Н10 - бутан (2 изомера)
СН3-СН2-СН2-СН3 - н-бутан изобутан (2-метилпропан)
С5Н12 - пентан (3 изомера)
С6Н14 - гексан , С7Н16 - гептан
С8Н18 - октан С9Н20 - нонан С10Н22 – декан
Химические св-ва:
1)Замещение: CH4+Cl2→CH3Cl+HCl (хлористый метил)
CH3Cl+HCl→CH2Cl2+HCl (хлористый метилен) CH2Cl2+Cl2→CHCl3+HCl (хлороформ)
2)При воздействие света наCl образуется радикал Cl·
CH4+Cl·→CH3·+HCl CH3·+Cl2→CH3Cl+Cl·
3)Нитрование:
характерно для имеющим вторичный или
третичный атом углерода.
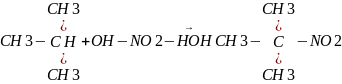
![]()
Р-я КОНОВАЛОВА
4)При температуре 100-500ºС и доступе кислорода образуются жирные кислоты, а при температуре 500-600ºС наблюдается крекинговый процесс
- р-я горения CH4+2O2
→CO2+H20
-Каталитическое окисление
2СН3-СН2-СН2-СН3 + 5О2 →4СН3СООН (уксусная кислота),
