
- •Квантово-механическая модель строения атома. Корпускулярно-волновые свойства электрона: уравнение Де Бройля, принцип неопределенности Гейзенберга.
- •Уравнение Шредингера. Квантовые числа, волновая функция, понятие об атомной орбитали.
- •Энергетическая диаграмма возможных состояний электрона в атоме водорода.
- •Распределение электронов по ао в многоэлектронных атомах. Принцип Паули, правило Гунда, правила Клечковского.
- •Периодический закон. Периодическая система. Электронные конфигурации атомов.
- •Периодические свойства атомов (радиусы атомов, энергия ионизации, сродство к электрону, электроотрицательность).
- •Характерные степени окисления элементов.
- •Ковалентная химическая связь: механизмы её образования, разновидности. Длина, энергия, порядок (кратность) ковалентной связи.
- •9, 10. Насыщаемость ковалентной связи и валентные возможности атомов.
- •Полярность и поляризуемость ковалентной связи. Полярность молекулы.
- •Металлическая связь. Деление элементов на металлы и неметаллы. Металлические структуры.
- •Ионная связь и её свойства. Ионные кристаллы.
- •Типы межмолекулярных взаимодействий.
- •Водородная связь и её влияние на физические свойства вещества.
- •Термохимические уравнения. Закон Гесса, следствия из него. Энтальпия.
- •Направление осуществления химических реакций. Энтропия. Энергия Гиббса.
- •Понятие о скорости реакции. Факторы, влияющие на скорость реакции. Влияние концентраций на скорость реакции.
- •Зависимость скорости реакции от температуры. Уравнение Вант-Гоффа, уравнение Аррениуса.
- •Понятие об энергии активации. Гомогенные и гетерогенные катализаторы, каталитические системы, механизм действия катализаторов.
- •Обратимые и необратимые реакции. Химическое равновесие и его признаки. Константа химического равновесия.
- •Факторы, влияющие на химическое равновесие. Принцип Ле-Шателье.
- •Классификация дисперсных систем. Понятие о растворах. Растворимость. Концентрации растворов.
- •Типы гетерогенных дисперсионных систем
- •Процентная концентрация по массе (ω, %)
- •Физико-химические свойства растворов нелетучих веществ (давление насыщенного пара, температура замерзания, температура кипения, осмотическое давление).
- •Понятие об электролитах, степень диссоциации. Растворы сильных электролитов. Ионная сила растворов. Активность ионов.
- •Растворы слабых электролитов. Константа диссоциации слабого электролита. Факторы, влияющие на степень диссоциации слабого электролита.
- •Диссоциация воды. Ионное произведение воды. Водородный и гидроксильный показатели.
- •Понятие о кислотах. Константы диссоциации слабых кислот. РН в растворах слабых кислот.
- •Понятие об основаниях. Константы диссоциации слабых оснований. РН в растворах слабых оснований.
- •Плохо растворимые электролиты. Произведение растворимости. Условия образования и растворения осадков.
- •Ионно-обменные реакции. Реакция нейтрализации.
- •Гидролиз солей, константа гидролиза. Степень гидролиза и факторы, влияющие на неё.
- •Окислительно-восстановительные реакции (овр). Основные понятия. Направление протекания овр.
- •Понятие об окислительно-восстановительном потенциале (овп). Стандартный водородный электрод. Стандартные овп. Ряд стандартных электродных потенциалов металлов.
- •Факторы, влияющие на величину овп. Уравнение Нернста.
- •Гальванические элементы. Элемент Даниэля-Якоби. Основные типы и области практического использования гальванических элементов.
- •Электролиз расплава соли. Основные понятия. Потенциал разложения. Перенапряжение.
- •Электролиз растворов солей. Ряд разряжаемости катионов и ряд разряжаемости анионов. Области практического применения электролиза. Растворы
- •Химические свойства металлов, взаимодействие металлов с неметаллами.
- •Взаимодействие металлов с водой.
- •Взаимодействие металлов с кислотами.
- •Взаимодействие металлов со щелочами.
- •Классификация неорганических веществ. Кислотно-основные свойства оксидов и гидроксидов металлов.
- •Коррозия металлов. Защита металлов от коррозии.
- •2) Применение коррозионно-стойких материалов.
- •Общая характеристика физических и химических свойств металлов iiа подгруппы. Магний, кальций. Жесткость воды. Умягчение воды.
- •Основные конструкционные металлы - хром, марганец, железо, алюминий. Общая характеристика физических и химических свойств.
- •Полимеры и олигомеры.
- •Химическая идентификация. Аналитический сигнал, химический анализ.
- •Классификация методов качественного анализа
- •Классификация методов количественного анализа
- •Классификация методов титриметрического анализа
- •Теоретические основы кислотно-основного, окислительно-восстановительного титрования. Индикаторы. Принцип их действия.
Гидролиз солей, константа гидролиза. Степень гидролиза и факторы, влияющие на неё.
Гидролиз солей - это ионно-обменное взаимодействие соли с водой. Реакция протекает, если в продуктах образуется слабая кислота и/или слабое основание. Она основана на поляризующем действии ионов соли на молекулы воды, в результате, которого нарушается равновесие диссоциации воды: Н2О Н+ + ОН-. Гидролиз - это реакция обратная нейтрализации, и следовательно идет с поглощением тепла, процесс эндотермический.
Количественно гидролиз характеризуется константой гидролиза (Кг) и степенью гидролиза (h). Константа гидролиза соли сильной кислоты и слабого основания рассчитывается по формуле:
Кг = [Кв ∕ Косн], где Кв – ионное произведение воды, Косн – константа диссоциации слабого основания.
Степень гидролиза соли (h) - это отношение количества вещества соли, подвергшегося гидролизу, к общему количеству вещества соли. Константа гидролиза (Кг) и степень гидролиза (h) связаны соотношением:
Кг=Ссоли.h2/(1-h), где Ссоли - молярная концентрация соли в растворе.
Если
h<<1,
то Кг
=
Ссоли.h2;
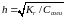 .
.
Степень гидролиза соли определяется следующими факторами.
1.Так как гидролиз процесс эндотермический, то повышение температуры усиливает гидролиз.
2. Чем слабее кислота и/или основание, образующиеся при гидролизе, тем выше степень гидролиза их солей.
3. Чем меньше молярная концентрация соли, тем степень гидролиза выше, т.е. с разбавлением гидролиз усиливается.
4. По принципу Ле-Шателье добавление продуктов гидролиза его подавляет.
Окислительно-восстановительные реакции (овр). Основные понятия. Направление протекания овр.
Окислительно-восстановительными реакциями (ОВР) называют реакции, протекающие с изменением степеней окисления участвующих в них элементов. Степень окисления элемента – формальный заряд, который был бы на атоме, если бы все связи в соединении были ионными. Характерные степени окисления элемента определяются конфигурацией валентного электронного слоя. Окислитель – акцептор электронов, то есть «принимает электроны» и восстанавливается. Восстановитель является донором электронов, то есть «отдает электроны» и окисляется. Окисление – процесс, в котором степень окисления элемента повышается вследствие отдачи электронов. Восстановление – процесс, в котором степень окисления элемента понижается вследствие присоединения электронов. Процессы окисления и восстановления протекают одновременно.
В уравнениях окислительно-восстановительных реакций должен быть отражен «электронный» и «материальный» баланс. Электронный баланс: число электронов, «отданных» восстановителем, должно быть равно числу электронов, «принятых» окислителем. Материальный баланс: число атомов одного элемента в левой и правой части уравнения должно быть одинаковым.
Метод электронного баланса применяют для составления уравнений реакций ОВР любого типа. Он включает определение степеней окисления элементов, наименьшего общего кратного числа «отданных» восстановителем и «принятых» окислителем электронов, определение коэффициентов электронного баланса:
K2Cr2O7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O
Сr+6 + 3e → Cr+3 1
I– – 1e → Io 3
Метод ионно-электронного баланса применяют для составления уравнений ОВР, протекающих в водных растворах с учетом диссоциации сильных хорошо растворимых электролитов на ионы. Он включает составление полуреакций окисления и восстановления. Причем материальный баланс подбирается с использованием частиц H2O и H+ - для реакций в кислой среде и частиц H2O и OH– - для реакций в щелочной среде.
MnO4– + 8H+ + 5e → Mn2+ + 4H2O 2 (процесс восстановления)
SO32– + H2O – 2e → SO42– + 2H+ 5 (процесс окисления)
Далее определяют заряд каждой из систем до и после превращения; рассчитывают число «отданных» восстановителем и «принятых» окислителем электронов и определяют коэффициенты электронного баланса; проводят сложение полуреакций окисления и восстановления, умноженных на соответствующие коэффициенты электронного баланса и «приведение подобных членов». В итоге получают краткое ионное уравнение:
2MnO4– + 6H+ + 5SO32– →2Mn2+ + 5SO42– + 3H2O (краткое ионное уравнение)
Коэффициенты, полученные в кратком ионном уравнении, переносятся в молекулярное уравнение (с учетом состава соединений):
2KMnO4 + 3H2SO4 + 5Na2SO3 → 2MnSO4 + 5Na2SO4 + 3H2O + K2SO4
Определяют коэффициенты перед элементами, не участвовавшими в ОВР (например, К).
ОВР между данным окислителем и данным восстановителем протекает самопроизвольно в прямом направлении, если ЭДС положительна: ЭДС = [φок – φвос ] > 0 или φок > φвос.
