
- •1. Основные положения теории химического строения а.М. Бутлерова. Изомерия.
- •2. Электронное строение атома углерода(самый главный билет в органике,сочувствую,кому это попадется)
- •3. Классификация органических соединений.Функциональные группы.
- •4. Строение,изомерия,номенклатура и способы получения алканов.( можно взять еще инфу из 5 билета)
- •5.Химические свойства алканов.Реакция Коновалова.Применение алканов.(можно взять еще инфу из 4 билета)
- •6.Строение, изомерия,номенклатура,способы получения алкенов.
- •Химическая формула и строение молекулы этилена.
- •Изомерия и номенклатура.
- •Гомологический ряд этилена
- •Получение
- •7.Химические свойства алкенов,правило Марковникова,полимеризация алкенов,применение. Химические свойства
- •Получение.
- •8.Строение,изомерия,номенклатура,способы получения алкинов.
- •9.Химические свойства алкинов. Реакция Кучерова.Полимеризация ацетилена.Применение алкинов.
- •10.Строение,изомерия,номенклатура алкадиенов. Способы получения дивинила и изопрена.Реакция Лебедева.
- •11.Химические свойства алкадиенов с сопряженными связями.Применение алкадиенов.Натуральный и синтетический каучук.Резина.Гуттаперча.
- •12.Строение,изомерия,номенклатура и способы получения алифатических одноатомных спиртов.
- •13.Химические свойства алифатических одноатомных спиртов. Применение спиртов.Этиленгликоль и глицерин.
- •14.Строение,изомерия,номенклатура и способы получения алифатических альдегидов и кетонов.
- •15.Хим.Свойства алифатических альдегидов и кетонов.Реакция серебрянного зеркала.Применение альдегидов и китонов.
- •16.Строение,изомерия,номенклатура,способы получения алифатических одноосновных кислот.
- •17.Химические свойства алифатических одноосновных кислот. Применение кислот.
- •18.Сложные эфиры.Получение и свойства.
- •19.Строение жиров и их переработка. Мыла.Поверхностно-активные вещества.
- •20.Строение,изомерия,номенклатура,способы получения алифатических нитросоединений и аминов.
- •21.Хим.Свойства нистросоединений и аминов.
- •Химические свойства
- •22.Хим.Свойства алифатических аминокислот.Белки.
- •23.Строение,изомерия,номенклатура ароматических углеводородов.Правило ароматичности Хюккеля.
- •24.Химические свойства бензола.
- •25.Правила замещения в бензольном ядре производных бензола.Ориентанты 1 и 2 рода.
- •26.Строение,изомерия,номенклатура,способы получения фенолов.
- •27.Хим.Свойства фенола.Реакции электрофильного замещения,применение фенола в ффс.
- •28.Строение,изомерия,номенклатура,способы получения ароматических аминов. Анилин. Реакция Зинина.
- •29.Основные понятия Химии вмс.Классификация и номенклатура вмс.Методы синтеза вмс в промышленности.
23.Строение,изомерия,номенклатура ароматических углеводородов.Правило ароматичности Хюккеля.
Ароматические
углеводороды (арены)
- углеводороды, в молекулах которых
есть одно или несколько бензольных
колец. Состав аренов с одним бензольным
кольцом отвечает общей формуле CnH2n-6.
В
молекуле простейшего арена - бензола
(C6H6)
-
![]() -связи
образуют единую делокализованную
сопряженную (ароматическую) систему
-связей.
Строение
молекулы простейшего арена - бензола
- может быть передано структурными
формулами различных типов:
-связи
образуют единую делокализованную
сопряженную (ароматическую) систему
-связей.
Строение
молекулы простейшего арена - бензола
- может быть передано структурными
формулами различных типов:
![]()
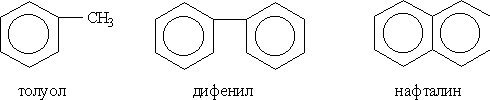
Номенклатура и изомерия. Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин):
Гомологический ряд бензола отвечает общей формуле С6Н2n-6.
Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре. Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров,
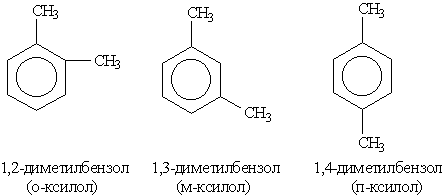
различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-).
Радикалы ароматических углеводородов называют арильными радикалами. Радикал С6Н5 — называется фенил.
Ароматические углеводороды — исходное сырьё для промышленного получения кетонов, альдегидов и кислот ароматического ряда, а также многих других веществ.
Практически всегда соблюдается Правило Хюккеля: ароматичной может быть лишь система, содержащая (в кольце) 4n+2 электронов (где n = 0, 1, 2, …). Система, содержащая 4n электронов является антиароматичной (в упрощенном понимании это обозначает избыток энергии в молекуле, неравенство длин связей, низкая стабильность — склонность к реакциям присоединения). В то же время, в случае пери-сочленения (есть атом(ы), принадлежащий(е) одновременно 3 циклам, то есть возле него нет атомов водорода или заместителей), общее число пи-электронов не соответствует правилу Хюккеля (фенален, пирен, коронен). Также предсказывается, что если удастся синтезировать молекулы в форме ленты Мёбиуса (кольцо достаточно большого размера, дабы закручивание в каждой паре атомных орбиталей было мало), то для таких молекул система из 4n электронов будет ароматичной, а из 4n+2 электронов — антиароматичной.
24.Химические свойства бензола.
Для бензола характерны реакции замещения — бензол реагирует с алкенами, хлоралканами, галогенами, азотной и серной кислотами. Реакции разрыва бензольного кольца проходят в жёстких условиях (температура, давление).
Взаимодействие с хлором в присутствии катализатора:
С6H6 + Cl2 -(FeCl3)→ С6H5Cl + HCl образуется хлорбензол
Катализаторы содействуют созданию активной электрофильной частицы путём поляризации между атомами галогена.
Cl-Cl + FeCl3 → Clઠ-[FeCl4]ઠ+
С6H6 + Clઠ--Clઠ+ + FeCl3 → [С6H5Cl + FeCl4] → С6H5Cl + FeCl3 + HCl
В отсутствие катализатора при нагревании или освещении идёт радикальная реакция замещения.
С6H6 + 3Cl2 -(освещение)→ C6H6Cl6 образуется смесь изомеров гексахлорциклогексана
Взаимодействие с бромом (чистый):
С6H6 + Br2 -(FeBr3 или AlCl3)→ С6H5Br + HBr образуется бромбензол
Взаимодействие с галогенопроизводными алканов (алкилирование бензола, реакция Фриделя-Крафтса):
С6H6 + С2H5Cl -(AlCl3)→ С6H5С2H5 + HCl образуется этилбензол
С6H6 + HNO3 -(H2SO4)→ С6H5NO2 + H2O
