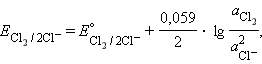- •2.Вопрос.(хз может не полный ) Стехиометрические расчеты по уравнениям реакций.
- •3.Вопрос
- •4.Вопрос
- •5.Вопрос.
- •Билет №6
- •Следствия из закона Гесса
- •Билет 9 Химическое равновесие в гомогенных системах
- •5.1.1. Константа химического равновесия
- •5.1.2. Влияние температуры на константу равновесия
- •5.1.3. Принцип Ле Шателье
- •5.2. Химическое равновесие в гетерогенных системах
- •Растворимость
- •Способы выражения концентрации растворов
- •Пересчет концентраций растворов из одних единиц в другие
- •Упаривание раствора
- •Концентрирование раствора
- •Смешивание растворов с разными концентрациями
- •Разбавление раствора
- •1. Теория электрической диссоциации Аррениуса.
- •2. Сильные и слабые электролиты
- •3. Константа диссоциации слабых электролитов
- •4. Закон разбавления Освальда
- •Билет 12
- •1.Электролитическая диссоциация — процесс распада электролита на ионы при растворении его в полярном растворителе или при плавлении. Диссоциация в растворах
- •Диссоциация при плавлении
- •Классическая теория электролитической диссоциации
- •Сильные электролиты
- •Вывод значения pH
- •Значения pH в растворах различной кислотности
- •5. Различные случаи гидролиза.
- •6. Степень гидролиза и зависимость ее от концентрации и температуры.
- •7.Смещение равновесия гидролиза.
- •13 Билет.
- •По составу
- •По назначению
- •Паста коки
- •Влияние пав на компоненты окружающей среды
- •17 Билет.
- •Химические источники тока.
- •Гальванические элементы
- •Электрические аккумуляторы
- •Топливные элементы
- •3.Концентрационные цепи
- •По значению э. Д. С. Гальванического элемента
- •4.Гальванические элементы с газовыми электродами
- •5. Окислительно-восстановительные
- •6.Аккумуляторы
- •7.Топливные элементы
- •Билет 19 Электролиз как окислительно-восстановительный процесс
- •Популярные места применения керамики
Топливные элементы
Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
Прямой метанольный топливный элемент
Твердооксидный топливный элемент
Щелочной топливный элемент
2. Необратимые и обратимые гальванические элементы
Химические источники тока делятся на две основные группы: обратимые (аккумуляторы), необратимые (гальванические элементы)
Аккумуляторы можно использовать многократно, так как их работоспособность может быть восстановлена при пропускании тока в обратном направлении от внешнего источника, а в гальванических элементах допускают лишь однократное использование, поскольку один из электродов (Zn в элементе Даниэля – Якоби) необратимо расходуется.
3.Концентрационные цепи
Концентрационные элементы, концентрационные цепи, один из видов гальванических элементов. Различают концентрационные элементы двух типов: с переносом ионов и без переноса ионов. Концентрационные элементы с переносом ионов получают погружением двух одинаковых электродов (например, серебряных) в разделённые полупроницаемой перегородкой растворы одного и того же электролита (например, нитрата серебра) различной концентрации. Электродвижущая сила в таких концентрационных элементах возникает в результате непосредственного переносаэлектролита из более концентрированного раствора в менее концентрированный. В концентрационных элементах второго типа выравнивание концентраций электролита происходит в результате химических процессов, происходящих на двух различных электродах. Пример концентрационного элемента без переноса ионов — серебряный и платиновый электроды, погруженные в раствор соляной кислоты. При одинаковом соотношении концентраций электролита электродвижущая сила концентрационного элемента без переноса ионов в два раза больше, чем у концентрационного элемента с переносом. Концентрационные элементы применяют при измерении коэффициента активности и чисел переноса.
По значению э. Д. С. Гальванического элемента
Электродвижущая сила концентрационной цепи с переносом может быть выражена следующим соотношением:
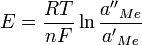
Соответственно, такую цепь можно использовать для нахождения активности и коэффициента активности. В некоторых случаях (например, для сложных сульфидных расплавов) побочноевзаимодейтсвие электролита с электродами может приводить к невозможности определения активности компонентов по ЭДС цепи, тогда используют концентрационные цепи без переноса. Нахождение активности компонента по ЭДС концентрационной цепи без переноса — один из самых точных способов определения активности.
4.Гальванические элементы с газовыми электродами
Газовый электрод в качестве одного из компонентов электродной пары содержит газ (H2, Cl2 и др.), адсорбированный на химически инертном проводнике первого рода (обычно платина, покрытая платиновой чернью). При контакте адсорбированного газа с раствором собственных ионов устанавливается равновесие. Для хлорного и водородного электродов это равновесие можно представить уравнениями:
|
|
|
|
|
|
Соответствующие им уравнения Нернста имеют вид:
|
|
|
|
|
|
Очевидно, что их электродный потенциал зависит от давления и активности (концентрации) ионов в растворе.