
- •Принцип работы электронного спектрометра и особенности метода фотоэлектронной спектроскопии
- •Содержание
- •Глава1. Фотоэлектронная спектроскопи.……………….….4
- •Глава2. Блок-схема электронного спектрометра эс3201………………………………………………………………....…...24
- •Глава 1. Фотоэлектронная спектроскопия
- •1.1Энергетика
- •1.2.Разрешение по энергии
- •1.3.Теорема Купманса
- •1.4. Спектры уфс
- •Глава 2. Блок-схема электронного спектрометра эс3201
- •Заключение
- •Литература
1.3.Теорема Купманса
Как УФС, так и РФС могут быть использованы для исследования валентных электронов в молекулах, и нас как раз интересует та информация, которую можно получить об этих электронах из фотоэлектронного спектра. На рис.2. в качестве примера изображен спектр УФС газообразного азота. В случае источника Не(1), устанавливающего предел ионизации в 21,21 эВ, можно наблюдать три колебательно-структурированных фотоионизационных процесса (~ 15,6, ~ 17,0 и ~ 18,18 эВ). Их можно приписать ионизации с трех высших заполненных молекулярных орбиталей N2(2σu-, πu- и Зσu-орбиталей). Отнесение пиков основано на наблюдаемой колебательной структуре. Следует отметить, что в спектре РФС имеются те же три линии (колебательная структура не видна из-за худшего разрешения) в дополнение к пику при 37,3 эВ для ионизации с 2σg-уровня и единственному пику при 409,9 эВ для 1σg- и 1σu-уровней.
Эти данные подводят нас к теореме Купманса, согласно которой энергия вертикальной ионизации для удаления электрона с молекулярной орбитали равна собственному значению с обратным знаком, полученному при расчетах молекулярных орбиталей с помощью метода самосогласованного поля (ССП МО) Хартри—Фока (стабильная орбиталь имеет отрицательное собственное значение). Основное допущение этой теоремы состоит в том, что молекулярные орбитали, соответствующие исходной молекуле, будут теми же, что и для ионизованной молекулы. При наличии электронной релаксации (т.е. при изменении молекулярных орбиталей в ионизованной молекуле, обусловленном изменением энергии электронного отталкивания) или при заметном изменении энергий корреляции (член, не включенный в расчет по методу МО; он учитывает зависимость координат каждого электрона от координат всех других электронов) теорема Купманса не выполняется.
Энергии
вертикальной ионизации легко определить
для рассмотренного образца N2
(рис. 2). В табл. 1 приведены энергии
вертикальной ионизации N2
и собственные значения, полученные при
нескольких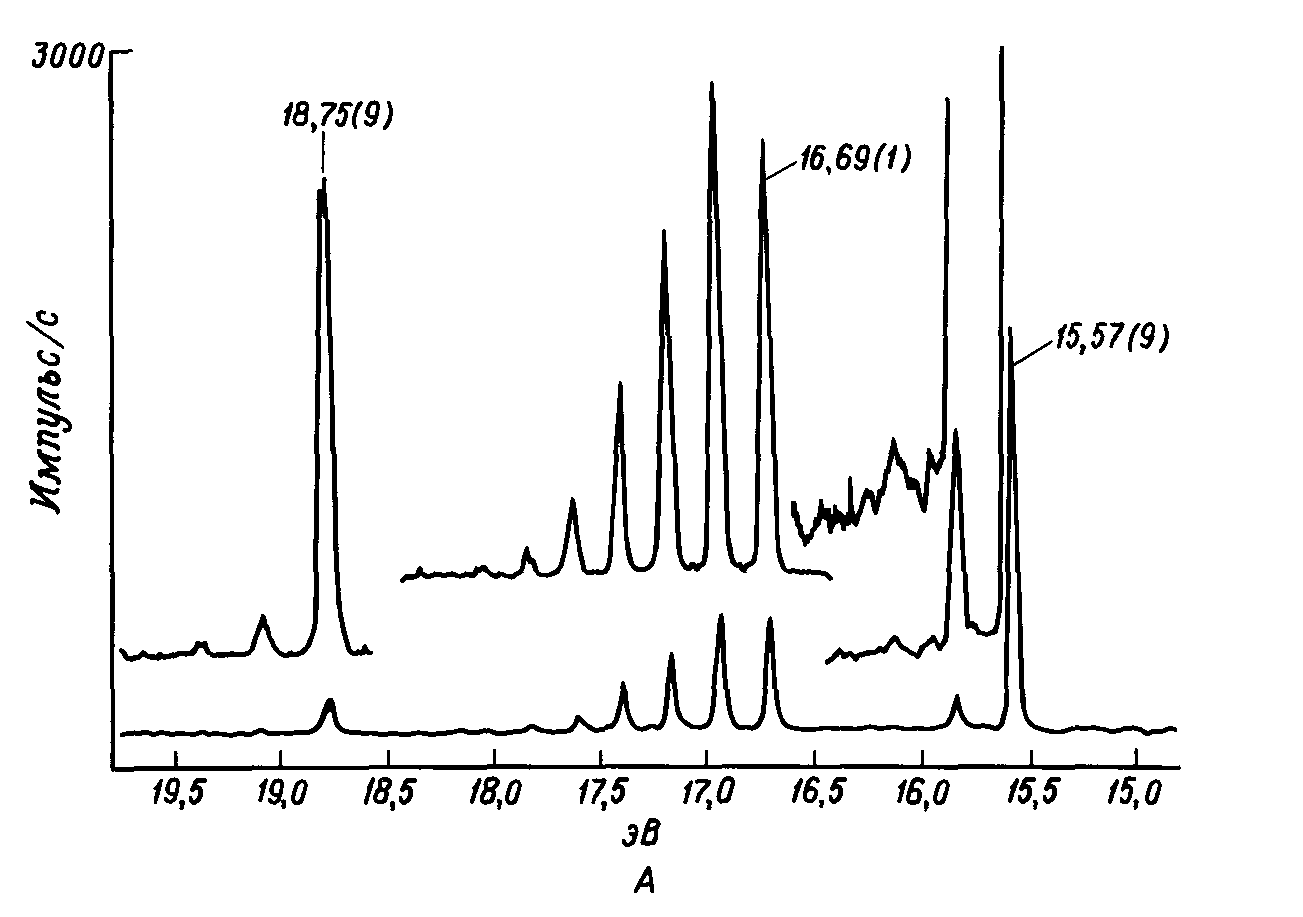
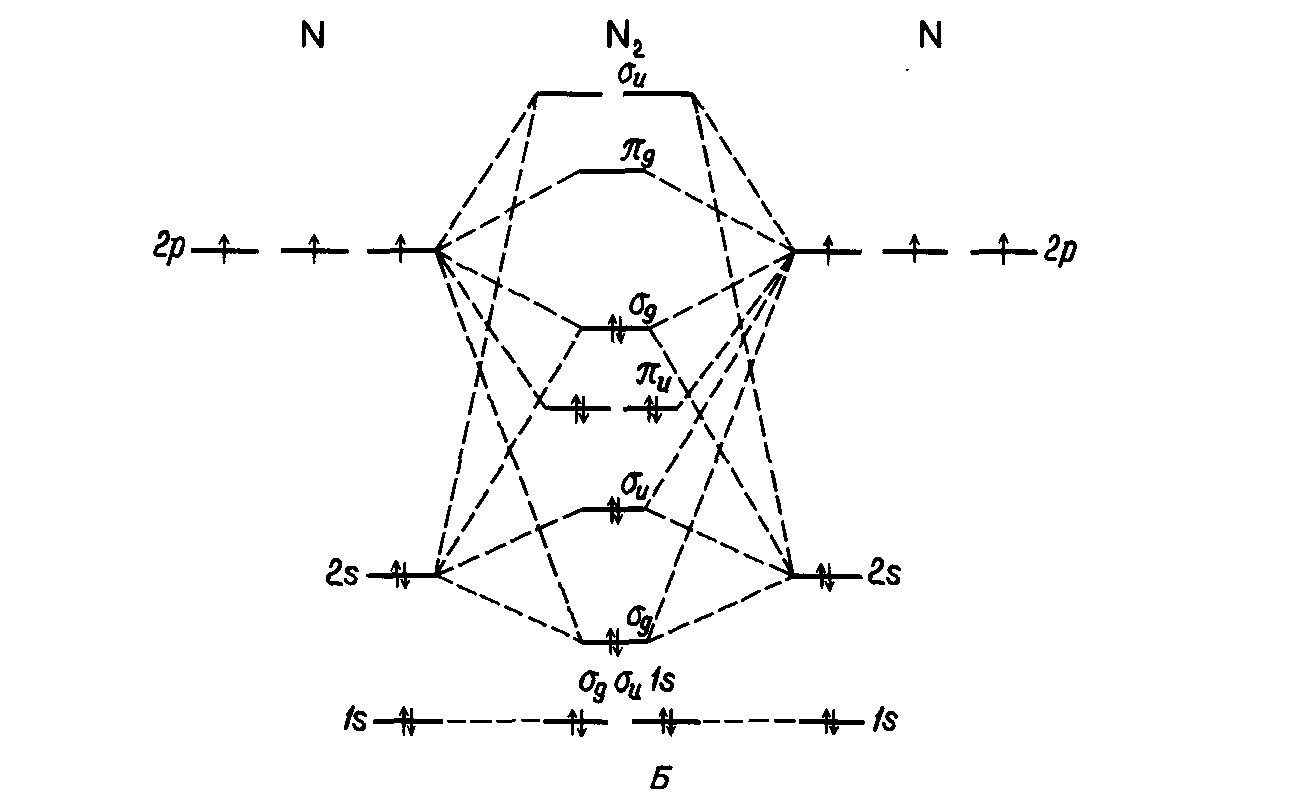
Рис. 2. УФС-спектр газообразного азота.
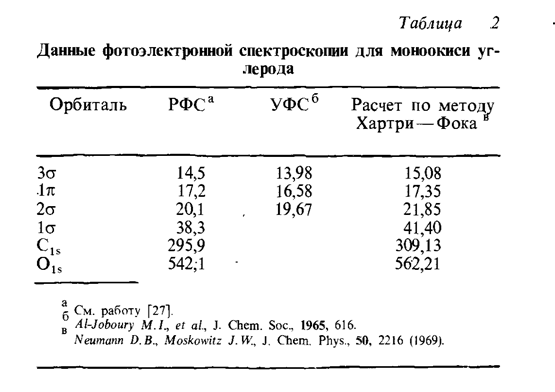
расчетах по методу МО. (Энергии даны в эВ.) Между значениями, полученными методами РФС и УФС, наблюдается хорошее соответствие, однако собственные значения, полученные методом самосогласованного поля Хартри—Фока, не согласуются с наблюдаемыми результатами. На самом деле порядок σg 2р и πu2р обращен, что может служить указанием на различие в энергиях релаксации. Если даже расчеты видоизменить путем учета энергий различных состояний N2 и N2+ и различия в полных электронных энергиях, то наблюдается только удовлетворительное соответствие. И снова происходит обращение σg 2р и πu2р. В этом примере теорема Купманса дает лишь качественное соответствие, что справедливо и в общем случае. Другой пример приведен в табл. 2. Некоторые типы полуэмпирических расчетов по методу МО дают, видимо, полуколичественное соответствие с наблюдаемыми энергиями вертикальной ионизации. В литературе продолжается обсуждение нарушения теоремы Купманса.


Если даже теорема Купманса строго и не выполняется, то все-таки полезно знать, какие пики в фотоэлектронном спектре могут быть связаны с различными молекулярными орбиталями в исходной молекуле. Например, в гл. 3 рассматривались симметрия и строение молекулярных орбиталей NH3. Было установлено, что семь атомных орбиталей в симметрии C3v образуют представление, которое сводится к трем неприводимым представлениям at и двум неприводимым представлениям е. Восемь валентных электронов NH3 заполняют две из и одну из е-молекулярных орбиталей, образуя конфигурацию основного состояния
...(2α1)2(1е)4(3α1)2.
Только другая заполненная орбиталь, 1α1-орбиталь, представляет собой по существу атомную ls-орбиталь азота. Спектр Не(I) (21,21 эВ) показан на рис.3, где наблюдаются вертикальные ионизации с уровня Зα1 при 10,88 эВ и с уровня 1е при 16,0 эВ (первый максимум). Это отнесение выполнено с помощью результатов различных расчетов по методу МО. Источник Не(II) (42,42 эВ) с более высокой энергией был использован для регистрации вертикальной ионизации с уровня 2α1 при 27,0 эВ . Интересно отметить, что пик 1е при ~ 16 эВ имеет характер дублета, т.е. расщепляется. Это расщепление отнесено за счет ян-теллеровского искажения в ионе, что обусловлено конфигурацией (2а1)2(1е)3(3а1)2. Расщепление составляет 0,78 эВ. Известны и другие примеры ян-теллеровского расщепления. Поперечные сечения и угловые распределения
Сравнительно недавно были получены спектры РФС газообразных веществ, ранее исследуемых методом УФС. Полученные интересные результаты основаны на относительных поперечных сечениях фотоионизации валентных электронов в зависимости от энергии источника. Например, для рентгеновского излучения с большей энергией электроны на молекулярной орбитали, составленной главным образом из атомных s-орбиталей, имеют более высокое относительное поперечное сечение (и, следовательно, большую интенсивность спектральной линии), чем электроны на молекулярной орбитали, составленной в основном из атомных 2р-орбиталей. Сопоставление спектров РФС и УФС указывает на различные относительные интенсивности соответствующих пиков. Пик, обусловленный электронами на молекулярных орбита-лях, составленных главным образом из атомных орбиталей s-типа, имеет большую относительную интенсивность в спектре РФС, чем в спектре УФС.
