
- •Принцип работы электронного спектрометра и особенности метода фотоэлектронной спектроскопии
- •Содержание
- •Глава1. Фотоэлектронная спектроскопи.……………….….4
- •Глава2. Блок-схема электронного спектрометра эс3201………………………………………………………………....…...24
- •Глава 1. Фотоэлектронная спектроскопия
- •1.1Энергетика
- •1.2.Разрешение по энергии
- •1.3.Теорема Купманса
- •1.4. Спектры уфс
- •Глава 2. Блок-схема электронного спектрометра эс3201
- •Заключение
- •Литература
МИНОБРНАУКИ РОССИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ ПЕДАГОГИЧЕСКИЙ
УНИВЕРСИТЕТ ИМ. М.АКМУЛЛЫ»
ФИЗИКО-МАТЕМАТИЧЕСКИЙ ФАКУЛЬТЕТ
Кафедра прикладной физики и нанотехнологий
Направление: Нанотехнология
Курс III
КУРСОВАЯ РАБОТА
Натеева Наиля Наильевича
Принцип работы электронного спектрометра и особенности метода фотоэлектронной спектроскопии
Научные руководитель:
Д.ф.-м.н., проф. А.Н.Лачинов
Консультант:
Д.ф.-м.н., с. н. с. Н.Л.Асфандиаров
Уфа 2011
Содержание
ВВЕДЕНИЕ…………………………………………….……………...……3
Глава1. Фотоэлектронная спектроскопи.……………….….4
1.1.ЭНЕРГЕТИКА……………………………………….………………….4
1.2.РАЗРЕШЕНИЕ ПО ЭНЕРГИИ.………………….….…………………8
1.3.ТЕОРЕМА КУПМАНСА……………………………………………..10
1.4. СПЕКТРЫ УФС………………………………………………………15
Глава2. Блок-схема электронного спектрометра эс3201………………………………………………………………....…...24
ЗАКЛЮЧЕНИЕ..............................................................................................26
ЛИТЕРАТУРА……………………………………………………………..27
ВВЕДЕНИЕ
Столкновение фотонов с атомами или молекулами приводит к испусканию фотоэлектронов. В течение последних двух десятилетий фотоэлектронная спектроскопия развилась в многообещающую область химии. Фотоэлектронная спектроскопия измеряет характеристики поглощенного, испущенного или рассеянного электромагнитного излучения. В этом методе предмет изучения - кинетическая энергия испущенных при ионизации электронов.
Частично из-за потребности в монохроматическом излучении возникли два раздела фотоэлектронной спектроскопии. Рентгеновская фотоэлектронная спектроскопия, сокращенно обозначаемая как РФС или ЭСХА (электронная спектроскопия для химического анализа), использующая рентгеновские лучи в качестве источника ионизирующего излучения, изучает в основном электроны оболочки (т.е. невалентные электроны). Создание этого метода связано с именем лауреата нобелевской премии К. Зигбана . В ультрафиолетовой фотоэлектронной спектроскопии (УФС) используют ультрафиолетовое излучение, имеющее более низкую энергию, и, таким образом, исследуют энергии связи валентных электронов. Этот метод был открыт советскими учеными Вилесовым, Терениным и Курбатовым [2]. Своим развитием он во многом обязан Тернеру и его сотрудникам , УФС предназначалась не только для измерения энергий связывания валентных электронов, но и для наблюдения за возбужденными колебательными состояниями молекулярного иона, образующегося в процессе фотоионизации.
Данная работа , в своей основной части, основана книге Драго [1] и докторской диссертации Ю.В. Чижова [2].
Глава 1. Фотоэлектронная спектроскопия
1.1Энергетика
При использовании уровня вакуума в качестве точки отсчета энергия Еь, необходимая для освобождения электрона из системы, может быть рассчитана из закона сохранения энергии:
Eb =E Source -Ekin - Er. (1)
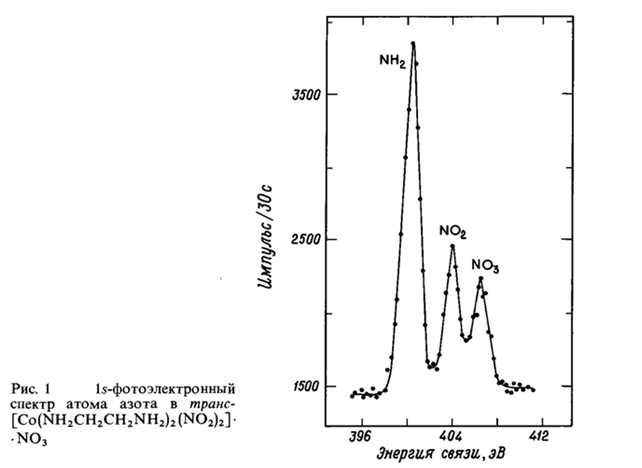
Здесь E Source — энергия ионизирующей радиации, Ekin — кинетическая энергия фотоэлектрона и Еr — энергия отдачи атома или молекулы. Можно показать, что энергия отдачи атома или молекулы при испускании фотоэлектрона пренебрежимо мала, за исключением случая рентгеновской фотоионизации атома водорода . Фотоэлектронный спектр представляет собой график зависимости числа фотоэлектронов, падающих на соответствующее счетное устройство, от кинетической энергии фотоэлектрона. Пики (т.е. максимумы в скорости счета) соответствуют фотоионизации электронов с различных уровней (т. е. молекулярных ор - биталей) образца. Типичный спектр РФС изображен на рис.1. В этом случае спектрометр РФС настроен таким образом, что регистрируются фотоэлектроны, возникающие за счет ионизации ls-электронов атомов азота в транс —[Co(NH2CH2CH2NH2)2(N02)2](N03). В фотоэлектронном спектре наблюдаются три максимума, и они отнесены к ионизации трех различных типов атомов азота. Таким образом, некоторая (небольшая) часть молекул твердого вещества теряет Nls-электрон с атома азота аниона NO3- ,а другие молекулы — Nls - электроны с атома азота либо NO2-, либо этилендиамина. В энергиях связи электронов оболочки наблюдаются химические сдвиги во много электрон-вольт (1 эВ = = 8067 см -1 = 23,06 ккал/моль); мы вернемся к этому позднее. Следует подчеркнуть, что из данной молекулы испускается только один электрон, либо Nls -электрон, либо валентный электрон со связывающей орбитали. Вероятность многократной ионизации мала.
В случае УФС, как мы увидим, разрешение таково, что можно легко регистрировать колебательную структуру, связанную с электронным состоянием ионизуемой молекулы. Аналогия с электронной абсорбционной спектроскопией очевидна. В эксперименте УФС фотоионизации с испусканием электрона сопутствует электронный переход из основного состояния исходной молекулы в основное электронное состояние (иногда в возбужденное состояние, см. ниже) ионизованной молекулы. В электронной абсорбционной спектроскопии колебательная структура наблюдается для возбужденного электронного состояния, а в УФС — для электронного состояния ионизованной молекулы. Тогда явная форма уравнения (1) для энергии, необходимой для освобождения электрона из молекулы, выглядит как
Еb = I +Evib +Erot = Esource -Eki (2)
где
I-адиабатическая
энергия удаления электрона, a
Evib
и Erot
—
квантованные энергии колебания и
вращения различных электронных
состояний ионов, которые являются
следствием фотоионизации. Энергия
адиабатической
ионизации
представляет собой энергию перехода
между основным состоянием молекулы и
основным состоянием иона. Энергия
вертикальной
ионизации
измеряется в переходе, для которого
межъядерные расстояния в ионе не отличаются от межъядерных расстояний в исходной молекуле. Таким образом, энергия вертикальной ионизации равна энергии адиабатической ионизации или превышает ее. Во многих случаях из спектра УФС можно определить обе энергии (см. ниже).
В эксперименте УФС в качестве ионизирующего излучения используют вакуумный ультрафиолет; обычно источником такого излучения является гелиевая [однократно ионизованный гелий, обозначаемый как Не(1)] резонансная лампа с энергией 21,21 эВ. Однако можно применять и другие разрядные лампы, например лампу Ar (I) или лампу с двукратно ионизованным гелием, Не(II). Энергия этих ламп ограничивает УФС исследованиями валентных электронов; как правило, измерения проводят с использованием газообразных образцов. Известно несколько работ, посвященных исследованию растворов и твердых веществ .
Поскольку составной частью прибора РФС является источник рентгеновского излучения, который ионизует образец, этим методом можно определять энергии связывания как валентных электронов, так и электронов оболочки. Обычно используют рентгеновское излучение Кос Mg и А1 с энергией соответственно 1253,6 и 1486,6 эВ. Методом РФС исследовали твердые вещества, газы, жидкости, растворы и замороженные растворы. В случае твердых веществ и замороженных растворов рассчитанные энергии связывания электронов относят к энергии уровня Ферми твердого вещества. Уровень Ферми соответствует высшему заполненному уровню электронного слоя структуры твердого вещества при 0 К. Уравнение сохранения энергии преобразуется к виду
Еb = Esonrct -Ekin – φsрес. (3)
В этом уравнении опущена незначительная энергия отдачи и введена работа выхода φsрес (~ 4 эВ) внутренних металлических поверхностей спектрометра РФС. Работа выхода материала спектрометра — это энергия, необходимая для удаления электрона с поверхности спектрометра. Работа выхода образца отличается от работы выхода материала спектрометра. Образец в спектрометре РФС находится в электрическом контакте со спектрометром, и, если имеется достаточное число носителей заряда (многие образцы представляют собой диэлектрики и носители заряда образуются в ходе облучения), уровни Ферми для образца и спектрометра будут одни и те же. Уравнение (3) можно понять, рассмотрев эксперимент РФС. При фотоионизации электрон образца получает некоторую кинетическую энергию Для того чтобы попасть в спектрометр, электрон должен пройти через входную щель. Поскольку рабочие потенциалы спектрометра и образца различны, кинетическая энергия электрона изменяется до Ekin, что обусловлено либо ускорением, либо замедлением фотоионизованного электрона входной щелью. В камере спектрометра электрон имеет кинетическую энергию Ekin, и эта энергия измеряется прибором. Таким образом, для соотнесения энергии связывания с уровнем Ферми в выражение вводится φsрес. К счастью, нет необходимости знать работу выхода каждого образца.
