
- •12. Элементы органической
- •12.1. Введение
- •12.2. Особенности органических соединений
- •12.3. Тип химических связей и валентность углерода в органических соединениях
- •12.4. Основные положения теории
- •Химического строения органических
- •Соединений
- •А. М. Бутлерова
- •Изомерия положения функциональной группы:
- •III. В молекулах органических веществ атомы и группы атомов влияют друг на друга. Это взаимное влияние определяет свойства веществ.
- •12.5. Классификация органических
- •12.6. Номенклатура органических соединений
- •12.8. Углеводороды
- •12.8.1. Классификация углеводородов
- •12.8.2. Алканы (парафины) Определение, общая формула
- •Изомерия и номенклатура алканов
- •Химические свойства алканов
- •II. Реакции окисления
- •IV. Реакции крекинга алканов
- •V. Изомеризация
- •Получение алканов
- •Применение
- •12.8.2. Алкены (олефины, этиленовые ув) Определение, общая формула
- •I. Реакции присоединения
- •III. Реакции полимеризации
- •IV. Изомеризация.
- •V. Реакции замещения
- •Получение
- •Реакции присоединения
- •12.8.4. Алкины (ацетиленовые ув)
- •Изомерия и номенклатура
- •Химические свойства
- •II.Реакции окисления
- •III. Реакции полимеризации
- •IV. Реакции замещения атомов «н», связанных с sp-гибридизованными атомами углерода
V. Реакции замещения
Алкены вступают и в реакцию замещения. В название соединения, образуемого в результате реакции замещения, входит название радикала.
СН2=СН2 + Br2 → СН2=СНBr + HBr
этен бромэтенил
бромвинил.
Получение
В промышленности:
1) крекинг алканов;
2) дегидрирование алканов
СnH2n+2 t°, кат. СnH2n + Н2
550 –600°С
С Н3–СН–СН3
CH2
= С –СН3
+ Н2
Н3–СН–СН3
CH2
= С –СН3
+ Н2
׀ K2O + Cr2O3 + Al2O3 ׀
СН3 СН3
3) гидрирование алкинов
Ni, Pt
СnH2n–2 + Н2 → СnH2n
Ni, Pt
CН3–
С![]() С
– СН3
+
Н2
→
СН3–СН=СН–СН3
С
– СН3
+
Н2
→
СН3–СН=СН–СН3
В лаборатории:
1) дегидратация спиртов ( t°, катализаторы: Н2SO4, H3PO4, Al2O3, ZnCl2):
170°С
 СН2–СН2
СН2=СН2
+ Н2О
СН2–СН2
СН2=СН2
+ Н2О
׀ ׀ Н2SO4конц.
 Н ОН
Н ОН
При дегидратации спиртов атом водорода отщепляется от атома углерода, связанного с наименьшим числом атомов водорода (правило А.М. Зайцева)
CH3 CH3
׀ t°, кат ׀
CH3– CH– C–CH3 → CH3–CH=C–CH3 + H2O
׀ ׀ 2-Метилбутен-2
OH H
3-Метилбутанол-2
2) Дегидрогалогенирование моногалогеналканов (-HHal) действием твердой щелочи или ее спиртового раствора.
Происходит по правилу А.М. Зайцева:
СН3 СН3
׀ t° ׀
Н3С–СН–С–СН3 + KOH → СН3– СН=С–СН3 + KCl + H2O
׀ ׀ (спирт. 2-Метилбутен-2
Н Cl р-р.)
2-Метил-2-хлорбутан
3) Дегалогенирование ( -2Hal) дигалогеналканов с атомами галогенов у соседних атомов «С» действием Zn и Mg:
t°
СН3– СН2– СН– СН– СН3 + Zn → СН3– СН2–СH=СН–CH3 + ZnBr2
׀ ׀
Br Br
2,3-Дибромпентан Пентен-2
Применение этилена
–
 СН–СН2–
(–СН2–СН2–)n
СН–СН2–
(–СН2–СН2–)n
׀ полиэтилен
С6Н5 n С2Н5–О– С2Н5
полистирол диэтиловый эфир

С2Н5ОН
 С6Н5–СН=СН
этанол
С6Н5–СН=СН
этанол
стирол С2Н4
 СН2–ОН
СН2=
СН–СH=СН2
СН2–ОН
СН2=
СН–СH=СН2
׀ дивинил
СН2–ОН
этиленгликоль
каучук

С2Н5Cl
хлорэтан
растворители СН2Cl–СН2Cl
дихлорэтан
12.8.3. Диеновые углеводороды (алкадиены). Каучуки
Диеновые УВ (алкадиены) – это УВ, в молекулах которых между атомами углерода имеются две двойные связи.
Общая формула: СnH2n–2, где n ≥ 3.
Классификация
Тип диена |
Взаимное расположение двойных связей в молекулах |
Примеры |
1.Диены с кумулированными связями |
Две двойные связи находятся у одного атома углерода |
СН2=С=СН2 Пропадиен (аллен) |
2. Диены с сопряженными связями |
Двойные связи разделены одной одинарной связью |
СН2= СН–СH=СН2 Бутадиен-1,3 |
3. Диены с изолированными связями |
Двойые связи разделены двумя или более одинарными связями |
СН2= СН–СН2–СH=СН2 Пентадиен -1,4 |
Изомерия и номенклатура
Рассмотрим изомерию и номенклатуру диенов на примере диенового углеводорода с эмпирической формулой С6Н10:
Структурная изомерия цепи |
СН3–СH=СН–СН=СН–СН3 Гексадиен-2,4 СН3–СH=С–СН=СН ׀ СН3 3-Метилпентадиен-1,3 |
Структурная изомерия взаимного положения двойных связей |
СH2=СН–СН2–СН=СН–СН3 Гексадиен-1,4 СH2=СН–СН2–СН2–СН=СН3 Гексадиен-1,5 |
Пространственная изомерия |
5 С Н3 СН3 4 3 С = С Н 2 1 Н С = С
Н Н цис-3-метилпентадиен-1,3
Н СН3 4 3 С = С Н 5 2 1 СН3 С = С
Н Н транс-3-метилпентадиен-1,3
|
Межклассовая изомерия |
СH С–СН2–СН2–СН2–СН3 Гексин-1 и его изомеры |
Наибольшее практическое значение имеют диены с сопряженными связями:
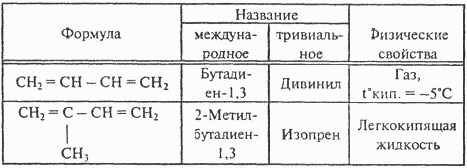
Химические свойства
