
- •2.8 Превращения чугунов…………………………………………...…… 34
- •1.1 Введение
- •1.2 Структура курса
- •1.3 Типы химических связей в веществе
- •1.4 Методы измерения твердости металлов
- •1.4.1 Измерение твердости по Бринеллю
- •1.4.2 Измерение твердости по Виккерсу
- •1 Рисунок 1.8 - Положение наконечника при определении твердости по Роквеллу, 1-3 этапы воздействия .4.3. Измерение твердости по Роквеллу
- •1.5 Кристаллизация веществ
- •1.5.1 Общие понятия о кристаллической решетке и ее дефектах
- •1.5.2 Дальний порядок и ближний порядок в веществе
- •1.5.3 Дефекты кристаллической решетки
- •1.5.4 Кристаллизация жидкостей и макроструктура слитка
- •1.5.5 Гомогенное зарождение кристаллов
- •1.5.6 Гетерогенное зарождение кристаллов
- •1.5.7 Необходимость управления процессом кристаллизации
- •1. Ковалентной связью называется:
- •2.2 Общие понятия о металлических сплавах
- •2.3 Диаграммы состояния двухкомпонентных сплавов
- •2.5 Структура и физические свойства сплавов железо-углерод
- •2.6 Процессы при структурообразовании железоуглеродистых сплавов
- •2.7 Превращения сталей в твердом состоянии
- •2.8 Превращения чугунов
- •1. Металлы – это…
- •2. В каком состоянии компоненты сплавов хорошо растворяются друг в друге
- •3. Сплавы механические смеси образуются
- •3.2 Превращения в стали при нагреве
- •3.2.2 Превращения в стали при охлаждении
- •3.2.2 Мартенситное превращение
- •3.2.3 Промежуточное (бейнитное) превращение аустенита
- •3.3 Отжиг стали
- •3.4 Закалка стали
- •3.4.1 Охлаждение при закалке стали
- •3.4.2 Режимы закалки стали
- •3.5 Отпуск стали
- •3.6 Отпускная хрупкость
- •3.7 Химико-термическая обработка стали
- •3.7.1 Цементация
- •3.7.2 Цементация в твердом карбюризаторе
- •3.7.3 Газовая цементация
- •3.7.4 Азотирование
- •3.7.4 Цианирование
- •3.7.5 Диффузионная металлизация
- •1. Под термической обработкой понимают процессы
- •4.2 Влияние примесей на свойства стали
- •4.2.1 Постоянные примеси
- •4.2.2 Легирующие примеси
- •4.3 Классификация железоуглеродистых сталей
- •4.3.1. Кипящая сталь
- •4.3.2 Спокойная сталь
- •4.3.3 Полуспокойная сталь
- •4.4 Маркировка, свойства, термическая обработка и область применения углеродистых сталей
- •4.4.1 Углеродистые конструкционные стали
- •4.4.2 Автоматные стали
- •4.4.3 Конструкционные низколегированные стали
- •4.4.4 Конструкционные цементуемые стали
- •4.4.5 Конструкционные улучшаемые стали
- •4.4.6 Рессорно-пружинные стали
- •4.4.7 Шарикоподшипниковые стали
- •4.4.8 Износостойкие стали
- •4.4.9 Стали и сплавы с особыми свойствами
- •4.5 Инструментальные стали и сплавы
- •4.5.1 Общая характеристика
- •4.5.2 Углеродистые инструментальные стали (гост 1435).
- •4.5.3 Легированные инструментальные стали
- •4.5.4 Быстрорежущие стали
- •4.5.5 Стали для измерительных инструментов
- •4.5.6 Штамповые стали
- •4.5.7 Твердые сплавы
- •4.6 Чугуны
- •4.6.1 Классификация чугунов
- •4.6.2 Влияние состава чугуна на процесс графитизации
- •4.6.3 Влияние графита на механические свойства отливок
- •4.6.4 Серый чугун
- •4.6.5 Высокопрочный чугун с шаровидным графитом
- •4.6.6 Ковкий чугун
- •4.6.7 Отбеленные и другие чугуны
- •5.2 Алюминий и его сплавы
- •5.3 Классификация алюминиевых сплавов
- •5.3.1 Деформируемые алюминиевые сплавы
- •5.3.1.1 Маркировка деформируемых сплавов
- •5.3.2 Термически неупрочняемые коррозионностойкие и свариваемые сплавы
- •5.3.2.1 Сплавы системы Al—Mn
- •5.3.2.2 Сплавы системы Al—Mg (магналии)
- •5.3.3 Сплавы повышенной пластичности и ковочные
- •5.3.3.1 Коррозионностойкие сплавы повышенной пластичности системы Al—Mg—Si (авиали)
- •5.3.3.2 Ковочные сплавы системы Al—Cu—Mg—Si (дюралюмины)
- •5.3.3.3 Сплавы системы Al-Si (силумины)
- •5.4 Медь и ее сплавы
- •5.4.1 Латуни
- •5.4.2 Бронзы
- •5.4.2.1 Оловянистые бронзы
- •5.4.2.2 Свинцовые бронзы
- •5.5 Титан и его сплавы
- •5.6 Магний
- •5.7 Бериллий
- •6.2 Полиэтилен
- •6.3 Поливинилхлорид
- •6.4 Фторопласт
- •6.5. Полистирол и пластики абс
- •6.6 Полипропилен
- •6.7 Поливинилацетат
- •6.8 Фенолоформальдегидные смолы
- •6.9 Кремнийорганические полимеры
- •6.10 Эпоксиполимеры
- •6.11 Полиуретан
- •6.12 Полиамиды
- •6.13 Пластмассы
- •7.1.1 Структура композиционных материалов
- •7.1.2 Полимерные композиционные материалы (пкм)
- •7.1.3 Композиционные материалы с металлической матрицей
- •7.1.4 Композиционные материалы на основе керамики
- •1. Композиционные материалы
- •Вайнгард, у. Введение в физику кристаллизации металлов [Текст] / у. Вайнгард. - м. : Мир, 1967. – 170 с.
- •Учебное пособие по курсу «Материаловедение. Технология конструкционных материалов»
1.5.4 Кристаллизация жидкостей и макроструктура слитка
Макроструктура детали, образующаяся сразу после затвердевания, определяет многие свойства изделия. Это справедливо даже для слитков, несмотря на распространенное, но неправильное мнение, что дефекты могут быть ликвидированы при ковке. На практике, многие дефекты, проходя через все стадии изготовления, доходят до готового изделия. Наличие значительных дефектов не позволяет получить требуемые механические свойства, а колебания в химическом составе приводят к тому, что коррозионные и усталостные свойства в разных местах изделия становятся различными.
Температура кристаллизации определяется как температура, при которой свободные энергии твердой и жидкой фаз равны. Внутренняя энергия жидкости выше внутренней энергии упорядоченного твердого тела, и при переходе из одного состояния в другое наблюдается выделение или поглощение теплоты. Данная теплота называется скрытой теплотой плавления.
Однако, несмотря на справедливость утверждения о существовании только одной термодинамической температуры кристаллизации, экспериментально часто наблюдается переохлаждение жидких металлов, так как их кристаллизация начинается при более низкой температуре, чем принятая температура кристаллизации. Это явление иллюстрируется на рисунке 1.10, а, где приводится кривая охлаждения, показывающая изменение температуры со временем, при затвердевании некоторого количества жидкости. Когда температура жидкости окажется ниже Тк, говорят, что жидкость находится в переохлажденном состоянии Те. Как только кристаллизация началась (если количество затвердевающего металла было достаточным) температура оставшейся жидкости быстро повышается до нормальной температуры кристаллизации вследствие выделения скрытой теплоты плавления. При кристаллизации небольшого количества металла выделившейся теплоты может оказаться недостаточно, чтобы поддерживать температуру равной Тк (рисунок 1.10, б).
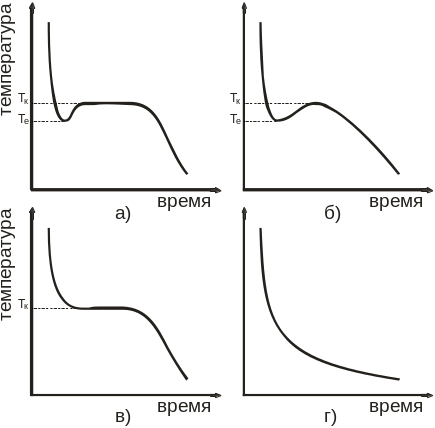
Рисунок 1.10 – Кривые охлаждения в случаях: а- кристаллизации чистого металла при наличии переохлаждения; б – кристаллизация небольшого количества чистого металла; в – кристаллизация без переохлаждения; г – охлаждение аморфного тела.
В случае отсутствия переохлаждения, т.е. если нет задержки в зарождении кристаллов, кривая охлаждения похожа на приведенную на рисунке 1.10, в. Все металлы склонны к образованию кристаллической решетки при охлаждении и имеют кривые охлаждения, аналогичные изображенным на рисунке 1.10, а-в. Однако аморфные вещества, структура которых напоминает структуру переохлажденной жидкости, при охлаждении ведут себя согласно рисунку 1.10, г. В этом случае в веществе не происходит изменения степени порядка и не выделяется скрытая теплота плавления.
1.5.5 Гомогенное зарождение кристаллов
Гомогенным зарождением кристаллов называется процесс кристаллизации абсолютно чистых веществ.
Зарождение кристаллов определяется как процесс образования в какой-либо части объема новой фазы (центров кристаллизации), отделенной от остального вещества границей раздела. Рассматривая только изменение внутренней энергии системы нельзя дать ответ на вопрос о причинах возникновения такого эффекта как переохлаждение.
Рассмотрим процесс возникновения зародыша кристалла более подробно. Когда атомы группируются таким образом, что образуется зародыш или центр кристаллизации, то между ним и жидкостью образуется поверхность раздела. Образование поверхности раздела приводит к затрате энергии, что вызывает увеличение свободной энергии системы при возникновении зародыша на величину:
![]() ,
,
где r – радиус зародыша, - удельная поверхностная свободная энергия.
С другой стороны само тело зародыша вызывает уменьшение свободной энергии системы на величину:
![]() .
.
Зародыш
может расти только в том случае, если
суммарная свободная энергия системы
![]() уменьшается.
уменьшается.
Рисунок 1.11 –
Изменение внутренней энергии системы
при образовании центра кристаллизации
Рисунок 1.12 –
Влияние температуры на изменение
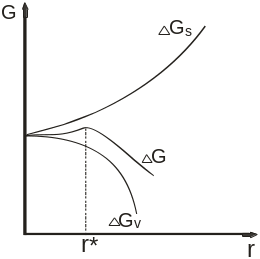
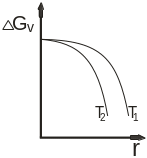
![]() в зависимости от температуры кристаллизации
в зависимости от температуры кристаллизации![]() ,
обязанное образованию границе раздела
между твердой и жидкой фазами, почти не
зависит от температуры, и, следовательно,
связь размеров критического зародыша
с величиной переохлаждения определяется
в основном только зависимостью
от температуры, как показано
на рисунке 1.12. Вблизи от точки плавления
размеры критического зародыша должны
быть бесконечно большими, так как при
приближении
,
обязанное образованию границе раздела
между твердой и жидкой фазами, почти не
зависит от температуры, и, следовательно,
связь размеров критического зародыша
с величиной переохлаждения определяется
в основном только зависимостью
от температуры, как показано
на рисунке 1.12. Вблизи от точки плавления
размеры критического зародыша должны
быть бесконечно большими, так как при
приближении
![]() к нулю уменьшение объема свободной
энергии, связанное с превращением
жидкости в твердую фазу, не может
компенсировать увеличение поверхностной
свободной энергии. По мере увеличения
переохлаждения размеры критического
зародыша уменьшаются. Таким образом,
зародыши, размер которых меньше
критического, имеют тенденцию к
исчезновению и наоборот.
к нулю уменьшение объема свободной
энергии, связанное с превращением
жидкости в твердую фазу, не может
компенсировать увеличение поверхностной
свободной энергии. По мере увеличения
переохлаждения размеры критического
зародыша уменьшаются. Таким образом,
зародыши, размер которых меньше
критического, имеют тенденцию к
исчезновению и наоборот.
Исходя из всего вышесказанного, можно сделать следующий вывод: причиной возникновения переохлаждения служит критический размер зародыша. При отсутствии переохлаждения (несмотря на то, что температура жидкости равна температуре кристаллизации) все появляющиеся зародыши будут исчезать и кристаллизация всего вещества не произойдет.
