
- •ВВЕДЕНИЕ
- •1. ОБЩИЕ СВЕДЕНИЯ О ДИСПЕРСНЫХ СИСТЕМАХ
- •1.1. Основные понятия и определения
- •1.3. Специфические особенности высокодисперсных систем
- •1.4. Классификации дисперсных систем
- •1.5. Методы получения дисперсных систем
- •1.5.1. Диспергационные методы
- •1.5.2. Конденсационные методы
- •1.5.3. Метод пептизации
- •1.6. Методы очистки дисперсных систем
- •1.7.1. Поверхностное натяжение
- •1.8. Поверхностно-активные вещества
- •1.9. Смачивание
- •1.10. Флотация
- •1.11. Строение коллоидных мицелл
- •1.12. Устойчивость и коагуляция дисперсных систем
- •2. НЕФТЯНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ
- •2.2. Строение и свойства дисперсионной среды
- •2.3. Способы описания механических свойств
- •2.4. Виды локальных образований в нефтяных системах. Строение сложных структурных единиц
- •2.5. Виды межмолекулярных взаимодействий
- •2.6. Влияние межмолекулярных взаимодействий на свойства молекулярных растворов и НДС
- •2.7. Факторы, влияющие на устойчивость дисперсных систем. Методы определения и способы регулирования устойчивости НДС
- •2.9. Способы получения и регулирования свойств НДС. Нефтяные эмульсии
- •2.9.1. Классификация эмульсий
- •2.9.2. Методы получения эмульсий
- •2.9.3. Механизм образования эмульсий
- •2.9.4. Факторы, влияющие на устойчивость эмульсий
- •3. ХАРАКТЕРИСТИКА ОСНОВНЫХ СОЕДИНЕНИЙ НЕФТИ
- •3.1. Алканы
- •3.1.1. СТРОЕНИЕ АЛКАНОВ
- •3.1.2. НОМЕНКЛАТУРА АЛКАНОВ. Правила построения названий алканов по номенклатуре ИЮПАК
- •3.1.3. ФИЗИЧЕСКИЕ СВОЙСТВА
- •3.1.4. Содержание алканов в нефтях
- •3.1.5. Теплофизические свойства
- •3.1.6. Газообразные алканы
- •3.1.7. Применение газов
- •3.1.8. Жидкие алканы
- •3.1.8.1. Углеводороды лёгких фракций нефти
- •3.1.8.2. Углеводороды средних фракций нефти
- •3.1.8.3. Изопреноидные углеводороды нефти
- •3.1.9. Твёрдые алканы
- •3.1.10. ХИМИЧЕСКИЕ СВОЙСТВА
- •3.2.2. Физические свойства циклоалканов
- •3.2.3. Химические свойства
- •3.3.2. СТРОЕНИЕ БЕНЗОЛА
- •3.3.3. Физические свойства аренов
- •3.3.4. ХИМИЧЕСКИЕ СВОЙСТВА аренов
- •3.3.5. Правило ориентации и реакционная способность
- •ВОПРОСЫ ДЛЯ САМОПРОВЕРКИ
- •Дисперсные системы
- •Нефтяные Дисперсные системы
- •ОБЩАЯ ХАРАКТЕРИСТИКА НЕФТИ. СОСТАВ НЕФТИ. ПЕРЕРАБОТКА НЕФТИ И ГАЗА
- •ФИЗИЧЕСКИЕ СВОЙСТВА НЕФТИ
- •ВЫВОДЫ
- •Библиографический список
- •Оглавление
- •ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ
- •Введение
- •Содержание
vk.com/club152685050 | vk.com/id446425943
(регулярное) чередование боковых метильных заместителей (2, 6, 10, 14, 18, 22 и т. д.), источником образования которых могут быть природные полиизопренолы. В последнее время в ряде нефтей обнаружены псевдо- и нерегулярные изопренаны. Углеводороды с псевдорегулярной структурой С12 и С14 (2,6- диметилалканы) не были обнаружены в нефти. В то же время присутствие 2,6,10-триметилалканов состава С17 и C19 указывает на то, что сквалан участвует в образовании псевдорегулярных структур. К этой же мысли приводит и наличие в нефтях нерегулярных изопреноидов типа 2,6,10,15-тетраметилалканов.
Ликопан также может рассматриваться как источник псевдорегулярных структур, таких, как 1,6,10,14тетраметилалканы С22 и С24.
В последние годы описан новый тип изопренанов, имеющих в качестве заместителя достаточно длинную алифатическую разветвленную цепь. Углеводороды этого строения представлены соединениями С20, С25 и С30 и отличаются изопентильным звеном. Присутствуют они в нефтях и в осадках. Родоначальник этой группы — 2,6,10- триметил-7- (3-метилбутил)додекан.
3.1.9. ТВЁРДЫЕ АЛКАНЫ
Твёрдые алканы нефти делятся на две группы – собственно парафины и церезины, различающиеся по кристаллической структуре, химическим и физическим свойствам.
Твёрдые алканы содержатся практически во всех нефтях, но в разных количествах. Парафины в нефтях находятся либо в растворенном, либо во взвешенно-кристаллическом состоянии.
137
vk.com/club152685050 | vk.com/id446425943
Состояние твёрдых парафинов в нефти определяется прежде всего температурой. Они растворяются в нефти неограниченно только при повышенных температурах (около 40 °С). При более низких температурах парафин выделяется из нефти в виде микрокристаллов. Так как температура нефти в недрах земли обычно близка к 40 °С или несколько выше, можно считать, что она представляет собой однородный раствор всех компонентов.
По химическому составу парафин является сложной смесью углеводородов. Полное разделение его на компоненты и идентификация их окончательно не завершены.
Исследования твёрдых углеводородов, выделенных из масляных фракций, показали, что наряду с парафином, имеющим ярко выраженную кристаллическую структуру, существует другой твердый продукт, более мягкий, внешне аморфный, такой продукт называется церезином.
Нефтяные парафины (дистиллятные - от С19Н40 до С35Н72) имеют сравнительно небольшую молекулярную массу и, соответственно, невысокие температуры кипения.
Парафины и церезины образуют два разных гомологических ряда, которые отвечают составу СnH2n+2. Однако в молекулы парафинов входят углеводородные радикалы нормального строения, а в молекулы церезинов – в основном изостроения, вместе с радикалами циклического строения (нафтеновыми и ароматическими).
Сырьём для получения парафинов служит обычно нефть, а церезин может быть выделен из остаточных нефтепродуктов, а также из озокерита. Озокерит, или горный воск, состоит главным образом из церезина с большим или меньшим
138
vk.com/club152685050 | vk.com/id446425943
содержанием других веществ (песчаник, нефтеобразные масла, смолы). Парафины и церезины имеют самое разнообразное применение. Огромная масса парафина расходуется в производстве свечей, в спичечной, бумажной, кожевенной, текстильной отраслях промышленности. Парафин применяется как загуститель в производстве пластичных смазок, является важной составной частью вазелина (и технического, и медицинского). Особенно большое значение приобрело производство из парафина синтетических жирных кислот и спиртов путём окисления кислородом воздуха.
3.1.10. ХИМИЧЕСКИЕ СВОЙСТВА
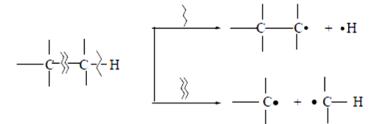
Алканы - малополярные и малореакционноспособные соединения. Для них характерны реакции замещения и крекинг, протекающие с разрывом связей С-Н и С -С, идущие по радикальному механизму, предполагающему гомолитический тип разрыва связи.
Эти процессы требуют больших энергетических затрат (высоких температур и облучения светом). Выход и состав продуктов во многом определяются относительной устойчивостью образующихся во время реакции радикалов. Устойчивость радикалов зависит от способности (возможности) свободного (неспаренного) электрона рассредоточиться по соседним связям С-С. Во время реакции в первую очередь
139
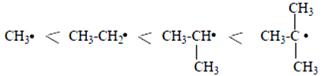
vk.com/club152685050 | vk.com/id446425943
образуются более устойчивые радикалы, для которых требуется затратить меньшее количество энергии.
Aлканы вступают в реакции, протекающие по механизму радикального замещения, обозначаемого символом SR (англ. Substitution radicalic). Устойчивость радикалов увеличивается от первичного к вторичному и далее к третичному.
Основные химические превращения алканов идут только при сообщении им достаточно высокой энергии (за счёт нагревания или УФ-облучения). При этом может произойти или разрыв связи С-Н с последующей заменой атома водорода на другой атом или группу атомов (реакции замещения), или же разрыв молекулы по связи С-С (реакции расщепления).
Несмотря на то, что энергии этих связей равны соответственно: 376,8-410,3 и 314-368,4 кДж/моль, разрыв предпочтительнее идёт по связи С-Н. Это связано с большей доступностью связи С-Н для атаки химических реагентов.
Реакции окисления алканов. Эти процессы сопровождаются изменением степеней окисления атомов. Жесткое окисление углеводородов приводит к разрыву всех связей С-С и С -Н и сопровождается выделением большого количества тепла (экзотермическая реакция) и называется горением. Если окисление идет слишком быстро, оно может сопровождаться взрывом:
CnH2n+2 + (3n+1)O2→ nCO2 + (n+1)H2O
140
vk.com/club152685050 | vk.com/id446425943
CH4 + 2O2 → CO2 + 2H2O + 880 кДж
С8H18 + 12,5 O2 → 8CO2 + 9H2O + Q
Низшие газообразные гомологи – метан, этан, пропан, бутан – легко воспламеняются и образуют с воздухом взрывоопасные смеси. Для предотвращения взрывов бытового газа в него добавляют одоранты (англ. Оdour – запах): небольшие примеси меркаптанов (R-SH). Меркаптаны являются крайне дурнопахнущими веществами, которые дают возможность вовремя обнаружить утечку газа. С увеличением молекулярной массы алканы загораются труднее. Вспомните, что газ на кухне (метан) загорается очень легко, а мазут или парафин поджечь довольно сложно. Процесс горения углеводородов широко используется для получения энергии (в двигателях внутреннего сгорания, в тепловых электростанциях и т.п.) и раньше для освещения (газовые рожки, парафиновые свечи).
В карбюраторных двигателях необходимо использовать бензин, пары которого устойчивы к детонации, то есть устойчивы к резкому сжатию в цилиндре. Количественной характеристикой стойкости к детонации является октановое число. Октановое число численно равно процентному (по объему) содержанию изооктана (октановое число которого принято за 100) в его смеси с н-гептаном (октановое число равно 0), эквивалентной по детонационной стойкости испытуемому топливу при стандартных условиях испытания.
Горение метана при недостатке кислорода происходит по уравнениям:
141

vk.com/club152685050 | vk.com/id446425943
Последняя реакция используется в промышленности для получения сажи из природного газа, содержащего 80-97% метана. Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов.
Например, при неполном окислении бутана (разрыв связи С2–С3) получают уксусную кислоту:
Важное промышленное значение приобрело каталитическое окисление высших алканов (С12-С25) с целью получения высших жирных спиртов и жирных кислот (ВЖС) (работы акад. С.С. Наметкина). Сырьём являются парафины, получаемые при депарафинизации нефтепродуктов:
KMnO4
 CH3 (CH2)m CH2OH
CH3 (CH2)m CH2OH
CH3 (CH2)n CH3 100-1200
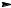 CH3 (CH2)m COOH
CH3 (CH2)m COOH
Образующиеся продукты используются для получения поверхностно-активных соединений, моющих средств, пластификаторов.
142

vk.com/club152685050 | vk.com/id446425943
Важное значение имеет реакция взаимодействия метана с водяным паром, в результате которой образуется смесь оксида углерода (II) с водородом – "синтез-газ":
CH4 + 0,5O2 800-9000 CO + 2H2
Эта реакция используется для получения водорода. Синтез-газ служит сырьем для получения различных углеводородов (метиловой спирт и др.).
Дегидрирование алканов. В присутствии катализатора при нагревании из алканов за счёт разрыва связи С-Н происходит отщепление атомов водорода, что приводит к образованию алкенов. Например, дегидрированием этана можно получить этилен:
CH3CH3 |
|
CH2 |
|
CH2 + H2 |
|
|
|||
|
|
|||
|
В результате дегидрирования бутана образуется бутилен или бутадиен:
C4H10 |
Cr2O3 |
|
CH3 |
|
|
|
|
CH |
|
CH |
|
|
CH3 |
||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
5800 |
|
CH2 |
|
|
|
CH |
|
|
CH3 |
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||||||||
Образующаяся смесь изомерных бутиленов широко применяется для получения полимербензинов и в синтезе алкилатов, являющихся высокооктановыми компонентами бензинов.
Особенно важен процесс дегидрирования бутана с целью получения бутадиена, который необходим для синтеза каучуков:
143
vk.com/club152685050 | vk.com/id446425943
C4H10 |
600-6200 |
CH2 |
|
|
CH |
|
CH |
|
|
CH2 + 2H2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||
Ca8 |
Ni (PO4)6 + Cr2O3 |
|||||||||
Дегидрированием изопентана, выделяемого из газового бензина и газов нефтепереработки, получают изопрен, также важный полупродукт для синтеза каучуков:
C5H12 |
|
CH2 |
|
|
C |
|
CH |
|
CH2 + 2H2 |
|
|
|
|||||||
|
|
|
|
|
CH3
Дегидрирование низших алканов при очень высоких температурах приводит к образованию ацетилена (пиролиз метана):
2 CH4 1500 °C HC CH +3 H2
CH +3 H2
1100-1200 °C |
|
H3C CH3 |
HC CH +2 H2 |
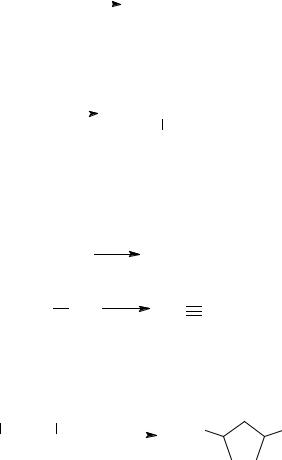
При нагревании алканов с большим количеством атомов углерода происходит дегидроциклизация – реакция дегидрирования, которая приводит к замыканию цепи в цикл.
|
|
|
CH3 |
|
|
|
CH3 |
300 °C, Pt H3C |
|
CH3 |
|||||
H3C |
|
|
CH |
|
CH2 |
|
|
CH |
|
CH3 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
2, 4-диметилпентан |
|
|
1, 3-диметилциклопентан |
||||||||||||
Алканы с основной цепью, состоящей из 6 или более атомов углерода, также вступают в реакцию дегидроциклизации, но в этом случае образуются шестичленный цикл. В условиях реакции образующийся цикл подвергается дальнейшему дегидрированию и превращается в энергетически
144

vk.com/club152685050 | vk.com/id446425943
более устойчивый бензольный цикл ароматического углеводорода (арена). Эти реакции лежат в основе процесса риформинга – переработки нефтепродуктов с целью получения аренов (ароматизация предельных углеводородов) и водорода. Превращение н-алканов в арены ведет к улучшению детонационной стойкости бензина.
CH3 |
|
|
CH2 |
|
CH2 |
|
CH3 300-4000C |
Cr |
O |
|
|
|
|
|
CH3 |
|
|
|
|
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
CH2 |
|
CH2 |
|
CH3 |
|
|
, |
2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
-H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
n-гептан |
|
|
|
|
метил- |
|
|
метилбензол |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
циклогексан |
|
|
|
|
(толуол) |
||||||||||
|
|
|
Изомеризация. Под влиянием катализаторов при |
||||||||||||||||||||||||
нагревании |
алканы |
изомеризуются |
в |
углеводороды |
|||||||||||||||||||||||
разветвлённого строения: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
CH3CH2CH2CH2CH3 |
|
AlCl3 |
|
|
CH3 |
|
CH |
|
CH2 |
|
CH3 |
||||||||||||||
|
|
|
1000 |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Реакция изомеризации используется для повышения октанового числа бензинов.
Крегинг. Крекинг – высокотемпературный процесс (450700оС) разложения алканов с большой молекулярной массой в присутствии катализаторов, в результате которого образуется смесь насыщенных и ненасыщенных низкомолекулярных углеводородов (за счет разрыва связей С-С и С-Н).
145
vk.com/club152685050 | vk.com/id446425943
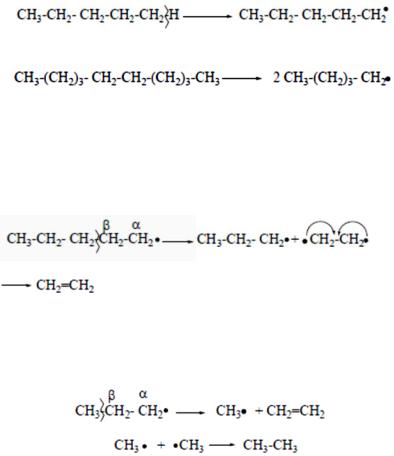
В процессе крекинга образуются углеводородные (алкильные) радикалы, превращения которых и определяют состав образующихся продуктов.
Рассмотрим возможные превращения алкильных радикалов на примере н-пентильного радикала, образование которого может явиться результатом термической диссоциации связи С-Н в н-пентане:
или связи С-С, например, н-декана:
Стабилизация свободного радикала, несущего неспаренный электрон, возможна за счет распада связей β (С-С) или β (С-Н).
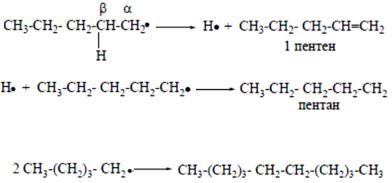
Так, при распаде связи β (С-С) образуется пропильный радикал и этилен:
Распад связи β (С-С) пропильного радикала приводит к образованию этилена и метильного радикала, димеризация которого дает этан:
146
vk.com/club152685050 | vk.com/id446425943
При распаде связи β (С-Н) имеет место диспропорционирование радикалов по схеме:
Возможна (но мало вероятна) димеризация радикалов:
Галогенирование алканов. Эта реакция идёт сравнительно легко с замещением атомов водорода в алканах на галогены. Из галогенов наиболее широко используется хлор, вследствие его доступности, дешевизны и высокой химической активности.
Как было установлено Н.Н. Семёновым, эта реакция протекает по радикально цепному механизму.
Молекулярный хлор под влиянием света расщепляется на атомный, который инициирует (начинает) радикальную реакцию; он отщепляет водород от метана, образуя радикал - метил и хлористый водород. Метильный радикал взаимодействует с молекулярным хлором и стабилизируется в первый продукт хлорирования метана - хлористый метил, который по аналогичной схеме подвергается дальнейшему хлорированию, образуя последовательно хлористый метилен, хлороформ и тетрахлорметан (четырёххлористый углерод):
Сl 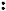 Cl
Cl  Cl
Cl + Cl
+ Cl 
147

vk.com/club152685050 | vk.com/id446425943
H3C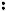 H + Cl
H + Cl
 H3C
H3C  + H
+ H 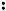 Cl
Cl
H3C |
+ Cl Cl |
H3C Cl + Cl |
||
|
|
|
Хлористый |
|
|
|
|
метил |
|
CH3Cl + |
Cl |
CH2Cl + HCl |
||
CH2Cl + Cl Cl |
CH2Cl2 + HCl |
|||
|
|
|
Хлористый |
|
|
|
|
метилен |
|
СH2Cl2 |
Cl2 |
CHCl |
Cl2 |
CCl4 |
|
-HCl |
Хлороформ3 |
- HCl |
Четырёххлористый |
|
|
|
|
углерод |
Реакционная способность галогенов убывает в ряду:
F2<Cl2<Br2<I2
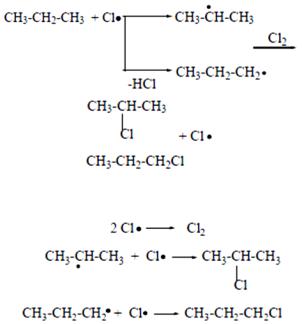
Наибольшее практическое значение имеет реакция хлорирования:
2-хлорпропан 1-хлорпропан
Механизм а) инициирование цепи
б) рост цепи
148
vk.com/club152685050 | vk.com/id446425943
в) обрыв цепи
Реакции галогенирования сильно различаются по энергетическим характеристикам. Тепловые эффекты уменьшаются в ряду F2>Cl2>Br2>I2, причём особое место занимают процессы фторирования и йодирования.
При галогенировании алкановых углеводородов важное значение имеет направление атаки реагента, приводящее к образованию изомерных алкилгалогенидов. Состав изомеров определяется относительной подвижностью различных атомов водорода. Реакционная способность атомов водорода меняется в следующем ряду:
третичный > вторичный > первичный
При низких температурах реакция хлорирования протекает региоселективно. Региоселективная реакция –
149
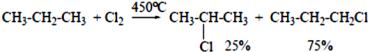
vk.com/club152685050 | vk.com/id446425943
реакция, в ходе которой химическим изменениям подвергается преимущественно одно из двух или нескольких положений молекулы, то есть избирательно по отношению к атомам водорода.
Относительная реакционная способность первичных, вторичных и третичных атомов водорода по отношению к хлору составляет 1:4:5. Выход продукта галогенирования зависит также от фактора вероятности замещения первичных, вторичных и третичных атомов водорода в углеводороде (их количества).
Если реакция хлорирования проводится при высокой температуре, то получается иное соотношение изомерных галогенопроизводных.
2-хлорпропан 1-хлорпропан
При 450°С реакционная способность первичных и вторичных связей С-Н одинакова (1:1). Региоселективность реакции при повышении температуры резко уменьшается, то есть радикал хлора реагирует неизбирательно по отношению к атомам водорода. Кроме этого происходит расщепление молекулы углеводорода.
Бромирование алканов происходит значительно более региоселективно (более избирательно) из-за меньшей активности бромирующего агента. Относительная реакционная способность первичных, вторичных и третичных атомов водорода составляет 1:100:200, поэтому, если требуется
150

vk.com/club152685050 | vk.com/id446425943
получить третичный или вторичный галогеналкил, целесообразно проводить реакцию бромирования.
2-бромпропан 1-бромпропан
Имеются данные и о большем различии в относительной реакционной способности связей С-Н в реакции бромирования при других температурах.
Хлорпроизводные метана и других низших алканов являются хорошими растворителями жиров, синтетических смол и каучуков, нитро- и ацетилцеллюлозы. Их можно использовать и для очистки призабойной зоны нефтяных скважин от асфальто-смолистых и парафиновых отложений. Применяют также и при депарафинизации масел.
Хлорпроизводные алканов используют для получения спиртов, в том числе и высших спиртов:
C5H11Cl + KOH  C5H11OH + KCl
C5H11OH + KCl
При пропускании хлористого метила (или смеси его с хлорзамещёнными ароматическими углеводородами) над медно-кремниевым сплавом при 300 0С образуются алкил- и арилхлорсиланы:
|
C6H5 |
|
CH3Cl + C6H5Cl + Si |
|
SiCl2 |
|
||
|
|
CH3 |
151

vk.com/club152685050 | vk.com/id446425943
Алкил- и арилхлорсиланы являются исходным продуктом в синтезе кремнийорганических соединений, применяемых в производстве силиконовых жидкостей, консистентных смазок, смол и каучуков.
Хлороформ и четырёххлористый углерод используют для получения хлорфтор- и фторпроизводных:
CCl4 + HF → CCl2F2,
которые, применяют в качестве хладоагентов - фреонов.
Полностью фторированные алканы применяют в качестве инертных теплоносителей, в производстве полимеровфторопластов.
Хлорирование твёрдых парафинов осуществляют для получения присадок, понижающих температуру застывания масел (депрессорные присадки).
Нитрование (реакция М.Коновалова). Нитрование алканов осуществляют с помощью азотной кислоты при температуре 200-450 0С. Нитрование всегда сопровождается частичным разложением углеводородов, что приводит к получению нитросоединений с меньшим числом атомов углерода. Из пропана таким путём помимо 1- и 2-нитропропанов образуются нитроэтан и нитрометан:
 CH3 CH2 CH2 NO2
CH3 CH2 CH2 NO2
 CH3 CH CH3
CH3 CH CH3
CH3 |
|
CH2 |
|
CH3 |
|
|
|
|
|
|
NO2 |
||||
|
|
|
 CH3CH2 NO2
CH3CH2 NO2  СH3 NO2
СH3 NO2
152
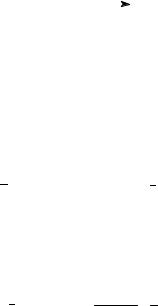
vk.com/club152685050 | vk.com/id446425943
Нитрометан, нитроэтан, нитропропан являются хорошими растворителями эфиров целлюлозы, полимеров, лаков. Они могут применяться в качестве добавок, снижающих температуру самовоспламенения дизельных топлив.
Восстановлением нитроалканов в кислой среде можно получить амины:
R |
|
NO2 + 3H2 |
H+ |
R |
|
NH2 + 2H2O |
|
Pt |
|
||||
|
|
|
|
|
|
Амины используют для получения ингибиторов коррозии, поверхностно-активных веществ, для очистки газов от сероводорода.
Сульфирование. При слабом нагревании дымящая серная кислота сульфирует алканы, т. е. атом водорода в них замещается на сульфогруппу:
RH + H2SO4  R SO3H + HCl
R SO3H + HCl
Врезультате образуются алкансульфокислоты.
Сульфохлорирование. При действии на алканы смеси сернистого газа и хлора идёт реакция сульфохлорирования:
R H + SO2 + Cl2 УФ 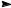 R SO2Cl + HCl
R SO2Cl + HCl
Сульфохлориды легко гидролизуются до сульфокислот:
R – SO2Cl + H2O → R – SO3H
Взаимодействием сульфохлоридов с избытком аммиака получают сульфамиды:
RSO2Cl + NH3 RSO2NH2 + HCl
RSO2NH2 + HCl
153

vk.com/club152685050 | vk.com/id446425943
Сульфокислоты могут быть получены также и реакцией сульфоокисления:
2R |
|
H + 2SO2 + O2 |
|
2R |
|
SO3H |
|
|
|
Алкансульфокислоты образуют со щелочами соли – сульфонаты:
R SO3H + NaOH  RSO3Na + H2O
RSO3Na + H2O
Сульфонаты и сульфамиды с 12-18 и выше атомами углерода, получаемые на основе жидких парафинов, выделяемых из дизельных фракций, служат в качестве поверхностно-активных и моющих веществ, эмульгаторов нефти и флотационных реагентов.
3.2. ЦИКЛОАЛКАНОВЫЕ УГЛЕВОДОРОДЫ (НАФТЕНЫ) 3.2.1. СОДЕРЖАНИЕ ЦИКЛОАЛКАНОВ В НЕФТЯХ
Циклоалканы относятся к основным компонентам нефти. Они находятся в нефти в преобладающем количестве. В некоторых нефтях их количество доходит до 75-80%.
Циклоалканы содержатся во всех нефтях и во всех нефтяных фракциях. С увеличением температуры кипения нефтяной фракции их количество увеличивается. Но уже в высококипящих нефтяных остатках их становится меньше. В нефти содержатся в основном пяти- и шестичленные циклоалканы, которые названы нафтенами.
В отличие от других углеводородов нафтены впервые обнаружены в самой нефти. В 80-х годах ХХ века В.В. Марковников и Н.Д. Зелинский выделили из бакинской нефти углеводороды ряда СnH2n, обладающие свойствами насыщенных соединений. В результате исследований было
154
vk.com/club152685050 | vk.com/id446425943
установлено, что основная масса нафтенов состоит из гомологов циклопентана и циклогексана. Число циклов в нафтенах может быть от 1 до 5. Они обычно содержат короткие или длинные алкильные радикалы. Моноциклические нафтены с длинной боковой цепью термодинамически менее устойчивы, чем замещённые двумя или тремя более короткими радикалами.
Распределение их по фракциям определяется составом нефтей и температурами кипения фракций. Так моноциклические нафтены содержатся во фракциях до 350 °С, бициклические – во фракциях от 160 до 500 °С, причём количество их убывает после 400 °С. Трициклические нафтены находятся во фракциях выше 350-400 °С. Нафтеновые углеводороды составляют значительную часть высококипящих фракций нефти.
Относительное концентрационное распределение нафтенов в зависимости от числа циклов в молекуле называется нафтеновым паспортом. Характер нафтеновых паспортов нефтей разнообразен. Например, в нефтях Южного Каспия преобладают би- и тетрациклические нафтены, в отличие от нефтей других регионов. Общей закономерностью нафтеновых паспортов является преобладание моно- и бицикланов над остальными нафтеновыми углеводородами. В среднем для большинства нефтей содержание моно- и бицикланов составляет 50-60 % от суммы нафтенов, а доля пентациклических структур не превышает 10 %. Основное различие нафтеновых паспортов нефтей проявляется в соотношении моно- и бицикланов. Есть нефти с примерно одинаковым содержанием этих углеводородов, а также с преобладанием моноцикланов над бицикланами. В нефтях с низким содержанием н-алканов обычно бицикланы преобладают
155
vk.com/club152685050 | vk.com/id446425943
над моноцикланами. Как правило, концентрация полициклических нафтенов снижается с увеличением числа циклов в молекуле.
Моноциклические нафтены, содержащие от пятидо восьми атомов углерода в молекуле, сосредоточены в основном во фракции н.к. – 125 °С. Содержание углеводородов ряда циклопентана в ней от 14,5 % до 53 % (сибирская нефть) 36,5 % (бакинская нефть) и циклогексанов – от 14 % (сургутская нефть) до 36,5 % (бакинская нефть).
Содержание самого циклопентана в нефтях незначительно: максимально 3 %, а содержание циклогексана составляет от 1 % до 18 %. В большем количестве представлены метилциклоалканы, обладающие меньшей свободной энергией и термодинамически более устойчивые. Так, содержание метилциклогексана во фракции н.к. – 125 °С составляет 36-50 %.
Среди ди- и тризамещённых цикланов преобладают 1,3- диметил-, 1,1,3-триметилциклопентаны, 1,2-диметил-, 1-метил- 3-этил-, 1,1,3-триметилциклогексаны. Это можно объяснить исходя из основного принципа конформационного анализа — минимального отталкивающего взаимодействия несвязанных атомов. В данном случае относительная термодинамическая устойчивость стереоизомеров определяется энергией взаимодействия атомов в замещающих (метильных и этильных) радикалах, т.е. зависит от взаимного пространственного расположения радикалов.
Во фракции С9 содержится реликтовый углеводород
(1,1,3-триметилциклогексан) – продукт деструкции каротиноидов.
156
vk.com/club152685050 | vk.com/id446425943
Идентифицированы гомологи 1,1,3-триметил-2- алкилциклогексана состава С10-С24:
Обнаружен также нафтен с изопреноидной цепью состава С40.
В тяжёлых фракциях нефти (400-550 °С) содержатся нафтены сложной структуры. Они имеют бициклическое строение.
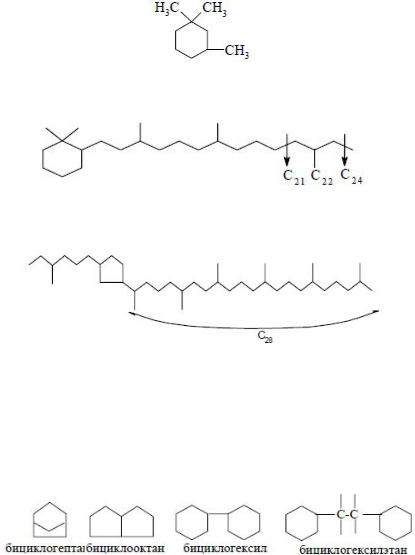
Бициклические нафтены бывают мостикового, конденсированного, сочленённого, изолированного типов строения.
В ряде нефтей обнаружены бицикланы и их метильные и диметильные гомологи:
157
vk.com/club152685050 | vk.com/id446425943
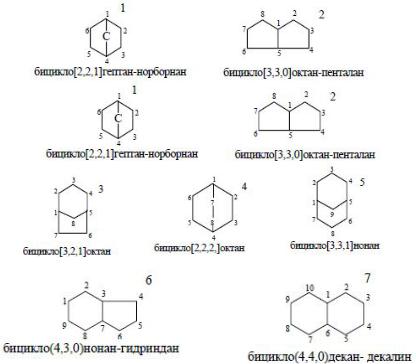
Среди бицикланов С8-С10 в наибольших количествах содержатся углеводороды ряда бицикло[3.2.1] октана и особенно бицикло[3.3.0]октана. Содержание бицикланов ряда пенталана — бицикло[3.3.0] октанов — составляет более 40 % от бицикланов С9-С10.
В нефтях наиболее распространены бициклические углеводороды, имеющие конденсированные кольца, затем идут углеводороды мостикового строения и сочлененные углеводороды.
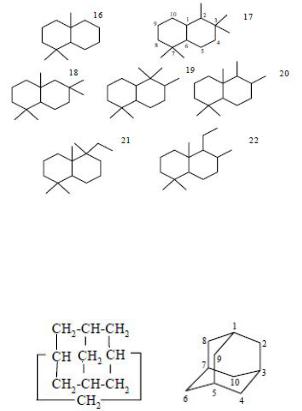
Сесквитерпановые углеводороды С11-C16 —
полиметилзамещённые декалины — это углеводороды
158
vk.com/club152685050 | vk.com/id446425943
реликтового характера (16-22). Сочленение колец везде транс-. Ориентация метильных и этильных заместителей при С=2 и С=3 всегда экваториальная:
Трициклические нафтены в зависимости от расположения колец бывают трёх типов – мостикового типа, с конденсированной системой колец и смешанные. К числу чисто мостиковых углеводородов относится трицикло(3,3,1,13,7) декан-адамантан – С10Н16.
Адамантан впервые был выделен из чехословацкой нефти в 1933 году, затем получен и в других странах. Этот углеводород образует кристаллы в форме октаэдров с температурой плавления 270 °С, способные возгоняться уже при комнатной температуре. Плотность адамантана необычно велика для насыщенного углеворода и составляет 1,07 при
159

vk.com/club152685050 | vk.com/id446425943
20 °С. Адамантан построен из трёх конденсированных циклогексановых колец в конформации кресла. Расположение углеродных атомов в такой структуре очень близко к их взаимному расположению в кристалле алмаза. Этому сходству адамантан обязан своим названием («адамант» по-чешски — алмаз). Содержание адамантана в нефтях невелико: 0,004- 0,01 %. Во фракции 200-225°С идентифицировано 24 алкилиадамантана состава С11-С14, содержащих метильные и этильные заместители. Общее содержание алкиладамантанов составляет 0,02 % от состава нефти. Некоторые функциональные производные адамантана обладают биологической активностью и используются в качестве противовирусных лекарственных средств (ремантадин, мидантан), а также проявляют активность при лечении болезни Паркинсона. Адамантан и его производные являются ценным исходным сырьём для получения полимерных композиций, термостабильных добавок к смазочным маслам и других технически важных продуктов.
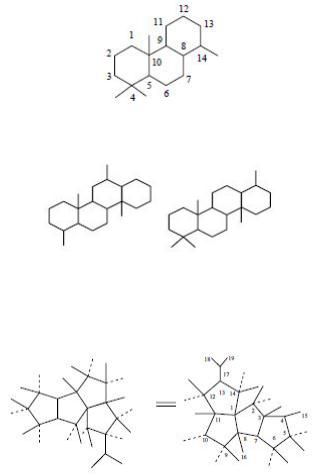
Нефтяные трицикланы С11-С12 являются в основном (проадамантановыми углеводородами) предшественниками адамантана. В нефти обнаружены:
160
vk.com/club152685050 | vk.com/id446425943
К трициклическим углеводородам нефти относятся также пергидрофенантрены (С12-С26), которые найдены в значительных количествах во фракциях 300-420 °С.
Внефтях были определены насыщенные углеводороды со структурой пергидрохризена.
Внефтях и конденсатах во фракции 300-550°С обнаружена группа насыщенных тетрациклических
углеводородов С19Н32, по строению являющихся
дитерпеноидами.
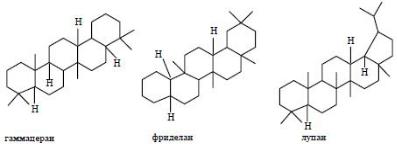
Кроме тетрациклододекана в нефти обнаружен пентациклотетрадекан (конгрессан). В нефти и других каустобиолитах был обнаружен ряд аналогов циклических
161
vk.com/club152685050 | vk.com/id446425943
политерпенов – дитерпены С20. Среди пентациклических тритерпеноидов следующие:
В нефти найдены и другие тетрациклические структуры C19-С23, у которых в основе тетрациклического ядра лежит система циклопентанопергидрофенантрена. Эти соединения принадлежат к стеранам.
Стераны и гопаны — важнейшие реликтовые углеводороды нефтей. В отличие от природных биологических соединений, стераны нефтей стереохимически и структурно преобразованы. Стераны в условиях диа- и катагенеза в земной коре претерпевают сложное постепенное изменение конфигурации нескольких хиральных центров, что является важным при прогнозировании наличия залежей нефти в определенном регионе.
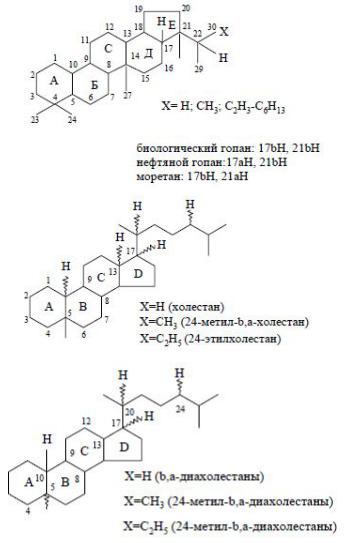
Исследование полициклических насыщенных углеводородов С27 и выше, имеющих углеродный скелет стероидов и тритерпеноидов, несет важную информацию благодаря связи этих продуктов с биологическими предшественниками (хемофоссилии). Тетрациклоалканы состава С27-С30 принадлежат к стеранам, а пентациклоалканы, содержащие от 27 до 35 атомов углерода,— к тритерпанам ряда гопана.
162
vk.com/club152685050 | vk.com/id446425943
Структурные формулы нефтяных тритерпанов, стеранов, перегруппированных стеранов:
163
vk.com/club152685050 | vk.com/id446425943
Согласно номенклатуре сплошной линией обозначены связи С-Н, расположенные над плоскостью молекулы, а расположенные ниже — штриховой, волнистыми линиями — связи С-Н тех хиральных центров, где реально возможна эпимеризация.
Происхождение стеранов (гидрированных стеринов) связывают со стероидами. Стероиды различаются характером заместителей (они могут содержать гидроксильную, кетонную и другие группы) и строением тетрациклического ядра. Гидрированные стерины могли образоваться из стероидов в результате ряда химических превращений, среди которых существенную роль должно было играть восстановление. Именно биологическое происхождение этих стеринов позволило рассматривать их как биологические «метки», а результаты исследования стеринов связать с общими вопросами происхождения нефти.
В высших фракциях нефти могут присутствовать моноциклические полиметиленовые углеводороды с 28 атомами углерода в цепи (в нескольких цепях). При близких молекулярных массах и одинаковой температуре перегонки тяжёлые нефти характеризуются содержанием циклоалканов с большим числом циклов, чем легкие.
Высшие фракции нефти содержат в основном би- и трициклические углеводороды, замещённые одной или несколькими короткими цепями.
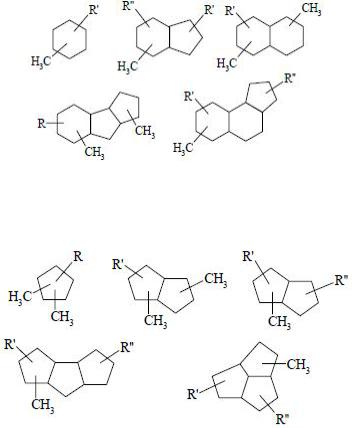
Строение циклоалканов первой группы (с шестичленными кольцами) может быть отражено следующими формулами:
164
vk.com/club152685050 | vk.com/id446425943
Соединения первых трех типов преобладают. Для пятичленных циклоалканов (вторая группа), приведённых ниже, характерно наличие конденсированных колец:
Здесь также наблюдается преобладание структур первых трёх типов.
Мостиковые высокомолекулярные циклоалканы являются производными бицикло[3.2.1]октана, бицикло[2.2.2]октана, адамантана:
165
