
- •Методичні вказівки
- •Зміст модуля II
- •7. Розчини
- •7.1 Загальна характеристика розчинів
- •7.2 Концентрація розчиненої речовини
- •7.3 Властивості розчинів
- •7.3. Питання та задачі для самоконтролю
- •8.Розчини електролітів
- •8.1. Загальна характеристика розчинів електролітів
- •8.2.Реакції в розчинах електролітів
- •8.3. Запитання для самоконтролю
- •8.4. Задачі для самоконтролю
- •9. Комплексні сполуки
- •9.1.Загальна характеристика комплексних сполук
- •9.2.Номенклатура комплексних сполук
- •9.3.Природа координаційного зв’язку
- •9.4.Класифікація комплексних сполук.
- •9.5.Дисоціація комплексних сполук у розчинах. Стійкість комплексних іонів.
- •9.6.Ізомерія комплексних сполук
- •9.7.Властивості комплексних сполук
- •9.8.Основні способи одержання комплексних сполук.
- •9.9.Значення та застосування комплексних сполук
- •9.10.Запитання та задачі для самоконтролю
- •8. Номенклатура комплексних сполук.
- •10. Окисно-відновні реакції
- •10.1.Загальна характеристика процесів окислення та відновлення
- •10.2.Складання рівнянь окисно-відновних реакцій
- •10.3. Запитання та задачі для самоконтролю
- •11. Загальні та електрохімічні властивості металів
- •11.1. Загальні властивості металів
- •11.2. Гальванічні елементи. Корозія металів
- •11.3. Електроліз
- •11.4. Запитання та задачі для самоконтролю
- •Список рекомендованої літератури
11.2. Гальванічні елементи. Корозія металів
Електрохімія вивчає процеси перетворення хімічної енергії в електричну і навпаки.
Електрохімія розглядає виникнення електричного потенціалу на межі поділу двох фаз метал – розчин, утворення електрорушійної сили (ЕРС) у гальванічних елементах, а також явище електролізу.
Гальванічний елемент – це прилад, в якому енергія окислювально-відновної реакції перетворюється безпосередньо в електричну. Прикладом може бути гальванічний мідно-цинковий елемент (елемент Якобі–Даніеля),
(-)ZnZnSO4CuSO4Cu (+)
Двома вертикальними рисками позначено межу поділу розчинів обох солей.
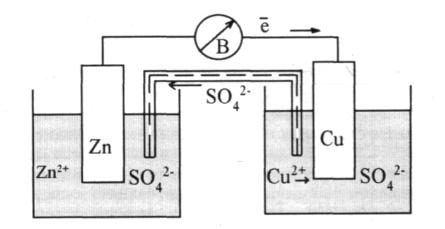
Рис.11.3. Схема мідно-цинкового гальванічного елемента
У цьому елементі цинковий електрод є анодом, а мідний – катодом. На аноді відбувається окислення (Zn - 2е-=Zn2+), на катоді – відновлення (Cu2++2е-=Cu). Сумарна реакція Zn+Cu2+=Zn2++Cu є джерелом електричного струму.
Електрорушійну силу (ЕРС) гальванічного елемента визначають як різницю електродних потенціалів. При цьому від потенціалу катода віднімають потенціал анода:
ЕРС=Eкатода-Eанода (11.3)
Приклад 2. Обчислити ЕРС гальванічного елемента Якобі-Даніеля, якщо концентрація розчину ZnSO4 - 0,1 моль/л, а розчину CuSO4 - 2 моль/л.
Розв’язання. Знаходимо потенціал мідного електрода (катода):
![]() В.
В.
Знаходимо потенціал цинкового електрода (анода):
![]() В;
В;
![]() В.
В.
Знаходимо ЕРС елемента:
ЕРС=0,35 - (-0,79)=1,14 В.
Гальванічний елемент, що складається із двох однакових електродів, занурених у розчин однорідної солі різних концентрацій, називається концентраційним елементом.
(-)AgAgNO3AgNO3Ag (+)
C2 C1
У концентраційних елементах катодом є електрод, що має більшу концентрацію солі C1, анодом – електрод з меншою концентрацією солі C2.
ЕРС таких елементів обчислюють за рівнянням:
![]() (11.4)
(11.4)
До окислювально-відновних відносять гальванічні елементи, в яких реакція окислення або відновлення проходить у розчині без участі матеріалу електрода, останній служить лише провідником електронів. Прикладом окислювально-відновного електрода може бути платина, занурена в розчин солей FeCl2 і FeCl3. Якщо такий електрод з’єднати з будь-яким іншим у замкнутий елемент, то в ньому проходитиме реакція окислення-відновлення.
Fe3++e-=Fe2+
Потенціал такого електрода обчислюють за формулою:
![]() (11.5)
(11.5)
де [oxyd], [red] - концентрація відповідно окисленої і відновленої форми.
Катод – це електрод, на якому відбуваються відновні процеси. Анод – це електрод, на якому проходять окислювальні процеси. У гальванічних елементах катод має позитивний знак /+/; анод – негативний /-/. При електролізі катод негативний, анод – позитивний.
У гальванічних елементах електродний потенціал катода завжди більший, ніж анода.
Приклад 3. Визначити катод і анод для таких двох металів: а)цинк – срібло; б) цинк – магній. Привести схеми цих елементів.
Розв’язання.
а)
![]() В;
В;
![]() В. Отже цинковий електрод – анод, срібний
– катод.
В. Отже цинковий електрод – анод, срібний
– катод.
б)
В;
![]() В. Таким чином, цинковий електрод буде
катодом, а магнієвий – анодом.
В. Таким чином, цинковий електрод буде
катодом, а магнієвий – анодом.
Схеми таких елементів:
а) (-) Zn Zn2+ Ag+ Ag (+)
б) (-) MgMg2+Zn2+Zn (+)
Корозія – це процес руйнування металу внаслідок хімічної або електрохімічної взаємодії його з навколишнім середовищем: повітрям, водою, газами, розчинами кислот, лугів і солей.
Розрізняють хімічну й електрохімічну корозії. В основі хімічної корозії лежать звичайні хімічні реакції утворення оксидів і солей у середовищах, що не проводять електричного струму (гази при високих температурах, нафтопродукти, мастила, продукти термічної деструкції полімерів).
Електрохімічна корозія виникає в системах, що проводять електричний струм у тих випадках, коли самовільно утворюються гальванічні елементи. Прикладом електрохімічної корозії є корозія чавуну і сталі у вологому середовищі: залізо іржавіє тому, що утворюються гальванічні елементи, в яких катодами є ділянки карбіду заліза Fe3C:
(-) Fe H2O, O2 Fe3C (+)
На анодних ділянках окислюється залізо:
Fe – 2e-= Fe2+
На катодних - відбувається відновлення:
2H2O+O2+4e-=4OH-
Внаслідок вторинних процесів:
Fe2++2OH-=Fe(OH)2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
Fe(OH)3=H2O+FeO(OH)
утворюється іржа – суміш нерозчинних продуктів - гідроксидів Fe(OH)2, Fe(OH)3 і оксигідроксидів заліза FeO(OH).
Приклад 4. Написати схеми гальванічних елементів, що утворюються при контактній корозії заліза, покритого цинком, і заліза, покритого оловом.
Розв’язання. У першому випадку утворюється гальванічний елемент
(-) Zn H2O, O2 Fe (+)
в результаті роботи якого руйнується цинк на анодних ділянках:
Zn – 2e-= Zn2+
На катодних ділянках утворюються гідроксид-іони:
2H2O+O2+4e-=4OH-
Утворення гідроксиду цинку – вторинний процес
Zn2++2OH-=Zn(OH)2
У другому випадку виникає гальванічний елемент:
(-) Fe H2O, O2Sn (+)
в результаті роботи якого руйнується залізо на анодних ділянках:
Fe – 2e-= Fe2+
На катодних ділянках утворюються гідроксид-іони, а потім бура іржа
Fe2++2OH-=Fe(OH)2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
У першому випадку цинк окислюється і захищає залізо від корозії (анодний захист); у другому випадку олово захищає залізо, якщо на поверхні заліза утворюється суцільна без тріщин олов’яна плівка (катодний захист).
Присутність іонів
H+, Cl-, Br-,
I-, CN-,
![]() помітно збільшує швидкість корозії.
помітно збільшує швидкість корозії.
Температура досить сильно впливає на швидкість корозії. Як правило, з підвищенням температури швидкість корозії збільшується.
Присутність карбонатів, фосфатів і хроматів сповільнює корозію.
Велике значення у процесах корозії має склад і мікроструктура металу (чим метал однорідніший, тим корозійна стійкість вища).
Для зменшення корозії застосовують різні методи: 1) обробляють навколишнє середовище з метою усунення речовин, які викликають корозію; 2) замінюють повітря (О2) на гелій або інший інертний газ, чи просто створюють вакуум; 3) додають різні інгібітори корозії; 4)створюють захисні плівки (оксидні, масляні, металічні або лакові); 5)вводять у метал компоненти, що підвищують його корозійну стійкість; 6) застосовують протекторний або катодний захист.
