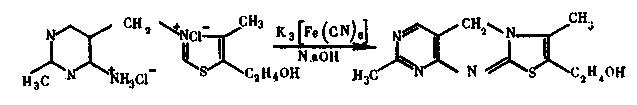- •Глава 2. Курс лекций
- •2.1. Оптические методы анализа
- •2.2. Рефрактометрический и поляриметрический методы анализа
- •2.3. Фотоколориметрические методы анализа
- •Люминесцентный анализ
- •Эмиссионный спектральный анализ
- •Методы атомной спектроскопии
- •1. Электрохимические и полярографические методы
- •2. Кондуктометрические методы исследований
- •Физико-химические методы разделения и концентрирования
Люминесцентный анализ
Теоретические основы
Данный анализ — один из физико-химических методов, основанный па измерении люминесценции определяемого вещества или продукта химической реакции, количество которого эквивалентно количеству определяемого вещества. Этот метод высокочувствительный и позволяет установить даже следовые количества некоторых металлов, микроэлементов и биологически активных веществ, пестицидов и продуктов их распада, содержащихся в растительной продукции.
Люминесценция — это способность некоторых веществ отдавать в виде излучения поглощенную энергию. Люминесценция, продолжающаяся только в период облучения вещества и угасающая при прекращении облучения называется флуоресценцией. Продолжающаяся некоторое время после прекращения люминесценция называется фосфоресценцией.
В дальнейшем речь пойдет только о флуоресценции, так как она представляет интерес для агрохимического анализа, особенно количественного.
Химический люминесцентный анализ обладает следующими преимуществами:
во время него, как правило, не происходит разложения исследуемого вещества;
для анализа можно использовать вещества в очень малых концентрациях, порядка 10-8 г/мл;
время анализа ограничивается всего .несколькими секундами, т. е. продолжительность количественного люминесцентного анализа такая же, как и колориметрического;
анализ легко автоматизировать.
Люминесценция
Люминесценция представляет собой испускание электромагнитного излучения молекулой или ионом, находящимся в возбужденном состоянии. По предложению (известного советского физика С. И. Вавилова (1891 — 1961) люминесценцией называют избыток над температурным излучением тела в том случае, если это .избыточное излучение обладает конечной длительностью примерно 10-10 с и более.
Если молекула или ион (переходит в возбужденное состояние в результате поглощения электромагнитного излучения, то последующую люминесценцию называют фотолюминесценцией (флуоресценцией или фосфоресценцией).
Упрощенно весь процесс можно описать в виде следующей схемы:
Молекула (основное состояние) |
+ Свет (высокая энергия) |
Поглощение
( |
Молекула (возбужденное состояние) |
Молекула (возбужденное состояние) |
излучение
|
Молекула (исконное состояние) |
+ Свет (более низкая энергия) |
Поглощение ультрафиолетового или видимого излучения вызывает переход электронов из основного состояния на один из колебательных подуровней первого возбужденного состояния. После возбуждения электроны быстро переходят на самый низкий подуровень первого возбужденного состояния, при этом возникает флуоресцентное излучение.
Основному и возбужденному состоянию соответствует множество колебательных и вращательных подуровней.
Часть энергии электромагнитного излучение необходимая для возбуждения электронов в молекуле, теряется при переходе с высшего на низший колебательный подуровень возбужденного состояния. Кроме того, электроны в молекуле обычно возвращаются на более высокий, чем колебательный, подуровень основного состояния. Поэтому флуоресцентное излучение характеризуется меньшей энергией, чем возбуждающее.
Закон Стокса гласит: максимум спектра флуоресцентного излучения находится в более длинноволновой области, чем максимум поглощенного при возбуждении света.
Спектры флуоресценции (рис. 23) обычно сходны с соответствующими спектрами поглощения (возбуждения). Если по оси абсцисс откладывать значения частоты излучения, то для многих сложных молекул спектры поглощения и флуоресценции станут зеркальными отражениями друг друга (правило В. Л. Левшина), причем спектр флуоресценции будет, сдвинут в область больших длин волн (или меньших частот). Расстояние между максимумами спектра поглощения и спектра флуоресценции называется стоксовым смещением. Чем больше стоксово смещение, тем легче отделить флуоресцентное излучение от возбуждающего света (с помощью светофильтров), тем надежнее определение вещества люминесцентным методом.
|
Рис. 23. Спектры поглощения (сплошная линия) и флуоресценции (пунктирная линия): а—-родамина; б — антрацена (справа соответствующие структурные формулы); А, —длина полны; v — частота |
Возбужденная молекула может перейти в основное состояние и без излучения, запасенная энергия при этом превращается в тепловую. Вероятность такого перехода возрастает с увеличением колебательной энергии молекул при повышении температуры (температурное тушение флуоресценции).
Превращение возбуждающего излучения в флуоресцентное излучение характеризуется квантовым выходом.
Квантовый выход — это отношение числа излученных квантов флуоресценции N ф к числу поглощенных квантов Nn :
Bкв = N ф/ Nn
Энергетический выход — это отношение энергии флуоресцентного излучения Еф к энергии поглощенного излучения Еn :
Bэн = Еф / Еn
Энергия кванта прямо пропорциональна частоте v или обратно пропорциональна длине волны λ:
-
ЕКВ = hv = h
c
λ
где h – постоянная Планка; с – скорость распространения электромагнитных волн.
Отсюда:
Вэн = |
Еф |
= |
hvфNф |
= |
vф |
; Вкв = |
λn |
Вкв |
Еn |
hvnNn |
vn |
λф |
По закону Стокса λn< λф, следовательно, Вэн< Вкт.
Согласно закону С. И. Вавилова фотолюминесценция может сохранять постоянный квантовый выход, если возбуждающая волна преобразуется в среднем в более длинную, чем она сама, при этом спектр флуоресценции λф также не изменяется. Следовательно, энергетический выход флуоресценции уменьшается при уменьшении длины волны возбуждающего излучения λn. Физический смысл этой закономерности заключается в том, что спектр флуоресценции определяется набором энергетических уровней молекулы.
С увеличением энергии квантов, применяемых для возбуждения молекулы, возрастает доля энергии, которая превращается не в излучение, а в тепловую энергию. При дальнейшем увеличении энергии возбуждающих квантов может произойти фотохимическое разложение молекул и возникнуть флуоресценция посторонних веществ. Чем больше выход флуоресценции для данного вещества, тем чувствительнее аналитическая реакция, основанная на использовании излучения этого вещества.
Для агрохимического анализа имеет значение в первую очередь связь интенсивности флуоресценции с концентрацией определяемого вещества. Интенсивность флуоресценции зависит, например, от интенсивности поглощенного излучения, которую можно рассчитать, используя закон светопоглощения. Этот закон связывает интенсивность прошедшего Р и падающего Р0 излучений с толщиной светопоглощающего слоя X и концентрацией определяемого вещества С:
Р = Р0е-εХС
где ε - величина, постоянная для данного вещества.
Для большинства веществ начало концентрированного тушения лежит в области 10-4….10-3 гмоль/л. Это соответствует такому расстоянию между молекулами, которое значительно меньше длины волны излучения, но превышает линейные размеры люминесцирующих молекул. В данных условиях явление хорошо объясняется теорией миграции энергии, согласно которой излучаемый свет вновь поглощается другими молекулами, которые непосредственно не соприкасаются с излучающей молекулой При более высоких концентрациях возникает возможность ассоциации молекул, при которой происходит перестройка энергетических уровней и возрастает вероятность переходов без излучения.
Важное преимущество флуориметрии перед спектрофотомерией — это высокая чувствительность первого метода. В спектрофотомерии измеряют соотношение Р0/Р, что существенно уменьшает надежность точного определения слабого поглощения на интенсивном фоне светового потока той же длины волны. Флуориметрия основана на измерении флуоресцентного излучения, которое зависит от возбуждающего излучения, то есть фон можно уменьшить почти до нуля, при этом интенсивность слабого сигнала измеряется значительно точнее. Так как измеряемая величина Рф прямо пропорциональна Р0, для получения более высоких значений интенсивности флуоресценции при постоянной концентрации вещества можно использовать более интенсивное возбуждающее излучение, чем в спектрофотомерии. Спектрофотометрический метод обычно позволяет определять концентрацию с точностью до 10-5 гмоль/л или до 1 мкг/мл вещества. Флуориметрический метод используют при определении концентраций до 10-8 гмоль/л или 0,001 мкг/мл.
Объекты флуориметрии.
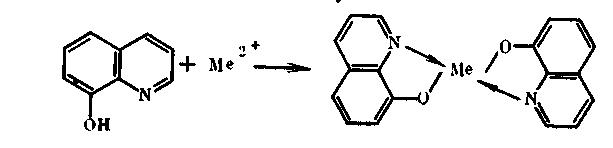
Лишь немногие неорганические ионы (урана, церия) флуоресцируют в растворе при комнатной температуре. Определение следов ионов некоторых металлов (алюминия, цинка и др.) основано на образовании внутрикомплексных, хелатных, соединений этих ионов с органическими реагентами (8-оксихинолин, морин, ацетилацетон). Продукт реакции обладает флуоресценцией. Например, раствор 8-оксихинолина в хлороформе (не флуоресцирует) при определенных условиях экстрагирует из водного слоя ионы металлов в виде соответствующих оксихинолинатов, которые флуоресцируют желто-зеленым светом при облучении ультрафиолетовыми лучами.
|
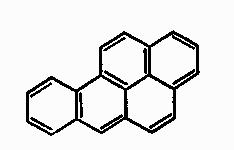
Органические соединения, имеющие циклические структуры с сопряженными двойными связями, в основном обладают флуоресценцией. Например, интенсивно флуоресцирует большинство полициклических ароматических соединений, которые относятся к основным загрязнителям воздуха. Так, одним из наиболее известных канцерогенных ароматических углеводородов является 3,4-бензпирен:
|
Предложен избирательный метод определения бензпирена в присутствии других ароматических углеводородов, основанный на использовании серной кислоты в качестве растворителя. В этой кислоте бензпирен находится в виде катиона, который дает интенсивную полосу поглощения при длине волны |
520 нм и полосу излучения при длине волны 545 нм. Некоторые другие ароматические углеводороды имеют при длине волны 520 нм менее интенсивные полосы поглощения, но ни одно из них (кроме бензпирена) не дает флуоресцентного излучения с длиной волны 545 нм.
Флуориметрические методы используют при анализе пищевых продуктов и лекарственных средств для определения малых количеств биологически активных веществ: и др. Например, витаминов A, В1, В2, С, никотиновой кислоты и ее производных, антибиотиков, гормонов количественное определение тиамина (витамина bi) основано на его окислении в тиохром — желтый пигмент, который имеет интенсивную синюю флуоресценцию при облучении ультрафиолетовыми лучами:
|
Точность флуориметрического метода резко снижается в присутствии многих посторонних веществ, поэтому необходимо применять посуду, реактивы и растворители очень высокой чистоты. Примеси веществ, обладающих собственной флуоресценцией, создают помехи. Тушение интенсивности флуоресценции посторонними веществами наблюдается под влиянием неорганических ионов, йода, брома, меди, железа и других, а также органических соединений — анилина, гидрохинона, гваякола.
Причина серьезных ошибок — присутствие растворенного кислорода, так как он гасит флуоресценцию многих ароматических соединений. Азот, аргон и некоторые другие газы не подавляют флуоресценцию. Насыщая раствор азотом, можно удалить растворенный кислород.
Небольшие колебания температуры люминесцирующей системы заметно не влияют на интенсивность люминесценции. При значительном увеличении температуры может наблюдаться температурное тушение. При глубоком охлаждении (замораживании) растворов вплоть до температур жидкого азота (—195°С) или водорода (—252°С) значительно увеличивается квантовый выход люминесценции, возникает люминесценция веществ, не излучающих при обычной температуре.
При выполнении флуориметрических измерений особенно важно учитывать устойчивость интенсивности люминесценции испытуемых растворов. Неустойчивостью отличается большинство люминесцирующих систем, используемых, в аналитической практике. Причины падения люминесцентной активности могут быть самыми разными, но основные — это кислородное тушение и фоторазложение.
Обязательное условие точности флуориметрических анализов— учет кислотности .растворов. Многие люминесцирующие вещества представляют собой слабые кислоты или основания, а поэтому форма их существования :в растворе (а значит, и люминесцентная активность) сильно зависит от рН. Обычно в методиках флуориметричеокого анализа веществ всегда указывают кислотность, чтобы избежать ошибок.
Устройство флуориметров
Любая флуориметрическая установка состоит, как правило, из следующих основных узлов: источника возбужденного излучения; первичного светофильтра или монохроматора для этого излучения; флуоресцирующего объекта; вторичного светофильтра или монохрома гора (для флуоресцентного излучения), приемника излучения.
Наиболее простым устройством характеризуются приборы, используемые при выполнении качественного анализа, визуальной флуориметрии и люминесцентного титрования (в них обязательны только три первых узла, а приемником излучения служит глаз). Более сложны по конструкции флуориметры, в которых для регистрации флуоресценции применяют фотоэлементы или фотоумножители. Значительно сложнее установки, предназначенные для изучения спектров и других количественных характеристик люминесцентного излучения. К данному типу относятся так называемые спектрофлуориметры.
В качестве источника, возбуждающего излучение, чаще применяют ртутные газоразрядные Лампы. Они характеризуются большим числом интенсивных линий в ультрафиолетовой области спектра. В зависимости от давления паров ртути, которое развивается при работе лампы, различают разряды низкого давления, высокого давления и сверхвысокого давления. Название газоразрядной лампы соответствует характеру разряда: лампы низкого давления (марки БУВ, ЭУВ, УФО и др.), высокого давления (марки ПРК-2, ПРК-4 и др.) и сверхвысокого давления (марки СВД, ДРШ и др.). Для возбуждения флуоресценции чаще всего используют лампы высокого давления. Процесс раз-горания ртутной лампы в зависимости от ее типа и от схемы включения продолжается от 3 до 15 мин. За это время интенсивность излучения достигает примерно 90% максимального значения и в дальнейшем возрастает очень медленно. При разгорании изменяется не только интенсивность, но и спектральный состав излучения, поэтому лампу следует включать за 15..20 мин до начала работы.
При работе с лампами высокого и сверхвысокого давления необходимо соблюдать некоторые меры предосторожности:
кварцевую колбу лампы перед включением следует очищать от загрязнений, которые во время работы лампы «вжигаются» в кварц и уменьшают прозрачность стенок лампы;
нельзя включать открытую лампу, так как сильное ультрафиолетовое (излучение может вызвать ожоги, особенно следует предохранять глаза;
лампу необходимо помещать в металлический кожух, чтобы избежать травм при возможном разрыве колбы во (время работы.
Ртутная лампа дает интенсивное излучение не только в ультрафиолетовой, но и в видимой области спектра, поэтому ее отделяют от люминесцирующего объекта специальным стеклом (первичный светофильтр), которое .иногда кажется непрозрачным, так как пропускает только ультрафиолетовое излучение. Первичный светофильтр подбирают так, чтобы максимум его пропускания соответствовал максимуму поглощения возбуждаемых молекул.
Интенсивность люминесценции регистрируют в направлении, перпендикулярном к направлению возбуждающего излучения. Кроме того, между люминесцирующим объектом и фотоэлементом устанавливают вторичный светофильтр, максимум пропускания которого должен соответствовать максимуму флуоресцентного излучения. Это позволяет отделить флуоресцентное излучение от возбуждающего и уменьшить фон практически до нуля.
Определение качества сельскохозяйственной продукции
Сортовой люминесцентный анализ осуществляют методом наблюдения собственной люминесценции объектов и люминесценции применяемых специально для этого флуоресцирующих красителей, которыми обрабатывают исследуемый объект. Название «сортовой анализ» предложено С. И. Вавиловым. Данный метод применяют для сортировки семян, пищевых .продуктов и ископаемых пород, обнаружения загрязнений, определения подделок и фальсификаций, выявления слабо видимых и невидимых записей и др.
Для визуального определения качества пищевых продуктов применяют люминоскоп ЛПК-1. Исследуемый объект в кювете из нелюминесцирующего материала (стекло, пластмасса) помещают в смотровую камеру прибора и закрывают заслонку. Сверху через специальное стекло на объект натравляют ультрафиолетовое излучение ртутной лампы. Люминесценцию объекта в камере (цвет и интенсивность) наблюдают в тубус на передней панели прибора.
Определение вида мяса. Куски мяса размером примерно 50 Х 50 Х 10 мм помещают в кювету. Одновременно с опытными образцами для сравнения люминесценции в качестве контроля кладут образец говядины. Вид мяса определяют по цвету люминесценции, учитывая следующие данные:
Вид продукции |
Цвет люминесценции |
Говядина |
Темно-красный или красновато-фиолетовый с бархатистым оттенком |
Баранина |
Темно-коричневый |
Свинина |
Розовый с коричневым оттенком |
Телятина |
Светло-коричневый |
Кости, сухожилия, фасции, хрящи |
Голубой |
Жир |
Светло-желтый |
Исследование фарша. Фарш располагают в кювете слоем толщиной около 5 мм и наблюдают цвет люминесценции его составных частей.
Исследование жиров и масел. Пробы жиров и масел размерами примерно 15 X 15 X 5 мм помещают в кювету. При исследовании кулинарных жиров и маргаринов рядом с опытными пробами в качестве контроля помещают пробу сливочного масла. При определении учитывают следующее:
Вид жира |
Цвет люминесценции |
Масло сливочное |
От бледно-желтого до ярко-желтого |
Маргарин «Сливочный», «Столовый» |
Беловато-розовый |
Сало растительное |
Интенсивно-голубой |
Исследование меда. Мед вносят в кювету слоем толщиной 5 мм. Рядом в качестве контроля помещают пробу натурального меда. Цвет люминесценции натурального - меда — ярко-желтый, фальсифицированного — беловатый, синеватый.
Определение доброкачественных овощей. Срезы овощей помещают в кювету и по интенсивности и цвету флуоресценции судят об их доброкачественности, обнаруживают ранние стадии заболеваний, обморожений. При этом руководствуются следующим:
Продукт |
Цвет люминесценции |
Картофель (поперечныйсрез): |
|
здоровый |
Желтоватый с различными оттенками у разных сортов |
подмороженный |
Беловатый |
пораженный: |
|
фитофторозом |
Голубоватый, интенсивный |
кольцевой гнилью |
Зеленоватый |
вирусным заболеванием
|
Различной окраски по сосудистой части клубней |
Лук (поперечный разрез): |
|
здоровый |
Бледно-синий |
пораженный серой гнилью |
Желтовато-белый |
Мандарины (поперечный разрез) |
|
здоровые |
Темно-оранжевый с матовой с фиолетовым оттенком |
пораженные голубой плесенью |
Темно-синие пятна с голубоватой и желтой каймой |

 возбуждение)
возбуждение)