
- •Дросселирование Методическое пособие
- •270109 «Теплогазоснабжение и вентиляция»
- •Предисловие
- •1. Общие сведения о дросселировании
- •2. Дросселирование идеального газа
- •3. Дросселирование пара
- •4. Дроссель-эффект Джоуля-Томсона
- •4.1. Молекулярно-кинетическая природа изменения температуры газа в процессе дросселирования
- •4.2. Общие формулы для дифференциального дроссель-эффекта
- •5. Дифференциальный дроссель-эффект в области двухфазных состояний вещества
- •6. Дифференциальный дроссель-эффект в критической точке
- •7. Дифференциальный дроссель-эффект в однофазных областях. Точки инверсии
- •8. Инверсионная кривая
- •9. Дросселирование рабочего тела, подчиняющегося уравнению Ван-дер-Ваальса
- •9.1. Основные сведения об уравнении Ван-дер-Ваальса
- •Критические параметры и zк для некоторых веществ
- •9.2. Качественный анализ процесса дросселирования с помощью уравнения Ван-дер-Ваальса
- •9.2.1. Построение инверсионной кривой
- •9.3. Расчетное определение термодинамических параметров в точке максимума инверсионной кривой
- •9.4. Расчетное определение максимальной и минимальной температуры инверсии
- •10. Сравнение дроссель-эффекта с температурным эффектом адиабатного расширения
- •Приложение п.1. Вывод формулы для дифференциального дроссель-эффекта (вариант автора пособия)
- •П.2. Вывод формулы для инверсионной кривой (вариант автора пособия)
- •П.3. Вывод приближенной формулы для дифференциального дроссель-эффекта (вариант автора пособия)
- •Список литературы
- •Содержание
9.2. Качественный анализ процесса дросселирования с помощью уравнения Ван-дер-Ваальса
9.2.1. Построение инверсионной кривой
Как указывалось в п.8, для получения инверсионной кривой необходимо знать конкретный вид уравнения состояния реального газа. Предположим, что реальный газ подчиняется уравнению Ван-дер-Ваальса.
Для вычисления дифференциального дроссель-эффекта по зависимости (4.4) необходимо знать частную производную для реального газа.
Запишем уравнение Ван-дер-Ваальса в виде:
 .
(9.10)
.
(9.10)
После дифференцирования этого уравнения при P = const получим:
![]() ,
,
откуда
 .
(9.11)
.
(9.11)
После подстановки уравнения (9.11) в уравнение (4.4) получим:
 .
(9.12)
.
(9.12)
Значения постоянных Ван-дер-Ваальса возьмем при определяющих параметрах TК и РК:
![]() ;
;
.
;
;
.
Как было указано в параграфе 9.1, при таком варианте сочетаний определяющих параметров, расчетная критическая изотерма ближе всего подходит к критической точке.
Для построения кривых зависимости дифференциального дроссель-эффекта от температуры при P = const, задаемся рядом значений V, затем по формуле (9.10) определяем Т, после чего эти V и Т подставляем в уравнение (9.12).
На рис. 9.2 представлены графически результаты определения αi для воздуха [1].
В расчетах принималось: TК = 133,46 °К, РК = 3,7 МПа, СР = 1015 Дж/(кг°К), R = 287 Дж/(кг°К). При этих исходных данных по формулам (9.8) определены значения двух остальных постоянных уравнения Ван-дер-Ваальса:
а = 164,78 (Н∙м4)/кг2; b = 1,28∙10-3 м3/кг.
На
рис. 9.2 точки пересечения кривых
![]() с осью температуры при P
= const
являются точками инверсии для данного
давления Р.
Из двух точек пересечения меньшему
значению температуры соответствует
нижняя точка инверсии, а большему
значению Т
– верхняя.
с осью температуры при P
= const
являются точками инверсии для данного
давления Р.
Из двух точек пересечения меньшему
значению температуры соответствует
нижняя точка инверсии, а большему
значению Т
– верхняя.
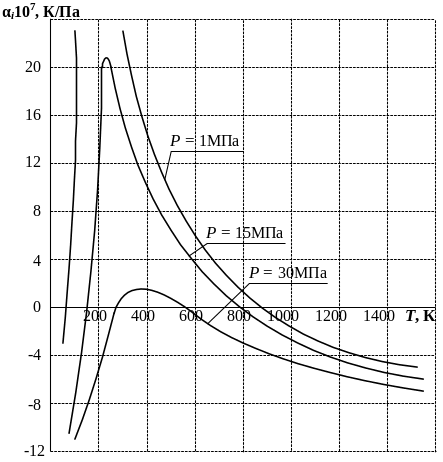
Рис. 9.2. Дифференциальный дроссель-эффект в зависимости от температуры перед дросселированием при различных начальных давлениях воздуха.
Точки инверсии, перенесенные в Р-Т координаты и соединенные плавной кривой, дают инверсионную кривую (рис. 9.3). Относительное превышение давления в точке максимума инверсионной кривой (Рim) над критическим давлением воздуха (РК = 3,7 МПа) по расчетам составляет Рi m/ РК = 9 (в опытах для воздуха Рi m/ РК = 10,8).

Рис. 9.3. Инверсионная кривая воздуха [1]
Аналогичным образом на рис. 9.4 построена расчетная инверсионная кривая для кислорода (ТК = 154,58 °К, РК = 5,043 МПа), из которой следует, что давление в точке максимума кривой инверсии (Рim) в девять раз превышает критическое давление РК (в опытах для кислорода Рi m/РК = 12).

Рис. 9.4. Инверсионная кривая кислорода в относительных параметрах [2]
При Р = 0,1 МПа большинство газов имеют довольно высокую температуру верхней точки инверсии (800 °К и более), за исключением водорода (193 °К) и гелия (37 °К).
9.3. Расчетное определение термодинамических параметров в точке максимума инверсионной кривой
Определим параметры точки максимума инверсионной кривой (Vi m, Ti m, Рi m) через параметры критической точки (VК, TК, РК). В соответствии с (8.4), условием максимума инверсионной кривой в общем случае является равенство:
.
По формуле (9.11)
 .
.
Подставим в это уравнение значение Р, выраженное в явном виде (9.9) из уравнения Ван-дер-Ваальса:
![]() .
.
Тогда

или
 .
(9.13)
.
(9.13)
Эта формула для анализа удобнее (9.11), поскольку не содержит Р. Продифференцировав (9.13) по Т при Р = const, получим:
 .
(9.14)
.
(9.14)
Эта формула обращается в нуль, если V = 3b (как показывалось выше, V >> b).
Но в соответствии с уравнением (9.7) равенство V = 3b выполняется только в критической точке. Так как (9.14) обращается в нуль при V = VК, то в точке максимума кривой инверсии объем газа равен VК:
Vi m = VК = 3b. (9.15)
Таким образом, в P-V координатах точки Рi m и РК находятся на одной прямой VК = const.
В точке максимума инверсионной кривой выполняется условие , которое в соответствии с (9.5) принимает вид:
![]()
или
![]()
или
![]() ,
,
откуда
![]() .
.
Но из (9.7)
![]() ,
,
следовательно
![]() .
(9.16)
.
(9.16)
Таким образом, в соответствии с уравнением Ван-дер-Ваальса, в точке максимума инверсионной кривой температура должна в три раза превышать критическую.
Уравнение (9.9) для точки максимума инверсионной кривой имеет вид:
![]() .
.
Так как Vi m = VК = 3b, а Ti m = 3TК, то
 ,
,
где
![]() .
.
Тогда
![]() .
.
Но из (9.8):
![]() .
.
Окончательно
![]() .
(9.17)
.
(9.17)
Таким образом, в соответствии с уравнением Ван-дер-Ваальса, в точке максимума инверсионной кривой давление должно в 9 раз превышать критическое.
Средние значения термодинамических параметров в точке максимума инверсионной кривой, полученные в экспериментах, составляют:
![]() ,
,
![]() ,
,
![]() .
.
Это среднее значение Ti m для различных веществ составляет (1,62 ÷ 2,06)ТК.
Как следует из рис. 9.3 и рис. 9.4 результаты расчетного определения Vim, Tim и Рim количественно удовлетворительно согласуются с их значениями, полученными в экспериментах.
Качественно инверсионные кривые, полученные с использованием уравнения Ван-дер-Ваальса, правильно описывают реальные процессы, что очень важно для выяснения сути процессов дросселирования и анализа их результатов.
