
- •Дросселирование Методическое пособие
- •270109 «Теплогазоснабжение и вентиляция»
- •Предисловие
- •1. Общие сведения о дросселировании
- •2. Дросселирование идеального газа
- •3. Дросселирование пара
- •4. Дроссель-эффект Джоуля-Томсона
- •4.1. Молекулярно-кинетическая природа изменения температуры газа в процессе дросселирования
- •4.2. Общие формулы для дифференциального дроссель-эффекта
- •5. Дифференциальный дроссель-эффект в области двухфазных состояний вещества
- •6. Дифференциальный дроссель-эффект в критической точке
- •7. Дифференциальный дроссель-эффект в однофазных областях. Точки инверсии
- •8. Инверсионная кривая
- •9. Дросселирование рабочего тела, подчиняющегося уравнению Ван-дер-Ваальса
- •9.1. Основные сведения об уравнении Ван-дер-Ваальса
- •Критические параметры и zк для некоторых веществ
- •9.2. Качественный анализ процесса дросселирования с помощью уравнения Ван-дер-Ваальса
- •9.2.1. Построение инверсионной кривой
- •9.3. Расчетное определение термодинамических параметров в точке максимума инверсионной кривой
- •9.4. Расчетное определение максимальной и минимальной температуры инверсии
- •10. Сравнение дроссель-эффекта с температурным эффектом адиабатного расширения
- •Приложение п.1. Вывод формулы для дифференциального дроссель-эффекта (вариант автора пособия)
- •П.2. Вывод формулы для инверсионной кривой (вариант автора пособия)
- •П.3. Вывод приближенной формулы для дифференциального дроссель-эффекта (вариант автора пособия)
- •Список литературы
- •Содержание
4.2. Общие формулы для дифференциального дроссель-эффекта
Как известно из общей термодинамики, энтальпия является функцией состояния, поэтому di является полным дифференциалом.
На этом основании, полагая i = i(T, P), получим по правилам математики
![]() .
.
Значения частных производных в этом уравнении определяются из первого начала термодинамики, записанного в энтальпийной форме:
![]() .
.
Так как
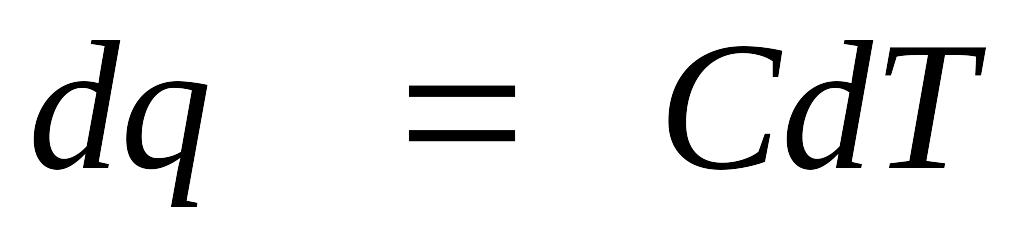 ,
то при P
= const,
,
то при P
= const,
 ,
dP
= 0 и
,
dP
= 0 и
 .
.Так как
 ,
то
,
то
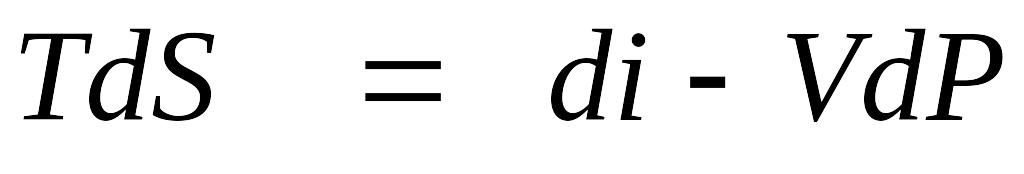 ,
откуда при Т
= const
,
откуда при Т
= const
![]() .
.
Эта частная производная относится ко второму типу дифференциальных соотношений термодинамики, поэтому
![]() .
.
Тогда
![]()
и
![]() .
.
Интегрирование этого уравнения приводит к следующему результату:
![]() .
.
Так как при дросселировании i2 = i1, то
![]()
или
 .
.
Интегрирование этого уравнения дает
 .
.
Из сравнения этого результата с формулой (4.3) для интегрального дроссель-эффекта следует:
 .
(4.4)
.
(4.4)
В этой формуле T, V, CP относятся к состоянию рабочего тела перед дросселем.
Ранее было показано, что при дросселировании идеального газа его температура не изменяется. Этот же результат можно получить, если в формулу для дифференциального дроссель-эффекта подставить значение частной производной для идеального газа.
Как известно из общей термодинамики для идеального газа
![]() .
.
Тогда
 .
.
Таким образом, у идеального газа αi = 0 при всех значениях давления и температуры.
У
реальных газов значения Ср,
V,
![]() зависят от величины давления и температуры,
поэтому αi
у этих газов так же зависит от Р
и Т.
зависят от величины давления и температуры,
поэтому αi
у этих газов так же зависит от Р
и Т.
Можно
получить еще одну формулу для αi,
если выразить частную производную
![]() как произведение двух частных производных:
как произведение двух частных производных:
![]() .
.
Задача при этом сводится к нахождению значений этих двух частных производных и выражения их через частные производные, не содержащие энтальпию i.
Подробный вывод второй формулы для αi в варианте автора данного пособия дается в приложении (П.1).
 . (4.5)
. (4.5)
Эта формула очень удобна для исследования процесса дросселирования в различных областях фазовых состояний вещества.
5. Дифференциальный дроссель-эффект в области двухфазных состояний вещества
В данном случае под двухфазным состоянием вещества понимается область его влажного насыщенного пара (ВНП).
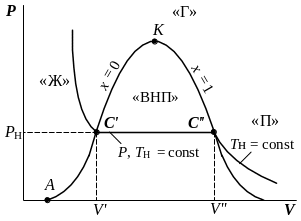
Рис. 5.1. Фазовая P-V диаграмма вещества
На рис. 5.1 это область внутри пограничной кривой – совокупности нижней (х = 0) и верхней (х = 1) пограничных кривых.
Как известно, в области двухфазных состояний вещества изотермические процессы (Т = const) являются одновременно и изобарными (отрезок С'С'').
Таким образом, в двухфазной области (ВНП)
![]() .
.
При этом формула (4.5) для αi принимает вид:
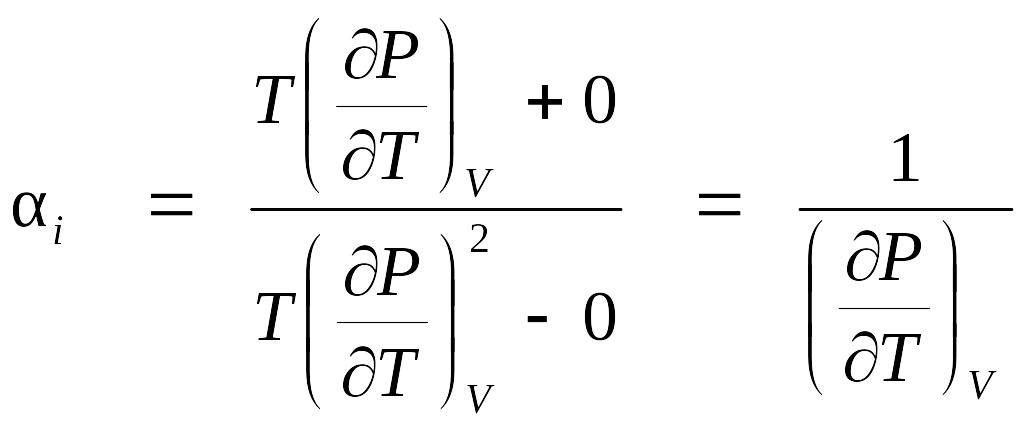 .
.
Но в области двухфазных состояний значение РН зависит только от ТН и не зависит от величины удельного объема (см. рис. 5.1), поэтому в области ВНП
![]() .
.
Окончательно
 .
(5.1)
.
(5.1)
Как следует из фазовой Р-Т диаграммы (рис 5.2), угловой коэффициент кривой АК (геометрическое место точек равновесного сосуществования жидкости «Ж» и пара «П»), всегда положителен
![]() ,
,
и поэтому
![]() .
(5.2)
.
(5.2)

Рис. 5.2. Фазовая Р-Т диаграмма
Таким образом, дросселирование в области ВНП всегда приводит к понижению температуры. Это хорошо иллюстрируется i-S диаграммой (рис. 5.3).

Рис. 5.3. Процесс дросселирования на i-S диаграмме.
Как известно, РН и ТН связаны уравнением Клайперона-Клаузиуса:
![]() .
.
Все точки на кривой АК (рис. 5.2) подчиняются этому уравнению. Поэтому
 .
(5.3)
.
(5.3)
Здесь V1' и V1'' – удельный объем (м3/кг) сухого насыщенного пара вещества и его кипящей (насыщенной) жидкости при начальном давлении дросселирования Р1 (Па);
![]() и
r1
– абсолютная температура насыщения
(°К) и скрытая теплота парообразования
(Дж/кг) при давлении Р1.
и
r1
– абсолютная температура насыщения
(°К) и скрытая теплота парообразования
(Дж/кг) при давлении Р1.
С
ростом давления отношение
![]() растет,
но разность
растет,
но разность![]() убывает быстрее, поэтому с ростом Р1
величина
убывает быстрее, поэтому с ростом Р1
величина
![]() убывает.
убывает.
