
- •Вопрос № 2
- •Вопрос № 3 Двойственная природа электрона. Корпускулярные и волновые свойства электрона. Уравнение де Бройля.
- •Вопрос № 4.
- •Вопрос № 5. Радиоактивный распад, его типы. Закон смещения. Радиоактивность. Виды радиоактивных лучей, их характеристика.
- •Принцип Паули (1925)
- •Емкость n/уровней
- •Способы образования ковалентной связи.
- •Свойства связи.
- •Причины образования химической связи. Основы виды химической связи (ковалентная, ионная, металлическая)
- •Вопрос № 9. Ионная связь и металлическая связь. Ионная связь, ее свойства
- •Свойства связи.
- •Вопрос № 10. Метод валентных связей. Валентность по донорно-акцепторному и обменному механизму.
- •Способы образования ковалентной связи.
- •Донорно-акцепторная связь – разновидность ковалентной связи.
- •Вопрос № 11. Метод молекулярных орбиталей. Его сравнение с методом валентных связей.
- •14. Термодинамические функции:
- •16. Энтропия образования химических соединений.
- •17. Энергия Гиббса образования вещества.
- •18. Обратимые химические реакции. Химическое равновесие. Условия термодинамического равновесия.
- •19. Скорость химических реакций в гомогенных и гетерогенных процессах. Факторы, изменяющие скорость химических реакций.
- •21. Влияние температуры на скорость реакций.
- •Топливный элемент. Принцип работы кислородно-водородного топливного элемента.
- •Основные методы защиты от коррозии. Протекторы, ингибиторы коррозии.
- •Методы получения полимеров. Привести примеры реакций полимеризации и поликонденсации.
Методы получения полимеров. Привести примеры реакций полимеризации и поликонденсации.
Макромолекулы обычно имеютцепеобразное строение. В этой цепи многократно повторяется определенная группа атомов, которая представляет собой элементарное звено цепи. Ур-ние р-ции полимеризации, напр поливинилхлорида, записывают след. образом

В левой части ур-ния указаны n отдельных молекул мономера, а в правой-одна молекула поливинилхлорида, состоящая из n элементарных звеньев: n – степень полимеризации.
Для того чтобы тот или иной мономер мог стать элементарным звеном в длинной макромолекулярной цепи, он должен перестроится таким образом, чтобы из мономерной молекулы получилась группа атомов, обладающая минимум двумя свободными валентностями, как это видно из приведенного примера. Это достигается в основном двумя путями:
путем полимеризации
в этом случае эти свободные валентности звена возникают за счет разрыва одной из двух валентных связей мономера: А=А→А-А-. Вещ-ва, мол-лы которых содержат кратные связи (двойную или тройную), назыв. непредельными. Следовательно, в качестве исходных вещ-в для реакции полимеризации могут служить только непредельные соединения.
путем поликонденсации
в этом случае необходимые две валентности структурного звена освобождаются за счет образования побочного низкомолекулярного продукта.
Напр: (Н-А)+(Б+ОН)→(-А-Б-)+
При этом звенья А и Б в молекулах исходных вещ-в могут иметь одинаковую или различную химическую природу.
Вопрос № 41
Реакция получения и применение наиболее распространенных полимеров:
полиэтилена, полипропилена, полистирола, поливинилхлорида, фторопласта, плексиглаза, фенолформальдегидной смолы, бутадиен-стирольного каучука.
Полиэтилен
Термопластичный высокополимер состав
(-CH -
CH
-)
-
CH
-) .
Молекулярная масса продукта, получаемого
при низком давлении 60 000-3000 000.
Синтезированный в любых условиях,
представляет собой смесь кристаллической
и аморфной модификации. Соотношение
этих 2-х фаз зависит от метода синтеза
полимера. Кристаллическая фаза
обусловливает плохую растворимость
полиэтилена, повышает механическую
прочность и твердость. Аморфная фаза
придает полимеру большую эластичность
и морозостойкость.
.
Молекулярная масса продукта, получаемого
при низком давлении 60 000-3000 000.
Синтезированный в любых условиях,
представляет собой смесь кристаллической
и аморфной модификации. Соотношение
этих 2-х фаз зависит от метода синтеза
полимера. Кристаллическая фаза
обусловливает плохую растворимость
полиэтилена, повышает механическую
прочность и твердость. Аморфная фаза
придает полимеру большую эластичность
и морозостойкость.
Полипропилен
Исходным вещ-вом в производстве
полипропилена служит пропилен CH
=
CH-CH .
Процесс полимеризации можно выразить
след. схематич. уравнением:
.
Процесс полимеризации можно выразить
след. схематич. уравнением:

CH CH
Средняя молекулярная масса используемых на практике образцов полипропилена составляет 150 000, плотность 0,85-0,92 г/см^3.
Полистирол
Полимер стирола:
CH
=
CH -стирол  -полистирол
-полистирол

Бесцветная, прозрачная масса, легко окрашивается в различные цвета.
Макромолекулы имеют преимущественно линейную структуру. Средняя молекулярная масса в технических образцах колеблется в пределах 3000-900 000.
Термопластичный, химически стойкий материал, растворимый в некоторых органических растворителях (бензол, дихлорэтан). Обладает хорошими электриозоляционными свойствами. Используется без прибавления пластификатора.
При нагревании до 300°С диполимеризуется (степень полимеризации n уменьшается), в результате чего из полимера может быть вновь получен мономер – стирол.
Полистирол находит широкое применение в электро- и радиотехнике. Из него изготовляют различные детали, аккумуляторные банки, трубы, емкости для минеральных кислот и т.д. Применяется также в виде сплавов с другими полимерами.
Поливинилхлорид (полихлорвинил)
Продукт полимеризации винилхлорида (хлористого винила)
CH = CH -винилхлорид -поливинилхлорид
Cl Cl
Термопластичен, стоек против действия кислот, щелочей, растворов солей. Отличается высокими электроизоляционными свойствами и большой механической прочностью.
На основе полихлорвинила получают два вида пластиков: винипластин и пластикат. Первый из них – твердый, жесткий материал. Из него готовят аккумуляторные банки, электролизные ванны. Второй – более мягок (изготовляется с приминением пластификаторов). Используется в качестве прочного и надежного электроизоляционного материала, а также для изготовления плащей, клеенки, сумок и др.
Фторопласт -4(тефлон)
Представляет собой полимер тетрафторэтилена
 -тетрафторэтилен
-тетрафторэтилен
 -фторопласт-4
-фторопласт-4
Смола в чистом виде – белое, в тонких смолах прозрачное в-во, напоминающее парафин, но со значительно более высокой плотностью. Средняя молярная масса фторопласта 142000-534000. Низкомолекулярный полимер представляет собой вязкую жидкость.
Тефлон по своей химич. стойкости превосходит все высокомолекулярные в-ва, как металлы – золото и платину. Вполне стоек против кислот, щелочей, солей, окислителей. Только фтор и щелочные металлы агрессивны в отношении тефлона. Устойчив к действию агентов, вызывающих коррозию. Один из лучших электроизоляционных материалов. Это обеспечивает ему широкое применение в электропромыш-ти. В химической промышленности используется для изготовления установок и аппаратуры, предназначенных для работы в агрессивных средах.
Плексиглаза
Гибкое органическое стекло, линейный термопластичный полимер. Мономер этой смолы имеет следующую хим. природу.
Если в этилене один атом Н на карбоксил –СООН, то получается непредельная акрилова кислота (1)
CH = CH -акриловая кислота
СООН
Плексиглас – твердая, прозрачная смола,
легко поддающаяся механической обработке
и склейке. Растворяется в дихлорэтане
(жидкость состава
 ,
называется также хлористым этиленом).
При 300°С разлагается (деполимеризуентся)
с выделением мономера (метилметилкрилата).
Смола за свою прозрачность поучила
название органического стекла. Широкое
применение для остекления самолетов,
автомобилей и др. Плексиглас мягче
силикатного стекла. Это его недостаток,
т.к. на поверхности изделий легко
образуются царапины.
,
называется также хлористым этиленом).
При 300°С разлагается (деполимеризуентся)
с выделением мономера (метилметилкрилата).
Смола за свою прозрачность поучила
название органического стекла. Широкое
применение для остекления самолетов,
автомобилей и др. Плексиглас мягче
силикатного стекла. Это его недостаток,
т.к. на поверхности изделий легко
образуются царапины.
Фенолформальдегидная смола
Смолы способные к сорбционному обмену иинов с р-ом электролита, назыв. ионообменными
Ионообменные смолы, применяемые на практике, обычно представляют собой твердый зернистый материал различного цвета, набухающий, но не растворимый в воде, спиоте и вообще в той жидкости, в кот-ой идет процесс обменной сорбции.
Ионообменные смлы по хар-ру действия подразделяются на катионы (обеспечивают обмен катионами между смолой и раствором) и аниониты (осуществляют анионный обмен).
Для сообщения смоле ионообразных св-в
к её макромолекулярному скелету
присоединяют определенные активные
группы. Такими группами для катионов
являются: - (ост. серной к-ты), карбонил –СООН,
гидроксильная группа –ОН. Все эти
радикалы имеют кислотный хар-р – они в
водных средах отщепляют
(ост. серной к-ты), карбонил –СООН,
гидроксильная группа –ОН. Все эти
радикалы имеют кислотный хар-р – они в
водных средах отщепляют
 -ионы.
-ионы.
Активные группы, характерные для
анионитов: - (первичная
аминогруппа), -NH-(вторичная
аминогруппа). В водной среде они образуют
радикалы типа -
(первичная
аминогруппа), -NH-(вторичная
аминогруппа). В водной среде они образуют
радикалы типа -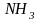 ОН,
ОН,
-
ОН-.
Эти группы в водных средах отщепляют
гидроксильные ионы OH ,
т.е. обладают щелочными св-ми.
,
т.е. обладают щелочными св-ми.
В качестве примера рассмотрим один из катионов-сульфофенольный.
Мономер этого катиона.
ОН
 Н- С=О -формальдегид
Н- С=О -формальдегид
Н- -Н -Феномерная
к-та Н
-Н -Феномерная
к-та Н
 -фенол,
-серная
кислота
-фенол,
-серная
кислота
Бутадиен-стирольный каучук
Получается сополимеризацией бутадиена
и стирола
 .
Отличается большой механической
прочностью и износостойкостью. Применяется
для изготовления покрышек автомобильных
шин, транспортных лент и др.
.
Отличается большой механической
прочностью и износостойкостью. Применяется
для изготовления покрышек автомобильных
шин, транспортных лент и др.
Вопрос № 41.
