- •Н а вопросы к экзаменационным билетам по предмету «Химия» для профессий «Оператор эвм», «Радиомеханик».
- •2001 – 2002 Учебный год
- •Вопрос №1
- •Периодический закон и периодическая система химических элементов
- •Д. И. Менделеева
- •Значение периодического закона
- •Простые и кратные связи
- •Вопрос №4 Классификация химических реакций Неорганическая химия
- •Вопрос №5 Обратимость химических реакций, химическое равновесие
- •Вопрос №6 Скорость химических реакций
- •Катализ и катализаторы
- •Вопрос №7 Реакции ионного обмена
- •Вопрос №8 Окислительно-восстановительные реакции (овр)
- •Вопрос №9 Оксиды
- •Вопрос №10 Кислоты
- •Классификация
- •Специфические свойства серной кислоты
- •Вопрос №11 Основания
- •Свойства Вопрос №12 Соли
- •Вопрос №13 Электролиз расплавов солей
- •Применение электролиза.
- •Вопрос №14 Металлы
- •Вопрос №15 Железо
- •Физические свойства
- •Применение и биологическая роль железа и его соединений
- •Вопрос №16 Электрохимический ряд металлов
- •Вопрос №17 Коррозия металлов
- •Способы борьбы с коррозией
- •Вопрос №18 Неметаллы
- •Характеристика неметалличности
- •Характеристика атомов-неметаллов 2-го периода
- •Вопрос №19 Сера (s)
- •Вопрос №20 Водородные соединения неметаллов
- •Вопрос №21 Теория химического строения органических веществ а. М. Бутлерова
- •Вопрос №22 Предельные углеводороды (Алканы)
- •Химические свойства
- •Вопрос №25 Диеновые углеводороды (Алкадиены)
- •Получение
- •Применение
- •Природный каучук
- •Физические свойства:
- •Химические свойства
- •Вопрос №29 Предельные одноатомные спирты
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №34 Глюкоза
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №35 Крахмал
- •Применение крахмала
- •Биологическая роль
- •Получение
- •Вопрос №36 Целлюлоза Строение молекулы
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №37 Анилин
- •Физические свойства
- •Важнейшие химические свойства анилина
- •Применение
- •Вопрос №38 Аминокислоты
- •Физические свойства
- •Химические вещества
- •Применение
- •Вопрос №39 Изомерия органических соединений
- •Вопрос №40 Белки
- •Структура белка
- •Физические свойства
- •Химические свойства
- •Функции белков в организме
- •Вопрос №41 (Вопросы №42 – 47) Общая характеристика высоко молекулярных веществ (вмв, полимеры)
- •Вопрос №50 Синтетический каучук
- •Вопрос №51 Металлы и сплавы
- •Вопрос №52 Физические свойства металлов
- •Способы борьбы с коррозией
- •Вопрос №53 Измерение разности потенциалов металлов
- •Вопрос №56 Алюминий
- •Вопрос №57 Медь и благородные металлы
- •Вопрос №58 Металлы побочных подгрупп
- •Вопрос №59 Полупроводники
- •Вопрос №60 Использование неорганических материалов в качестве проводников и диэлектриков
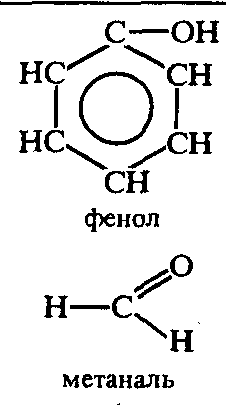
Структура белка
Первичная структура белка – это последовательность аминокислотных звеньев в линейной полипептидной цепи. (Полипептидную теорию строения белков предложил немецкий химик Э. Фишер в начале XX века).
Вторичная структура – это пространственная конфигурация белковой молекулы, напоминающая спираль, которая образуется в результате скручивания полипептидной цепи за счёт водородных связей между группами: CO и NH.
Третичная структура – это пространственная конфигурация, которую принимает закрученная в спираль полипептидная цепь.
Четвертичная структура – это полимерные образования из нескольких макромолекул белка.
Физические свойства
Свойства белков так же разнообразны, как и функции, которые они выполняют. Одни белки растворяются в воде, образуя, как правило, коллоидные растворы (например, белок яйца); другие растворяются в разбавленных растворах солей; третьи нерастворимы (например, белки покровных тканей).
Химические свойства
Денатурация – разрушение вторичной, третичной структуры белка.
Цветные реакции
Белок +HNO3 жёлтая окраска белка
Раствор белка +NaOH + CuSO4 красно-фиолетовая окраска
Раствор белка + (CH3COO)2Pb + NaOH чёрный осадок
Гидролиз
При гидролизе белков образуются аминокислоты.
Функции белков в организме
Пластическая |
Строительный материал клетки |
Например, коллаген, мембранные белки |
Транспортная |
Переносят различные вещества |
Например, гемоглобин (перенос O2 и CO2) |
Защитная |
Обезвреживают чужеродные вещества |
Например, глобулин сыворотки крови |
Энергетическая |
Снабжают организм энергией |
При расщеплении 1 г белка освобождается 17,6 кДж энергии |
Каталитическая |
Ускоряет протекание химических реакций в организме |
Все ферменты по своей химической природе являются белками. Например, рибонуклеза |
Сократительная |
Выполняет все виды движений, к которым способны клетки и организмы |
Например, миозин (белок мышц) |
Регуляторная |
Регулируют обменные процессы |
Гормоны, например, инсулин (обмен глюкозы) |
Существуют белки, выполняющие специфические функции, например рецепторные, – обеспечивают передачу импульсов между нервными клетками и другие.
Белки – необходимая составная часть пищи человека, отсутствие или недостаток их в пище может вызвать серьёзные заболевания.
Вопрос №41 (Вопросы №42 – 47) Общая характеристика высоко молекулярных веществ (вмв, полимеры)
ВМВ или полимерами называются вещества, имеющие большую молекулярную массу, состоящую из множества повторяющихся структурных звеньев. Существуют природные полимеры (крахмал, белки, целлюлоза, каучук) и синтетические полимеры (полиэтилен, фенопласты). Низко молекулярные вещества, из которых синтезируют полимеры, называются мономерами.
CH2=CH2 мономер полиэтилена
этилен
(-CH2-CH2-)n –макромолекула полимера
-CH2-CH2- – структурное звено – многократно повторяющаяся группа атомов
n – Степень полимеризации
Молекулярная масса полимера не постоянна и зависит от числа n. Макромолекулы полимеров могут иметь различную пространственную структуру:
Линейную (полиэтилен, полипропилен);
Разветвлённую (крахмал);
Пространственную (резина).
Физические свойства
Полимеры имеют высокую механическую прочность. Химически стойкие (с кислотами и щелочами не реагируют). Не имеют определённой tплавления, не растворяются в воде и в большинстве органических растворителей.
Синтез полимеров
Полимеры синтезируют двумя способами:
Реакцией полимеризации;
Реакцией поликонденсации.
Реакцией полимеризации называется процесс соединения молекул мономера в более крупные молекулы.
![]()
этилен
Реакцией поликонденсации называется процесс получения высоко молекулярных веществ, идущих с выделением побочного низкомолекулярного продукта.
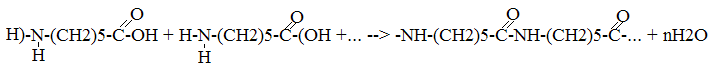
Вопрос №42
Пластмассы
Пластмассами называется вещества, полученные на основе полимеров, способные при нагревании размягчаться, принимать заданную форму и сохранять её после охлаждения.
В состав пластмасс кроме полимера (связующего вещества) могут входить наполнители, стабилизаторы, пластификаторы, красители, антистарители.
Пластмассы делятся на термопластичные и термореактивные.
К термопластичным пластмассам относятся полимеры линейной структуры способные при нагревании многократно размягчаться, изменять свою форму и сохранять её после охлаждения. К ним относятся полиэтилен, полипропилен, поливинилхлорид (ПВХ), полистирол.
Свойство тел изменять форму в нагретом состоянии и сохранять её после охлаждения называют термопластичностью.
К термореактивным пластмассам относятся полимеры, которые при нагревании становятся пластичными, размягчаются, сохраняют заданную форму при охлаждении и утрачивают пластичность, так как образуется пространственная структура полимера. Они не подвергаются вторичной переработке. К ним относят фенопласты. (С.29)
С.30 – 31
При повышенной температуре и давлении между разветвленными молекулами полимера происходит химическое взаимодействие и образуется полимер с пространственной структурой. Такой материал теряет термопластичность и становится более прочным.
Полимеры, которые при повышенной температуре не размягчаются и не плавятся в отличие от термопластичных полимеров, называются термореактивными.
Применение. Из фенолформальдегидного полимера (смолы), добавляя различные наполнители (древесная мука, хлопчатобумажная ткань, стеклянное волокно, различные красители и т.д.), получают фенолформальдегидные пластмассы, которые сокращенно называют фенопластами (табл. 3).
. ..
в недалеком будущем значительно возрастет
выпуск красивых пластмассовых легковых
автомобилей, моторных лодок, новых
легких образцов мебели, прочной обуви,
новых красивых тканей, не боящихся
дождя.
..
в недалеком будущем значительно возрастет
выпуск красивых пластмассовых легковых
автомобилей, моторных лодок, новых
легких образцов мебели, прочной обуви,
новых красивых тканей, не боящихся
дождя.
Таблица 3. Важнейшие фенопласты*
Характеристика фенопластов |
Виды фенопластов |
||||
Текстолит |
Волокнит |
Гетинакс |
Стеклопласт |
Карболит |
|
Исходные вещества и материалы.
|
Хлопчатобумажная ткань, пропитанная фенолформальдегидной смолой и спрессованная при повышенной температуре |
Очески хлопка, отходы тканей, пропитанные фенолформальдегидной смолой
|
Бумага, пропитанная фенолформальдегидной смолой и спрессованная
|
Стеклянна ткань и стеклянное волокно, пропитанные фенолформальдегидной смолой и спрессованные
|
Древесная мука, пропитанная фенолформальдегидной смолой и спрессованная
|
Свойства
|
Устойчив к нагрузкам. Легко поддается механической обработке |
Износоустойчив
|
Хороший электроизолятор
|
Механически и коррозионноустойчивый материал
|
Хороший электроизолятор. Устойчив против коррозии
|
Применение
|
Изготовляют шарикоподшипники и шестерни для машин, предусмотренных для больших нагрузок. В качестве мазки деталей можно использовать воду |
Изготовляют тормозные накладки для автомашин и мотоциклов, ступеньки для эскалаторов и т. д. |
Широко применяют в радио- и электротехнике в качестве хорошего электроизоляционного материала
|
Изготовляют детали больших размеров (автоцистерны, кузовы автомобилей и т. д.)
|
Изготовляют телефонные аппараты, электрические контактные платы
|
* Для производства текстолита, волокнита и других пластмасс применяются и другие полимеры.
Таблица 4. Общий обзор важнейших полимеров
Название |
Исходные вещества (мономеры) |
Формула полимера |
Способ получения |
Применение |
Полиэтилен |
СН2=СН2 этилен |
(—СН2—СН2—)n
|
Полимеризация |
Для производства деталей различных аппаратов, водопроводных, дренажных и других труб, различных пленок (в том числе для парников), предметов бытового назначения |
Полипропилен |
СН2=СН СН3 пропилен
|
(—СН2—СН—)n CH3 |
» |
По сравнению с полиэтиленом обладает большей прочностью. Используется для производства деталей различных аппаратов, пленок, канатов, труб, высокопрочных изоляционных материалов |
Поливинилхлорид
|
СН2=СН Cl винилхлорид
|
(—CН2—CH—)n Cl
|
» |
Для производства искусственной кожи, плащей, клеенки, труб, изоляционного материала для электрических проводов |
Полистирол |
|
» |
Для изготовления электроизоляционных материалов, кислотоупорных труб, разных бытовых изделий, а также пенопластов (легкие пористые материалы) |
|
Полиметилметакрилат |
|
» |
Для производства прозрачных пластмасс, в том числе органического стекла, превосходящего в десятки раз прочность обычного, силикатного. Органическое стекло применяют в самолетах и в различных аппаратах и приборах (в виде предохранительного стекла) |
|
Фенолформальдегидная смола |
|
|
Поликонденсация |
О применении фенолформальдегидной смолы см. таблицу 3 |
В таблице 4 дается только общий обзор о важнейших полимерах, применяемых для изготовления различных пластических материалов.