
- •Н а вопросы к экзаменационным билетам по предмету «Химия» для профессий «Оператор эвм», «Радиомеханик».
- •2001 – 2002 Учебный год
- •Вопрос №1
- •Периодический закон и периодическая система химических элементов
- •Д. И. Менделеева
- •Значение периодического закона
- •Простые и кратные связи
- •Вопрос №4 Классификация химических реакций Неорганическая химия
- •Вопрос №5 Обратимость химических реакций, химическое равновесие
- •Вопрос №6 Скорость химических реакций
- •Катализ и катализаторы
- •Вопрос №7 Реакции ионного обмена
- •Вопрос №8 Окислительно-восстановительные реакции (овр)
- •Вопрос №9 Оксиды
- •Вопрос №10 Кислоты
- •Классификация
- •Специфические свойства серной кислоты
- •Вопрос №11 Основания
- •Свойства Вопрос №12 Соли
- •Вопрос №13 Электролиз расплавов солей
- •Применение электролиза.
- •Вопрос №14 Металлы
- •Вопрос №15 Железо
- •Физические свойства
- •Применение и биологическая роль железа и его соединений
- •Вопрос №16 Электрохимический ряд металлов
- •Вопрос №17 Коррозия металлов
- •Способы борьбы с коррозией
- •Вопрос №18 Неметаллы
- •Характеристика неметалличности
- •Характеристика атомов-неметаллов 2-го периода
- •Вопрос №19 Сера (s)
- •Вопрос №20 Водородные соединения неметаллов
- •Вопрос №21 Теория химического строения органических веществ а. М. Бутлерова
- •Вопрос №22 Предельные углеводороды (Алканы)
- •Химические свойства
- •Вопрос №25 Диеновые углеводороды (Алкадиены)
- •Получение
- •Применение
- •Природный каучук
- •Физические свойства:
- •Химические свойства
- •Вопрос №29 Предельные одноатомные спирты
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №34 Глюкоза
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №35 Крахмал
- •Применение крахмала
- •Биологическая роль
- •Получение
- •Вопрос №36 Целлюлоза Строение молекулы
- •Физические свойства
- •Химические свойства
- •Применение
- •Вопрос №37 Анилин
- •Физические свойства
- •Важнейшие химические свойства анилина
- •Применение
- •Вопрос №38 Аминокислоты
- •Физические свойства
- •Химические вещества
- •Применение
- •Вопрос №39 Изомерия органических соединений
- •Вопрос №40 Белки
- •Структура белка
- •Физические свойства
- •Химические свойства
- •Функции белков в организме
- •Вопрос №41 (Вопросы №42 – 47) Общая характеристика высоко молекулярных веществ (вмв, полимеры)
- •Вопрос №50 Синтетический каучук
- •Вопрос №51 Металлы и сплавы
- •Вопрос №52 Физические свойства металлов
- •Способы борьбы с коррозией
- •Вопрос №53 Измерение разности потенциалов металлов
- •Вопрос №56 Алюминий
- •Вопрос №57 Медь и благородные металлы
- •Вопрос №58 Металлы побочных подгрупп
- •Вопрос №59 Полупроводники
- •Вопрос №60 Использование неорганических материалов в качестве проводников и диэлектриков
Вопрос №29 Предельные одноатомные спирты
Спиртами называются производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами.
Гидроксильная группа – ОН является функциональной группой спиртов.
Функциональными группами называются группы атомов, которые обуславливают характерные химические свойства данного класса веществ.
Общая формула одноатомных спиртов: СnH2n + 1OH
Гомологический ряд
CH3 – OH метанол, метиловый спирт
C2H5 – OH этанол
C3H7 – OH пропанол
C4H9 – OH бутанол
C5H11 – OH пентанол
Изомерия
C4H9OH
CH3 – CH2 – CH2 – CH2 – OH 1-бутанол
 2-метил
1-пропанол
2-метил
1-пропанол
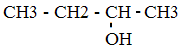 2-бутанол
2-бутанол
Физические свойства
Одноатомные предельные первичные спирты с короткой цепью углеродных атомов – жидкости, а высшие (начиная с С12Н25ОН) – твёрдые вещества. Метанол, этанол, пропанол – бесцветные жидкости, растворимы в воде, имеют алкогольный запах. Метанол – сильный яд.
Химические свойства
Растворы спиртов имеют нейтральную реакцию на индикаторы;
Взаимодействие с активными металлами
2C2H5OH + Na 2C2H5ONa + H2
этанол этилат натрия
Взаимодействие с галогеноводородными веществами
C2H5OH + HCl C2H5Cl + H2O
хлорэтан
Дегидратация
C2H5OH C2H4 + H2O (при t и в присутствии H2SO4)
Взаимодействие с кислородом
C2H5OH + 3O2 2CO2 + 3H2O
Окисление

этанол уксусный альдегид
Взаимодействие с карбоновыми кислотами

уксусная кислота | этиловый спирт | укс. этиловый эфир
Получение спиртов
Этанол получают из:
Этилена
C2H4 + HOH C2H5OH (при катализаторе и t)
Брожением глюкозы
C6H12O6 2C2H5OH + 2CO2
Применение этанола:
Получение уксусной кислоты, лекарства, фруктовых вод, духов и одеколонов, бутадиенового и бутадиен-стирольного каучука, горючего для двигателей, красителей, лаков и политур, растворителей, бездымного пороха.
Вопрос №30
Фенол
К фенолам относятся производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным ядром.



фенол 1,2-бензолдиол 1,2,4-бензолтриол
Строение молекулы фенола
Фенол является слабой кислотой.

Физические свойства
Фенол – бесцветное, кристаллическое вещество с характерным запахом. Его t плавления = 40,9 С. В холодной воде он мало растворим, но уже при 70 С растворяется в любых отношениях. Фенол ядовит!
Химические свойства
Реакции, протекающие по гидроксильной группе
Взаимодействие с активными металлами
2C6H5OH + 2Na 2C6H5ONa + H2
фенолят натрия
Взаимодействие со щелочью
C6H5OH + NaOH C6H5ONa + H2O
Реакции, протекающие по бензольному ядру. Реакции, протекающие по положениям 2, 4, 6.
Бромирование

2,4,6-трибромфенол
Нитрование

2,4,6-тринитрофенол
или пикриновая кислота
Получение
C6H6 C6H5Cl C6H5OH
C6H6 + Cl2 C6H5Cl + HCl
C6H5Cl + NaOH NaCl + C6H5OH
Применение
Получение лекарств, веществ для дезинфекции, фотореактивов, красителей, капрона, взрывчатых веществ, текстолита, гетинакса, карболита, стеклотекстолита, волокнита.
Вопрос №31
Альдегиды
Альдегиды – органические вещества,
содержащую функциональную группу
 (альдегидную группу).
(альдегидную группу).
Альдегидная группа
Карбонильная группа
![]()
Гомологический ряд
Н метаноль (муравьиный, формальдегид)
СН3 этаноль (ацетальальдегид, уксусный альдегид)
С2Н5 пропаноль
С3Н7 бутаноль
Физические свойства
Формальдегид – газ, его 40% раствор называется формалином. Остальные жидкие и твёрдые.
Химические свойства
Реакция «серебряного зеркала», качественная реакция
CH3
+ Ag2O
CH3 + 2Ag
+ 2Ag
укс. альдегид укс. кислота
С гидроксидом меди
CH3 + 2Cu(OH)2 CH3 + 2CuOH (жёлт. цвет) (разлагается на Cu2O (кр. цвет) и H2O) (реакция при t)
Восстановление водородом
CH3 + H2 CH3 – CH2 – OH (при катализаторе и t)
этанол
Получение
Окисление спиртов
R – CH2 – O + H + O R + H2O
Окисление метана
СH4 + O2 H + H2O (при t = 500 С и катализаторе)
Окисление метанола
2CH3OH + O2 2H + 2H2O (при Cu или Ag)
Гидратация ацетилена
H – С
![]() C – H + H2O
CH
(в присутствии H2SO4)
C – H + H2O
CH
(в присутствии H2SO4)
--------------------------------
Применение:
Наибольшее применение имеют метаноль и этаноль, для получения фенолформальдегидной смолы.
Вопрос №32
Карбоновые кислоты
Карбоновыми кислотами называются органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединённых с углеводородным радикалом или водородным атомом.
– карбоксильная группа
– COOH – карбоксильная группа
Карбоновые кислоты |
||
Одноосновные (имеется одна карбоксильная группа) |
двухосновные |
многоосновные |
Карбоновые кислоты |
||
Предельные |
Непредельные |
Ароматические |
