
- •Введение
- •Системный анализ Основные понятия и определения системного анализа
- •Внешние связи системы
- •Классификация систем по их свойствам
- •Моделирование технологических процессов и объектов
- •Структурный подход для построения математических моделей
- •Использование структурного подхода для составления моделей на молекулярном уровне
- •Описание стехиометрии системы химических реакций
- •Метод направленных графов
- •Матричный метод
- •Моделирование равновесия в системах химических реакций
- •Моделирование кинетики химических реакций
- •Скорость сложной химической реакции
- •Интегрирование уравнений кинетики
- •Численные методы интегрирования
- •Химические реакции в потоке вещества
- •Моделирование явлений тепло- и массопереноса
- •Массоперенос
- •Моделирование тепловых явлений
- •Тепловая работа аппарата с частичным теплообменом
- •Математические методы оптимизации технологических систем
- •Методы построения обобщённых критериев
- •Классификация оптимизационных задач
- •Аналитические методы решения оптимизационных задач
- •Поисковые (численные) методы решения однофакторных оптимизационных задач
- •Экспериментальные методы оптимизации
- •Методы линейного программирования
Скорость сложной химической реакции
Моделирование кинетики системы сложных химических реакций рассмотрим на следующем примере. Пусть имеется технологический процесс, суть которого отображается следующими химическими реакциями:
k![]() 1;
1 по В
1;
1 по В
A
 + 2B C
+ 2B C
k2; 0,7 по С
k3; 1 по А; 0,35 по Н
A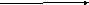 2D
2D
k4; 1 по С; 1 по D
C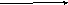
 + D 3Е
+ D 3Е
k5; 2 по Е;
r![]() A
= –k1CB
+ k2CC0.7
– k3CACH0.35
A
= –k1CB
+ k2CC0.7
– k3CACH0.35
rB = –2k1CB + 2k2CC0.7
rC = k1CB – k2CC0.7 – k4CCCD + k5CE2
rD = k3CACH0.35– k4CCCD + k5CE2
rE = k4CCCD – 3k5CE2
rH = 0
Кинетические константы (порядки по веществам и значения констант скорости для стадий) определены экспериментально. На схеме процесса над стрелками, соответствующими стадиям, показаны величины порядков по веществам. Не указанные порядки нулевые.
В процессе принимают участие 6 веществ: А и В являются исходными, С и D – промежуточными, Е – конечный продукт, Н – катализатор одной из стадий. Три химические реакции имеют пять стадий, три из которых являются прямыми, две – обратными.
Все реакции осуществляются гомогенно и проходят в замкнутой по веществу системе, что дает основания использовать для характеристики скорости выражения:
![]() .
.
На основании изложенного выше запишем выражения для скоростей по каждому веществу-участнику. Всего получим 6 выражений по числу веществ. Для каждого из веществ скорость расходования или образования есть алгебраическая сумма скоростей всех стадий с участием данного вещества. Так, веществ А участвует в трех стадиях, в первой в качестве исходного вещества, во второй- как продукт, в третьей вновь как исходное вещество. Слагаемые скорости для первой и третьей стадий будут отрицательны, для второй стадии скорость имеет положительный знак. Значения скорости для каждой стадии по закону действующих масс являются произведением константы скорости соответствующей стадии и концентраций веществ в степенях, равных порядкам по веществам. С учетом этого выражения для скоростей по веществам будут следующими:
![]()
![]() =
–k1CB
+ k2CC0.7
– k3CACH0.35
=
–k1CB
+ k2CC0.7
– k3CACH0.35
![]() =
–2k1CB
+ 2k2CC0.7
=
–2k1CB
+ 2k2CC0.7
![]() =
k1CB
– k2CC0.7
– k4CCCD
+ k5CE2
=
k1CB
– k2CC0.7
– k4CCCD
+ k5CE2
![]() =
k3CACH0.35–
k4CCCD
+ k5CE2
=
k3CACH0.35–
k4CCCD
+ k5CE2
![]() =
3k4CCCD
– 3k5CE2
=
3k4CCCD
– 3k5CE2
![]() = 0.
= 0.
Последняя скорость по веществу Н, катализатору третьей стадии, равна нулю. Масса катализатора не изменяется по ходу реакции.
В левой части всех уравнений присутствует производная концентрации вещества по времени, следовательно, уравнения кинетики являются дифференциальными. Концентрации в правой части уравнений в произвольный момент времени должны одновременно удовлетворять всем уравнениям, а это означает, что совокупность уравнений кинетики в математическом смысле есть система уравнений.
Модель химической кинетики является системой дифференциальных уравнений, решением которой является набор функций Ci = fi(t):
![]()
СА=f1(t)
СB=f2(t)
СC=f3(t)
СD=f4(t)
СE=f5(t)
СH=f6(t).
Для того, чтобы установить конкретный вид функций, необходимо решить систему дифференциальных уравнений, т.е. проинтегрировать систему уравнений кинетики. Интегрирование уравнений кинетики рассмотрим ниже на более простом примере, а после этого вновь вернемся к задаче, рассмотренной выше.
