
- •Введение
- •Системный анализ Основные понятия и определения системного анализа
- •Внешние связи системы
- •Классификация систем по их свойствам
- •Моделирование технологических процессов и объектов
- •Структурный подход для построения математических моделей
- •Использование структурного подхода для составления моделей на молекулярном уровне
- •Описание стехиометрии системы химических реакций
- •Метод направленных графов
- •Матричный метод
- •Моделирование равновесия в системах химических реакций
- •Моделирование кинетики химических реакций
- •Скорость сложной химической реакции
- •Интегрирование уравнений кинетики
- •Численные методы интегрирования
- •Химические реакции в потоке вещества
- •Моделирование явлений тепло- и массопереноса
- •Массоперенос
- •Моделирование тепловых явлений
- •Тепловая работа аппарата с частичным теплообменом
- •Математические методы оптимизации технологических систем
- •Методы построения обобщённых критериев
- •Классификация оптимизационных задач
- •Аналитические методы решения оптимизационных задач
- •Поисковые (численные) методы решения однофакторных оптимизационных задач
- •Экспериментальные методы оптимизации
- •Методы линейного программирования
Моделирование явлений тепло- и массопереноса
Для технологических процессов более характерным являются гетерогенные химические реакции. В таких реакциях участвующие вещества находятся в разных фазах, собственно химическая реакция осуществляется на поверхности раздела фаз. Доставка реагентов к поверхности реагирования и отвод продуктов реакции в соответствующие фазы осуществляется в результате массопереноса.
Массоперенос
Рассмотрим взаимодействие сульфида железа, одного из компонентов медного штейна, с дутьем и флюсом в условиях конвертирования медного штейна. В первом периоде конвертирования медного штейна эта реакция является основной:
FeS(ж1) + О2(г) + SiO2(тв) → 2FeO(тв) + SiO2(ж2) + SO2(г).
О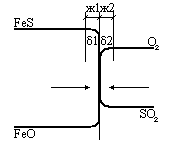 бозначим
концентрацию вещества Ся
– концентрация в ядре фазы вдали от
межфазной границы;
бозначим
концентрацию вещества Ся
– концентрация в ядре фазы вдали от
межфазной границы;
У поверхности раздела фаз концентрация этого вещества иная, обозначим ее Сп – поверхностная концентрация.
Перенос вещества
из объема фазы к поверхности реагирования
осуществляется в соответствии с законом
Фика:
![]() ,
,
где
D – коэффициент диффузии;
δ – толщина диффузионного слоя;
(Ся-Сп) – движущая сила процесса, разность концентраций.
При заданных условиях (например, температуре), известном характере химической реакции, известных размерах частиц диффундирующих веществ D=const, определяется характером диффундирующих частиц и среды.
δ – зависит от гидродинамических особенностей процесса;
β – константа скорости диффузии;
rg – диффузионный поток – число молей вещества, доставляемых диффузией в зону реакции и отнесённое к единице поверхности.
![]()
![]() ,
k
– константа, Сп
– поверхностная концентрация.
,
k
– константа, Сп
– поверхностная концентрация.
Справедливо для реакции 1-го порядка:
k – кинетическая константа скорости (истинная).
![]()
kCп заменим на k'Cя; известная концентрация в объёме Ся.
![]()
![]()
![]()
![]()
Величина, обратная экспериментальной константе скорости, является суммой обратных величин истинной константы и константы диффузии.
1.
![]() – наблюдается быстрая диффузия при
относительно медленной химической
реакции. Скорость гетерогенной реакции
определяется скоростью самой медленной
стадии.
– наблюдается быстрая диффузия при
относительно медленной химической
реакции. Скорость гетерогенной реакции
определяется скоростью самой медленной
стадии.
![]()
![]()
Поверхностная концентрация выравнивается с концентрацией в объёме фазы. Таким образом, диффузия доставляет вещество в зону реакции с высокой скоростью.
2.
![]() – химическая реакция быстрая при
медленной диффузионной стадии.
Лимитирующая стадия – диффузионная,
при этом
– химическая реакция быстрая при
медленной диффузионной стадии.
Лимитирующая стадия – диффузионная,
при этом
![]() ,
,
![]() .
.
3.
![]()
В реальных задачах моделирования определение константы диффузии и кинетической константы скорости представляет собой сложную задачу. Кинетическая константа скорости определяется экспериментально, для расчёта констант диффузии используются критериальные уравнения.
Моделирование тепловых явлений
Технологические процессы представляют собой совокупность химических реакций, сопровождающихся тепловыми эффектами. Технологические процессы происходят при высоких температурах, что требует, при составлении модели, учитывать процессы тепловыделения и теплопоглощения, а так же обмена с внутренней средой.
Технологические аппараты, как объекты моделирования могут быть отнесены к одному из трёх типов:
-
изотермические;
-
адиабатические;
-
с частичным теплообменом.
По ходу технологического процесса за счёт происходящих химических реакций либо образуется некоторое количество избыточного тепла, либо поглощается некоторое количество тепла извне. Количество выделившегося или поглощённого тепла в единицу времени зависит от скорости химической реакции.
Технологические аппараты в большинстве случаев обмениваются теплом с внешней средой, таким образом, избыточное тепло путём теплообмена отдаётся внешней среде.
Тип аппарата определяется тем, как соотносятся между собой тепловые эффекты, связанные с химической реакцией, идущей внутри аппарата и возможности теплообмена с внешней средой.
В изотермическом аппарате в единицу времени количество выделившегося и поглощённого тепла невелико:
-
скорость химической реакции невелика;
-
количество тепла, отведённое во внешнюю среду в единицу времени много больше, чем тепловой эффект внутри аппарата.
Возможности теплообмена значительно больше теплового эффекта внутри аппарата; в результате температура в аппарате приблизительно равна температуре внешней среды и остаётся постоянной.
В адиабатическом аппарате возможности внешнего теплообмена значительно уступают тепловому эффекту внутри аппарата. Такой аппарат подобен термосу- выделяющееся в ходе химической реакции тепло практически полностью расходуется на нагрев содержимого внутри аппарата, во внешнюю среду потери незначительны.
Величина теплового эффекта внутри аппарата с частичным теплообменом сопоставима с возможностями теплообмена, если в аппарате идет экзотермический процесс; часть тепла успевает рассеяться во внешнюю среду, часть расходуется на разогрев содержимого реактора, таким образом, устанавливается новая температура внутри аппарата, соответствующая тепловому балансу.
