
- •Раздел I введение в физиологию
- •Глава 1
- •1.1. Профилизация преподавания физиологии
- •1.2. Периоды развития организма человека
- •1.3. Основные физиологические понятия
- •1.4. Надежность физиологических систем
- •1.5. Характеристика процессов старения
- •1.6. Биологический возраст
- •Глава 2
- •2.1. Функции клетки
- •2.2. Функции клеточных органелл
- •2.5. Механизмы транспорта веществ через клеточную мембрану
- •Глава 3
- •3.1. Нервный механизм регуляции
- •3.2. Характеристика гормональной регуляции
- •3.3. Регуляция с помощью метаболитов и тканевых гормонов. Миогенный механизм регуляции
- •3.4. Единство и особенности регуляторных механизмов. Функции гематоэнцефалического барьера
- •3.5. Системный принцип регуляции
- •3.6. Типы регуляции функций организма и их надежность
- •4.3. Потенциал действия (пд)
- •4.5. Изменения возбудимости клетки во время ее возбуждения. Лабильность
- •4.7. Действие постоянного тока на ткань
- •Глава 5
- •5.1. Общая физиология сенсорных рецепторов
- •1. Двустороннее проведение возбуждения.
- •Глава 6
- •6.2. Гладкие мышцы
- •6.4. Изменения мышечной ткани в процессе старения
- •7Л. Функции центральной нервной системы
- •2. Регуляция работы внутренних органов
- •1. Двустороннее проведение возбуждения.
- •Глава 6
- •6.2. Гладкие мышцы
- •6.4. Изменения мышечной ткани в процессе старения
- •V Глава 7 общая физиология центральной нервной системы
- •7Л. Функции центральной нервной системы
- •2. Регуляция работы внутренних органов
- •7.4. Медиаторы и рецепторы цнс
- •7.6. Особенности распространения возбуждения в цнс
- •3. Иррадиация (дивергенция) возбуждения в
- •7.7. Свойства нервных центров
- •7.10. Интегрирующая роль нервной системы
- •Глава 8
- •8.1. Спинной мозг
- •8.2. Ствол головного мозга
1. Двустороннее проведение возбуждения.
Прямые доказательства этой закономерности были получены во второй половине XIX в. А.И.Бабухиным и Э.Дюбуа-Реймоном. Если стимул действует на средний участок изолированного нерва (Дюбуа-Реймон), то распространение возбуждения регистрируется как в проксимальном, так и в дистальном участках нерва. В опытах на электрическом органе у рыб, иннервируемом разветвлениями аксона одного нейрона, было показано (А.И.Бабу-хин), что при раздражении перерезанной веточки аксона возбуждение распространяется в необычном центростремительном направлении, передается на другие разветвления аксона, по которым идет в центробежном направлении (так называемый аксон-рефлекс). В условиях организма двустороннее проведение показано в аксонном холмике: возникший в этом месте ПД распространяется не только в аксон, но и в тело нейрона.
-
Изолированное проведение возбуждения. В обычных условиях деятельности нервного ствола (возбуждение только части нервных волокон, асинхронное распространение в них ПД) проведение возбуждения в составля ющих его волокнах происходит практически изолированно. Это обусловлено тем, что петли тока в межклеточной жидкости ствола, имеющей низкое сопротивление, почти #е проникают в невозбужденные волокна нерва из-за большого сопротивления их оболочек. Изолированное проведение импульсов по нервным волокнам обеспечивает точное аф ферентное и эфферентное влияния функцио нально разнородных волокон нерва. Однако при одновременном раздражении значитель ного количества волокон в межклеточной жидкости ствола возникает достаточно силь ный внешний ток, способный возбудить не активные (прежде всего высоковозбудимые) волокна и таким образом увеличить количе ство функционирующих нервных волокон в нерве, его эфферентное или афферентное влияние.
-
Большая скорость проведения возбужде ния. Скорость проведения ПД в различных типах волокон нерва равна 0,5—120 м/с (см. табл. 5.2). Она значительно выше в миелино-
вых волокнах в связи с сальтаторным типом проведения ПД (см. раздел 5.2.3), а среди ми- ■ елиновых волокон прямо пропорциональна диаметру волокна. Скорость проведения возбуждения в миелиновых нервных волокнах значительно выше, чем в других удлиненных возбудимых структурах, — в гладких миоци-тах (0,02—0,10 м/с), рабочих кардиомиоцитах (около 1 м/с), и только в миоцитах проводя-шей системы сердца и скелетных миоцитах скорость проведения ПД (2—5 м/с) достигает величин распространения ПД в низкоскоростных нервных волокнах (тип С и В). Передача возбуждения по нервным волокнам является наиболее скоростным из известных способов передачи информации на значительные расстояния в организме. Для сравнения отметим, что скорость передачи гуморальных влияний ограничена скоростью кровотока, которая равна от 0,5 мм/с в капиллярах до 0,25 м/с в аорте (средняя скорость).
-
Малая утомляемость нервного волокна. При нормальном кровоснабжении (доставке кислорода и питательных веществ) проводя щий возбуждение нерв практически неутом ляем. «Изумительно долгая неутомляемость нерва» впервые была показана Н.Е.Введен ским (1883): в его опытах нерв сохранял спо собность к проведению возбуждения в тече ние 6—8 ч непрерывного раздражения не сильными токами в условиях наличия кисло рода в окружающей среде и поддержания влажного состояния нерва. Это обусловлено тем, что при проведении ПД по нервным во локнам используется всего лишь одна милли онная часть запасов трансмембранных ион ных градиентов и, следовательно, нужны не большие количества АТФ для восстановле ния (например, посредством Na/K-насоса) ионных градиентов. Об энергетической эко номности проведения возбуждения свиде тельствует и низкая величина теплопро дукции в работающем нерве, отражающая степень окислительного фосфорилирования в митохондриях. Ее величина в нерве (0,06 кал/г ткани в течение 1 ч) примерно в 16 раз меньше, чем на соответствующую еди ницу массы в целом организме в условиях ос новного обмена, и в миллион раз меньше, чем в работающей мышце.
-
Возможность функционального блока проведения возбуждения при морфологической целостности волокон. Н.Е.Введенский (1901) показал, что при действии различных факто ров на нерв в нем сначала возникает транс формация ритма проводимого возбуждения (блокируется проведение высокочастотных потенциалов действия, и проводятся только
72
низкочастотные ПД), а в дальнейшем может возникать полный блок проведения нервных импульсов —- участок парабиоза. В этом участке возникает длительная деполяризация мембраны волокон, которая в результате закрытия инактивационных h-ворот в натриевых каналах сначала затрудняет генерацию ПД (уменьшается его амплитуда, увеличивается длительность, затягивается фаза абсолютной рефрактерности), а в дальнейшем, если инактивация натриевых каналов превысит 50 %, приводит к полной невозбудимости этого участка нервного волокна. Для возникновения блока в проведении возбуждения протяженность парабиотического участка должна превысить постоянную длину мембраны (Хт), иначе ПД может распространиться через этот участок электротонически (см. раздел 5.2.3). Нарушение физиологической непрерывности нервных волокон возникает при действии анестетиков, электрического тока, при гипоксии, воспалении, охлаждении. После прекращения действия этих факторов проведение возбуждения по волокнам нерва восстанавливается.
5.2.5. АКСОННЫЙ ТРАНСПОРТ
Наличие у нейрона отростков, длина которых может достигать 1 м (например, аксоны, ин-нервирующие мускулатуру конечностей), создает серьезную проблему внутриклеточной связи между различными участками нейрона и ликвидации возможных повреждений его отростков. Основная масса веществ (структурных белков, ферментов, полисахаридов, липидов и др.) образуется в трофическом центре (теле) нейрона, расположенном преимущественно около ядра, а используются они в различных участках нейрона, включая его отростки. Хотя в аксонных окончаниях существуют синтез медиаторов, АТФ и повторное использование мембраны гузырьков после выделения медиатора, все же необходима постоянная доставка ферментов и фрагментов мембран из тела клетки. Для транспорта этих веществ (например, белков) путем диффузии на расстояние, равное максимальной длине аксона (около 1 м), потребовалось бы 50 лет! Для решения этой задачи эволюция сформировала специальный вид транспорта в пределах отростков нейрона, который более хорошо изучен в аксонах и получил название аксонного транспорта. С помощью этого процесса осуществляется трофическое влияние не только в пределах различных участков нейрона, но и на иннервируе-
мые клетки. В последнее время появились данные о существовании нейроплазматичес-кого транспорта в дендритах, который осуществляется из тела клетки со скоростью около 3 мм в сутки. Различают быстрый и медленный аксонный транспорт.
А. Быстрый аксонный транспорт идет в двух направлениях: от тела клетки до аксонных окончаний (антеградный транспорт, скорость 250—400 мм/сут) и в противоположном направлении (ретроградный транспорт, скорость 200—300 мм/сут). Посредством анте-градного транспорта в аксонные окончания доставляются везикулы, образующиеся в аппарате Гольджи и содержащие гликопротеины мембран, ферменты, медиаторы, липиды и другие вещества. Посредством ретроградного транспорта в тело нейрона переносятся везикулы, содержащие остатки разрушенных структур, фрагменты мембран, ацетилхоли-нэстераза, неидентифицированные «сигнальные вещества», регулирующие синтез белка в соме клетки. В патологических условиях по аксону к телу клетки могут транспортироваться вирусы полиомиелита, герпеса, бешенства и столбнячный экзотоксин. Многие вещества, доставленные путем ретроградного транспорта, подвергаются разрушению в лизосомах.
Быстрый аксонный транспорт осуществляется с помощью специальных структурных элементов нейрона: микротрубочек и микрофиламентов, часть которых представляет собой актиновые нити (актин составляет 10—15 % белков нейрона). Для транспорта необходима энергия АТФ. Разрушение микротрубочек (например, колхицином) и микрофиламентов (цитохолазином В), снижение уровня АТФ в аксоне более чем в 2 раза и падение концентрации Са2+ блокируют аксонный транспорт.
Б. Медленный аксонный транспорт осуществляется только в антеградном направлении и представляет собой передвижение всего столба аксоплазмы. Он выявляется в опытах со сдавлением (перевязкой) аксона. При этом происходит увеличение диаметра аксона проксимальнее перетяжки в результате «наплыва гиалоплазмы» и утончение аксона за местом сдавления. Скорость медленного транспорта равна 1—2 мм/сут, что соответствует скорости роста аксона в онтогенезе и при его регенерации после его повреждения. С помощью этого транспорта перемещаются образованные в эндоплазм этической сети белки микротрубочек и микрофиламентов (тубулин, актин и др.), ферменты цитозоля, РНК, белки каналов, насосов и другие вещества. Медленный аксонный транспорт не на-
73
рушается при разрушении микротрубочек, но прекращается при отделении аксона от тела нейрона, что свидетельствует о разных механизмах быстрого и медленного аксонного транспорта.
В. Функциональная роль аксонного транспорта. 1. Антеградный и ретроградный транспорт белков и других веществ необходимы для поддержания структуры и функции аксона и его пресинаптических окончаний, а также для таких процессов, как аксонный рост и образование синаптических контактов.
-
Аксонный транспорт участвует в трофи ческом влиянии нейрона на иннервируемую клетку, так как часть транспортируемых ве ществ выделяется в синаптическую щель и действует на рецепторы постсинаптической мембраны и близлежащих участков мембра ны иннервируемой клетки. Эти вещества участвуют в регуляции обмена веществ, про цессов размножения и дифференцировки ин- нервируемых клеток, формируя их функцио нальную специфику. Например, в опытах с перекрестной иннервацией быстрых и мед ленных мышц показано, что свойства мышц меняются в зависимости от типа иннервиру- ющего нейрона, его нейротрофического воз действия. Передатчики трофических влияний нейрона до сих пор точно не определены, важное значение в этом плане придается полипептидам и нуклеиновым кислотам.
-
Роль аксонного транспорта особенно ярко выявляется при повреждении нерва. Если нервное волокно на каком-либо участке прервано, его периферический отрезок, ли шенный контакта с телом нейрона, подверга ется разрушению, которое называется валле- ровской дегенерацией. В течение 2—3 сут на ступает распад нейрофибрилл, митохондрий, миелина у синаптических окончаний. Надо отметить, что распаду подвергается участок волокна, снабжение которого кислородом и питательными веществами с кровотоком не прекращается. Считают, что решающим ме ханизмом дегенерации является прекраще ние аксонного транспорта веществ от тела клетки до синаптических окончаний.
-
Аксонный транспорт играет важную роль и при регенерации нервных волокон.
5.2.6. РАЗВИТИЕ И РЕГЕНЕРАЦИЯ ОТРОСТКОВ НЕЙРОНА
После рождения у человека деления нейронов и нейробластов практически не происходит, хотя отдельные случаи митоза могут быть и сохраняется способность нейрона к
размножению, что показано при культивировании нервной ткани. Созревание нервной системы в процессе онтогенеза и усложнение структуры при функциональной нагрузке осуществляется в результате развития нервных отростков — увеличения их числа и степени ветвления. Например, у взрослого человека по сравнению с новорожденным число точек ветвления дендритов увеличивается в 13 раз, а общая длина дендритов нейронов коры — в 34 раза. Увеличивается также число коллатералей и терминальных разветвлений аксона. В результате роста нервных отростков осуществляется также их регенерация при повреждении. Конечной целью развития и регенерации нервных волокон является образование синаптических контактов, новых или на месте разрушения.
Важным структурным элементом при развитии или регенерации отростка нейрона является образование конуса роста волокна — утолщение неправильной формы с множеством длинных и тонких отростков толщиной 0,1—0,2 мкм и длиной до 50 мкм, отходящих в разные стороны. Конус роста является зоной интенсивного экзо- и эндоцитоза. Мембранный материал, образованный в теле нейрона, переносится посредством быстрого аксонного транспорта в виде пузырьков к конусу роста и посредством экзоцитоза встраивается в клеточную мембрану, удлиняя ее. Для передвижения конуса роста необходимы актиновые филаменты, повреждение которых прекращает рост. Для стабилизации структуры удлиняющегося волокна важное значение имеют микротрубочки, разрушение которых приводит к укорочению растущего волокна. Белки, необходимые для образования микротрубочек и микрофиламентов (тубулин, актин и др.), доставляются посредством медленного аксонного транспорта.
В механизмах передвижения конуса роста выделены два фактора, направляющих этот процесс: «фактор адгезивности клеток» представляет собой гликопротеид, который находится на плазматической мембране отростков нейрона и обеспечивает сцепление между развивающимися отростками, группируя их в пучки; другим веществом является белок — «фактор роста нервов», который выделяется в межклеточную жидкость клеткой-мишенью для растущего нервного волокна и оказывает хемотаксическое влияние, направляя движение конуса роста в сторону клетки-мишени. При регенерации поврежденных волокон в периферической нервной системе важную роль в контроле направления роста играют шванновские клетки дистального (от зоны
74
травмы) участка волокна. Они образуют после распада осевого цилиндра трубковид-ный тяж, в который должно попасть в случае успешной регенерации одно из ответвлений конуса роста. Как только конус роста достигает клетки-мишени, он превращается в пре-синаптическое окончание; при этом процессы экзо- и эндоцитоза обеспечивают выделение и последующие поглощение медиатора.
5.2.7. ОСОБЕННОСТИ ФИЗИОЛОГИИ НЕРВОВ ДЕТЕЙ
Критериями структурно-функциональной зрелости мякотных и безмякотных нервных волокон являются увеличение их толщины и уменьшение проницаемости клеточной мембраны, что оказывает существенное влияние на свойства нервного волокна. Однако главными критериями степени зрелости мякотных нервных волокон являются их миелини-зация, интенсивно происходящая к концу антенатального периода, увеличение расстояния между перехватами Ранвье. Изменяется при этом и распределение ионных каналов.
У плода и ребенка первых лет жизни при неполной миелинизации нервных волокон распределение натриевых и калиевых каналов в мембране является равномерным; после завершения миелинизации ионные каналы концентрируются в области перехватов Ранвье. Это обусловлено перераспределением в мембране белковых молекул, являющихся основой каналов. В безмякотных волокнах распределение ионных каналов остается равномерным по всей длине волокна. К моменту рождения двигательные окончания в мышцах руки достигают более высокого уровня диф-ференцировки, чем в мышцах груди или спины, голени. Филогенетически старые пути миелинизируются раньше, чем филогенетически новые.
У новорожденного в нервах голени, например, количество миелинизированных волокон составляет около i/з. Передние спинномозговые корешки у детей достигают состояния, свойственного взрослым, между 2— 5 годами жизни, а задние спинномозговые корешки — между 5—9 годами. Миелиниза-ция в целом близка к завершению к 9 годам жизни ребенка. Число аксонов в нерве с возрастом не изменяется, однако в результате его созревания возбудимость, скорость проведения возбуждения и лабильность увеличиваются.
Возбудимость нервных волокон плода и новорожденного значительно ниже, чем у
взрослых, но уже с 3-месячного возраста ребенка она начинает повышаться. Величина хронаксии в несколько раз больше, чем у взрослых. Потенциал покоя нервных волокон у детей значительно меньше, чем у взрослых, вследствие большей проницаемости клеточной мембраны для ионов. В процессе созревания нервного волокна проницаемость его мембраны уменьшается, улучшается работа ионных помп, возрастают потенциал покоя и потенциал действия, что свидетельствует о функциональном созревании нервного волокна. Небольшая величина потенциала действия новорожденного сочетается с большей его продолжительностью и часто с отсутствием инверсии. Это объясняется меньшей, чем у взрослых, ионной асимметрией. Фазовые изменения возбудимости во время возбуждения в раннем постнаталь-ном онтогенезе также имеют свои особенности. В частности, длительность абсолютной рефрактерной фазы равна 5—8 мс, а у взрослых 1—2 мс.
Проводимость нерва плода и детей низкая. У новорожденных, например, скорость проведения возбуждения по нервным волокнам не превышает 50 % от скорости взрослых. Плохо выражена изолированность проведения возбуждения. С возрастом скорость проведения возбуждения по нервным волокнам увеличивается в результате их миелинизации, увеличения толщины волокна и его потенциала действия.
Скорость распространения возбуждения по нервным волокнам у детей становится такой же, как у взрослых, к 5—9 годам, что связано с завершением миелинизации различных волокон в разные сроки и окончанием увеличения диаметров осевых цилиндров.
Лабильность нервного волокна плода и детей первых лет жизни низкая, с возрастом она также увеличивается: число потенциалов действия, которое способно воспроизвести волокно в 1 с у новорожденных, например, составляет 4—10, а у детей 5—9 лет приближается к норме взрослых — 300—800 импульсов.
5.3. СИНАПТИЧЕСКАЯ ПЕРЕДАЧА
В нервной ткани имеются различные формы межклеточных контактов, среди которых главное место по функциональной значимости занимают химические синапсы. Основной функцией межклеточных контактов является их системообразующая роль, т.е. функция интеграции клеток в более сложные системы (тканевые, органные), что обеспечивается
75

передачей от клетки к клетке различных сигналов.
Синапс (греч. synapsis — соединение) — специализированная структура, обеспечивающая передачу возбуждающих или тормозных влияний между двумя возбудимыми клетками. Через синапс наряду с прямым влиянием на возбудимость иннервируемой клетки осуществляется и более медленное трофическое влияние, приводящее к изменению метаболизма иннервируемой клетки, ее структуры и функции. Понятие синапс как тип межклеточного соединения, при котором осуществляется перенос нервной информации, ввел в науку Ч.Шеррингтон (1897). По данным современной нейрофизиологии, в области синапсов происходят важнейшие процессы регуляции нейронной активности. Большое значение имеют синапсы в образовании условных связей, памяти, формировании пластичности нервных центров. Синапсы являются ареной деятельности многих лекарств, механизмов заболевания и выздоровления.
5.3.1. КЛАССИФИКАЦИЯ СИНАПСОВ И ИХ ХАРАКТЕРИСТИКА
А. Классификация. 1. По виду соединяемых клеток синапсы можно разделить на межнейронные, нейроэффекторные и нейрорецепторные. Межнейронные синапсы находятся в ЦНС и вегетативных ганглиях. Нейроэффекторные (нейромышечные и ней-росекреторные) синапсы соединяют эфферентные нейроны соматической и вегетативной нервной системы с исполнительными клетками — поперечнополосатыми и гладкими миоцитами, секреторными клетками. К нейрорецепторным синапсам относят контакты во вторичных рецепторах между рецеп-торной клеткой и дендритом афферентного нейрона.
-
По эффекту синапсы делят на воз буждающие, т.е. запускающие генерацию по тенциала действия, и тормозные, препятст вующие возникновению потенциала дейст вия.
-
По способу передачи сиг нала синапсы делят на химические, электрические и смешанные. Химические си напсы являются специфическим межклеточ ным контактом для нервной системы. В них передача влияния на постсинаптическую клетку осуществляется с помощью химичес кого посредника — медиатора. Этот тип си напсов преобладает в нервной системе чело-
века и высших позвоночных. В электрических синапсах потенциалы действия непосредственно (электротонически) передаются на постсинаптическую клетку. Эти синапсы являются разновидностью щелевых межклеточных контактов (высокопроводимые контакты), которые встречаются и в других тканях (например, нексусы в миокарде и глад-комышечной ткани). Электрические синапсы немногочисленны в нервной системе млекопитающих, особенно в постнатальном периоде. Обнаружены также смешанные синапсы, в которых наряду с химической передачей имеются участки с электротоническим механизмом передачи (например, в реснитчатом ганглии птиц, спинном мозге лягушки).
4. По природе медиатора химические синапсы делят на холинергические (медиатор — ацетилхолин), адренергические (норадреналин), дофаминергические (дофамин), ГАМКергические (у-аминомасляная кислота), глутаматергические (глутамат), ас-партатергические (аспартат), пептидергичес-кие (пептиды), пуринергические (АТФ).
Б. Структурно-функциональная характеристика синапсов. Нервно-мышечный синапс имеет общие для всех синапсов структурные элементы: пресинаптическое окончание, постсинаптическую мембрану и связывающую их синаптическую щель (рис. 5.6). Вместе с тем структура нервно-мышечного синапса имеет и отличия от других синапсов, связанные с иннервацией длинных клеток (мио-цитов) и необходимостью из одного синапса при передаче одного импульса практически одновременно активировать все сократительные единицы (саркомеры) миоцита.
1. Пресинаптическое окончание образуется расширениями по ходу разветвления аксона, иннервирующего мышечное волокно. В нервно-мышечном синапсе пресинаптическое окончание имеет большую длину (около 1—2 мм). Главным ультраструктурным фрагментом пресинаптического окончания являются синаптические пузырьки (везикулы) диаметром около 40 нм. Они образуются в комплексе Гольджи, с помощью быстрого аксонного транспорта доставляются в пресинаптическое окончание и там заполняются медиатором и АТФ. В пресинаптическом окончании содержится несколько тысяч везикул, в каждой из которых имеется от 1 до 10 тыс. молекул химического вещества, участвующего в передаче влияния через синапс и в связи с этим названного медиатором (посредником). В нервно-мышечном синапсе везикулы преимущественно расположены
76

I — ветвь аксона; 2 — пресинаптическое окончание аксона; 3 — митохондрия; 4 — синаптические пузырьки, содержащие ацетилхолин; 5 — синаптическая щель; 6 — молекулы медиатора в синаптической щели; 7 — постсинаптическая мембрана мышечного волокна с рецепторами.
вблизи периодических утолщений пресинап-тической мембраны, называемых активными зонами. В неактивном синапсе везикулы с помощью белка синапсина связаны с белками цитоскелета, что обеспечивает их иммобилизацию и резервирование. Важными структурами пресинаптического окончания являются митохондрии, осуществляющие энергетическое обеспечение процесса синаптической передачи, цистерны гладкой эндо-плазматической сети, содержащие депонированный Са2+, а также микротрубочки и мик-рофиламенты, участвующие во внутриклеточном передвижении везикул. Часть мембраны пресинаптического окончания, ограничивающая синаптическую щель, называется пресинаптической мембраной. Через нее осуществляется выделение (экзоцитоз) медиатора в синаптическую щель.
-
Синаптическая щель в нервно-мышеч ном синапсе имеет ширину в среднем 50 нм. Она содержит межклеточную жидкость и му- кополисахаридное плотное вещество в виде полосок, мостиков, которое обеспечивает связь между пре- и постсинаптической мем бранами и может содержать ферменты. Это вещество хорошо выражено в щели нервно- мышечного синапса, где оно формирует ба- зальную мембрану и содержит фермент аце тил холи нэстеразу.
-
Постсинаптическая мембрана — утол щенная часть клеточной мембраны иннерви- руемой клетки, содержащая белковые рецеп торы, имеющие ионные каналы и способные
связать молекулы медиатора. Ее особенностью в нервно-мышечном синапсе является наличие множества мелких складок, которые образуют слепые карманы, открывающиеся в синаптическую щель. Благодаря им резко увеличиваются площадь постсинаптической мембраны и количество ее рецепторов, которое в одном синапсе достигает 10—20 млн. Постсинаптическую мембрану нервно-мышечного синапса называют также концевой пластинкой.
5.3.2. МЕХАНИЗМ СИНАПТИЧЕСКОЙ ПЕРЕДАЧИ И ЕЕ РЕГУЛЯЦИЯ
Передача в синапсе имеет два главных этапа. 1. Преобразование электрического сигнала в химический (электросекреторное сопряжение). Потенциал действия (ПД), поступивший в пресинаптическое окончание, вызывает деполяризацию его мембраны, открывающую потенциалзависимые Са-каналы. Ионы кальция входят, согласно концентрационному и электрическому градиентам, внутрь клетки, что ведет к увеличению его содержания в цитозоле в 10—100 раз. Ионы кальция активируют фосфорилирование си~ наптосина, что ослабляет связь везикулы с цитоскелетом, и везикула перемещается вдоль микротрубочек на позицию у активной зоны. При контакте везикулы с пресинаптической мембраной происходит ферментативное «плавление» ее стенки, а также
77
активация белка синаптопорина, формирующего канал, через который медиатор выходит в синаптическую щель посредством первично-активного транспорта — экзоцитозаЛ В нервно-мышечном синапсе медиатором является ацетилхолин, который образуется в пресинаптическом окончании из ацетилко-энзима А и холина под действием фермента холинацетилтрансферазы. Впервые экспериментальное доказательство химического механизма передачи возбуждения в нервно-мышечном синапсе получил А.Ф.Самойлов (1924). Он показал, что скорость передачи возбуждения с нерва на мышцу в отличие от проведения возбуждения по нерву зависит от температуры в такой же степени, как и скорость химических реакций. Английский физиолог Г.Дейл (1934) установил, что медиатором нервно-мышечного синапса является ацетилхолин.
Выделение молекул медиатора из преси-наптического окончания пропорционально количеству поступившего туда Са в степени п=4. Следовательно, химическое звено пре-синаптического окончания работает как усилитель. Один из возможных механизмов усиления связан с тем, что поступивший в пре-синаптическое окончание Са2+ активирует рианодиновые рецепторы в цистернах эндоплазм ати чес кой сети, имеющие в своем составе Са-каналы, что приводит к дополнительному выделению Са** в цитозоль из цистерн. Выделение ацетилхолина в синаптическую щель осуществляется квантами, каждый из которых в нервно-мышечном синапсе содержит от нескольких тысяч до 10 тыс. молекул. На один ПД из пресинаптического окончания нервно-мышечного синапса выделяется 200—300 квантов медиатора. В промежутках между ПД из пресинаптического окончания происходит спонтанное выделение 1—2 квантов медиатора в синаптическую щель в течение 1 с.
Молекулы медиатора, поступившие в синаптическую щель, диффундируют к пост-синаптической мембране и вступают во взаимодействие с ее рецепторами. В нервно-мышечном синапсе ацетилхолин действует на Н-холинорецепторы, которые способны активизироваться и под влиянием никотина, вследствие чего они и получили свое название. Н-холинорецептор состоит из субъединиц (а)2) р, у, 6 и имеет в своем составе Na/K-канал. Скорость диффузии молекул медиатора позволяет им пройти расстояние синаптической щели в течение 0,1—0,2 мс. Длительность действия медиатора на рецепторы постсинаптической мембраны, опре-
деленная по продолжительности открытия в ней ионных каналов, равна около 1 мс. Это значительно меньше периода полураспада медиатора и свидетельствует о его удалении из синаптической щели. Оно осуществляется путем диффузии ацетилхолина из щели в окружающую жидкость и разрушения его под действием ацетилхолинэсте-разы.
Этот фермент выделяется миоцитом и прикрепляется к мукополисахаридному веществу в синаптической щели. Одна молекула ацетилхолинэстеразы может гидролизо-вать до ацетата и холина 10 молекул ацетилхолина в 1 мс, что обеспечивает его разрушение в синаптической щели в течение нескольких десятых долей миллисекунды. При этом большая часть (около 60 %) холина захватывается обратно пресинаптическим окончанием.
2. Преобразование химического сигнала обратно в электрический. Этот этап осуществляется в постсинаптической мембране. Действие молекул медиатора на ее рецепторы ведет к открытию ионных каналов и перемещению ионов, имеющих высокий электрохимический градиент на протяжении канала. Присоединение двух молекул ацетилхолина к а-субъединицам Н-холинорецептора открывает канал. Открытое состояние сохраняется 1 мс, в течение которой через него проходит около 500 000 ионов. Канал на внутреннем суженном конце имеет диаметр 0,65 нм, хорошо проницаем для Na+ и К+, плохо проницаем для Са2+. Поскольку канал имеет слабую избирательность в отношении Na+ и К+, то ионные токи через канал зависят главным образом от электродвижущей силы (ЭДС) этих ионов.
ЭДС иона равна разности между мембранным потенциалом покоя и равновесным потенциалом данного иона (ЭДС = МПП -ЕцОна)- Отрицательная величина ЭДС характеризует движение иона в клетку, положительная — из клетки.
В связи с этим входящий в клетку ток натрия (ЭДС = —140 мВ) резко преобладает над выходящим из клетки током калия (ЭДС = 14 мВ). Иными словами, ион Na+ движется в клетку согласно концентрационному и электрическому градиенту (клетка внутри имеет положительный заряд), а ион К+ выходит из клетки только согласно концентрационному градиенту, причем вопреки электрическому (снаружи клетка имеет положительный заряд). Поэтому суммарный ток ионов Na+ в клетку превосходит ток К+ из клетки, что и приводит к деполяризации постсинап-
КУД
Юме
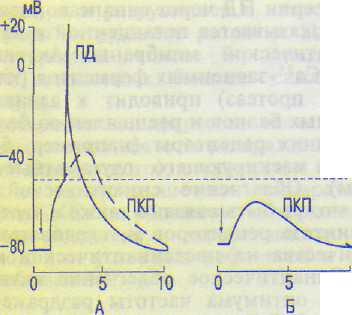
КУД — критический уровень деполяризации; ПД — потенциал действия; А — ПКП в нормальной мышце, переходящий в ПД; Б — ослабленный ПКП, записанный в ку-рарезированной мышце.
тической мембраны (концевой пластинки). Эта деполяризация называется возбуждающим постсинаптическим потенциалом (ВПСП), который в нервно-мышечном синапсе называют потенциалом концевой пластинки (ПКП) (рис. 5.7). Особенностью нервно-мышечного синапса фазного мышечного волокна является то, что при одиночной его активации формирующийся ПКП имеет большую амплитуду (30—40 мВ), которая превышает критический уровень деполяризации и вызывает генерацию ПД в миоците. Тоническое мышечное волокно имеет 7—10 синапсов, принадлежащих, как правило, нескольким мотонейронам. При этом ПКП не вызывает генерации ПД, а непосредственно запускает мышечное сокращение.
Как было отмечено, в промежутках между передачей нервного импульса происходит спонтанное выделение 1—2 квантов медиатора в синаптическую щель. При этом в пост-синаптической мембране формируется деполяризация амплитудой 0,12—0,24 мВ, возникающая в среднем 1 раз в 1 с. Такие потенциалы, изученные в нервно-мышечном синапсе, были названы миниатюрными потенциалами концевой пластинки. Они, вероятно, поддерживают высокую возбудимость синапсов в условиях функционального покоя нервных центров. Кроме экзоцитоза медиатора, существует постоянная неквантовая утечка молекул медиатора в синаптическую щель. Предполагают, что неквантовая секреция играет трофическую роль.
Саморегуляция в синапсе осуществляется с использованием функциональных обратных связей. Веществами, влияющими на эффективность синаптической передачи, могут быть медиаторы, продукты их распада. В нервно-мышечном синапсе ацетилхолин, выделившийся в небольшом количестве в синаптическую щель, может стимулировать более сильный выброс ацетилхолина из пре-синаптического окончания по механизму обратной связи (самоусиление секреции). Высокие концентрации ацетилхолина в синаптической щели, напротив, угнетают секрецию его из пресинаптического окончания.
Показано, что холин (продукт гидролиза ацетилхолина) в концентрации 10~4—10~5 М тормозит выделение ацетилхолина из пресинаптического окончания.
5.3.3. ХАРАКТЕРИСТИКА ПРОВЕДЕНИЯ ВОЗБУЖДЕНИЯ В ХИМИЧЕСКИХ СИНАПСАХ
1. Синапсы функционально асимметричны и работают по принципу физиологического клапана, осуществляя одностороннее проведение возбуждения только в направлении от пресинаптического окончания в сторону постси-наптической мембраны. Это связано с тем, что медиатор выделяется из пресинаптического окончания, а взаимодействующие с ним рецепторы, имеющие ионные каналы, необходимые для формирования синаптических потенциалов, находятся только на постси-наптической мембране.
-
Имеется синоптическая задержка в проведении нервного импульса от нейрона на иннервируемую клетку, равная в нервно- мышечном синапсе 0,5—1,0 мс (время от мо мента поступления импульса к нервному окончанию до момента возникновения ПД в мышечном волокне). Это время затрачивает ся на процессы секреции медиатора, диффу зию его к постсинаптической мембране, дей ствие на рецепторы, возникновение ионных токов, формирование постсинаптических по тенциалов и их суммацию, способную вы звать ПД.
-
Синапсы имеют низкую лабильность (по сравнению с нервным волокном). Она равна около 100 Гц, что в 5—6 раз ниже лабильнос ти аксона. Главной причиной низкой лабиль ности синапса является синаптическая за держка проведения возбуждения.
-
В синапсах происходит трансформация ритма возбуждения: частота потенциалов
79
действия, поступающих в синапс, обычно не совпадает с частотой ПД, генерируемых нейроном, имеющим данный синаптический вход. Однако в нервно-мышечном синапсе быстрого мышечного волокна трансформация ритма не выражена: один импульс нервного волокна вызывает один ПД в мышечном волокне.
-
Проводимость химических синапсов сильно изменяется под влиянием биологи чески активных веществ, лекарств и ядов. Например, в нервно-мышечном синапсе ток син возбудителя ботулизма подавляет синтез ацетилхолина в пресинаптическом оконча нии, угнетая обратное поглощение холина из синаптической щели. Кураре и курареподоб- ные вещества (диплацин, тубокурарин и др.) обратимо связываются с Н-холинорецептора- ми постсинаптической мембраны, блокируя действие на нее ацетилхолина. Необратимо связывает холинорецепторы и полностью блокирует передачу возбуждения через си напс полипептид из яда змей а-бунгароток- син. Ряд веществ (прозерин, фосфороргани- ческие отравляющие вещества и инсектици ды) подавляют активность ацетилхолинэсте- разы, разрушающей ацетилхолин в синапти ческой щели. При небольшой ее инактива ции происходят умеренное накопление аце тилхолина и облегчение синаптической пере дачи (например, действие лечебных доз про- зерина). При большой инактивации ацетил- холинэстеразы и значительном накоплении ацетилхолина синаптическая передача бло кируется — развивается синаптическая деп рессия.
-
Синоптическое облегчение и депрессия. Эти изменения синаптической передачи воз буждения более детально изучены в нервно- мышечных синапсах, хотя имеют место и в синапсах ЦНС. Передача ПД через синапс, как было рассмотрено выше, сопровождается повышением концентрации Са2+ в пресинап тическом окончании, которая снижается до межимпульсного уровня в течение несколь ких десятков миллисекунд. Если следующий ПД попадает в этот следовый период, то вы брос медиатора в синаптическую щель увели чивается и формируется более высокоампли тудный ВПСП (в нервно-мышечном синап се — ПКП), что приводит к повышению эф фективности синаптической передачи — си ноптическому облегчению).
Активация пресинаптического окончания может осуществляться ретроградными посредниками (окисью азота, арахидоновой кислотой, нейропептидами), которые выделяются постсинаптической клеткой. При
передаче серии ПД через синапс концентрация Са2+ оказывается повышенной и вблизи постсинаптической мембраны. Активация при этом Са2+-зависимых ферментов (киназ, фосфатаз, протеаз) приводит к активации рецепторных белков и расщеплению белков, блокирующих рецепторы (например, белка фодрина, маскирующего глутаматные рецепторы). Облегчение синаптической передачи может быть связано также с увеличением синтеза рецепторов и, следовательно, их количества на постсинаптической мембране. Синаптическое облегчение является причиной оптимума частоты раздражения, открытого Н.Е.Введенским (1885) на нервно-мышечном препарате. В ЦНС синаптическое облегчение обозначается как феномен длительной потенциации. Он имеет важное значение в образовании условных рефлексов, формировании памяти и обучения.
При более высоких частотах передачи импульсов через синапс (например, для нервно-мышечного синапса более 100 Гц) снижается эффективность синаптической передачи, что получило название «синаптическая депрессия» (пессимум Н.Е.Введенского) — блок проведения возбуждения в результате стойкой деполяризации постсинаптической мембраны мышечного волокна, поскольку механизмы инактивации ацетилхолина не успевают срабатывать (пессимальное торможение). Синаптическая депрессия может развиться и при редкой, но длительной активации синапса. Ее механизм на пресинаптическом уровне связывают с истощением запаса медиатора в пресинаптическом окончании, которого по расчетам хватает на 10 000 синаптических передач и который может иссякнуть в течение нескольких минут. Другие механизмы депрессии связаны с накоплением высокой концентрации медиатора в синаптической щели вследствие того, что выброс медиатора в щель превышает возможности систем его разрушения и удаления. Высокий же уровень медиатора оказывает тормозящее влияние на секрецию его из пресинаптического окончания. Происходит также уменьшение чувствительности (десенситизация) рецепторов постсинаптической мембраны к медиатору. Механизм десенситизации может быть связан с фосфорилированием рецепторов постсинаптической мембраны, что в несколько раз снижает их сродство к медиатору. Другим механизмом десенситизации является эндоци-тоз комплекса медиатор+рецептор внутрь клетки. Поглощенные рецепторы могут опять встраиваться в мембрану (при ослаблении
80
стимула) или разрушаться в лизосомах. Эти процессы затрудняют развитие ПД в пост-синаптической клетке и, следовательно, могут привести к блокаде синаптической передачи.
Синаптическая депрессия является причиной пессимума частоты раздражения (торможение Введенского), открытого в исследованиях на нервно-мышечном препарате. В синапсах ЦНС она обозначается термином длительная депрессия и играет важную роль в торможении условных рефлексов и процессах забывания.
5.3.4. ОСОБЕННОСТИ ФИЗИОЛОГИИ СИНАПСОВ ДЕТЕЙ
Структурно-функциональное созревание нервно-мышечных синапсов охватывает период антенатального и раннего постнаталь-ного периодов развития. Оно имеет свои особенности для пре- и постсинаптических мембран.
А. Созревание пре синаптической мембраны. Двигательные нервные окончания в мышцах появляются на 13—14-й неделе внутриутробного развития. Формирование их продолжается длительное время и после рождения. Мышечное волокно новорожденного, как и взрослого человека, имеет один синапс в виде типичной концевой бляшки. Созревание пресинаптической мембраны проявляется в увеличении терминального разветвления аксона, усложнении его формы, увеличении площади всего окончания. Степень созревания нервных окончаний значительно увеличиваются к 7—8 годам, при этом проявляются более быстрые и разнообразные движения.
В процессе развития усиливается синтез ацетилхолина в мотонейронах, увеличиваются количество активных зон в пресинапти-ческом окончании и количество квантов медиатора, выделяющегося в синаптическую щель.
Б. Созревание постсинаптической мембраны. Когда окончание аксона достигает миот-рубки, в соответствующем ее участке появляются скопления митохондрий, рибосом, микротрубок. На поверхности миотрубки образуются выемки, в которых помещается окончание аксона. Образуется примитивное нервно-мышечное соединение. Особенностью ранних стадий развития мышечных волокон
является разлитая чувствительность всей поверхности мембраны к ацетилхолину, присущая донервной стадии развития мышц. В процессе развития на каждом мионе сохраняется единственный синапс, формирование его сопровождается появлением в постсинаптической мембране холинэстеразы, увеличение концентрации которой приводит к повышению скорости гидролиза ацетилхолина. Образуются складки на постсинаптической мембране, в результате чего растет амплитуда ПКП и повышается надежность передачи возбуждения через синапс. Внесинапти-ческая поверхность мышечного волокна постепенно теряет чувствительность к ацетилхолину. После денервации в эксперименте чувствительность к ацетилхолину вновь распространяется на всю поверхность мембраны.
Вследствие незрелости нервно-мышечного синапса у плода и новорожденного синаптическая передача возбуждения происходит медленно. Без трансформации ритма через такой синапс передается не более 20 импульсов в 1 с, а к 7—8 годам жизни — около 100 импульсов в 1 с, т.е. как у взрослого.
В. Утомляемость синапса объясняется истощением медиатора и снижением чувствительности постсинаптической мембраны к медиатору в результате накопления продуктов обмена, закислением среды — все это приводит к снижению ПКП.
5.4. ИЗМЕНЕНИЯ НЕРВНЫХ ПРОВОДНИКОВ, ПЕРИФЕРИЧЕСКИХ СИНАПСОВ И РЕЦЕПТОРОВ В ПРОЦЕССЕ СТАРЕНИЯ
В нервных стволах и ганглиях в процессе старения развиваются дегенеративные изменения, появляются участки демиелинизации, повышается доля соединительнотканных элементов. После 75 лет количество нервных волокон в корешках спинного мозга уменьшено на 32 %.
С увеличением возраста снижаются возбудимость и лабильность нервных проводников и нервно-мышечных синапсов, повышается длительность рефрактерных фаз.
После 55 лет развиваются атрофические процессы в волосковых клетках кортиева органа, уменьшается число вкусовых и обонятельных рецепторов, появляются дистрофические изменения кожных рецепторов.
81
