
Журнал неврологии и психиатрии / 2007 / NEV_2007_06_07
.pdf
МЕТОДЫ ИССЛЕДОВАНИЯ И ДИАГНОСТИКИ
Нейрофизиологический анализ симптоматической посттравматической эпилепсии
С.А. КУРБАНОВА, О.М. ОЛЕЙНИКОВА, Г.Н. АВАКЯН
The neurophysiological analysis of symptomatic post-traumatic epilepsy
S.A. KURBANOVA, Î.Ì. OLEINIKOVA, G.N. AVAKYAN
Кафедра неврологии и нейрохирургии лечебного факультета Российского государственного медицинского университета, Москва
Провели сравнительную оценку пространственной организации биоэлектрической активности головного мозга у больных с последствиями закрытой ЧМТ без эпилепсии (53 пациента) и больных с посттравматической эпилепсией (43 больных) с целью выявления коррелятов развития эпилепсии у лиц, перенесших травму мозга, и 15 здоровых. Установили, что спектрально-когерентный анализ ЭЭГ позволяет прогнозировать симптоматическую посттравматическую эпилепсию (СПЭ) и дифференцированно подходить к назначению противосудорожной терапии лицам, перенесшим травму головного мозга.
Ключевые слова: посттравматическая эпилепсия, закрытая черепно-мозговая травма, спектрально-когерентный анализ.
Òî identify correlates of epilepsy development in patients after brain injury, the authors carried out a comparative assessment of the spatial organization of brain electrical activity in patients with consequences of closed craniocerebral injury without epilepsy (53 patients) and in patients with post-traumatic epilepsy (43 patients). A control group included 15 subjects. The EEG study with spectral coherent analysis allows to predict post-traumatic epilepsy and to use a differential approach in prescribing the appropriate anticonvulsive therapy to people after head injury.
Key words: posttraumatic epilepsy, closed craniocerebral injury, spectral coherent analysis.
Одним из наиболее частых последствий черепномозговой травмы является посттравматическая эпилепсия [15, 25], развивающаяся, как правило, в сроки от 3 до 18 мес от момента травмы, полученной впервые или повторно [14, 17]. Симптоматическую посттравматическую эпилепсию (СПЭ) можно трактовать как клиническую форму симптоматической эпилепсии, связанной с определенной локализацией посттравматического эпилептогенного очага и характеризующуюся сочетанием последствий травмы и эпилептических припадков [6]. Одной из наиболее частых и идентифицированных причин эпилепсии, особенно у молодых людей в возрасте 15—30 лет, является черепно-мозговая травма (ЧМТ) — 40%. По данным ВОЗ, число разного рода ЧМТ в мире увеличи- вается на 2%. У 11—20% пострадавших развивается посттравматическая эпилепсия, причем ее частота и тяжесть течения часто зависят от тяжести и характера ЧМТ [5, 19]. Припадки могут возникать как сразу после ЧМТ, так и в более отдаленном периоде [9], через один год и более от времени травмы [12].
После широкого внедрения в клиническую практику методов рентгеновской и магнитно-резонансной компьютерной томографии (КТ, МРТ) появился ряд работ, подтверждающих значимость наличия морфологического очага для развития эпилептических припадков после ЧМТ [23].
© Коллектив авторов, 2007
Zh Nevrol Psikhiatr Im SS Korsakova 2007;107:6:50—53
Основным методом диагностики эпилепсии любой этиологии, в том числе посттравматической, является электроэнцефалография. Многие авторы диагностическую роль ЭЭГ считают значительной, особенно при динамическом наблюдении [6, 24]. Но если изменения биоэлектрической активности в раннем посттравматическом периоде изучены достаточно подробно, то в отдаленном периоде ЧМТ они немногочисленны [16].
Ряд авторов [26] указывают на неинформативность визуальной оценки ЭЭГ в отдаленном периоде ЧМТ. Недостатками визуального анализа ЭЭГ объясняется большой процент «нормальных» или «пограничных» электроэнцефалограмм у больных с посттравматическими припадками, поскольку в межприступном периоде на ЭЭГ у таких больных часто не наблюдается типич- ных эпилептических разрядов [15, 27]. В дополнение к традиционному визуальному анализу ЭЭГ в ряде работ [13, 21] проводился спектрально-когерентный анализ, позволивший более объективно оценить степень дезорганизации основного ритма и количественно определить выраженность нарушений основных ритмов.
Цель настоящего исследования состояла в выявлении коррелятов эпилептических припадков на ЭЭГ при ее спектрально-когерентном анализе у больных с СПЭ.
Материал и методы
Обследовали 111 больных. В их числе были 53 больных с закрытой ЧМТ без припадков, 25 из которых обследовались в раннем периоде и 28 — в отдаленном. Их распределение по
50 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2007 |

тяжести травмы дано в табл. 1. Пациенты с СПЭ составили группу из 43 (табл. 2); в контрольную группу вошли 15 здоровых, у которых травм в анамнезе не было. В группах с закрытой ЧМТ и СПЭ преобладали мужчины молодого и среднего возраста.
Известно, что они в 2—3 раза чаще женщин подвержены травме и являются социальной группой риска. Все обследованные больные были в возрасте от 18 до 50 лет.
При обследовании больных использовался 16-каналь- ный нейрограф Нейросенсор, работающий на базе IBM-PC 586 с установленными фильтрами на 32 Гц и постоянной времени 0,03. Для оценки взаимосвязи отдельных частотных составляющих ЭЭГ разных областей головного мозга был использован метод вычисления комплексной функции когерентности (КОГ) [1—3]. Этот метод позволяет исследовать статистические линейные связи электрических процессов двух областей мозга и давать оценку по величине связанности на каждой отдельной частоте колебаний независимо от их амплитуды. КОГ может принимать значения от 0 до 1. КОГ равна нулю для полностью независимых процессов. Если КОГ равна 1, это свидетельствует о том, что между процессами существует линейная связь. По величине КОГ можно судить о степени связи двух процессов: при КОГ <0,3 — связь слабая, от 0,3 до 0,7 — умеренная, от 0,7 до 1
— высокая [3, 6—8, 10]. Методом когерентного анализа, позволяющим оценить сочетанность биоэлектрических процессов, исследовались меж- и внутриполушарные связи.
Результаты и обсуждение
Наиболее информативными для оценки функционального состояния головного мозга оказались показатели когерентности ЭЭГ.
При качественном анализе ЭЭГ было выделено 3 типа: I тип ЭЭГ: при визуальном анализе ЭЭГ регионарные различия выражены, основной компонент ЭЭГ — α-ритм, регулярный по частоте или фрагментарный со средним или высоким α-индексом; β-ак- тивность высокой и средней частоты, малой амплитуды, медленные волны почти не выражены. II тип ЭЭГ («дезорганизованный»): регионарные различия сглажены или отсутствуют; при этом электрическая активность характеризовалась либо наличием α-рит- ма достаточно высокой амплитуды и распространенностью α- по всем областям мозга, либо плохой выраженностью α-активности; θ- и δ-волны регистрировались без какой-либо четкой последовательности и имели достаточно высокую амплитуду. III тип ЭЭГ («плоский»): низкоамплитудный тип ЭЭГ характеризовался отсутствием регулярного α-ритма и наличи- ем диффузной быстрой активности, пиков, острых α-подобных волн с амплитудой до 30 мкВ.
Впервые был произведен детальный математиче- ский анализ не только фоновой ЭЭГ больных с закрытой ЧМТ в раннем и отдаленном периодах, симптоматической посттравматической эпилепсии (СПЭ), но и ЭЭГ больных этих групп во время пробы с гипервентиляцией. Это позволило выявить особенности спектрально-когерентных характеристик в указанных двух группах больных.
По медленноволновым формам активности в фоновой ЭЭГ больных с закрытой ЧМТ в раннем периоде с I «организованным» типом превышала спектральную мощность в отдаленном периоде травмы и контрольной группы. Вероятно, это связано с проявлением как тормозного процесса в ответ на травматическое повреждение, так и началом компенсатор-
ПОСТТРАВМАТИЧЕСКАЯ ЭПИЛЕПСИЯ
Таблица 1. Распределение больных согласно клинической классификации ЧМТ по А.Н. Коновалову и соавт. [11]
|
Ранний период |
Отдаленный период |
||
Травма |
закрытой ЧМТ |
закрытой ЧМТ |
||
|
|
|
|
|
|
àáñ. |
% |
àáñ. |
% |
|
|
|
|
|
Легкая закрытая |
8 |
32 |
10 |
35,7 |
×ÌÒ |
|
|
|
|
Закрытая ЧМТ |
11 |
44 |
13 |
46,4 |
средней степени |
|
|
|
|
Тяжелая закрытая |
6 |
24 |
5 |
17,9 |
×ÌÒ |
|
|
|
|
Всего |
25 |
100 |
28 |
100 |
|
|
|
|
|
Таблица 2. Распределение больных с симптоматической посттравматической эпилепсией с разными припадками по классификации эпилептических припадков Международной противоэпилептической лиги (1981)
Припадки |
Àáñ. |
% |
|
|
|
Простые парциальные |
1 |
2,3 |
Сложно-парциальные |
6 |
14 |
Парциальные с вторичной |
36 |
83,7 |
генерализацией |
|
|
Всего |
43 |
100 |
|
|
|
но-восстановительного процесса, направленного на функциональную перестройку, обеспечивающую новый режим деятельности. По θ-активности были выявлены отличия по спектрам мощности в раннем периоде по сравнению с отдаленным периодом закрытой ЧМТ в центрально-теменно-затылочных отведениях.
По медленноволновым формам активности для «дезорганизованного» и «плоского» типов ЭЭГ максимальные значения спектров мощности регистрировались в отдаленном периоде закрытой ЧМТ с акцентом по левому полушарию головного мозга, что скорее всего было связано с латерализацией закрытой ЧМТ. Выявленные различия между типами ЭЭГ для «организованного» и «дезорганизованных» типов, вероятно, связаны с тем, что у больных с хорошо выраженной α-активностью появляются элементы дезорганизации в ответ на закрытую черепно-мозго- вую травму, что и проявляется усилением мощности медленноволновой активности, а в отдаленном (позднем восстановительном периоде) — уменьшением мощности спектров, которое не достигало значений контрольной группы.
У больных с закрытой ЧМТ во время пробы с гипервентиляцией при всех типах ЭЭГ отмечалось достоверное увеличение показателей спектров мощности по медленноволновым формам активности только в отдаленном периоде закрытой ЧМТ. В раннем периоде закрытой ЧМТ показатели мощности по медленноволновым формам активности во время гипервентиляции достоверно не изменялись, что, возможно, связано с пониженным метаболизмом как в зоне травмы, так и мозга в целом [18].
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2007 |
51 |
МЕТОДЫ ИССЛЕДОВАНИЯ И ДИАГНОСТИКИ
По α-активности в отдаленном периоде закрытой ЧМТ отмечалось преобладание в фоновой ЭЭГ показателей спектров мощности только по I типу ЭЭГ, что может свидетельствовать о явлениях ирритации срединно-стволовых структур. Во время гипервентиляционной пробы достоверных изменений выраженности α-диапазона не наблюдалось. Гипервентиляция достоверно усиливала спектральную мощность у больных с закрытой ЧМТ, особенно в раннем периоде, с II и III типом ЭЭГ, приводя к усилению зональных различий.
При сравнении ЭЭГ I типа в группах отдаленного периода закрытой ЧМТ и симптоматической посттравматической эпилепсии максимальные показатели мощности отмечались в группе закрытой ЧМТ как в диапазоне медленных волн, так и по α- и β-активности. Для II типа ЭЭГ, напротив, регистрировались высокие значения спектральной мощности для всех видов активности головного мозга больных с СПЭ по сравнению с отдаленным периодом закрытой ЧМТ. Это может быть связано с более высокими
показателями спектральной мощности в группе больных посттравматической эпилепсией для II типа ЭЭГ головного мозга.
Изучение особенностей пространственной организации биоэлектрической активности головного мозга на основе когерентного анализа у больных с закрытой ЧМТ выявило характерные особенности распределения когерентности для больных отдаленного и раннего периодов закрытой ЧМТ: показатели когерентности в медленноволновом диапазоне по межцентральным парам отведений были ниже в отдаленном периоде по сравнению с ранним периодом закрытой ЧМТ для всех трех типов ЭЭГ головного мозга. Наиболее заметные влияния по α- и β-актив- ности были получены для межполушарных КОГ с уменьшением в отдаленном периоде закрытой ЧМТ для I и III типа ЭЭГ. Показатели КОГ всех диапазонов по межцентральным парам отведений для «дезорганизованного» и «плоского» типов были ниже в отдаленном периоде закрытой ЧМТ по сравнению с контрольной группой.
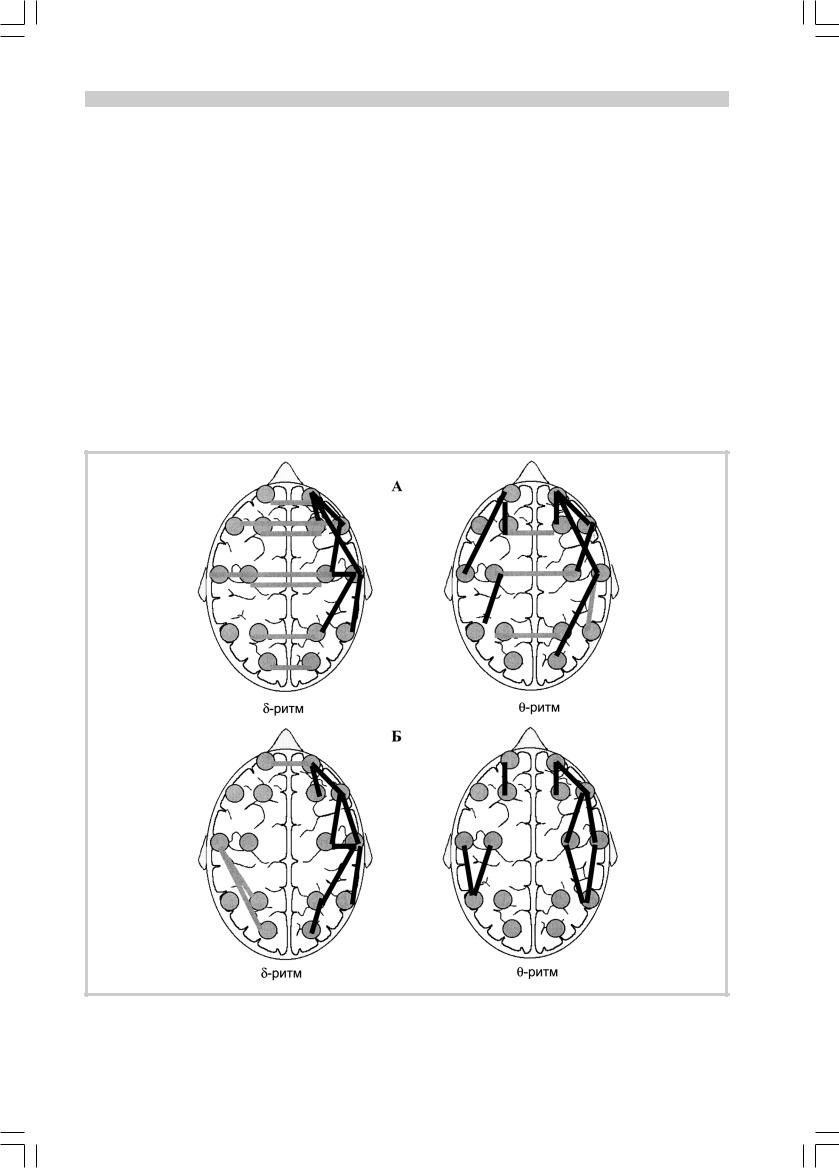
Сравнительный анализ показателей КОГ ЭЭГ больных с посттравматической эпилепсией.
А — фоновая ЭЭГ, Б — время гипервентиляции. Черные линии — достоверное (р<0,05) увеличение показателей когерентности по сравнению со здоровыми, серые линии (р<0,05) — уменьшение показателей когерентности по сравнению со здоровыми.
52 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2007 |

В отличие от внутриполушарной КОГ межполушарная в большей степени характеризует корковоподкорковые взаимодействия и состояние срединных структур мозга. Симметричные лобные и центральные области находятся под большим влиянием подкорковых синхронизирующих структур преимущественно диэнцефального уровня [20]. В экспериментальных исследованиях даже после сотрясения мозга в отдаленном периоде выявляются четкие признаки выраженной активации клеточных мембран и их частичной дезорганизации, преимущественно в диэнцефальной и мезэнцефальной областях [18, 22].
По внутриполушарным связям медленноволнового диапазона в отдаленном периоде закрытой ЧМТ регистрировалось повышение значений КОГ по отношению к ее раннему периоду по левому полушарию для всех типов ЭЭГ; по-видимому, это связано с завершающим этапом компенсаторных процессов, когда возрастает роль левого полушария в формировании характера асимметрии, свойственного здоровому мозгу [4, 10]. Это подтверждается и отсутствием достоверных различий в показателях КОГ как по медленноволновым, так и по α-активности I типа ЭЭГ при закрытой ЧМТ отдаленного периода и при сравнении с контрольной группой.
У больных с СПЭ по всем видам активности (δ-, θ-, α-, β-) отмечается снижение межполушарных связей по сравнению с контрольной группой (см. рисунок). Однако при СПЭ отмечалось увеличение КОГ
ПОСТТРАВМАТИЧЕСКАЯ ЭПИЛЕПСИЯ
преимущественно в правой височной области по сравнению с контролем, что может быть обусловлено левосторонней внутриполушарной асимметрией у здоровых лиц [4].
Гипервентиляция достоверно не изменяет пространственную организацию медленноволновых форм активности ЭЭГ больных с закрытой ЧМТ как в раннем, так и в отдаленном периодах. У пациентов с симптоматической посттравматической эпилепсией (см. рисунок) во время гипервентиляции наблюдалось повышение межполушарных связей по δ- и особенно θ-активности по большинству пар отведений, в основном лобных, центральных, теменных межполушарных пар по сравнению со здоровыми.
В данном исследовании проведен не только сравнительный анализ пространственной организации фоновой ЭЭГ больных с симптоматической посттравматической эпилепсией с контрольной группой (здоровых), но и больных, перенесших закрытую ЧМТ в ее различные сроки и изменения пространственновременных характеристик ЭЭГ во время гипервентиляции. Эти исследования с учетом спектральных характеристик медленноволновых форм активности позволили выявить отличия закрытой ЧМТ от СПЭ, что может быть использовано не только для выявления группы риска возникновения эпилепсии в отдаленном периоде закрытой ЧМТ, но и качественного скрининга противоэпилептических препаратов у больных с симптоматической посттравматической эпилепсией.
ЛИТЕРАТУРА
1.Абзолеев В.А. Системные механизмы эпилепсии. Иркутск 2001.
2.Авакян Г.Н., Генералов В.О., Олейникова О.М. и др. Симптомати- ческая посттравматическая эпилепсия. Клиника, диагностика и лечение. Методические рекомендации. М 2004.
3.Болдырева Г.Н., Манелис Н.Г., Скорятина И.Г., Фролов А.А. Межцентральные отношения электрических процессов мозга человека при вовлечении в патологический процесс лимбических структур. Физиол чел 1997; 23: 2: 42—49.
4.Болдырева Г.Н., Шарова Е.В., Жаворонкова Л.А., Доброхотова Т.А.
Отражение разных уровней регуляции мозговой деятельности человека в спектрально-когерентных параметрах ЭЭГ. Журн высш нерв деят 1992; 42: 1: 62.
5.Бородкин С.М., Гриндель О.М., Болдырева Г.Н. и др. Динамика спектрально-когерентных характеристик ЭЭГ человека в норме и при патологии мозга. Журн высш нерв деят 1987; 37:1: 22—30.
6.Гриндель О.М. Межцентральные отношения электрических процессов мозга человека и их функциональное значение. В кн.: Электрофизиологическое исследование стационарной активности в головном мозге человека. М: Наука 1983.
7.Гриндель О.М. Электроэнцефалограмма человека при ЧМТ. М: Наука 1988; 56—60.
8.Гриндель О.М., Коптелов Ю.М., Машеров Е.Л., Пронин И.Н. Очаги патологической активности в головном мозге человека и их влияние на пространственно-временные отношения ЭЭГ. Журн высш нерв деят 1998; 48: 4: 671—686.
9.Гусев Е.И., Бурд Г. С. Эпилепсия. М 1994.
10.Жаворонкова Л.А., Максакова О.А., Смирнова Н.Я., Кроткова О.А.
Межполушарные соотношения когерентности ЭЭГ при реабилитации больных с тяжелой черепно-мозговой травмой. Физиол чел 2001; 27: 2: 5—14.
11.Коновалов В.Н., Васин Н.Я., Лихтерман Л. Б. Клиническая классификация и построение диагноза ЧМТ. Методические указания. М 1986.
12.Коновалов А.Н., Лихтерман Л.Б., Потапов А.А. Нейротравматология (справочник). М: Вазар-Ферро 1994.
13.Лекомцев В.Т. Ранняя диагностика травматической эпилепсии. Журн невропатол и психиат 1989; 89: 6: 43—46.
14.Лихтерман Л.Б., Потапов А.А., Кравчук А.Д. Классификация последствий ЧМТ. Неврол журн 1998; 3: 3: 12—14.
15.Макаров А.Ю., Садыков Е.А., Киселев В.Н. Посттравматическая эпилепсия: диагностика и клинические варианты. Журн неврол и психиат 2001; 101: 6: 7—11.
11.Макаров А.Ю., Садыков Е.А. Картированная ЭЭГ у больных с эпилептическими припадками в отдаленные периоды череп- но-мозговой травмы. Неврол журн 2000; 5: 2: 15—18.
17.Мерцалов B.C. Нейротравматология. Справочник 1999; 314—316.
18.Ромоданов А.П. Нейрохирургические аспекты последствий закрытой ЧМТ. Республиканский межведомственный сборник. Киев 1989; 22: 36.
19.Садыков Е.А. Посттравматическая эпилепсия (клиника, диагностика, медико-социальная экспертиза): Дис. ... канд. мед. наук. Ст-Петербург 1999.
20.Трофимова Е.В. Особенности межполушарного взаимодействия у правшей и левшей по данным когерентного анализа ЭЭГ. Журн высш нервн деят 2000; 50: 6: 943— 951.
21.Черченко А.П., Белоус А.И., Омельченко Л.Н. Нейрохирургия. Республиканский межведомственный сборник. Киев 1989; 22: 88—91.
22.Черченко А.П., Белоус А.И. Роль гипоталамуса в судорожной готовности травматического генеза. Республиканский межведомственный научный сборник. Киев 1991; 25: 85—86.
23.D’Alessandro R., Ferrara R., Cortelli P. Posttraumatic epilepsy prediction and profilaxis. Arch Neur 1983; 40: 12: 831.
24.Marshall C., Walker E. The Value of electroencephalography in the prognostication and prognosis of posttraumatic epilepsy. Epilepsia 1961; 2: 138—143.
25.Powiektowski H. Posttraumatic. Epilepsy and Pharmakolodicfal prophylaxis. Warszawa 1977; 27—29.
26.Riesner Ò., Zeiler Ê., Wessely P. The Value of CT and EEG in cases of posttraumatic epilepsy. 1979; 93—100.
27.RizzoM., Trannel D. Head injuri and postconcussive syndrome. Livingstone 1996.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2007 |
53 |
