- •Лекция 1 Биоорганическая химия (бох), ее значение в медицине
- •Органическая химия
- •Структурная изомерия
- •Пространственная изомерия (стереоизомерия)
- •Формулы Ньюмена
- •Конфигурационные изомеры
- •Лекция 2 Сопряженные системы
- •Ароматичность
- •Индуктивный эффект
- •Мезомерный эффект
- •Классификация органических реакций
- •Лекция 3 Кислотность и основность
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Монофункциональные соединения Спирты
- •Физические св-ва
- •Химические св-ва
- •Карбокатион
- •Простой эфир
- •Бутен-2
- •Этилфосфат
- •Этаналь
- •Многоатомные спирты
- •Лекция 4 Фенолы
- •Химические свойства
- •Тиоспирты и тиоэфиры
- •Химические св-ва
- •Роль в организме
- •Номенклатура
- •Изомерия
- •Физические св-ва
- •Строение молекулы амина
- •Химические св-ва
- •Алкиламид
- •Замещенный имин
- •Лекция 5 Альдегиды и кетоны
- •Номенклатура
- •Изомерия
- •Физические св-ва
- •Химические свойства
- •Лекция 6 Карбоновые кислоты (кк)
- •Классификация
- •Номенклатура
- •Физические св-ва
- •Химические св-ва
- •Трихлоруксусная Хлороформ
- •Угольная к-та и ее производные
- •Мочевина
- •Химические св-ва
Лекция 6 Карбоновые кислоты (кк)
КК наз-ся соединения, содержащие в молекуле карбоксильную группу – СООН.
Классификация
По числу групп – СООН различают:
одноосновные – СН3–СН2–СООН пропионовая к-та,
двухосновные – НООС–СН2–СООН малоновая к-та,
НООС–СН = СН–СООН фумаровая к-та (транс-форма),
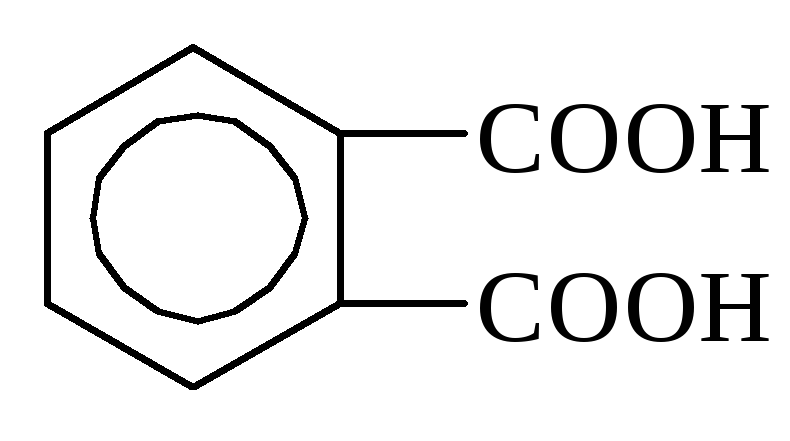
орто-фталевая
к-та,
многоосновные.
По характеру радикала (R) различают:
предельные – СН3–СООН уксусная к-та,
непредельные – СН2 = СН–СООН акриловая к-та,
ароматические – С6Н5–СООН бензойная к-та.
По числу атомов С различают:
низкомолекулярные – уксусная, малоновая, бензойная к-ты,
высокомолекулярные – С17Н35СООН стеариновая к-та,
С17Н33СООН олеиновая к-та.
Следует отметить, что высшие КК, входящие в состав организма имеют четное число атомов С, а непредельные – цис-изомеры. ВКК являются составной частью биологически важных соединений липидов.
Номенклатура
Тривиальная:
|
Н–СООН муравьиная, |
С15Н31СООН пальмитиновая, |
|
СН3–СООН уксусная, |
С17Н35СООН стеариновая, |
|
С2Н5–СООН пропионовая, |
С17Н33СООН олеиновая, |
|
С3Н7–СООН масляная, |
С17Н31СООН линолевая, |
|
С4Н9–СООН валериановая, |
С17Н29СООН линоленовая, |
|
СН2=СН–СООН акриловая, |
НООС–СООН щавелевая, |
|
СН2–СН =СН–СООН кротоновая, |
НООС–СН2–СООН малоновая, |
|
С6Н5–СООН бензойная, |
НООС–(СН2)2–СООН янтарная. |
МН: корень + суффикс + окончание – «овая к-та».
![]()
Остаток к-ты без гидроксильной группы наз-ся ацилом. Название конкретных ацилов производят от латинских названий соответствующих к-т:
![]()
![]()
![]()
Формил Ацетил Бензоил
Название солей строят по названию ацила с заменой окончания –ИЛ на –АТ: формиат, ацетат, бензоат и т.д.
Изомерия обусловлена:
изомерией углеродной цепи;
положением кратной связи для непредельных к-т;
положением заместителей и карбоксильной группы в циклах;
цис-, транс-изомерией.
С троение
карбоксильной группы
троение
карбоксильной группы

|
|
группа проявляет –М и –I, |
|
|
группа проявляет +М > –I. |
В целом группа –СООН – сильный ЭА.
В результате р, -сопряжения связь О Н ослабевает.
Вследствие
близкого расположения ![]() и –ОН групп они оказывают взаимное
влияние друг на друга. Два атома О имеют
-.
Атом С имеет очень малый +.
Поэтому для к-т не характерны р-ции АN
по
и –ОН групп они оказывают взаимное
влияние друг на друга. Два атома О имеют
-.
Атом С имеет очень малый +.
Поэтому для к-т не характерны р-ции АN
по ![]() группе. По причине р, -сопряжения
карбоновые к-ты более сильные к-ты, чем
соответствующие им спирты. Электронная
плотность в карбоксилат-анионе выравнена
и нет двойных и одинарных связей:
группе. По причине р, -сопряжения
карбоновые к-ты более сильные к-ты, чем
соответствующие им спирты. Электронная
плотность в карбоксилат-анионе выравнена
и нет двойных и одинарных связей:
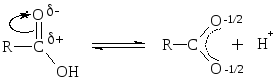
Поэтому карбоксилат-ион стабилен, энергетически устойчив. На силу к-т влияет характер радикала (R). Следовательно, самой сильной к-той гомологического ряда предельных КК является муравьиная. Уксусная к-та уже слабее муравьиной за счет +I радикала –СН3. Ароматические к-ты сильнее алифатических. Бензойная к-та сильнее СН3СООН (бóльшая цепь сопряжения). ЭА заместители увеличивают кислотность, поэтому щавелевая к-та сильнее уксусной, а трихлоруксусная к-та сильнее щавелевой за счет –I трех атомов хлора.
Для карбоновых к-т характерны р-ции замещения Н –ОН группы карбоксила, р-ции замещения –ОН группы, а также замещение атома Н в положении -углеродного атома, т.к. группа –СООН за счет –I увеличивает подвижность атома Н в радикале.