
01.Лечебное дело / Биоорганическая химия / 06.Дополнительно / Всякое / Органическая химия
.pdf
Задачи
I. Строение, изомерия и номенклатура
1. Напишите структурные формулы: а) хлористого пиридиния, β-аминопиридина; б) N-оксида пиридиния, 2-оксипиридина (две таутомерные формы); в) 5-нитроникотиновой кислоты, 4-оксипиридина (две таутомерные формы); г) 2-аминопиридина, 3-нитропиридина; д) γ-пиридона, гидроксида 4-метилпиридиния; е) 2-метилхинолина, иодида N-метилпиридиния; ж) 3-гидроксихинолина, γ-метилпиридина; з) 5-нитроизохинолина, 2-амино-5-винилпиридина; з) 3-метилизо- хинолина, 2,4-диоксипиримидина (три таутомерные формы); и) 6-окси- пурина (две таутомерные формы), 2,5-диизопропоксипиридина; к) 2,6,8- триоксипурина (мочевая кислота) (две таутомерные формы), 2,6- диоксипурина (ксантина) (две таутомерные формы); л) 6-аминопурина, 2- амино-6-оксипурина (две таутомерные формы); м) амида никотиновой кислоты, 5-О-оксиметиленфосфат-2-метил-3-оксипридин-4-карбальдегид (пиридоксальфосфат) (две таутомерные формы).
2.Дайте определение лактим-лактамной таутомерии. Напишите механизм и таутомерные формы (необходимо указать лактим и лактам) для соединений: а) 2-оксипиридин; б) 4-оксипиридин; в) 2-оксипиримидин; г) 4-оксипиримидин; д) 1-оксиизохинолин; е) 3-оксиизохинолин; ж) 2,4- диоксипиридин; з) 2,4-диоксипиримидин (урацил); и) 2-оксипурин; к) 6- оксипурин (гипоксантин); л) 2,6-диокси-пурин (ксантин); м) 2,6,8- триоксипурин (мочевая кислота).
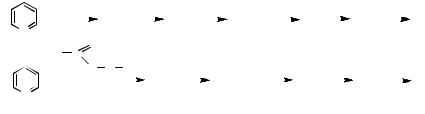
3.Рассмотрите строение молекулы пиридина. Какой тип гибридизации атомных орбиталей атомов углерода и азота? Охарактеризуйте ароматичность пиридина. Опишите распределение электронной плотности. Почему пиридин в отличие от бензола имеет дипольный момент (2,2 D)? Назовите нижеприведённые соединения (в некоторых случаях учтите наличие таутомерных форм соединений):
160
4. Составьте структурные формулы всех возможных изомеров перечисленных ниже соединений, назовите их: а) метилпиридинов (пиколинов), б) диметилпиридинов, в) метилимидазолов, г) диметилимидазолов; д) метилпуринов, е) диметилпуринов, ж) триметилпуринов, з) метилхинолинов, и) диметилхинолинов, к) триметилхинолинов, л) метилизохинолинов, м) диметилизохинолинов.
II. Химические свойства и способы получения. Механизм SN- и SE-реакций
5.Объясните пониженную основность пиридина (Кв = 2∙10-9) по сравнению с триметиламином (Кв = 0,6∙10-4). Сравните взаимодействие пиридина и пиррола с сильными кислотами на холоду. Почему для пиридина не наблюдается осмоления, характерного в этих условиях для пиррола?
6.Сравните основные свойства пиридина, пиперидина и пиримидина и объясните.
7.Получите β-пиколин из акролеина и окислите его.
8.Получите синтезом Скраупа хинолин. Какое соединение получится, если акролеин заменить кротоновым альдегидом?
9.Какия соединения образуются при применении синтеза Скраупа к
следующим соединениям: а) о-нитроанилину, б) о-аминофенолу, в) о-фенилендиамину, г) м-фенилендиамину, д) п-толуидину?
10.Напишите схему получения хинолина способом Скраупа. Приведите все стадии синтеза. Из каких соединений можно осуществить этим путём синтез: а) 6-бромхинолина, б) 8-бромхинолина, в) 2-метилхинолина.
11.Используя синтез изохинолинов по Бишлеру-Напиральскому, получите: а) 1-фенилизохинолин, б) 1-бензилизохинолин, в) 1,5-диметил- изохинолин.
12.Из пиридина перегруппировкой галогеналкилатов получите α- и γ- метилпиридины.
13.Из пиридина получите α-хлорпиридин и напишите уравнения реак-
ций его взаимодействия с CH3ONa, KSH, NН2NH2, NH3. Укажите условия реакций. Напишите механизмы всех реакций.
14.Из пиридина получите β-оксипиридин и β-аминопиридин. Напишите формулы их таутомеров.
161
15. |
Напишите уравнения реакций конденсации α-пиколина с уксусным |
26. Расположите в порядке уменьшения основности следующие соеди- |
|||||||||||||||||||||||
альдегидом, формальдегидом, ацетоном, бензальдегидом (в присутствии |
нения: пиридин, пиррол, анилин, аммиак, метиламин, пиперидин. Объяс- |
||||||||||||||||||||||||
хлорида цинка). Напишите механизмы всех реакций. |
|
ните. |
|||||||||||||||||||||||
16. |
Напишите реакции пиридина |
со следующими |
соединениями: |
27. Какой смысл несут термины «пиррольный атом азота» и «пириди- |
|||||||||||||||||||||
а) соляной кислотой; б) серной кислотой на холоду; в) иодистым метилом; |
новый атом азота»? Чем они отличаются? Для перечисленных ниже со- |
||||||||||||||||||||||||
г) триоксидом серы; д) пероксидом водорода. Какие свойства проявляет |
единений напишите уравнения реакций с растворами бромистоводород- |
||||||||||||||||||||||||
пиридин в этих реакциях? Назовите полученные соединения. |
ной и серной кислот, иодистым этилом, перекисью водорода: а) пурин, |
||||||||||||||||||||||||
17. |
Как отличить хинолин от изохинолина? |
|
б) аденин, г) гуанин, д) имидазол, е) имидазолил-2-карбоновая кислота, |
||||||||||||||||||||||
18. |
На каком свойстве изохинолина основано отделение его от хиноли- |
ж) мочевая кислота, з) 2,6-диоксипурин (ксантин). |
|||||||||||||||||||||||
на? |
|
|
|
28. Укажите все возможные типы реакций и ориентацию реагентов |
|||||||||||||||||||||
19. |
Напишите уравнения реакций взаимодействия пиперидина с HCl, |
(где нужно) для: а) цитозина; б) урацила; в) тимина; г) аденина; |
|||||||||||||||||||||||
HNO2, (CH3CO)2O, C6H5COCl, CH3I. Какие свойства проявляет пиперидин |
д) гуанина. |
||||||||||||||||||||||||
в этих реакциях? Назовите полученные соединения. |
|
29. Получите акридин из дифенила и муравьиной кислоты. Подвергни- |
|||||||||||||||||||||||
20. |
Напишите уравнения реакций хинолина с CH3I, NaNH2, KOH, |
те акридин окислению и восстановлению. Где используется акридин? |
|||||||||||||||||||||||
HNO3, Na в кипящем спирте. |
|
|
30. Какие гетероциклы входят в состав рибофлавина? Укажите хими- |
||||||||||||||||||||||
21. |
Отметьте сходство и различие в свойствах пиридина и бензола. |
ческие изменения при участии его в окислительно-восстановительных |
|||||||||||||||||||||||
Объясните малую активность пиридина в реакциях электрофильного за- |
процессах. |
||||||||||||||||||||||||
мещения и повышенную активность в реакциях нуклеофильного замеще- |
31. Установите строение соединения состава C11H11N, при окислении |
||||||||||||||||||||||||
ния. Приведите следующие реакции пиридина: а) бромирования; б) нитро- |
которого хромовым ангидридом образуется 8-хинолинкарбоновая кислота. |
||||||||||||||||||||||||
вания; в) сульфирования; г) взаимодействия с амидом натрия; д) с гидро- |
32. При окислении вещества С9H7N щелочным раствором KMnO4 обра- |
||||||||||||||||||||||||
ксидом калия. В каких условиях протекает каждая реакция? В какое поло- |
зуется 2,3-пиридиндикарбоновая кислота и выделяется газ, вызывающий |
||||||||||||||||||||||||
жение вступают замещающие группы? Дайте объяснения. |
|
помутнение баритовой воды. Установите структуру данного вещества. |
|||||||||||||||||||||||
22. |
С какими из приведенных ниже соединений реагирует пиридин? |
33. При сжигании (н.у.) азотсодержащего гетероциклического соеди- |
|||||||||||||||||||||||
Приведите схемы возможных реакций: а) бромоводород; б) серная кисло- |
нения, не содержащего заместителей в кольце, образовалось 0,75 моль |
||||||||||||||||||||||||
та, 0° С; в) серная кислота, триоксид серы, 350° С; г) азотная кислота, сер- |
диоксида углерода, 0,375 моль воды и 0,075 моль азота. Установите струк- |
||||||||||||||||||||||||
ная кислота, 300° С; д) Вr2, ССl4; е) |
Вr2, 350° С; ж) |
КМnO4, НОН; |
туру вещества. |
||||||||||||||||||||||
з) СН3СООН; и) С2Н5Вr; к) уксусный ангидрид; л) хлорангидрид уксусной |
34. Определите структуру вещества С9H7N, если известно, что при |
||||||||||||||||||||||||
кислоты, АlСl3; м) КОН, НОН; н) КОН (тв.), O2, t°; о) NaNH2, NН3(ж). |
окислении его кислым раствором KMnO4 образуется смесь фталевой и 3,4- |
||||||||||||||||||||||||
23. |
Приведите реакции получения N-оксида пиридина. Сравните его |
пиридиндикарбоновой (цинхомероновой) кислот. |
|||||||||||||||||||||||
отношение и отношение пиридина к электрофильным и нуклеофильным |
35. Определите строение вещества C5H6N2, если известно, что при по- |
||||||||||||||||||||||||
реагентам. Напишите для N-оксида пиридина реакции: а) нитрования, |
пытке диазотировать его происходит гидролиз, а при взаимодействии с |
||||||||||||||||||||||||
б) сульфирования, в) взаимодействия с бутиллитием. В какое положение |
концентрированной H2SO4 образуется аминопиридинсульфокислота. |
||||||||||||||||||||||||
вступают замещающие группы? Приведите объяснения. |
|
36. Заполните схемы превращений, назовите полученные продукты по |
|||||||||||||||||||||||
24. |
Рассмотрите отношение к действию окислителей: а) бензола; |
номенклатуре IUPAC: |
|||||||||||||||||||||||
б) нафталина; в) фурана; г) пиррола; д) пиридина; е) хинолина. Напишите |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
уравнения реакций: а) нафталин + оксид хрома (VI) (уксусная кислота); |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
б) хинолин + КМnO4, НОН, нагревание; в) бензофуран + дихромат калия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
(серная кислота). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
25. |
Расположите в порядке возрастания реакционной способности в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
условиях электрофильного замещения: бензол, нафталин, тиофен, пири- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
дин. Напишите уравнения реакций бромирования каждого соединения. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Укажите условия их проведения. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
162 |
|
163 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
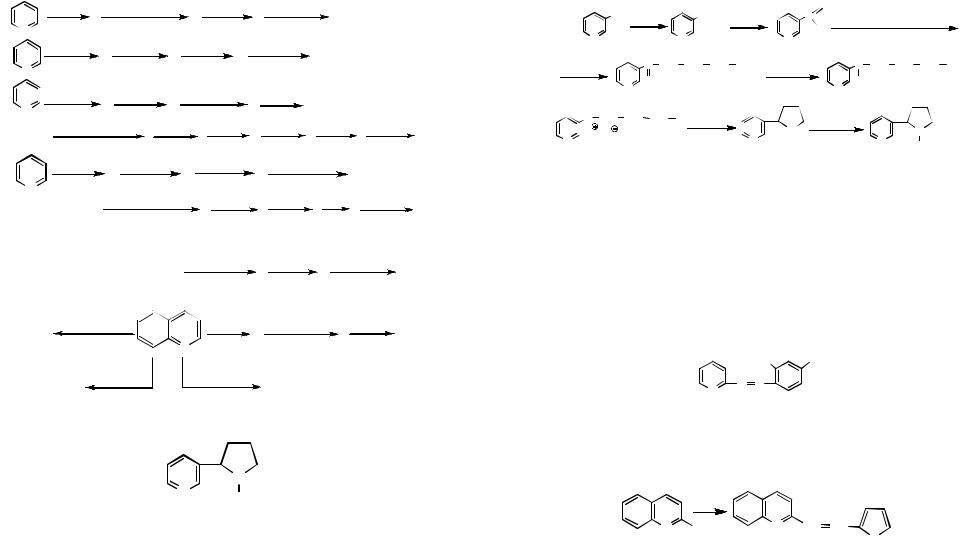
37. Напишите уравнения реакций, обозначенных на схеме. Приведите структурные формулы веществ А– К.
38. Алкалоид никотин
был впервые выделен из листьев табака Nicotiana tabacum. Ниже представлена схема одного из лабораторных методов синтеза никотина. Напишите реагенты и условия протекания реакций, обозначенных на схеме цифрами 1–7:
164
III. Задания по синтезу веществ
39.Сульфидин получают из α-аминопиридина и хлорангидрида ацетилсульфаниловой кислоты. В вашем распоряжении имеются пиридин, бензол, уксусная кислота и необходимые неорганические вещества. Осуществите синтез сульфидина.
40.Как можно осуществить переход от α-пиколина к α-амино- пиридину?
41.Приведите схемы получения из пиридина: а) 2-, 3- и 4-амино- пиридинов; б) никотиновой кислоты; в) 2-фенилпиридина.
42.Предложите синтез металлохромного индикатора 1-(2-пиридилазо)- 2,4-дигидроксибензола (ПАР) из бензола, пиридина и неорганических веществ.
43.Из пиридина и других необходимых реагентов получите изомерные α-, β- и γ-фторпиридины.
44.Предложите метод синтеза 3-ацетилпиридина, исходя из пиридина
ииспользуя другие необходимые реагенты.
45.Получите 3-оксипиридин из пиридина и неорганических реагентов.
46.Как осуществить следующее превращение:
47.Предложите схемы следующих переходов: а) пиридин → N-метил- 2-аминопиридин, б) пиридин → 3-(бромфенилметил)пиридин.
165
МОДУЛЬ 6. МНОГОФУНКЦИОНАЛЬНЫЕ И ПРИРОДНЫЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Тема 25. Дикарбоновые кислоты. Альдегидо- и кетокислоты
Контрольные вопросы
1.Как меняется сила кислот в зависимости от расположения второй функциональной группы?
2.Сравните реакционную способность карбонильной группы в альдегидо- и кетонокислотах с карбонильной группой альдегидов и кетонов. Ответ поясните.
3.Дайте понятия «О-Н» и «С-Н» кислотам. Приведите уравнения реакций, подтверждающие кислотные свойства по С-Н связям у дикарбоновых кислот и кетонокислот.
4.Какие особые свойства дикарбоновых кислот и кетонокислот используют в органическом синтезе? Приведите примеры.
Задачи
I. Строение, изомерия и номенклатура
1.Составьте структурные формулы следующих кислот; назовите кислоты по номенклатуре IUPAC: а) этилмалоновой, глиоксиловой; б) диметилмалоновой, пировиноградной; в) α,α-диметилянтарной, ацетоуксусной; г) β,β-диметилглутаровой, α-метил-α-изопропилацетоуксусной; д) α,β-ди- метилглутаровой, левулиновой; е) α,β-диметоксиглутаровой, δ-оксо- валериановой; ж) лимонной, фумаровой кислот; з) щавелевоуксусной, фумаровой; и) малеиновой, янтарной.
2.Напишите структурные формулы изомерных двухосновных кислот,
имеющих общую формулу: а) С3Н6(СООН)2 – четыре изомера; б) С4Н8(СООН)2 – восемь изомеров. Назовите их по тривиальной и систематической номенклатурам.
3. Напишите все возможные изомеры α-кетоглутаровой кислоты. Назовите их по тривиальной и систематической номенклатурам.
I) Химические свойства и способы получения
4.Как, имея этанол и необходимые неорганические вещества, можно получить: а) щавелевую; б) малоновую кислоты? Напишите уравнения реакций. Назовите вещества.
5.Уксусную, пировиноградную, щавелевую кислоты расположите в порядке понижения кислотности. Выберите для них константы ионизации: 5,90∙10-2; 3,2 10-4; 1,76∙10-5. Ответ аргументируйте.
166
6.Расположите перечисленные ниже кислоты в порядке увеличения их кислотности; ответ аргументируйте: щавелевая, малоновая, янтарная и адипиновая.
7.Напишите уравнение реакции взаимодействия ацетоуксусного эфира с: а) циановодородом, б) гидросульфитом натрия, в) гидроксиламином, г) хлористым ацетилом, д) натрием, е) бромом. Назовите все вещества.
8.Напишите структурную формулу алкилацетоуксусного эфира, который при кислотном расщеплении образует 3-метилпентановую кислоту. Какие продукты образуются при кетонном расщеплении этого эфира?
9.Имея этанол и необходимые неорганические вещества, синтезируйте янтарную кислоту.
10.Имея пропионовую кислоту, получите метилмалоновую кислоту.
11.Напишите уравнения реакций, происходящих при нагревании щавелевой, малоновой, метилмалоновой, диметилмалоновой, глутаровой кислот. Назовите вещества.
12.Напишите уравнения реакций глиоксиловой кислоты с гидросульфитом натрия, циановодородом, гидроксиламином, аммиачным раствором гидроксида серебра, гидроксидом натрия (40%) в избытке. Назовите продукты.
13.Напишите уравнения реакций взаимодействия пировиноградной кислоты (ПВК) со следующими веществами: гидрокарбонатом натрия, этанолом в кислой среде, циановодородом, фенилгидразином, гидросульфитом натрия. Что происходит с ПВК при нагревании? Назовите продукты.
14.Напишите уравнения реакций взаимодействия этилового эфира хлоруксусной кислоты с натриймалоновым эфиром, гидролиза полученного вещества и последующего за этим декарбоксилирования.
15.Имея пропионовую кислоту и необходимые вещества, получите диэтилмалоновую кислоту.
16.Напишите уравнения реакций получения: а) из пропена – метилянтарной кислоты; б) из этанола – метилмалоновой кислоты; в) из метилэтилкарбинола – 2,3- диметилбутановой кислоты; г) из этанола – щавелевой кислоты; д) из глицерина – метилмалоновой кислоты.
17.Составьте схему таутомерного кето-енольного превращения ацетоуксусного эфира. Объясните механизм превращения.
18.На этиловый эфир α-хлорпропионовой кислоты подействовали натрийацетоуксусным эфиром. Полученное производное было подвергнуто кислотному расщеплению. Напишите уравнение реакции и назовите полученные вещества.
19.На ацетоуксусный эфир подействовали этилатом натрия, а затем бромбутаном. Реакционную массу разделили попалам. На одну её часть
167
подействовали разбавленной щёлочью, на другую – концентрированной щёлочью. Назовите полученные вещества.
20.Объясните причину подвижности атомов водорода в метиленовой группе ацетоуксусного эфира. Напишите уравнения реакций конденсации ацетоуксусного эфира с уксусным альдегидом; с этиловым эфиром акриловой кислоты (реакция Михаэля).
21.Предскажите, какие соединения (в зависимости от их мольных со-
отношений) образуются в следующих реакциях: а) адипиновая кислота
(146 г) + 95%-ный этанол (146 г) + бензол + конц. H2SO4, 100оС; б) адипи-
новая кислота (146 г) + 95%-ный этанол (50 г) + бензол + конц. H2SO4, 100оС; в) адипиновая кислота (146 г) + этиладипинат (101 г) + конц. H2SO4, 160оС; г) этилоксолат (избыток) + (C2H5)2NH; д) этилоксолат +
(C2H5)2NH (избыток); е) этилоксолат (1 моль) + о-фенилендиамин (1 моль); ж) янтарный ангидрид (1 моль) + этанол (1 моль), HÅ.
22. Приведите схемы синтеза получения кетокислот путём конденсации соответствующих сложных эфиров по Кляйзену: а) этил-α- фенилбензоилацетата (С6Н5-С(О)-СН(С6Н5)-С(О)-ОС2Н5); б) С6Н5С(О)СН(СН3)С(О)ОС2Н5.
II. Синтезы С-С-связей на основе ацетоуксусного и малонового эфиров
23.Напишите уравнения реакций получения на основе ацетоуксусного эфира: а) метилпропилкетона; б) 3-метил-2-пентанона; в) гексанона-2; г) 4-метилпентанона-2; д) 3-метилпентанона-2; е) пентандиона-2,4 (ацетилацетона); ж) гександиона-2,5 (ацетонилацетона); з) 1- фенилпентадиона-1,4; и) пропановой кислоты; к) диметилуксусной кислоты; л) изопропилуксусной кислоты; м) метил-втор-бутилкетона.
24.Напишите уравнения реакций получения на основе малонового эфира: а) метилянтарной кислоты, б) пропионовой кислоты, в) изомасля-
ной кислоты, г) изовалериановой кислоты, д) валериановой кислоты, е) лейцина (α-аминоизокапроновой кислоты), ж) капроновой кислоты, з) β- метилмасляной кислоты, и) глутаровой кислоты, к) дибензилуксусной кислоты, л) 2-этилбутановой кислоты, м) α,β-диметилянтарной кислоты.
III. Определение строения соединений
25.Вещество С7Н12O3 не реагирует с раствором соды, не даёт окрашивания с хлоридом железа (III). При нагревании с концентрированным раствором щёлочи подвергается расщеплению, одним из продуктов которого является изомасляная кислота (выделяется при подкислении). Установите строение исходного вещества.
26.Установить строение вещества состава С4Н6О4, которое обладает кислотными свойствами, при взаимодействии с этанолом в присутствии минеральной кислоты даёт новое вещество состава С8Н14О4. Исследуемое
168
соединение при нагревании выделяет СО2 и образует вещество состава С3Н6О2, обладающее кислотными свойствами. Напишите уравнения соответствующих реакций.
27.Определите строение вещества состава С4Н6О4, водный раствор которого даёт кислую реакцию на лакмус, а при взаимодействии с разбав-
ленным раствором гидроксида натрия даёт вещество состава С4Н4О4Na2. При нагревании исследуемое вещество даёт соединение состава С4Н4О3. Напишите уравнения соответствующих реакций.
28.Определите строение вещества состава С5Н8О4. При нагревании это вещество выделяет СО2 и образует кислоту нормального строения. При взаимодействии с этанолом в присутствии минеральной кислоты образу-
ется вещество состава С9Н16О4. Последнее взаимодействует с металлическим натрием и выделяет при этом водород. Напишите уравнения соответствующих реакций.
29.Установите строение соединений по брутто-формуле и их химиче-
ским превращениям. Напишите уравнения реакций: а) С3Н4О4, обладает кислыми свойствами, с этанолом даёт соединение состава С7Н12О4, при нагревании исходного вещества выделяется СО2 и образуется вещество С2Н4О2, водный раствор которого также имеет рН<7; б) С6Н8О4, обесцвечивает раствор брома, при озонолизе даёт только пировиноградную кислоту, а при нагревании выделяет воду и превращается в циклическое со-
единение С6Н6О3; в) С6Н10О4, при обрабоке водным раствором NaOH образует метанол и соединение С4Н4О4Na2, последнее при подкислении выделяет С4Н6О4, легко теряющее при нагревании СО2 с образованием пропионовой кислоты; г) С4Н6О4, водный раствор соединения при обработке гидрокарбонатом натрия выделяет газ, который с известковой водой обра-
зует белый осадок, при этом образуется С4Н4О4Na2, исходное вещество при нагревании теряет воду, превращаясь в С4Н4О3; д) С5Н8О4, при взаимодействии с этанолом в прис. HCl образует С9Н15О4, при нагревании декарбоксилируется с превращением в вещество С4Н8О2, которое реагирует
ссодой с выделением СО2.
30.Установите строение β-кетоэфира по брутто-формуле и продуктам кетонного и кислотного распадов (в сложноэфирной группе радикалы
имеют нормальное строение): а) С9Н16О3, гексанон-3, масляная кислота; б) С7Н12О3, бутанон, пропионовая кислота; в) С7Н12О3, пентанон-3, пропионовая кислота.
Тема 26. Оксикислоты
Контрольные вопросы
1. Чем объяснить сходство и отличие свойств спиртовой и кабоксильной гидроксигрупп? Ответ подтвердите уравнениями реакций.
169
2.Как проявляется взаимное влияние атомов на кислотные, основные и особые свойства гидроксикислот? Ответ подтвердите соответствующими уравнениями реакций.
3.Какие виды изомерии характерны для гидроксикислот? Приведите примеры.
4.На примере гидроксикислот дайте характеристику оптической изомерии. Что понимают под асимметрией углеродного атома, молекулы? Дайте определение понятиям: проекционная формула Фишера, абсолютная (R-, S-) и относительная конфигурации центра хиральности, D- и L- стереохимические ряды, энантиомеры (оптические антиподы), диастереоизомеры, мезоформы, рацемат, «+» и «-» вращение. Как определяют число оптических изомеров?
5.Напишите уравнения реакций, отражающие основные способы получения гидроксикислот.
Задачи
I. Строение, изомерия и номенклатура
1.Напишите проекционные формулы Фишера хлоряблочных кислот. Почему у хлоряблочных кислот нет изомера, подобного мезовинной кислоте?
2.Приведите проекционные формулы Фишера стереоизомерных яблочных (оксиянтарных) кислот. Существут ли среди этих изомеров мезо- форма?
3.Винные кислоты относятся к двухосновным четырёхатомным оксикислотам. Изобразите их проекционные формулы и определите абсолютную конфигурацию.
4.В молекулах бромяблочных кислот, так же, как и в молекулах винных кислот, имеется два асимметрических углеродных атома. Объясните, а) почему у бромяблочных кислот четыре оптически активных изомера, а
увинных – два, б) почему среди бромяблочных кислот нет изомера, подобного мезовинной кислоте?
5.Известно, что при окислении по реакции Вагнера фумаровая кислота образует D-, L-винные кислоты (рацемическую смесь), а малеиновая — мезовинную. Объясните это явление.
6.Из двух альтернативных выберите правильное. «Рацематы имеют: а) такую же температуру плавления, как и стереоизомеры, составляющие смесь, б) плавятся при иной температуре; а) рацематы можно разделить физическими и химическими способами, б) рацематы нельзя разделить физическими способами». Ответ мотивируйте.
7.Приведите проекционные формулы всех оптических изомеров и определите их абсолютную конфигурацию для следующих соединений:
170
8.Напишите структурные формулы
 оксикислот: а) α-окси- валериановой, β-оксивалериановой; б) γ-оксикапроновой, α-окси- капроновой; в) δ-оксикапроновой, молочной.
оксикислот: а) α-окси- валериановой, β-оксивалериановой; б) γ-оксикапроновой, α-окси- капроновой; в) δ-оксикапроновой, молочной.
9.Для соединений, которые приведены ниже, определите число оптических изомеров и их абсолютную конфигурацию: а) 2-окси-3-метил- бутановая кислота; б) яблочная кислота; в) аминояблочная кислота; г) α,β- диоксимасляная кислота; д) 2-оксициклогексанкарбоновая кислота.
10.Приведите структурные формулы все изомеров оксикислот (в том
числе оптических, если таковые существуют) состава: а) С2Н4О3,
б) С3Н6О3, в) С4Н8О3, г) С5Н10О3. Назовите их по систематической номенклатуре.
II. Химические свойства и способы получения
11.В лаборатории имеются следующие реактивы: натрий, карбонат натрия, гидроксид натрия, этанол, фенол, хлористый бензоил, уксусный ангидрид, аммиак, бромистоводородная кислота, пятихлористый фосфор, алюмогидрид лития и пероксид водорода (окислитель). Как эти вещества будут реагировать с приведёнными ниже оксикислотами? Напишите уравнения реакций в тех случаях, когда они имеют место. Для оксикислот, содержащих асимметрический атом углерода, изобразите проекционные формулы Фишера для D- и L-изомеров: а) молочная кислота; б) салициловая (о-оксибензойная) кислота; в) яблочная (2-оксибутадионовая) кислота; г) миндальная (α-оксифенилуксусная) кислота; д) глицериновая (2,3- диоксипропановая) кислота; е) винная (2,3-диоксибутадионовая) кислота; ж) п-оксибензойная кислота; з) тартроновая (2-оксипропандиовая) кислота; и) сиреневая (4-окси-3,5-диметоксибензойная) кислота; к) гликолевая (оксиуксусная) кислота; л) β-оксимасляная кислота; м) γ-окси- валериановая кислота.
12.Молочную кислоту можно получить несколькими способами: из уксусного альдегида, из 2-хлорпропановой кислоты, из пировиноградной кислоты, из ацетилена. Напишите уравнения реакций.
13.Как можно получить из пропанола: а) молочную, б) 2-гидрокси-2- метилпропановую кислоты. Напишите уравнения реакций. Назовите все вещества.
14.3-Гидроксибутановую кислоту можно получить исходя из уксусного альдегида. Приведите соответствующие уравнения реакций.
171
15.Напишите уравнения реакций получения лимонной кислоты, взяв за исходное соединение ацетон.
16.Какие β-оксикислоты можно получить в условиях реакции Рефор-
матского, если за исходные соединения взять следующие вещества: а) этиловый эфир 2-бромпропановой кислоты и этаналь, б) этиловый эфир бромуксусной кислоты и ацетон, в) этиловый эфир 4-бром-2-бутеновой кислоты и пропаналь. Напишите уравнения реакций.
17.Имея пропанол и необходимые органические вещества, получите 2- гидроксибутановую кислоту.
18.Напишите уравнения и механизмы реакций, характеризующие свойства следующих гидроксикислот: а) молочной, б) 4-гидроксигеп- тановой, в) 2,3-дигидроксибутандиовой.
19.Осуществите следующие превращения. Назовите конечные продукты по номенклатуре IUPAC:
20.Напишите схемы синтеза оксикислот и их производных: а) 3-окси- 3-метилбутановой кислоты по реакции Реформатского; б) 3-окси-3- метилпентановой кислоты по реакции Реформатского; в) β-окси-β-фенил- α-метилпропионовой кислоты по реакции Реформатского; г) β-окси-β- фенилмасляной кислоты по реакции Реформатского; д) β-окси- валериановой кислоты по реакции Реформатского; е) этиллактата из ацетилена; ж) аспирина (О-ацетилсалициловой кислоты) из фенола.
21.Как с помощью химических проб различить изомерные вещества: а) миндальную и салициловую кислоты; б) метиловый эфир гликолевой кислоты и метоксиуксусную кислоту?
III. Определение строения соединений
22. Определите строение вещества состава С4Н8О3, которое при взаимодействии с этанолом даёт сложный эфир состава С6Н12O3. Исследуемое вещество при нагревании выделяет воду и образует соединение состава С4Н6O2. Последнее обнаруживает кислую реакцию, присоединяет бром, а при энергичном окислении кислым раствором перманганата калия даёт уксусную и щавелевую кислоты. Напишите уравнения реакций и назовите все вещества.
172
23.Определите строение вещества состава С3Н6О3, которое обнаруживает кислотные свойства, при взаимодействии с этанолом образует веще-
ство состава С5Н10O3, а с уксусной кислотой – С5Н8O4. Последнее вещество при действии щёлочи вновь образует исходное вещество. Если исследуемое вещество нагреть, то образуется новое вещество состава С6Н8О4.
24.Вещество состава С4Н8О3 обладает кислотными свойствами, вращает плоскость поляризованного света, при взаимодействии с хлороводо-
родом даёт соединение состава С4H7O2Cl, а при действии хлорида фосфора (V) — C 4H6OCl2. При нагревании исследуемое вещество образует соединение C8H12O4. Определите строение вещества. Напишите уравнения реакций. Назовите все вещества.
25.Вещество состава С4Н8О3 в растворе обнаруживает кислую реакцию, при нагревании выделяет воду, образуя вещество состава С4Н6O2, которое при восстановлении образует тетрагидрофуран, а при действии
хлороводорода исходное вещество даёт соединение состава С4Н7O2Сl. Вещество С4Н6O2 может быть получено восстановлением янтарного ангидрида. Установите строение вещества. Напишите все уравнения реакций. Назовите вещества.
26.Определите строение молекулы вещества состава С3Н6О3, которое обнаруживает кислотные свойства; при взаимодействии с этанолом обра-
зует вещество состава С5Н10О3, а с уксусной кислотой – С5Н8О4. При нагревании исследуемое вещество образует соединение состава С6Н8О4.
27.Определите строение молекулы вещества состава С4Н8О3, которое при взаимодействии с этанолом образует соединение состава С6Н12О3. При нагревании исследуемое вещество образует соединение состава С4Н6О2, которое обнаруживает кислую реакцию, присоединяет бром, а при энер-
гиичном окислении кислым раствором KMnO4 даёт уксусную и щавелевую кислоты.
28.Установите строение соединений по брутто-формуле и их химиче-
ским превращениям. Напишите уравнения реакций: а) С8Н8О3, растворяется в воде и водном растворе щёлочи, образует сложные эфиры с кислотами и спиртами, не даёт реакции с FeCl3, реагирует с PCl5, образуя вещест-
во С8Н6OCl. Известно в виде двух оптически активных изомеров; б) С6Н12О3, оптически активно, с основаниями образует соль, при нагревании даёт соединение С6Н10О2, которое, окисляясь перманганатом калия при нагревании, превращается в смесь изомасляной и щавелевой кислот; в) С9Н10О3, получают из алкалоида атропина, находящегося в белладонне Atropa belladonna, при окислении горячим перманганатом калия в кислом растворе даёт бензойную кислоту, реагирует с одним эквивалентом NaOH и двумя эквивалентами Na; г) С4Н8О3, водный раствор имеет рН<7, обладает оптической активностью, при взаимодействии с HCl образует соединение C4H7O2Cl, а при обработке PCl5 – соединение C4H6OCl2, может быть
173
получено |
циангидридным синтезом из карбонильного соединения; |
д) С5Н10О3, |
вещество кислого характера, при дегидратации образует |
С5Н8О2 (также кислого характера), которое присоединяет бром с образованием дибромпроизводного, при окислении даёт смесь пропионовой и щавелевой кислот; е) С8Н8О3, реагирует с одним эквивалентом NaOH, не даёт окрашивания с FeCl3, окисляясь перманганатом калия при нагревании, переходит в терефталевую кислоту.
Тема 27. Аминокислоты
Контрольные вопросы
1.Свойства каких соединений проявляют аминокислоты? Приведите уравнения соответствующих реакций.
2.Как влияют функциональные группы друг на друга? Ответ мотивируйте. Почему рН растворов аминокислот близка к нейтральной?
3.Что понимают под амфотерностью свойств?
4.В каких реакциях проявляются амфотерные свойства аминокислот? Приведите уравнения реакций.
5.Какие свойства аминокислот рассматривают как особые? Приведите уравнения реакций.
6Что называют пептидной связью? В чем заключаются особенности синтеза пептидной связи in vitro и in vivo?
7.Почему аминокислоты относят к биогенным соединениям? Какова роль аминокислот в живой природе?
8.Какие аминокислоты называют незаменимыми? Приведите способы получения некоторых незаменимых аминокислот,
Задачи
I. Строение, изомерия и номенклатура
1. Составьте структурные формулы аминокислот: а) β-амино- валериановая, α-аминоизовалериановая; б) γ-аминоизокапроновая, 2-амино-3-метилпентановая; в) 2,5-диаминогексановая, 2-аминобутан- диовая; г) N-ацетиламиноуксусная, 2-аминоциклогексанкарбоновая, д) 3- амино-4-метилпентановая, 2-амино-3-меркаптопропановая кислота; е) α-аминоциклогексанкарбоновая, 2-амино-3-оксипропановая; ж) α,δ-ди- аминовалериановая, α-аминоглутаровая; з) β-аминопропионовая, аминомалоновая; и) α-амино-β-оксимасляная, 2-амино-4-метилтиобутановая; к) 2-амино-3-(4-имидазолил)пропионовая, 2-амино-3-метилпентановая; л) п- аминобензойная, N-бензоил-2-аминопропионовая, м) аминобутандиовая, аминоацетиламид.
2. Приведите структурные формулы приведённых ниже изомерных аминокислот. Для оптически активных изомеров определите конфигура-
174
цию антиподов по Кану– Прелогу– Ингольду: а) C5H9NO4, б) C6H13NO2,
в) C6H14N2O2, г) C4H9NO3, д) C4H7NO4, е) C5H11NO2, ж) C7H13NO2 (произ-
водные циклогексана), з) C6H11NO2, и) C7H7NO2.
3. Напишите структурные формулы всех возможных изомеров для следующих природных аминокислот: а) аланина, б) лейцина, в) серина. Назовите их. Для оптически активных изомеров определите конфигурацию антиподов по Кану– Прелогу– Ингольду.
II. Химические свойства и способы получения
4. Напишите уравнения реакций и назовите образующиеся соединения: а) β-фенил-α-аланина с пятихлористым фосфором, серина с гидроксидом калия, глицина с избытком иодистого метила, окисления цистеина кислородом воздуха, разложения 4-аминогексановой кислоты при нагревании, восстановления 3-аминопропионовой кислоты алюмогидридом лития;
б) валина с п-нитрофенолом, 3-оксипролина с разбавленной серной кислотой, метилового эфира серина с азотистой кислотой, изолейцина с пятихлористым фосфором, глицина с гидроксидом меди, β-фенил-α-аланина с изопропиловым спиртом (в прис. НСl);
в) β-аланина с гидроксидом натрия, гиппуровой кислоты с хлористым тионилом, циклизации при нагревании метилового эфира α-амино- валериановой кислоты, дихлоргидрата лизина с нитратом серебра (1:2), щелочного гидролиза аспарагина, натриевой соли фенилаланина с 2,4- динитрофторбензолом;
г) глицина с избытком бромистого этила, аспарагина с азотистой кислотой (1:2), хлоргидрата изолейцина с аммиаком, восстановления цистина цинком в соляной кислоте, α-аланина с формальдегидом, лейцина с бутиловым спиртом (в прис. НСl);
д) серина с водным раствором аммиака, тирозина с метанолом (в прис. НСl), натриевой соли метионина с 2,4-динитрофторбензолом, циклизации при нагревании метилового эфира 4-амино-5-метилгексановой кислоты, валина с азотистой кислотой; декарбоксилирования орнитина;
е) валина с метиловым спиртом (в прис. НСl), аспарагиновой кислоты с гидроксидом натрия (1:2), разложения 3-аминопентановой кислоты при нагревании, лейцина с избытком хлористого метила, натриевой соли пролина с хлористым ацетилом, лизина с азотистой кислотой (1:2);
ж) валина с трет-бутилоксикарбонилхлоридом, глицина с ангидридом трифторуксусной кислоты, аспарагиновой кислоты с азотистой кислотой, α-аланина с этиловым спиртом (в прис. НСl), изолейцина с формальдегидом, гидролиза дикетопиперазина при кипячении с НСl;
з) лизина с раствором гидроксида натрия, этилового эфира α-аланина с азотистой кислотой, валина с избытком иодистого метила, 2,4-ди-
175
нитрофторбензола с изолейцином, циклизации ε-аминокапроновой кислоты при нагревании; окисления цистеина;
и) метилового эфира метионина с п-толуолсульфохлоридом, α-аланина
сбромистым нитрозилом, изолейцина с п-нитрофенолом, циклизации этилового эфира валина при нагревании, глицина с азотистой кислотой, α-фенил-β-аланина с пятихлористым фосфором;
к) валина с соляной кислотой, серина с хлористым ацетилом, α-аланина
сизобутиленом (в прис. минеральной кислоты); глутаминовой кислоты с гидроксидом калия (1:2), глицина с пропиловым спиртом (в прис. НСl), циклизации δ-аминовалериановой кислоты при нагревании;
л) N-бензоилглицина (гиппуровой кислоты) с хлористым тионилом, валина с гидроксидом натрия, лизина с хлористым ацетилом (1:2), изолейцина с азотистой кислотой, глицина с формальдегидом, лейцина с 2,4-ди- нитрофторбензолом;
м) α-аланина с гидроксидом меди (II), валина с хлорангидридом пропионовой кислоты, лизина с метанолом (в прис. НСl), N-ацетилпролина с пятихлористым фосфором, изолейцина с избытком иодистого метила.
5.Напишите перечисленные ниже аминокислоты в цвиттер-ионной форме. Напишите уравнения реакций цвиттер-иона соответствующей аминокислоты с хлористоводородной кислотой, после чего подействуйте на образовавшийся продукт гидроксидом натрия: а) тирозин, б) фенилаланин, в) гистидин, г) глицин, д) изолейцин, е) серин, ж) цистеин, з) пролин, и) лейцин, к) лизин, л) глутаминовая кислота, м) триптофан.
6.Что образуется при действии на аланин: КОН, аммиака, НСl, уксусного ангидрида, нагревания? Напишите уравнения реакций. Назовите все вещества.
7.Какое вещество получится при последовательном действии на пропановую кислоту брома (1 моль), триметиламина, влажного оксида серебра. Напишите уравнения реакций. Назовите все вещества.
8.Уксусный альдегид был обработан НСN. Полученное соединение – аммиаком, а затем подвергнуто кипячению с НСl. Составьте уравнения реакций. Назовите вещества.
9.Напишите уравнения реакций взаимодействия 2-аминопентановой кислоты с хлоридом фосфора (V), этанолом в кислой среде, иодметаном, азотистой кислотой, серной кислотой, КОН. Назовите все вещества.
10.Что получится при нагревании α-аминовалериановой кислоты, β-аминовалериановой кислоты, γ-аминоизовалериановой кислоты. Назовите все вещества.
11.С помощью каких реакций можно отличить изомеры: 2-амино- пропановую кислоту и N-метил-2-аминоэтановую кислоту? Напишите уравнения реакций.
176
12.Какие вещества образуются при действии на пропеновую кислоту аммиака, затем НСl, затем щёлочи, затем иодметана? Напишите уравнения реакций. Назовите все вещества.
13.Что образуется при взаимодействии пропаналя со смесью хлорида аммония и КСN и последующем гидролизе? Напишите уравнения реакций. Назовите все вещества.
14.Какие соединения образуются при действии на 2,5-диамино- пентановую кислоту аммиака, НСl, КОН, метанола, уксусного ангидрида, НNO2. Напишите уравнения реакций. Назовите все вещества.
15.Имеющееся количество динитрила адипиновой кислоты разделили на две части. Первую часть подвергли восстановлению, вторую гидролизу, затем провели реакцию поликонденсации полученных продуктов. Напишите уравнения реакций. Какой продукт был получен?
16.Как можно получить α-аланин всеми возможными способами?
17.Написать структурные формулы возможных трипептидов из следующих аминокислот: а) аланин, аланин, глицин; б) изолейцин, валин, глицин; в) глицин, пролин, аспарагиновая кислота; г) лейцин, фенилаланин, аланин.
18.Сравните рН водных растворов валина, глутаминовой кислоты и лизина. В каких формах они существуют в зависимости от рН среды? Что такое изоэлектрическая точка аминокислоты? В чём сущности разделения аминокислот методом электрофореза?
19.Объясните, почему сульфаниловая кислота растворяется в щелочах, но не расворяется в кислотах.
20.При декарбоксилировании α-аминокислот образуются биогенные амины, выполняющие в организме важные биологические функции. Так, получающийся при декарбоксилировании гистидина гистамин, в частности, имеет отношение к аллергическим реакциям организма. Чем объясняется способность α-аминокислот декарбоксилироваться? В каких условиях протекает этот процесс?
21.Противоопухолевый препарат сарколизин имеет формулу:
По какому атому азота образована соль с хлористым водородом? Какое минимальное количество моль щёлочи может вступить в реакцию с 1 моль сарколизина? Напишите уравнение реакции.
22. Пантотеновая кислота (витамин В3) применяется при нарушении обменных процессов. В водных растворах она устойчива лишь при рН 5,5–7,0. В щелочных или более кислых средах она подвергается гидролизу, особенно при нагревании. Какие продукты при этом образуются? Воз-
177
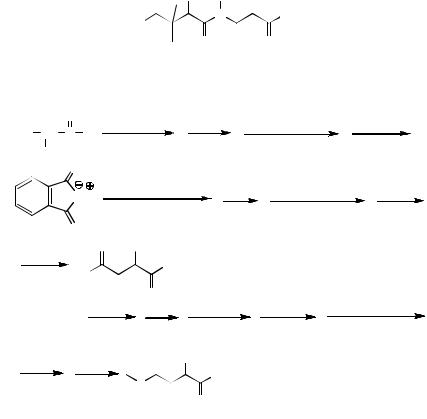
можна ли пространственная изомерия (геометрическая, оптическая) для её молекулы?
OH H |
|
N |
OH |
HO |
|
OO
23.Как взаимодействуют изомерные аминокислоты C3H7NO2 с азоти-
стой кислотой? Напишите соответствующие уравнения реакций.
24. Осуществите схемы превращений. Назовите конечные продукты по номенклатуре IUPAC:
III. Задания по синтезу веществ
25.Из пропилена получите амид α-аминомасляной кислоты.
26.Как по методу Родионова получить β-аминовалериановую кислоту? Напишите уравнения реакций.
27.Получите α-аминомасляную кислоту, исходя из пропанола-1?
28.Как можно получить α-аминоизовалериановую кислоту, имея про- панол-2 и неорганические вещества?
29.Предложите схемы синтеза: а) α-аланина из α-бромпропионовой кислоты (по методу Габриэля); б) α-аланина из ацетальдегида (по методу Штреккера); в) α-аланина из малонового эфира; г) α-аланина из пировиноградной кислоты; д) 2-амино-3,3-диметилбутановой кислоты по методу Штреккера; е) 2-амино-2-метилбутановой кислоты по методу Штреккера;
178
ж) γ-аминовалериановой кислоты из левулиновой (4-оксопентановой) кислоты; з) валина из изобутанола; и) α-аланина из бутанола-2; к) лизина из 1,4-дибромбутана; л) лейцина из изоамилового спирта; м) N-бензоил- глицина (гиппуровой кислоты) из уксусной и бензойной кислот; н) β- фенил-α-аланина фталлоимидомалоновым методом; о) β-фенил-α-аланина из α-оксинитрила по методу Штреккера; п) глицина из уксусной кислоты; р) 3-аминобутановую кислоту по методу Родионова; с) изолейцина из оптически активного пентанола; т) серина из гликолевого альдегида по методу Штреккера; у) дикетопиперазина из этанола; ф) лейцина, используя малоновый эфир.
IV. Определение строения соединений
30.Установите строение вещества состава С3H7O2N, если оно растворяется в щёлочи и кислоте, при реакции с НNО2 выделяется азот, с этанолом образует вещество С5Н11O2N, при нагревании даёт вещество состава С6H10O2N2 . Напишите уравнения реакций.
31.Установите строение вещества С3Н7O2N, если оно обладает амфотерными свойствами, с метанолом даёт вещество состава С4Н9NO2, при нагревании выделяет аммиак и образует вещество С3Н4O2, обнаруживающее кислотные свойства. Напишите уравнения реакций. Назовите все вещества.
32.Установите строение вещества C4H9O2N, которое при взаимодействии с НСl образует С4Н10O2NСl, а при взаимодействии с КОН – С4Н8O2NК. При нагревании даёт вещество С4Н7NО. Назовите все вещества.
33.Установите строение вещества состава С3Н7О2N, если известно, что оно растворяется в щелочах и кислотах, при реакции с азотистой кислотой
выделяет азот, с этанолом образует соединение состава С5Н11О2N, а при нагревании даёт новое вещество состава С6Н10О2N2.
34.Установите строение вещества состава С4Н9NO2, которое при взаимодействии с соляной кислотой образует соединение состава С4Н10О2NCl,
апри действии раствора гидроксида натрия – С4Н8О2NNa. При нагревании исследуемое вещество превращается в соединение состава С4Н7NО.
35.Установите строение вещества состава C5H11O2N, если известны его следующие свойства: а) растворяется в кислотах и щелочах, б) с этанолом образует C7H15O2N, в) при нагревании выделяет аммиак и образует
C3H4O2.
36.Бетаин C5H11O2N встречается в мелассе сахарной свёклы. Он не реагирует с NaOH, с HCl даёт C5H12O2NCl. Бетаин получают реакциями глицина с иодметаном или хлоруксусной кислоты с триметиламином. Установите формулу бетаина.
37.Охарактеризуйте отношение к нагреванию α-, β- и γ-аминокислот. Три изомерные аминокислоты А, Б и В (C5H11O2N) при нагревании пре-
179
