
01.Лечебное дело / Биоорганическая химия / 06.Дополнительно / Всякое / Органическая химия
.pdf
а) CH3-CH2-CH2-CH3 |
Br2 |
A |
|
Na |
B |
Br2, 1 моль |
C |
|
KOH |
D |
1. O3 |
|
E; |
|||||
свет |
|
o |
|
свет |
|
o |
2. H2O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
t C |
|
|
|
|
|
|
спирт, t C |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
18.Из пропена и неорганических реагентов предложите схемы получения: а) пропанола-2; б) пропанола-1; в) пропандиола-1,2; г) гексана; д) 2,3- диметил-2,3-дибромбутана. Какие качественные реакции возможны для алкенов? Приведите уравнения реакций и механизмы.
19.Приведите уравнения реакций, с помощью которых устанавливают положение кратной связи.
20.Каким образом из пентанола-1 можно получить пентандиол-2,3? Приведите уравнения соответствующих реакций.
21.Циклогексен, полученный при дегидрировании циклогексана, со-
держит примесь исходного вещества. Эту смесь трудно разделить фракционной перегонкой из-за близости температур кипения циклогексана (80оС)
ициклогексана (83оС). Какие химические превращения можно использовать, чтобы разделить смесь на индивидуальные углеводороды?
22.Из каких органических соединений можно получить а) бутен-1; б) пентен-2; в) 2-метилгексен-3? Приведите уравнения и механизмы реакций.
23.2,2,4-триметилпентан (изооктан) прибавляют к бензину для повышения октанового числа. Этот углеводород можно получить, гидрируя димеры изобутилена. Написать уравнения реакций образования изооктана.
24.Какое строение имеют дигалогенпроизводные, которые при взаимодействии с цинком дают следуюшие алкены: симм-этил- изопропилэтилен, тетраметилэтилен, несимм-пропил-втор-бутилэтилен?
25.Напишите уравнения реакций получения этиленовых углеводородов из следующих соединений: а) 3-бром-2-метилпентана, вторичного бромистого бутила; б) 2-бром-3-метилгексана, 3-иод-2,5-диметилгексана.
II. Механизм электрофильного присоединения (АЕ)
26.Напишите реакции пентена-2 со следующими реагентами: а) бро-
мом в ССl4; б) хлором и водой; в) бромоводородом; г) хлороводородом; д) серной кислотой; е) водой в присутствии кислоты; ж) НОСl в присутствии протонов; з) озоном и последующим действием воды; и) перманганатом калия (разбавленный раствор в присутствии соды); к) перманганатом калия (концентрированный раствор в присутствии серной кислоты). Для реакций а) – г), е) и ж) приведите механизмы реакций.
27.В каком направлении преимущественно протекают реакции электрофильного присоединения? Предскажите главные продукты и напишите механизм реакций:
40
а) (СН3)2С=СН2 + НСl; б) ССl3-СН=СН2 + НВr; в) СН3-СН=СН2 + НОСl; г) СН2=СН-Сl + НI;
д) СН2=СН-О-СН3 + НВr; е) СН3-СН=СН-Сl + НВr.
28. Объясните изменение реакционной способности в реакциях электрофильного присоединения (AE) в следующих рядах алкенов и реагентов:
а) СН2=СН2 < СН3СН=СН2 < (СН3)2С=СН2; б) Cl2 > Вr2 > I2; в) НСl <
НВr < НI.
29.Пропилен СН3-СН=14СН2 (меченный 14С – радиоактивный изотоп) превращается в бромистый аллил в результате свободнорадикального бромирования. Что можно сказать о положении меченого атома (14С) в полученном веществе? Объясните ваш вывод.
30.При хлорировании изобутилена, меченного 14С по метиленовой группе, и последующем озонолизе были получены формальдегид и меченый хлорацетон. Напишите механизм хлорирования изобутилена.
31.Напишите уравнения реакции гидробромирования бутена-1: а) в присутствии пероксида; б) в отсутствии пероксида. Рассмотрите механизмы. Сформулируйте правило Марковникова и дайте ему объяснение.
32.Какой продукт образуется при взаимодействии пентена-1 с монохлоридом иода ICl? Напишите механизм реакции.
33.Предложите механизм присоединения бромистого водорода к 3,3,3- трифторпропену-1.
34.Изобутилен конденсируется с этиленом и хлористым водородом, образуя 3,3-диметил-1-хлорбутан. Покажите ионный механизм этой реакции.
35.Рассмотрите механизм бромирования дивинила.
36.Напишите схему получения полихлорвинила в присутствии пероксида. Дайте определение понятиям «полимеризация», «мономер», «полимер», «степень полимеризации».
37.При бромировании 2-метилпропена-1 в присутствии хлористого лития был получен 1-бром-2-хлор-2-метилпропан. Объясните результат.
38.Напишите уравнения реакций 1,2- и 1,4-присоединения для изопрена. Рассмотрите условия и механизм этих реакций.
39.Запишите уравнения и приведите механизм реакции присоединения
HBr к бутену-1: а) в среде растворителя CCl4; б) в присутствии пероксида. Отметьте различия и общие закономерности этих реакций. Изложите правило Марковникова в эмпирической форме и в современной трактовке.
40.Изооктан (2,2,4-триметилпентан) получают димеризацией изобутилена в присутствии 60%-го раствора серной кислоты с последующим гидрированием продукта. Напишите уравнения всех реакций и механизм димеризации изобутилена.
41.Напишите механизм гидратации следующих алкенов: а) 3-метил- гексена-3, б) 2-метилбутена-1. Какие спирты при этом образуются?
41
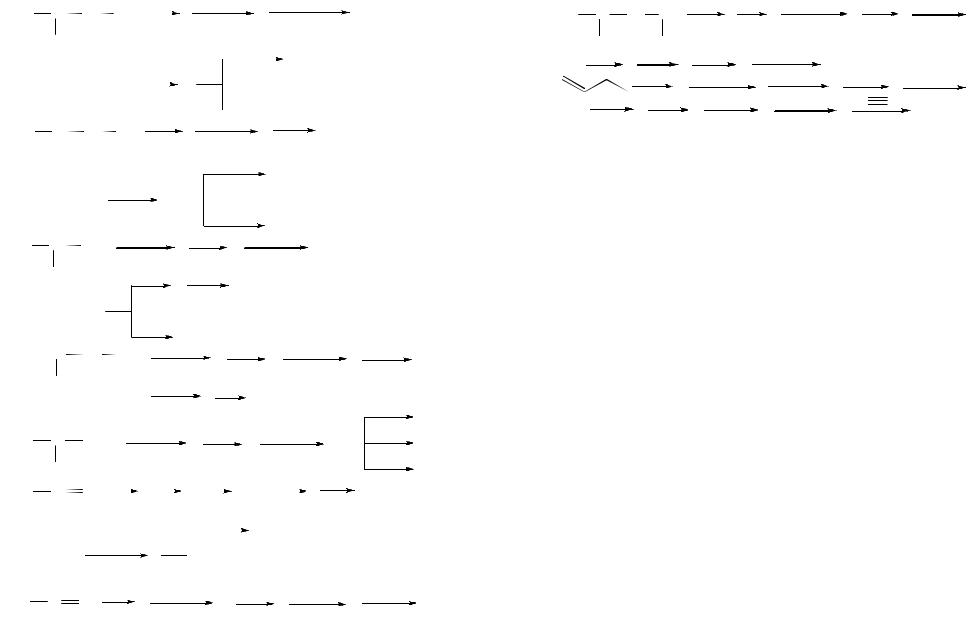
III. Определение строения алкенов и диенов
42. Установите строение алкенов, если при озонолизе а) С5H10 образо-
вались этаналь и пропаналь; |
б) С5Н10 – метаналь и 2-метилпропаналь; |
в) С6Н12 – ацетон; г) С7Н14 – |
ацетон и изомасляный альдегид; д) С8Н16 – |
пропанон и 3-метилбутанон. |
|
43. Определите строение веществ по брутто-формуле и продуктам превращений. Напишите уравнения реакций:
а) С5Н10, каталитическое гидрирование даёт 2-метилбутан, а гидробромирование в присутствии Н2О2 с последующей обработкой натрием приводит к 2,7-диметилоктану; б) С6Н12, при обработке бромистым водородом образуется 2-бром-2-метилпентан (приведите два варианта ответа); в) С6Н10, при окислении азотной кислотой образуется адипиновая (гексан- диовая-1,6) кислота; г) С8Н16, при окислении по Вагнеру даёт октандиол- 3,4; е) нервоновая кислота, обесцвечивает бромную воду, восстанавливается в тетракозановую кислоту СН3(СН2)22СООН, при окислении хромовой смесью превращается в соединения СН3(СН2)7СООН и НООС-(СН2)13-СООН; ж) алкен образуется при дегидратации двух изомерных спиртов С8Н18О, при окислении озоном с последующим гидролизом даёт ацетон и валериановую кислоту. Какова структура спиртов?
Тема 6. Алкины (ацетиленовые углеводороды)
Контрольные вопросы
1.Дайте характеристику тройной связи. Как меняется длина, энергия и реакционная способность связи, образуемой атомами углерода, находящимися в первом, втором и третьем валентном состоянии (sp3-, sp2-, spгибридизация)? Ответ обоснуйте.
2.Дайте классификацию химических реагентов, с которыми взаимодействуют ацетиленовые углеводороды. Приведите механизмы реакций. В чём сходство и отличие механизмов реакций у алкинов и алкенов?
3.Какие реакции ацетиленовых углеводородов используются в промышленном синтезе?
4.Назовите классы веществ, из которых получают ацетиленовые углеводороды в промышленности и лаборатории. Приведите уравнения и механизмы реакций
Задачи
I. Строение, изомерия и номенклатура алкинов
1. Приведите структурные формулы всех возможных изомерных алкинов. Назовите их по рациональной и международной номенклатурам: а) С5Н8; б) С6Н8, содержащих циклопропильный радикал; в) С6Н8, содержащих одновременно двойные и тройные связи; г) C6H6, содержащих две
42
тройные связи; д) С6Н10; е) C9H8, содержащих бензольное ядро.
2.Напишите структурные формулы углеводородов и назовите их по международной номенклатуре: а) метилэтилацетилен, этилизопропилацетилен; б) трет-бутилацетилен, втор-бутилизобутилацетилен; в) метилвинилацетилен, фенилацетилен.
3.Назовите соединения по рациональной и международной номенклатурам:
а) СН3-С≡С-СН3; б) (СН3)2СН-С≡С-СН2-СН3; в) СН3-СН2-СН(СН3)-С≡С-СН2-СН3; г) (СН3)2-СН-С≡СН;
д) (СН3)3С-С≡С-СН2-СН(СН3)2; е) СН2=СН-С≡СН;
ж) СН≡С-СН2-СН=СН2; з) СН3-С≡С-СН2-СН=СН2.
4. Напишите и назовите по систематической номенклатуре ацетиленовые углеводороды, которые изомерны приведённым ниже диенам и имеют тот же самый углеродный скелет: а) бутадиен-1,3; б) 2-метилбутадиен-1,3; в) 3,3-диметилпентадиен-1,4; г) 2,3-диметилпентадиен-1,3; д) 2,3-диметил- бутадиен-1,3.
5. Приведите структурные формулы углеводородных остатков: а) этинил; б) винил; в) пропаргил; г) аллил. Напишите структурные формулы винилацетилена, диаллилацетилена, пропаргилацетилена. Назовите их по международной номенклатуре.
6. На примере молекулы аллилацетилена охарактеризуйте первое, второе, третье валентные состояния атомов углерода.
II. Способы получения и химические свойства
7. Напишите схемы синтеза следующих соединений: а) бутина-1 из бу- тена-1; б) пентина-1 из ацетилена; в) гептина-3 из ацетилена; г) пентина-2 из пропина-1 с помощью реагента Йоцича; д) 4-метилпентина-2 из 1-бром- 4-метилпентана; е) бутанона-2 из 1-бромбутана; ж) акрилонитрила из 1,2- дибромэтана; з) 1,2-дихлорэтена их карбида кальция; и) 1,1-дибромэтана из 1,2-дибромэтана; к) бальзама Шостаковского (поливинилбутилового эфира) из ацетилена и бутанола-1; л) гексахлорэтана из этилена; м) фенилацетилена из ацетофенона (метилфенилкетона).
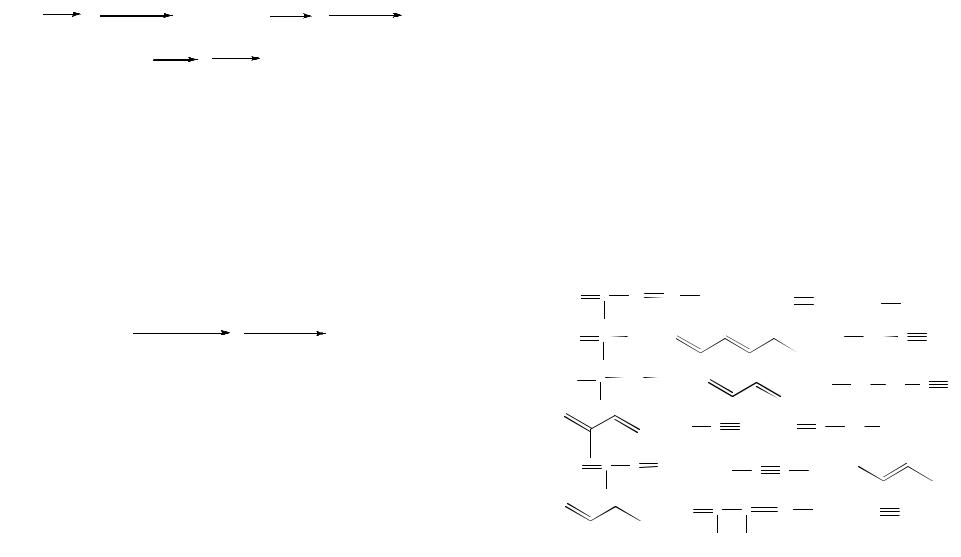
8. Запишите уравнения последовательно протекающих реакций и назовите исходные соединения, а также промежуточные и конечные продукты:
43
|
|
|
|
|
|
Br |
2, |
hν |
|
KOHспирт., toC |
|
KMnO HOH, 20oC |
|||
б) H3C |
CH |
CH2 CH3 |
|
|
|
|
|
|
|
|
4, |
||||
|
|
|
|
|
|
A |
|
|
B |
|
|
||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,4-полимеризация |
||||
|
|
|
|
Al O |
toC |
|
|
|
|
|
E |
||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
C |
|
2 |
3, |
|
|
|
D |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||
HBr
 F
F
ж) C2H5 |
CH |
CH2 |
HBr |
|
2Na |
Br2, hν |
|
|
|
KOHспирт., toC |
D |
Br2 |
||||||
|
|
A |
|
B |
|
|
|
|
C |
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
K |
Cr O |
H+, toC |
|
|
|||||
|
|
|
|
|
|
|
2 |
2 |
7, |
|
|
|
G |
|
|
|||
|
|
|
KOH , toC |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
спирт. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
|
|
F |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
HBr
 H
H
44
 9. Объясните изменение кислотных свойств
9. Объясните изменение кислотных свойств  в следующем ряду: ацети-
в следующем ряду: ацети-
лен (pKа = 25), этилен (pKа = 36), этан (pKа = 40).
10.Расположите в порядке уменьшения кислотности указанные ниже соединения: а) метилацетилен; б) серная кислота; в) пропан; г) аммиак; д) вода; е) бутен-1. Дайте объяснение выбранному вами порядку.
11.Как можно объяснить более кислые свойства циановодорода по сравнению с этином?
12. С какими реагентами бутин-1 будет реагировать как кислота:
а) NаН; б) КОН; в) КNН2; г) СН3СООNа; д) н-С4Н9Li; е) LiСl? Дайте объяснения. Назовите образующиеся вещества.
13. Напишите формулы и названия органических соединений, которые получаются при реакции бутина-1 с реагентами: а) водород (1 моль); б) водород (2 моль), никель; в) бром (1 моль); г) бром (2 моль); д) хлороводород (1 моль); е) хлороводород (2 моль); ж) вода (в прис. H+ и Hg2+);
з) амид натрия в аммиаке (ж); и) [Аg(NН3)2]ОН; к) [Сu(NН3)2]ОН; л) Nа в аммиаке (ж); м) HBr в присутствии пероксидов; н) О3, затем НОН. Отметьте реагенты, с которыми не взаимодействует бутен-1.
14.Сравните отношение пропена и пропина к следующим реагентам:
а) бром в CCl4; б) бромоводород; в) вода в кислой среде; г) вода в присутствии кислоты и солей ртути; д) гипохлорит в кислой среде; е) бром в присутствии пероксидов; ж) водород в присутствии платины; з) перманганат калия в присутствии серной кислоты; и) амид натрия в жидком аммиаке. Там, где есть взаимодействие, напишите уравнения реакций (оформите ваш ответ в виде таблицы). Напишите механизмы для реакций а), б), в), е).
15.Предложите реакции, с помощью которых можно различить пары соединений: а) пентан и пентин-2; б) пентен-2 и пентин-2; в) пентин-2 и пентин-1; г) пентадиен-1,3 и пентин-1.
16.Напишите схемы реакций ацетилена с указанными соединениями: а) этанолом в присутствии щёлочи; б) уксусной кислотой в присутствии оксида цинка при нагревании; в) этиламином в присутствии оксида кадмия при нагревании; г) этантиолом в присутствии щёлочи; д) циановодородом. Приведите механизм реакции а). Почему эти реакции называют винилированием?
17.Приведите все реакции, лежащие в основе промышленного метода
45
получения этина из известняка и угля. Как ещё получают этин в промышленности?
18. Назовите алкины, которые являются конечными продуктами следующих реакций:
19. Осуществите  следующие превращения: а) н-бутан → бутин-2; б) 3-метилбутен-1 → 3-метилбутин-1; в) бутен-1 → бутин-2; г) пропин → метилизопропилацетилен; д) бутанол-1 → этилбутилацетилен.
следующие превращения: а) н-бутан → бутин-2; б) 3-метилбутен-1 → 3-метилбутин-1; в) бутен-1 → бутин-2; г) пропин → метилизопропилацетилен; д) бутанол-1 → этилбутилацетилен.
20. Напишите уравнения реакций, с помощью которых можно получить из ацетилена: а) ацетальдегид, б) этилвиниловый эфир, в) винилацетат, г) винилацетилен, д) бутин-2-диол-1,4, е) бутандиол-1,4, ж) бутадиен-
1,3.
21.Напишите уравнения реакций получения пентина-1 из пентена-1.
22.Приведите уравнения реакций получения всеми возможными способами а) пропина; б) бутина-1; в) бутина-2.
23.Напишите уравнения трёх реакций, характеризующих кислотный характер атомов водорода в фенилацетилене. Объясните причину появления кислотных свойств в алкинах.
24.Клей ПВА представляет собой водную эмульсию полимера В. Получите это соединение по предлагаемой схеме. Напишите уравнения реакций.
25.Исходя из ацетилена, покажите схему синтеза хлоропренового каучука. Напишите уравнения реакций.
26.Имея этанол, иодметан и все необходимые неорганические вещества, получите метилэтилацетилен.
27.Напишите уравнения реакций:
а) бромирования изопропилацетилена, метилацетилена с формальдегидом, гидратации гептина-1 в прис. HgSO4, циклотримеризации бутина-2, бензилацетилена с натрием; б) бутина-2 с хлором, гидратации дифенилацетилена, трет-бутилацетилена с аммиакатом серебра, циклотримеризации пропина, ацетилена с пропанолом-2 (в прис. КОН); в) бромирования пропина, пентина-1 с HCl, ацетилена с пропиловым спиртом (в прис. КОН), гидратации втор-бутилацетилена в прис. HgSO4, этилацетилена с однохлористой медью; г) гидрирования пропина, гидробромирования пен- тина-1, этилацетилена с HCN (1 моль), линейной тримеризации ацетилена, изомасляной кислоты с ацетиленом (в прис. H3PO4); д) бромирования ок-
46
тина-1, фенилацетилена с амидом натрия, пропилацетилена с бутиловым спиртом (в прис. КОН), ацетилена с ацетоном, гидратации трет- бутилацетилена в прис. HgSO4; е) димеризации ацетилена, изопропилацетилена с ацетоном, бромирования гексина-2, гидратации бутина-2 в прис. HgSO4, фенилацетилена с аммиакатом серебра.
III. Механизм реакций и реакционная способность
28. Используя ваши знания о механизме электрофильного присоединения, предскажите главные продукты следующих реакций:
а) СН3-С≡СН + НСl →...; |
б) СF3С≡СН + НВr →...; |
в) СН3-С≡СН + СН3СООН, (кат) →…; |
г) НС≡СН + 2НВr →... |
Напишите механизм реакции. |
|
29.Объясните, почему для непредельных углеводородов реакции электрофильного присоединения протекают с различной скоростью. Обсудите причины этих различий: а) используя особенности электронного строения молекл; б) учитывая механизм превращения.
а) Этилэтилен и этилацетилен; б) бутен-1 и бутин-1; в) бутин-1 и бута-
диен-1,3.
30.Запишите уравнения реакций электрофильного присоединения бромоводорода к углеводородам. Рассмотрите строение интермедиатов, образующихся на лимитирующей стадии процесса, и сравните их стабильность. На основании этих данных расположите углеводороды в порядке увеличения скорости присоединения.
47
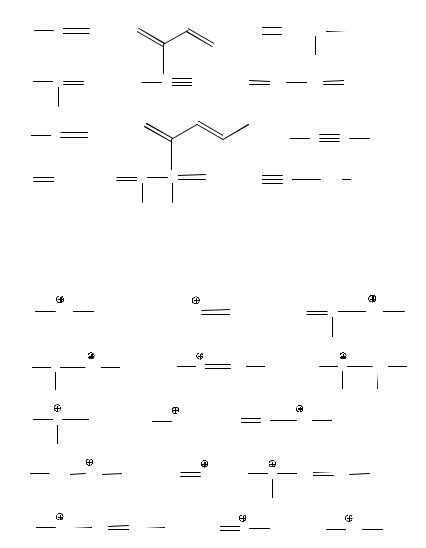
31. Расположите карбокатионы в порядке увеличения стабильности. Объясните причины наблюдаемой закономерности. Запишите структурные формулы углеводородов, из которых могут образовываться эти карбокатионы. Приведите примеры реакций, в которых указанные карбокатионы могут являться промежуточными частицами.
 32. Напишите
32. Напишите уравнение реакции
уравнение реакции конденсации (реакция
конденсации (реакция Фаворского– Назарова): а) винилацетилена с ацетоном (СН3-С(О)-СН3); б) метилацетилена с формальдегидом (НСНО).
Фаворского– Назарова): а) винилацетилена с ацетоном (СН3-С(О)-СН3); б) метилацетилена с формальдегидом (НСНО).
33. Напишите уравнение двухстадийного присоединения брома к бу- тину-2. Как будут влиять два первых присоединившихся атома брома на реакционную способность двойной связи? Как это будет влиять на конкурентную реакцию галогена с бутином-2 и 2,3-дибромбутеном-2? В каком
соотношении необходимо смешать реагенты, чтобы ограничить реакцию первой стадией? Будете ли вы пропускать бутин-2 в раствор Br2 в CCl4 или прибавлять по каплям раствор брома к раствору бутина-2?
IV. Определение строения алкинов
34.С помощью каких реакций можно установить положение тройной связи? Приведите уравнения реакций.
35.Установите строение соединений по известной брутто-формуле и продуктам химических превращений:
а) C5H8, которое с [Ag(NH3)2]OH образует осадок, а при окислении перманганатом калия в кислой среде превращается в изомасляную кислоту;
б) С8Н14, в результате исчерпывающего гидрирования образуется октан, а при обработке аммиакатом серебра – С8Н13Ag;
в) С7Н12, с аммиакатом серебра образуется соединение С7Н11Ag, а при гидратации по Кучерову – 5- метилгексанон-2;
г) С6Н10, имеет симметричное строение молекулы, не реагирует с амидом натрия в жидком аммиаке, при гидратации в прис. соли ртути образует несимметричное карбонильное соединение;
д) С6Н10, в результате последовательной обработки эквимолярным количеством амида натрия в жидком аммиаке и бромистого изопропила образуется 2,6-диметилгептин-3;
е) С5Н8, не образует соединения с однохлористой медью, не вступает в реакцию Дильса– Альдера с малеиновым ангидридом, имеет несимметричное строение молекулы;
ж) С5Н8, исчерпывающее гидрирование даёт 2-метилбутан, аммиакат серебра образует соединение С5Н7Ag;
з) С4Н6, при исчерпывающем гидрировании образуется бутан, вступает
вреакцию гидратации по Кучерову, но не образует осадка при обработке аммиакатом серебра;
и) С4Н4, при последовательной обработке эквимолярными количествами амида натрия в жидком аммиаке и иодистого аллила образуется гепта-
диен-1,6-ин-3;
к) С5Н8, обесцвечивает бромную воду и водный раствор перманганата калия, окисляется хромовой смесью в уксусную и пропионовую кислоты, с аммиакатом серебра не реагирует;
л) С6Н10, не реагирует с натрием, при действии воды в прис. соли ртути даёт смесь метилизобутилкетона и этилизопропилкетона.
48 |
49 |
Тема 7. Циклоалканы (нафтены, цикланы, циклопарафины)
Контрольные вопросы
1.Какие соединения называются алициклическими? Как их классифицируют?
2.Какие виды структурной изомерии возможны для алициклических углеводородов?
3.Что вы понимаете под конформационной (поворотной) изомерией? Почему нельзя выделить в свободном виде отдельные конформации (поворотные изомеры)?
4.О чём говорит «теория напряжения» А. Байера? Что было положено
воснову этой теории?
5.Почему циклогексан не менее устойчив, чем циклопентан, хотя это противоречит теории А. Байера?
6.В каких пространственных формах (конформациях) может существовать циклогексан? Какая из этих форм более предпочтительна и почему?
7.Чем вы объясните склонность циклоалканов к реакциям присоединения?
8.Какие способы получения циклоалканов вы знаете?
Задачи
I. Строение, изомерия и номенклатура циклоалканов
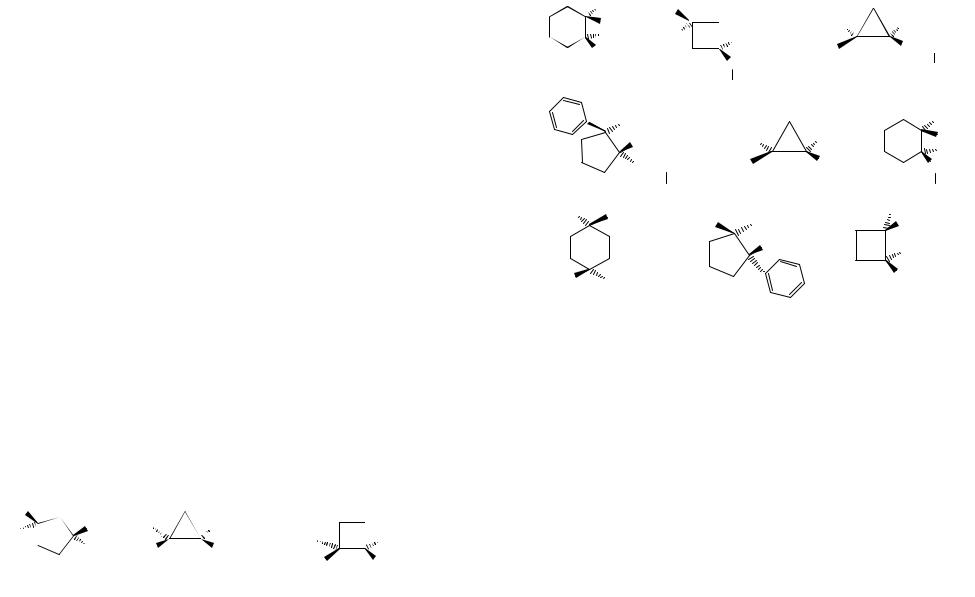
1.Напишите формулы следующих соединений: а) метилциклопропан; б) 1,1-диэтилциклопропан; в) трет-бутилциклопентан; г) цис-1,3-ди- метилциклобутан; д) транс-1,2-диэтилциклопропан; е) цис-1-изопропил-2- метилциклопропан; ж) цис-1-трет-бутил-3-этилциклогексан; з) транс-1- метил-4-этилциклогексан; и) цис-1-метил-3-фенилциклопентан; к) (1R,2S)- 1,2-диметил-1-этилциклопентан; л) (R)-1,1,2-триметил-2-этилциклогексан; м) цис-1-втор-бутил-3-этилциклопентан.
2.Назовите следующие соединения:
50
|
H |
|
|
|
CH3 |
CH2CH3 |
|
|
H |
|
H C |
CH3 |
|||
|
|
3 |
|
|
H |
|
|
|
CH CH |
|
CH CH |
CH2CH3 |
|
||
|
2 |
CH |
|
||||
|
2 |
3 |
2 |
|
2 |
|
|
ж) |
CH |
|
з) |
и) |
C H |
5 |
|
CH3 |
|
3 |
|
|
H |
6 |
|
H |
CH3 |
CH2CH3 |
|
|
|||
|
|
CH2CH=CH2 |
|||||
|
|
|
|
H |
CH3 |
|
|
|
|
|
|
|
|
||
H |
C(CH3)3 |
|
|
|
CH2CH3 |
|
|
к) |
|
|
л) |
|
м) |
|
|
3. Изобразите равновесие двух кресловидных конформаций для сле- |
|||||||
дующих |
соединений |
и |
укажите |
энергетически наиболее |
выгодную: |
||
а) трет-бутилциклогексан; б) цис-1,3-дифенилциклогексан; в) транс-1,3- дифенилциклогексан; г) цис-1,4-диэтилциклогексан; д) транс-1,4-диэтил- циклогексан; е) 1-метил-1-фенилциклогексан; ж) цис-1-метил-2-изо- пропилциклогексан; з) транс-1-метил-2-изопропилциклогексан; и) фенилциклогексан; к) цис-1-фенил-3-этилциклогексан; л) транс-1-фенил-3- этилциклогексан; м) цис-1-втор-бутил-4-метилциклогексан.
4. Напишите все возможные изомеры циклоалканов. Назовите их по номенклатуре IUPAC. Для оптически активных изомеров определите конфигурацию хиральных центров по Кану− Прелогу− Ингольду. а) C5H10, б) С8Н16 (с шестичленным циклом).
II. Способы получения и химические свойства
5. Получите следующие соединения путём взаимодействия соответствующих дигалогенопроизводных алканов с цинком: а) метилциклопропан; б) этилциклопропан; в) трет-бутилциклопропан; г) 1,1-диметилцикло- пропан; д) 1-метил-2-этилциклопропан; е) 1-изобутил-2-этилциклопропан; ж) трет-бутил-2-этилциклопропан; з) 1,1-диметил-2,2-диэтилцикло-
51
пропан; и) изобутил-2-этилциклопропан; к) фенилциклопропан; л) 1,1-ди- пропилциклопропан; м) метилциклогексан.
6. Используя пиролиз кальциевых солей алифатических дикарбоновых кислот, получите следующие соединения. Укажите условия реакций. а) Метилциклопентан; б) 1,2-диметилциклопентан; в) 1,3-диметилцикло- пентан; г) 1,2-диэтилциклопентан; д) циклогексан; е) этилциклогексан; ж) 1,2,3-триметилциклогексан; з) 1,4-диэтилциклогексан; и) 1,2-дипропил- циклопентан; к) 1,2-диизопропилциклопентан; л) изобутилциклогексан; м) 1,3-диэтилциклопентан.
7. Получите следующие соединения из соответствующих производных бензола. Укажите условия реакций. а) Метилциклогексан; б) циклогексанол; в) 1,4-диэтилциклогексан; г) 1,3-диметилциклогексан; д) 4-метил-1-циклогексанол; е) 1,2-диметилциклогексан; ж) этилциклогексан; з) изопропилциклогексан; и) 1,2,3,4,5,6-гексаметилциклогексан; к) 4-аминоциклогексанол-1; к) 1,2,3-триэтилциклогексан; л) 1-метил-3- изопропилциклогексан; м) трет-бутилциклогексан.
8. Напишите уравнения следующих реакций, указав, где необходимо, условия и катализатор: а) циклогексан и хлор; б) метилциклопентан и бром; в) циклопропан и бром; г) 1,2,3-триметилциклопропан и бром; д) 1,3-диметилциклобутан и водород; е) 1,2,3-триэтилциклопропан и водород; ж) метилциклопентан и азотная кислота; з) циклопропан и бромоводород; и) 1,2-диметилциклопропан и водород; к) 1,2,3-триметил- циклопропан и бром; л) циклопентан и хлор; м) циклогексан, диоксид серы и хлор.
9.Из соответствующего дигалогеноалкана получите 1,2,3-три- метилциклопропан и напишите уравнения его взаимодействий: а) с бромом при нагревании; б) с водородом на никеле; в) с бромоводородом при нагревании.
10.Из соответствующего дигалогеноалкана получите 1,2,3-трифенил- циклопропан и напишите уравнения его взаимодействий: а) с бромом при нагревании; б) с водородом на никеле; в) с бромоводородом при нагревании.
11.Из соответствующих алкенов и диазометана получите циклоалканы, которые при нагревании с бромом превращаются в следующие соединения: а) 1,3-дибромбутан; б) 1,3-дибромпентан; в) 2,4-дибромпентан; г) 2,4-дибром-2,4-диметилпентан.
12.С использованием реакции Дильса− Альдера с последующим восстановлением водородом на никеле Ренея получите метилциклогексан и напишите для него уравнения реакций: а) с разбавленной азотной кислотой при нагревании; б) с бромом на свету. Объясните высокую региоселективность реакции «б».
52
13.Какой продукт получится при последовательном взаимодействии бутадиена-1,3 с пропеналем (непредельный альдегид) при нагревании под давлением, затем с гидразином и гидроксидом калия при нагревании (реакция Кижнера− Вольфа) и, наконец, с водородом на никеле?
14.Напишите уравнения следующих реакций: а) пиролиз кальциевой соли 2-метилгександиовой кислоты; б) продукт реакции «а» и амальгама цинка в соляной кислоте; в) продукт реакции «б» и бром на свету. Объясните высокую региоселективность реакции «в».
15.Напишите уравнения следующих реакций: а) 2,3-диметилбутадиен- 1,3 и этилен при нагревании; б) продукт реакции «а» и водород на никеле.
16.Напишите уравнения следующих реакций: а) 2,3-дифенилбутадиен- 1,3 и этилен при нагревании; б) продукт реакции «а» и водород на никеле.
17.Напишите уравнения следующих реакций: а) 2,3-диметилбутадиен- 1,3 и акриловый альдегид при нагревании под давлением; б) продукт реакции «а» с бромом в тетрахлорметане в темноте; в) продукт реакции «б»
игидросульфид натрия (2 моль).
18.Напишите уравнения следующих реакций: а) пиролиз кальциевой соли 2-метилгептандиовой кислоты; б) продукт реакции «а» и амальгама цинка в соляной кислоте; в) продукт реакции «б» и бром на свету. Объясните высокую региоселективность реакции «в».
19.На бромистый бензил (PhCH2Br) вначале подействовали натрием в инертном растворителе, затем избытком водорода на никеле, после чего 1 молем брома на свету. Напишите полные уравнения реакций.
Тема 8. Арены (ароматические углеводороды)
Контрольные вопросы
1.Какие признаки характеризуют ароматические, неароматические и антиароматические свойства?
2.Сформулируйте и поясните правило Хюккеля на примере бензола.
3.Почему формула Кекуле для бензола отвечает современным представлениям о строении бензола? Какие химические реакции используются для доказательства строения бензольного кольца?
4.Чем обусловлена инертность бензола при обычных условиях по отношению к бромной воде и раствору КМnO4?
5.Какие типы реакций характерны для бензола? Почему реакции замещения легче протекают с электрофильными реагентами?
6.Покажите образование электрофильных частиц, возникающих при бромировании, алкилировании, нитровании, сульфировании бензола.
7.Напишите механизм реакции SE2 для бензола. Что называется π-комплексом, σ-комплексом (σ-аддуктом)? Почему π-комплекс нестоек? Почему π-комплекс переходит в σ-комплекс? Почему происходит на ко-
53
нечном этапе реакции депротонирование? Объясните энергетическую диаграмму реакциии SE2 в бензольном ядре.
8.Почему гомологи бензола более реакционноспособны в условиях реакций электрофильного ароматического замещения (SE2 Ar), чем бензол?
9.Какие продукты реакций образуются при окислении гомологов бензола кислым раствором перманганата калия при нагревании?
10.Как влияет на ароматичность введение в бензольное ядро заместителей (функциональных групп)?
11.Рассмотрите влияние функциональных групп в аминах, нитросоединениях, сульфокислотах, альдегидах, карбоновых кислотах, галогенозамещенных, простых и сложных эфирах, фенолах, гомологах бензола и других ароматических соединениях на распределение электронной плотности в бензольном ядре. Выделите заместители – ориентанты электронодонорные (+I и +М; +I; -I и +М эффекты); ориентанты электроноакцепторные (-I; -I и -М эффекты).
Какие ориентанты облегчают SE2- и затрудняют SN2-реакции? Какие ориентанты затрудняют SE2- и облегчают SN2-реакции?
12.Рассмотрите ориентирующее действие электронодонорных и электроноакцепторных заместителей. Что называется статическим фактором, динамическим фактором?
13.Определите, учитывая статический и динамический эффекты, глав-
ное направление SE2- и SN2-реакций при наличии двух заместителей в бензольном ядре в о-, м- или п-положениях:
— два ориентанта электронодонорных;
— два ориентанта электроноакцепторных;
— два различных по характеру ориентанта.
Задачи
I. Строение, изомерия и номенклатура аренов
1. Напишите структурные формулы соединений: а) этилбензола; б) 1,3- диметилбензола; в) 1,3,5-триметилбензола; г) изопропилбензола (кумола); д) 3-фенилпентана; е) винилбензола (стирола); ж) фенилацетилена; з) транс-дифенилэтилена (транс-стильбена).
2. Приведите структурные формулы следующих веществ: а) несимм- метилфенилэтилена; б) симм-дифенилэтилена; в) фенилацетилена; г) этилфенилацетилена; д) 2-фенилбутена-2; е) 1,3-дифенилбутена-1. Для соединений, существующих в виде геометрических изомеров, приведите проекционные формулы.
3. Напишите структурные формулы всех изомерных ароматических углеводородов состава: а) С8Н10; б) C9H12. Назовите их по международной номенклатуре. Какие из них имеют тривиальные названия? Приведите их.
54
4.Приведите структурные формулы изомерных алкилбензолов состава
С10Н14: а) однозамещённых; б) двузамещённых. Назовите их. Есть ли среди них оптически активные соединения? Определите их конфигурацию по Кану– Прелогу– Ингольду.
5.Назовите радикалы: а) С6Н5-; б) С6Н5-СН2-; в) п-Н3С-С6Н4-; г) -С6Н4-; д) -С6Н2(СН3)3; е) С6Н5-СН=; ж) С6Н5-СН=СН-.
6.Назовите по рациональной и систематической номенклатурам сле-
дующие |
ароматические |
углеводороды: |
а) С6Н5-СН=СН-СН3; |
|
б) С6Н5-СН=СН2; |
в) С6Н5-С(СН3)=СН2; |
г) С6Н5-С≡С-СН3; |
||
д) С6Н5-С≡С-С6Н5. Для соединений, существующих в виде геометрических изомеров, приведите проекционные формулы.
7.Сравните свойства бензола и циклогексадиена-1,3 и покажите, что бензолу присущ «ароматический» характер. В чем причина имеющихся различий?
8.Пользуясь правилом Хюккеля, установите, какие из указанных ниже соединений проявляют ароматические свойства:
Дайте определения понятиям «ароматическое соединение» и «антиароматическое соединение».
9. Сколько изомеров имеют трёхзамещённые бензолы, содержащие различные заместители? Приведите конкретные примеры.
II. Способы получения и химические свойства
10. Запишите уравнения реакций, укажите условия и названия реакций, если они отсутствуют в задании, назовите образующиеся продукты.
а) Бромирование метоксибензола; (СН3)2СH-Cl + C6H5-Cl + 2Na →; сульфирование 4-бромбензойной кислоты; окисление 1,2,4-триметил- бензола KMnO4/HÅ; хлорирование на свету изопропилбензола; стирол + O2/Ag →;
б) нитрование хлорбензола; CH3-Cl + C6H5-Cl + 2Na →; сульфирование 4-метилбензойной кислоты; окисление 1,3,5-триметилбензола KMnO4/HÅ; бромирование на свету этилбензола; стирол + KMnO4/Na2CO3, HOH, 20oC; в) нитрование бромбензола; алкилирование бензола бутеном-1; бромирование в кольцо п-диметилбензола; бромирование 3-нитрохлорбензола;
окисление м-ксилола KMnO4/HÅ; фенилацетилен + [Cu(NH3)2]OH →;
г) алкилирование толуола пропиленом; получение этилбензола по Вюрцу– Фиттигу; бромирование 4-метоксихлорбензола; сульфирование 4-нитротолуола; окисление 4-нитроэтилбензола KMnO4/HÅ; нитрование пропилбензола по Коновалову;
55
д) гидрирование бензола; получение изопропилбензола по Фриделю– Крафтсу; нитрование 4-метилбензойной кислоты; окисление 4-метил- изопропилбензола KMnO4/HÅ; хлорирование на свету этилбензола; стирол + HBr/пероксид →;
е) бромирование бензойной кислоты; бензол + СН3-СН=СН2 →; нитрование п-бромметоксибензола; сульфирование м-толуолсульфокислоты; окисление м-диэтилбензола KMnO4/HÅ; винилбензол + бромная вода →;
ж) нитрование метоксибензола; получение этилбензола по Вюрцу– Фиттигу; сульфирование 3-нитротолуола; окисление п-хлоризопропил- бензола KMnO4/HÅ; нитрование по Коновалову изобутилбензола; монобромирование на свету п-диметилбензола;
з) сульфирование толуола; алкилирование бензола этиленом; бромирование 4-бромбензойной кислоты; нитрование 4-метокситолуола; окисление 4-нитропропилбензола KMnO4/HÅ; фенилацетилен + [Ag(NH3)2]OH;
и) нитрование изопропилбензола в кольцо; алкилирование бензола пропилхлоридом по Фриделю– Крафтсу; сульфирование п-нитротолуола; бромирование 4-этоксихлорбензола; окисление 1-метил-2-этилбензола
KMnO4/HÅ; 1-фенилпропен-1 + Cl2/400oC →;
к) нитрование нитробензола; получение бензола из бензойной кислоты; нитрование 3-метоксибензойной кислоты; хлорирование 4-нитрохлор- бензола; окисление м-бромтолуола KMnO4/HÅ; бромирование пропилбензола в боковую цепь;
л) нитрование толуола; алкилирование бензола пропиленом; сульфирование п-толуолсульфокислоты; бромирование в кольцо 3-метилбензойной кислоты; окисление п-бромэтилбензола KMnO4/HÅ; винилбензол + HBr;
м) бромирование нитробензола; этилбензол + СН3СН2СН2Cl/AlCl3 →; нитрование 4-бромбензотрихлорида; окисление 1,2,3-триметилбензола
KMnO4/HÅ; винилбензол + KMnO4/Na2CO3, HOH, 20oC; бромирование изобутилбензола в боковую цепь.
11.Какие соединения образуются из этилбензола и п-ксилола при дей-
ствии указанных окислителей: а) О3, затем воды; б) КМnO4 в воде, t°; в) К2Сr2O7 в серной кислоте, t°? Приведите полные уравнения реакций.
12.Напишите структурные формулы главных продуктов, образующихся при взаимодействии стирола со следующими реагентами: а) Вr2 (Fe);
б) Br2 (CCl4); в) НВr; г) КМnO4 в Н2О, t°; д) H2 (Ni), 20° С; е) Н2 (Ni), 200° С,
давление.
13.С помощью каких реакций можно различить следующие пары соединений: а) этилбензол и стирол; б) о- и п-ксилолы; в) стирол и фенилацетилен?
14.Приведите уравнения реакций, лежащих в основе промышленных методов получения а) бензола; б) толуола; в) этилбензола; г) кумола (изопропилбензола) д) стирола.
56
15. Предложите схемы синтеза этилбензола из этилциклогексана; бензола; бромбензола; метилфенилкетона (ацетофенона). Объясните, почему этилбензол нельзя получить действием бромбензола на этан в присутствии АlСl3.
16.Напишите формулы соединений, образующихся по реакции Фриделя– Крафтса– Густавсона при взаимодействии следующих веществ: п-ксилола и бромистого этила; бензола и бромистого изопропила; толуола
ихлористого метила; о-ксилола и бромистого пропила. Дайте названия продуктам реакций.
17.Исходя из бензола и любых других реагентов, получите следующие соединения: а) п-трет-бутилтолуол; б) этил-п-толилкетон; в) аллилбензол; г) п-бромбензойную кислоту.
18.Имея ацетилен, этанол и неорганические вещества, получите стирол. Приведите формулу бутадиенстирольного каучука.
19.По реакции Вюрца– Фиттига получите: а) пропилбензол; б) втор- бутилбензол; в) м-ксилол; г) 1,4-диэтилбензол; д) 1,3-дипропилбензол.
20.Получите из бензола 2-нитро-1-метилциклогексан. Напишите уравнения реакций, назовите промежуточные продукты.
21.Получите дициклогексил из бензола. Напишите уравнения реакций. Назовите промежуточные продукты.
22.По систематической номенклатуре назовите углеводороды, которые являются продуктами следующих реакций:
23.Составьте уравнения реакций, протекающих при нагревании с натронной известью бензоата натрия; натриевой соли п-толуиловой кислоты.
24.Напишите уравнения реакций согласно схеме:
Назовите вещества А– С.
А– С.
25.Как будет реагировать аллилбензол со следующими реагентами:
а) холодной концентрированной серной кислотой; б) Br2 в CCl4; в) холодным разбавленным нейтральным раствором перманганата калия; г) CHCl3
иAlCl3; д) CrO3 и H2SO4.
26.Напишите схемы озонолиза бензола; 1,3,5-триметоксибензола;
57
1,2,3-триэтилбензола.
27. Осуществите схему превращений:
III. Механизм SE2-реакций и реакционная способность бензольного кольца
28. На примере взаимодействия бензола с бромистым пропилом в присутствии АlВr3 рассмотрите особенности алкилирования ароматических углеводородов по Фриделю– Крафтсу. Какова роль катализатора? Почему реакционная способность алкилгалогенидов с одним и тем же радикалом изменяется в следующем порядке:
RF > RCl > RBr > RI?
29.Сопоставьте условия и результаты сульфирования бензола и толуола. Дайте объяснения имеющимся различиям.
30.Сравните отношение изопропилбензола к брому: в присутствии АlВr3; при освещении и нагревании. Приведите механизмы реакций.
31.Трет-пентилбензол в основном образуется в результате реакции
бензола в присутствии BF3 с каждым из следующих спиртов: а) 2-метил- бутанолом-1; б) 3-метилбутанолом-2; в) 3-метилбутанолом-1 и г) неопентиловым спиртом. Объясните эти факты с помощью механизмов реакций.
32.Объясните, почему для бензола типичны реакции электрофильного замещения. Чем объяснить необходимость предварительной активации
реагента в SE2-реакциях? Укажите способы активации реагента в реакциях нитрования, бромирования и алкилирования. Рассмотрите особенности образования электрофила в реакции сульфирования.
33.Запишите уравнение и укажите механизм нитрования бензола. Поясните, как образуется σ-аддукт и изобразите его строение с помощью предельных структур и в мезомерной форме. Как скажется на стабильно-
сти σ-аддукта наличие в о- или п-положении группы -ОСН3? Почему? Как это отразится на скорости реакции?
34.Запишите уравнения и рассмотрите механизм SE2-реакций. Поясните роль катализатора. Изобразите строение σ-аддуктов с помощью предельных структур при о-, м- и п-замещении. Сравните их стабильность и оцените, в каком направлении будет преимущественно протекать замещение. а) Нитрование толуола; б) нитрование бромобензола; в) нитрование бензойной кислоты; г) бромирование метоксибензола; д) бромирование бензотрихлорида; е) алкилирование толуола пропиленом; ж) сульфирова-
ние хлорбензола; з) алкилирование феноксибензола трет-бутанолом; и) хлорирование нитробензола; к) сульфирование резорцина; л) ацетили-
58
рование толуола хлористым ацетилом; м) алкилирование N-ацетиланилина бутанолом-1.
35.Запишите уравнения реакций и рассмотрите механизм для первого соединения в нижеследующем ряду. Расположите соединения в порядке
увеличения скорости SE2-реакций. Объясните полученную закономерность с точки зрения стабильности интермедиатов, образующихся на скоростьопределяющей стадии реакции. а) Нитрование: этилбензола, бензола, бензойной кислоты; б) нитрование: нитробензола, метоксибензола, толуола; в) хлорирование в присутствии катализатора: бензола, хлорбензола, этилбензола; г) бромирование в присутствии катализатора: изопропилбензола, бензола, бензотрихлорида; д) сульфирование: бензола, фенола, бромобензола; е) алкилирование хлористым пропилом по Фриделю– Крафтсу: толуола, бензола, метоксибензола; ж) алкилирование пропиленом: бензола, этилбензола, этоксибензола; з) ацилирование хлористым ацетилом: бензола, м-диметоксибензола, хлорбензола; и) сульфирование серным ангидридом: толуола, бензола, п-дибромбензола; к) алкилирование этанолом: метилового эфира бензойной кислоты, изопропилбензола, пропоксибензола; л) нитрование: кумола, п-толуидина, о-крезола; м) хлорирование: иодбензола, нитрозобензола, хлористого бензила.
36.Какие продукты образуются при мононитровании следующих соединений в присутствии катализатора: а) бромбензола; б) толуола; в) нитробензола. Какое соединение должно нитроваться легче остальных? Почему? При объяснении используйте представления о строении и стабильности интермедиатов, образующихся на скоростьопределяющей стадии реакции.
37.Почему сульфирование толуола протекает с большей скоростью, чем сульфирование бензола, а продукт реакции представляет собой в основном смесь о- и п-изомеров? Объясните наблюдаемые результаты с точки зрения стабильности интермедиатов, образующихся на скоростьопределяющей стадии реакции.
38.Запишите уравнения и подробно рассмотрите механизм нитрования бромбензола и бензотрибромида. Строение σ-аддуктов, образующихся на скоростьопределяющей стадии, изобразите с помощью предельных структур. Объясните, почему оба заместителя, дезактивируя бензольное кольцо, направляют электрофил в разные положения.
39.Обработка кумола хлором в присутствии хлорида железа (III) приводит к получению п-хлоркумола, а при действии на кумол хлора на свету при нагревании образуется 2-фенил-2-хлоропропан. Объясните, какими факторами обусловлено это различие. Приведите уравнения и механизм этих превращений.
40.Запишите уравнения и подробно рассмотрите механизм реакций хлорирования бензальдегида и изопропилбензола в присутствии бромида
59
