
01.Лечебное дело / Биоорганическая химия / 06.Дополнительно / Всякое / Оксикислоты
.docОксикислоты: особенности химических свойств. Явление оптической изомерии. Понятие о рацематах.
Оксикислоты - производные кислот, которые получаются в результате замещения одного или нескольких атомов водорода в радикале кислоты одной или несколькими гидроксильными (спиртовыми) группами.
В простейших случаях оксикислоты содержат одну карбоксильную и одну гидроксогруппу, тогда их общая формула будет:

Более общая формула оксикислот:

Таким образом, оксикислоты имеют две различные функциональные группы: карбоксильную (кислотную) и гидроксильную (спиртовую) группы.
Соединения, содержащие различные функциональные группы, обычно называются соединениями со смешанными функциями.
В зависимости от наличия одного или нескольких карбоксилов оксикислоты делят на одноосновные (с одним карбоксилом), двухосновные (с двумя карбоксилами), трехосновные (с тремя карбоксилами) и т. д.
По числу спиртовых гидроксилов различают монооксикислоты (с одним гидроксилом), диоксикислоты (с двумя гидроксилами) и т. д.
В большинстве случаев оксикислоты обозначают эмпирическими наименованиями – по нахождению в том или ином продукте и т.д.
Н апример,
одноосновная кислота с тремя атомами
углерода, найденная впервые в молоке,
называется молочной кислотой; двухосновная
оксикислота с четырьмя атомами углерода,
впервые найденная в яблоках – яблочной
кислотой, и т. д.
апример,
одноосновная кислота с тремя атомами
углерода, найденная впервые в молоке,
называется молочной кислотой; двухосновная
оксикислота с четырьмя атомами углерода,
впервые найденная в яблоках – яблочной
кислотой, и т. д.
Наряду с этими названиями пользуются и другими, например, прибавляя слово окси- к названию той кислоты, от которой производится данная оксикислота путем замещения водорода на гидроксил. Так, молочной кислоте (с тремя атомами углерода) соответствует пропионовая СН3–СН2–СООН, и поэтому молочную кислоту называют также оксипропионовой кислотой, а яблочную – оксиянтарной кислотой. Место гидроксильной группы оксикислоты обозначают обычно греческой буквой, начиная обозначения атомов в углеродной цепи в порядке греческого алфавита от того атома углерода, который непосредственно связан с карбоксильной группой. Поэтому более точное название молочной кислоты – с обозначением места гидроксила – α-оксипропио-новая кислота (альфа-оксипропионовая кислота):
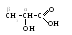
С огласно
международной номенклатуре, названия
оксикислот производят от названий
соответствующих кислот, прибавляя
приставку окси- и указывая положение
углеродного атома, у которого стоит
спиртовая группа. Например, молочная
кислота по международной номенклатуре
называется 2-оксипропановой.
огласно
международной номенклатуре, названия
оксикислот производят от названий
соответствующих кислот, прибавляя
приставку окси- и указывая положение
углеродного атома, у которого стоит
спиртовая группа. Например, молочная
кислота по международной номенклатуре
называется 2-оксипропановой.
Изомерия оксикислот зависит от нескольких причин:
1) от наличия прямой или в той или иной степени разветвленной цепи атомов углерода в ее молекуле;
2) от положения спиртовой группы в цепи атомов углерода. В зависимости от положения гидроксила различают a-оксикислоты, b-ок-сикислоты, g - оксикислоты и т. д.
Т ак,
оксимасляная кислота существует в виде
трех изомеров:
ак,
оксимасляная кислота существует в виде
трех изомеров:
3) зеркальная изомерия:
Зеркальная изомерия – это вид пространственной изомерии, зависящий от различного расположения в пространстве четырех различных групп вокруг асимметрического атома углерода и характеризующийся тем, что оба изомера похожи один на другой так же, как предмет и его зеркальное изображение.
Асимметрический атом углерода – это атом углерода, связанный с четырьмя различными группами атомов. В формулах асимметричный атом углерода обозначают звездочкой:

В формуле одного изомера гидроксил обращен вправо, а атом водорода – влево, тогда как в формуле другого изомера гидроксил обращен влево, а атом водорода – вправо. Различие формул можно заметить и иначе. Обозначим в одной формуле стрелкой направление заместителей от атома водорода через карбоксил к гидроксилу – направление это соответствует ходу часовой стрелки. Если теперь проследить в том же порядке расположение атома водорода, карбоксила и гидроксила в другой формуле и соединить их стрелкой, то эта стрелка будет направлена против хода часовой стрелки.
В качестве вещества, принятого для сравнения, был предложен глицериновый альдегид. Оптически активные вещества, имеющие конфигурацию, сходную с конфигурацией D- и L- глицеринового альдегида, называются веществами D- и L- ряда.

Если в молекуле имеется несколько асимметрических центров, то число оптических изомеров возрастает и равняется: 2n, где n – число асимметричных атомов С.
Понятие об оптической активности
Свет, согласно электромагнитной теории, представляет собой поперечные волны, для которых характерно то, что колеблющиеся частицы совершают движения, перпендикулярные направлению распространения волн. Колебания в луче обычного света происходят в пространстве во всевозможных плоскостях. Если такой луч пропустить через поляризатор, то луч выйдет поляризованным, т. е. колебания в нем будут происходить в определенной плоскости. Плоскость, перпендикулярная плоскости колебаний в поляризованном луче, называется плоскостью поляризации (рисунок 9).
Способность некоторых веществ вращать плоскость поляризации называется оптической активностью. Обнаружено, что одни вещества вращают плоскость поляризации вправо (+) правовращающие, а другие – влево (-) левовращающие.
Оптическая активность связана с асимметрией молекулы, т. е. наличием различных групп атомов, которые могут различным образом располагаться в пространстве.
Рисунок 9 – Схема
колебаний в луче обыкновенного и
поляризованного света
1 – обыкновенный
свет;
2 – призма Николя;
3 – поляризованный
свет;
4- плоскость
поляризации
Так как два зеркальных изомера обладают оптической активностью, т.е. вращают плоскость поляризованного света на определенный угол (один вправо, а другой – влево), зеркальную изомерию называют также оптической изомерией.
Так, для глицеринового альдегида D-изомер вращает плоскость поляризации вправо, L – влево. Далеко не во всех случаях вещества D-ряда вращают вправо, а вещества L-ряда – влево плоскость поляризации, так как вращение зависит не только от общего расположения тождественных или сходных атомных групп, но и от того, какие именно группы связаны с центром асимметрии. Так, D-молочная кислота имеет левое вращение, а L – правое.
Когда хотят обозначить не только конфигурацию, но и вращение, при наименовании веществ ставят не только букву D или L, но и знак «+» или «-», обозначающие соответственно правое или левое вращение.
Зеркальные изомеры обладают равным, но противоположным по знаку вращением – правым и левым, а потому они часто называются оптическими антиподами.
Оптически неактивные соединения, состоящие из равных количеств оптических антиподов, называются рацемическими соединениями или рацематами. Оказалось, что рацемические соединения можно получить, если смешать равные количества правого и левого антипода. Наоборот, существует ряд способов, при помощи которых можно разделить, рацематы на оптически активные изомеры – антиподы.
Химические свойства
Оксикислоты, содержащие карбоксил и гидроксил, дают все реакции, свойственные карбоксильной группе, спиртовому гидроксилу, и реакции, характерные лишь для оксикислот:
а) свойства, зависящие от наличия гидроксила:
1) диссоциация:
Оксикислоты, как правило, являются более сильными кислотами, чем обычные кислоты с тем же числом атомов углерода. Чем ближе спиртовой гидроксил находится к карбоксильной группе, тем сильнее данная оксикислота;
2) образование солей:
О ксикислоты,
подобно
обычным
кислотам.
ксикислоты,
подобно
обычным
кислотам.
3) образование сложных эфиров:
При замещении гидроксила в карбоксиле на остаток спирта оксикислоты дают сложные эфиры, например:

б) свойства, зависящие от наличия спиртового гидроксила:
1) способность окисляться:
О ксикислоты,
подобно спиртам, способны окисляться
(в отличие от обычных кислот, которые,
как правило, стойки к окислению). При
окислении спиртовая группа превращается
в карбонильную группу альдегида или
кетона в зависимости от наличия
первичной или вторичной спиртовой
группы. При этом оксикислоты
превращаются в альдегидокислоты или
кетонокислоты:
ксикислоты,
подобно спиртам, способны окисляться
(в отличие от обычных кислот, которые,
как правило, стойки к окислению). При
окислении спиртовая группа превращается
в карбонильную группу альдегида или
кетона в зависимости от наличия
первичной или вторичной спиртовой
группы. При этом оксикислоты
превращаются в альдегидокислоты или
кетонокислоты:
2) образование сложных эфиров:
П
 ри
замещении в спиртовом гидроксиле атома
водорода кислотным остатком оксикислоты
дают сложные эфиры:
ри
замещении в спиртовом гидроксиле атома
водорода кислотным остатком оксикислоты
дают сложные эфиры:
3) образование простых эфиров:
П ри
замещении в спиртовом гидроксиле атома
водорода радикалом образуются простые
эфиры, например:
ри
замещении в спиртовом гидроксиле атома
водорода радикалом образуются простые
эфиры, например:
Таким образом, оксикислоты могут дать ряд эфиров, а именно:
сложные эфиры (со спиртами), в которых оксикислоты играют роль кислоты;
сложные эфиры (с кислотами), в которых оксикислоты играют роль спиртов;
простые эфиры, в которых оксикислоты играют роль спиртов;
дважды сложные эфиры (со спиртами и кислотами), в которых оксикислоты одновременно играют роль и кислот и спиртов.
Примером эфиров этого типа может служить метиловый эфир аце- тилгликолевой кислоты:

Спиртовой гидроксил оксикислот – способен обмениваться на галогены с образованием галогенокислот и вступать в другие реакции, характерные для спиртов.
в) реакции, характерные лишь для оксикислот:
1) расщепление a-оксикислот на альдегиды (или кетоны) и муравьиную кислоту:
 Эта
реакция протекает легко при нагревании
a-оксикислот
с минеральными кислотами:
Эта
реакция протекает легко при нагревании
a-оксикислот
с минеральными кислотами:
2 )
выделение воды:
)
выделение воды:
Протекает легко и приводит в случае a-, b- и g-оксикислот к образованию различных продуктов.
a -оксикислоты
вступают в реакцию таким образом, что
из двух молекул кислоты выделяются две
молекулы
воды и образуется соединение с шестичленным
кольцом, называемое лактидом:
-оксикислоты
вступают в реакцию таким образом, что
из двух молекул кислоты выделяются две
молекулы
воды и образуется соединение с шестичленным
кольцом, называемое лактидом:
Как видно из реакции, лактиды являются сложными эфирами. От ранее изученных сложных эфиров они отличаются тем, что образуются из двух молекул соединений, имеющих одновременно кислотные и спиртовые группы, а также тем, что содержат в молекулах шестичленные циклы. Как все сложные эфиры, лактиды легко гидролизуются при нагревании с кислотами, переходя в исходные оксикислоты;
b- оксикислоты очень легко (при нагревании) дегидратируются таким образом, что из каждой молекулы оксикислоты выделяется молекула воды и получается непредельная кислота:
g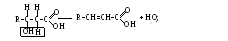 -оксикислоты
(а также d-оксикислоты)
также выделяют из каждой молекулы
оксикислоты одну молекулу воды, но эта
молекула воды образуется за счет
карбоксила и спиртового гидроксила;
при этой реакции получаются соединения
с пятичленным циклом (из g-оксикислот)
или с шестичленным циклом (из d-оксикислот),
носящие название лактонов.
-оксикислоты
(а также d-оксикислоты)
также выделяют из каждой молекулы
оксикислоты одну молекулу воды, но эта
молекула воды образуется за счет
карбоксила и спиртового гидроксила;
при этой реакции получаются соединения
с пятичленным циклом (из g-оксикислот)
или с шестичленным циклом (из d-оксикислот),
носящие название лактонов.
Л актоны
получаются обычно очень легко, часто
даже при стоянии водных растворов при
комнатной температуре.
актоны
получаются обычно очень легко, часто
даже при стоянии водных растворов при
комнатной температуре.
Лактоны представляют собой сложные эфиры, образованные за счет карбоксила и гидроксила в пределах одной молекулы. Лактоны чрезвычайно легко гидролизуются. Щелочи особенно сильно ускоряют этот процесс, причем в результате действия щелочей на лактоны получаются соли оксикислот:

