- •§1.Общая характеристика атомов.
- •§2.Законы теплового излучения.
- •§3.Испускание и поглощение излучения по квантовой теории. Вывод формулы Планка по Энштейну., 1916г.
- •§5. Ядерная модель атома. Формула резерфорда.
- •§14. Дифракция рентгеновских лучей (рл) на кристаллической решетке.
- •§15. Формула Вульфа-Брегга.
- •§16. Экспериментальное наблюдение дифракции
- •§17. Корпускулярно волновой дуализм.
- •§18. Эффект Комптона.
- •§19. Волновые свойства частиц.
- •§20. Экспериментальное подтверждение гипотезы де Бройля.
- •§21. Статистическая интерпретация волн де Бройля.
- •§22. Соотношение неопределенностей Гейзенберга 1927г.
- •§23. Постулаты квантовой физики.
- •§24. Принцип суперпозиции квантовых состояний.
- •§25. Примеры движения квантовой частицы в стационарных
- •§26. Момент импульса квантовой теории.
- •§27. Гипотеза Уленбека (Юленбека) и Гаудсмита о спине электрона.
- •§28. Спектр атома водорода.
- •§29. Щелочные металлы.
- •§36. Эффект Зеемана.
- •§37. Неразличимость тождественных квантовых частиц.
- •§ 38. Периодическая система элементов (псэ)
§36. Эффект Зеемана.
Эффект Зеемана состоит в расщеплении спектральных термов и соответствующих спектральных линий в МП.
В
слабом МП
 - связь сохраняется, т.е. взаимодействие
- связь сохраняется, т.е. взаимодействие и
и между собой сильнее, чем взаимодействие
отдельных моментов
между собой сильнее, чем взаимодействие
отдельных моментов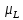 и
и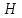 ,
,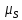 и
и с МП. В таком случае наблюдается аномальный
эффект Зеемана, при котором спектральные
линии расщепляются больше, чем на три
компоненты.
с МП. В таком случае наблюдается аномальный
эффект Зеемана, при котором спектральные
линии расщепляются больше, чем на три
компоненты.
В
сильном МП спин – орбитальное
взаимодействие разрывается, т.к. энергия
взаимодействия отдельных моментов с
МП превосходит энергию спин – орбитального
взаимодействия
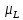 и
и .
.
В
МП любой уровень расщепляется на
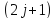 компонент, которые расположены на
одинаковом расстоянии друг от друга,
это расщепление много меньше, чем
расстояние между компонентами тонкой
структуры.
компонент, которые расположены на
одинаковом расстоянии друг от друга,
это расщепление много меньше, чем
расстояние между компонентами тонкой
структуры.
Рассмотрим пример главной серии щелочных металлов:

Любой переход данной серии имеет две компоненты тонкой структуры.
Рассмотрим
терм
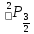 :
:

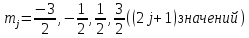
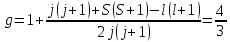
Рассмотрим
терм
 :
:


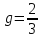
Рассмотрим
терм
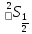 :
:
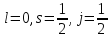


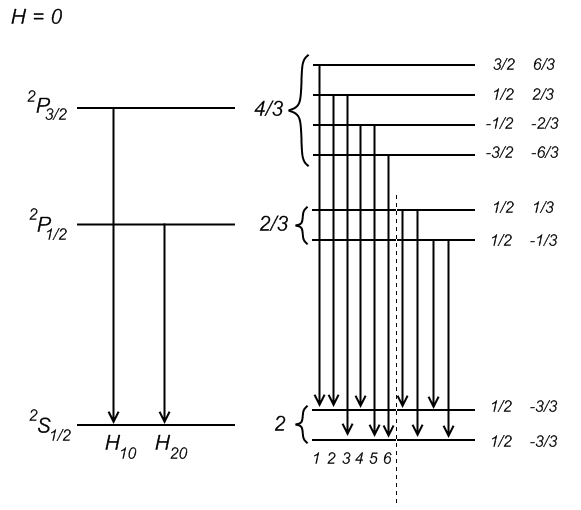
Правила отбора в слабом МП:

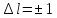

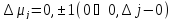
Рассмотрим
частоты перехода
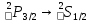 :
:
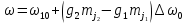
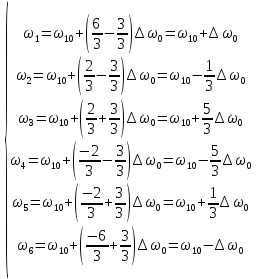
Спектральные линии при этом расщепляются на три компоненты. Этот эффект называют эффектом Пашена – Бака.
Для
 термов в слабом МП также наблюдается
ращепление на три компоненты. Этот
эффект называют нормальным эффектом
Зеемана для
термов в слабом МП также наблюдается
ращепление на три компоненты. Этот
эффект называют нормальным эффектом
Зеемана для термов.
термов.
В МП сохраняется только проекция механического момента на выделенное направление.
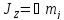

В общем случае в МП энергия атома зависит от трех квантовых чисел: главного квантового числа, орбитального квантового числа, спинового квантового числа.
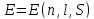
В
МП энергия атома оказывается зависящей
от дополнительного квантового числа
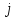 .
.
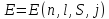
Таким
образом, в МП один энергитический уровень
атома расщепляется на
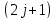 Зеемановский подуровень.
Зеемановский подуровень.
Значит,
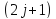 - есть статистический вес уровня или
кратность его вырождения в отсутствии
МП.
- есть статистический вес уровня или
кратность его вырождения в отсутствии
МП.

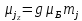
Атом в МП обладает дополнительной энергией, которая определяется, как:
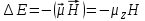
Аномальный эффект Зеемана.
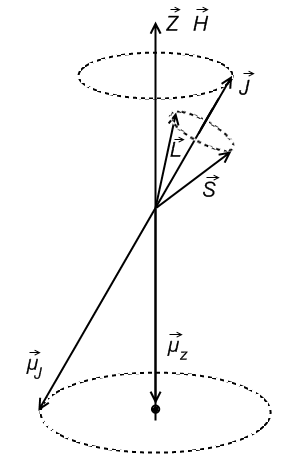

Для
случая
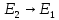 с испусканием света в отсутствии МП:
с испусканием света в отсутствии МП:
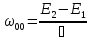
В присутствии МП энергия атома:
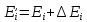


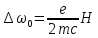
 –Лоренцева
частота или частота нормального
расщепления спектральной линии.
–Лоренцева
частота или частота нормального
расщепления спектральной линии.
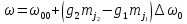
Д/З:
рассчитать частоты переходов,
соответствующих второй компоненте
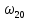 .
.
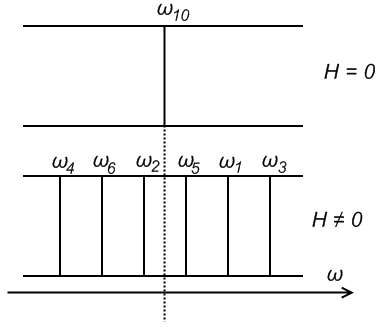
Нормальный эффект Зеемана.
Расщепление спектральных линий, соответствующих синглетным уровням, на три компоненты. Лоренцев триплет.
Для синглетных уровней:
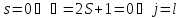
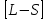 –связь
отсутствует.
–связь
отсутствует.

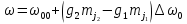
Согласно правилам отбора
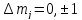
Лоренцев триплет:

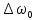 -
частота нормального расщепления.
-
частота нормального расщепления.
Можно считать, что для синглетных уровней любое магнитное поле сильное, т.к. оно взаимодействует только с магнитным орбитальным моментом.
Расщепление спектральных линий в сильном МП. Эффект Пашена – Бакка.
В
сильном МП
 - связь разрывается и поле взаимодействует
по отдельности с орбитальным и спиновым
магнитным моментами.
- связь разрывается и поле взаимодействует
по отдельности с орбитальным и спиновым
магнитным моментами.
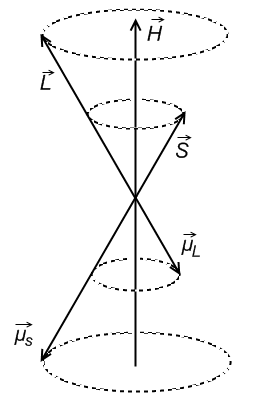
Результирующий магнитный момент атома:
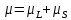

Дополнительная энергия, приобретенная атомом:

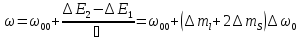
Правила отбора в сильном МП:
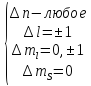
Т.о., в сильном МП каждая компонента расщепляется на три.

Расщепление спектральных линий в ЭП называют эффектом Штарка.
§37. Неразличимость тождественных квантовых частиц.
Принцип Паули (пятое начало квантовой механики).
Рассмотрим
СС одинаковых квантовых частиц, например
электронов. Все они имеют одинаковые
характеристики:
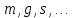 ,
однако в отличии от классических частиц,
все эти электроны принципиально не
различимы. Если классическим частицам
можно сопоставить определенную
траекторию, другими словами - пронумеровать,
то для квантовых частиц это невозможно
в силу соотношений неопределенности.
,
однако в отличии от классических частиц,
все эти электроны принципиально не
различимы. Если классическим частицам
можно сопоставить определенную
траекторию, другими словами - пронумеровать,
то для квантовых частиц это невозможно
в силу соотношений неопределенности.

Вероятность нахождения СС в таком состоянии, что:

В
элементе объема
 :
:
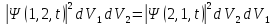
Т.к. частицы принципиально не различимы, это равенство возможно в двух случаях:
1)
 – волновая функция симметрична
относительно перестановки двух частиц.
– волновая функция симметрична
относительно перестановки двух частиц.
2)
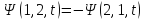 – волновая функция антисимметрична.
– волновая функция антисимметрична.
Общая формулировка принципа Паули:
Волновая функция СС тождественных частиц с полуцелым спином полностью антисимметрична относительно перестановки двух частиц. Частицы с полуцелым спином называются фермионами и говорят, что они подчиняются статистике Ферми – Дирака.
Волновая функция тождественных частиц с целым спином полностью симметрична относительно любых перестановок частиц, сами такие частицы называют бозонами и говорят, что они относятся к статистике Бозе – Энштейна.
Для
фотона:
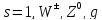
Рассмотрим атом, как многоэлектронную СС, будем считать, что взаимодействие электронов между собой незначительно. Тогда состояние любого электрона в атоме описывается четырьмя степенями свободы, другими словами, четырьмя квантовыми числами, эти четверки могут быть выбраны любыми:
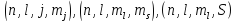
Рассмотрим
наиболее общий случай
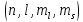 :
:
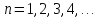 - главное квантовое число
- главное квантовое число
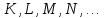 - обозначение квантового слоя
- обозначение квантового слоя
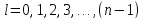 - орбитальное квантовое число
- орбитальное квантовое число
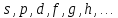
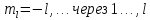 - магнитное орбитальное квантовое число
- магнитное орбитальное квантовое число
 способом орбитальный момент импульса
может ориентироваться относительно
выбранного направления.
способом орбитальный момент импульса
может ориентироваться относительно
выбранного направления.
 – магнитное спиновое квантовое число
– магнитное спиновое квантовое число
 способом спиновый механический момент
может ориентироваться на выделенное
направление.
способом спиновый механический момент
может ориентироваться на выделенное
направление.
Частная формулировка принципа Паули:
В атоме не может быть двух или более электронов с одинаковой четверкой квантовых чисел.
Рассмотрим основное триплетное состояние атома гелия. Докажем, что для него невозможно состояние:

Из
вышестоящего следует, что
 .
Значит, гелий может находиться только
в основном
.
Значит, гелий может находиться только
в основном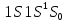 синглетном состоянии, а состояние
синглетном состоянии, а состояние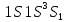 - запрещено принципом Паули, т.к. для его
реализации необходимо противоречащее
принципу Паули равенство всех четырех
квантовых чисел.
- запрещено принципом Паули, т.к. для его
реализации необходимо противоречащее
принципу Паули равенство всех четырех
квантовых чисел.
Очевидно,
что терм
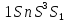 , где
, где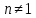 возможен:
возможен:
С одинаковыми квантовыми числами
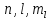 . В атоме может быть только два электрона
. В атоме может быть только два электрона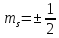
С одинаковыми квантовыми квантовыми числами
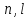 в атоме может быть только
в атоме может быть только электрона.
электрона.
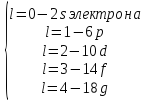
С одним и тем же квантовым числом
 в атоме может быть
в атоме может быть электронов.
электронов.
Электроны
с одинаковым значением
 образуют электронную оболочку атома
образуют электронную оболочку атома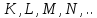 Оболочки электронов с одинаковыми
числами
Оболочки электронов с одинаковыми
числами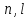 называют эквивалентными, они образуют
подоболочку атома
называют эквивалентными, они образуют
подоболочку атома