
- •1. Методы исследования органических соединений, содержащих ковалентно-связанный галоген
- •Идентификация галогенид-ионов
- •Количественное определение галогенидов
- •Методы идентификации органических соединений, содержащих ковалентно-связанный атом серы
- •Методы количественного определения органических соединений, содержащих ковалентно-связанный атом серы
- •3. Методы исследования органических соединений, Содержащих кратные связи
- •Методы идентификации органических соединений, содержащих кратные связи
- •Методы количественного определения органических соединений, содержащих кратные связи
- •4. Методы исследования веществ, содержащих спиртовый гидроксил
- •Методы идентификации веществ, содержащих спиртовый гидроксил
- •Количественное определение веществ, содержащих спиртовый гидроксил
- •5. Методы исследования веществ, содержащих енольный гидроксил
- •Методы идентификации веществ, содержащих енольный гидроксил
- •Количественное определение веществ, содержащих енольный гидроксил
- •6. Методы исследования веществ, содержащих альдегидную и кетонную группы
- •Методы идентификации веществ, содержащих альдегидную и кетонную группы
- •Количественное определение веществ, содержащих альдегидную группу
- •Количественное определение веществ, содержащих кетогруппу
- •Методы идентификации карбоновых кислот и их солей
- •Методы количественного определения карбоновых кислот
- •Методы количественного определения солей карбоновых кислот
- •8. Методы исследования веществ, содержащих сложноэфирную и амидную группы
- •Количественное определение веществ, содержащих сложноэфирную и амидную группы
- •9. Методы исследования веществ, содержащих третичный атом азота и алифатическую аминогруппу
- •Методы идентификации веществ, содержащих третичный атом азота, алифатическую аминогруппу
- •Методы количественного определения веществ, содержащих третичный атом азота и алифатическую аминогруппу
- •10. Методы исследования веществ, содержащих ароматическую аминогруппу и нитрогруппу
- •Методы идентификации веществ, содержащих ароматическую аминогруппу и нитрогруппу
- •Количественное определение веществ, содержащих ароматическую аминогруппу и нитрогруппу
- •11. Методы исследования веществ, содержащих фенольный гидроксил
- •Методы идентификации веществ, содержащих фенольный гидроксил
- •Количественное определение фенолов
- •Литература

Эту реакцию можно положить в основу количественного определения фторсодержащих веществ фотоэлектроколориметрическим методом или титриметрическим, используя в качестве титранта циркония нитрат.
Также фториды можно определять по реакции с солями кальция по образованию нерастворимого белого осадка кальция фторида:
Количественное определение галогенидов
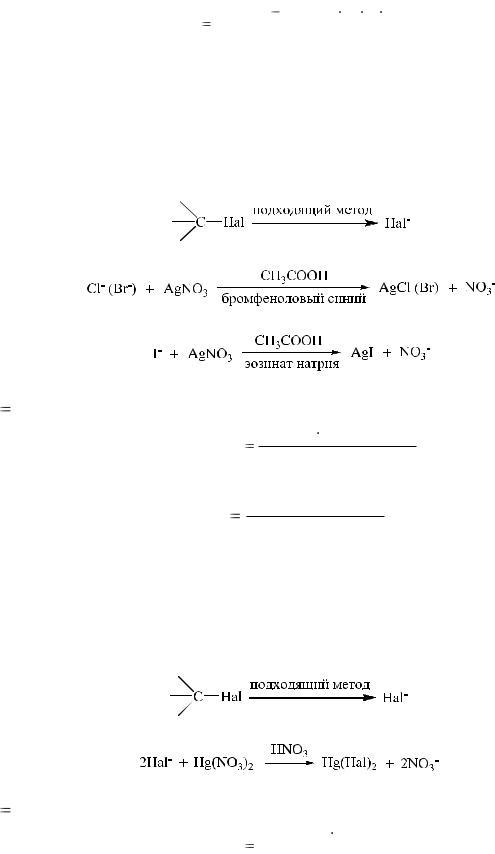
Для количественного определения галогенидов используются аргентометрические методы Фольгарда и Фаянса, меркуриметрические методы.
1. Метод Фольгарда (аргентометрия).
Этот метод является универсальным. После переведения ковалентносвязанного галогена в ионное состояние подходящими методами проводят титрование избытка серебра нитрата раствором аммония тиоцианата в азотнокислой среде, в качестве индикатора используют раствор железоаммониевых квасцов:
f 1.
X%
TAgNO / препарат |
Сэ( AgNO ) M (1/ z)препарата |
, |
|
|||
|
3 |
|
|
|
||
|
1000 |
|
|
|
||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
(VAgNO3 K AgNO3 |
VNH4 NCS |
K NH4 NCS ) T 100 |
||||
|
|
|
|
|
|
. |
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
8
Расчетная формула содержания препарата с учетом контрольного опыта:
|
(V к.о. |
V |
NH NCS |
) K T 100 |
|
X % |
NH NCS |
|
|
. |
|
4 |
|
4 |
|
||
|
|
|
|
a
2. Метод Фаянса (аргентометрия).
После перевода галогена в ионное состояние осуществляют титрование в слабо уксуснокислой среде в присутствии адсорбционных индикаторов. При титровании хлоридов и бромидов применяют бромфеноловый синий, а при титровании йодидов – эозинат натрия:
f 1.
TAgNO / препарат
3
X%
Сэ( AgNO ) M (1/ z)препарата ,
3
1000
VAgNO3  K
K  T
T  100 .
100 .
a
3. Меркуриметрический метод.
После перевода галогена в ионное состояние проводят титрование раствором ртути (II) нитрата в азотнокислой среде. В качестве индикатора используют дифенилкарбазид:
f 1.
THg( NO ) / препарат |
Сэ( Hg( NO ) |
) |
M (1/ z)препарата |
, |
|||
3 |
2 |
|
|
|
|||
|
|
|
1000 |
|
|||
3 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||
9
X% |
|
VHg( NO ) |
|
K T 100 |
|
||||||
|
|
|
3 |
|
2 |
|
. |
|
|||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
a |
|
|
|
Расчетная формула содержания препарата с учетом контрольного |
|||||||||||
опыта: |
|
|
|
|
|
|
|
|
|
|
|
|
(V |
Hg ( NO ) |
|
V |
к.о. |
|
) K T 100 |
|
|||
X % |
|
Hg ( NO ) |
|
|
. |
||||||
3 |
2 |
|
|
|
3 |
2 |
|
||||
|
|
|
|
|
|
|
|||||
a
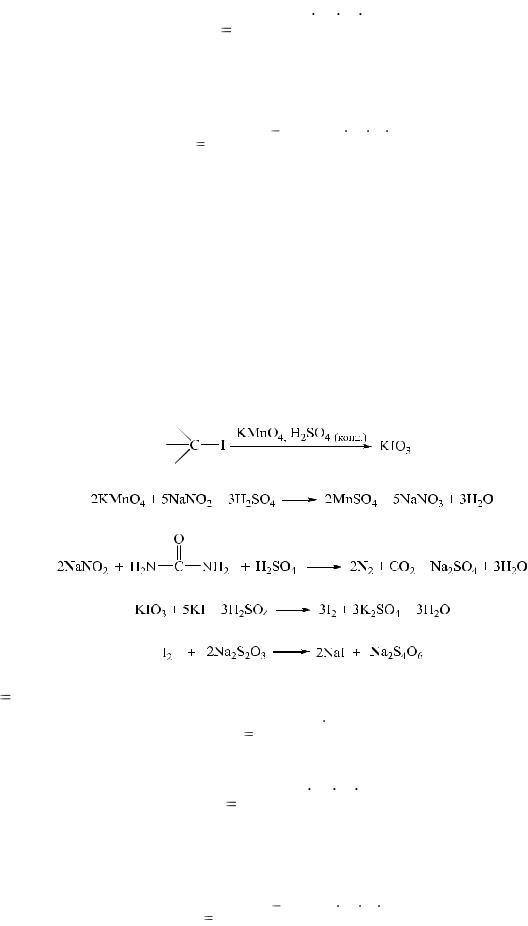
4.Йодиметрия.
Вслучае мокрой окислительной минерализации количественное определение сводится к следующему. Минерализацию проводят калия перманганатом в кислой среде. Избыток калия перманганата восстанавливают натрия нитритом, а избыток последнего удаляют мочевиной, в противном случае эти окислители будут реагировать с калия йодидом. В полученный раствор добавляют калия йодид и титриметрически определяют выделившийся йод. Таким образом, этот метод можно использовать для количественного определения йодсодержащих лекарственных веществ.
f 1/ 2 .
|
|
|
Сэ( Na S O ) |
M (1/ z)препарата |
|
|||
|
|
2 |
2 |
3 |
|
|
|
|
TNa S O / препарат |
|
|
|
|
|
, |
||
|
|
|
1000 |
|
||||
2 |
2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VNa S O |
|
K T 100 |
|
|||||||
X% |
|
2 |
2 |
|
3 |
|
|
. |
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
a |
|
|
|
|
Расчетная формула содержания препарата с учетом контрольного |
||||||||||||
опыта: |
|
|
|
|
|
|
|
|
|
|
|
|
|
(VNa S O |
|
к.о. |
|
|
) K T 100 |
|
|||||
X % |
VNa S O |
. |
||||||||||
2 |
2 |
3 |
|
|
2 |
2 |
3 |
|
|
|||
|
|
|
|
|
|
|||||||
a
10
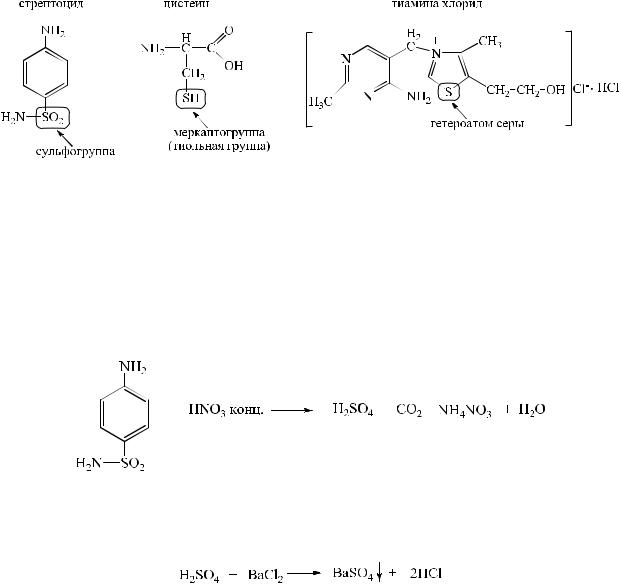
2.МЕТОДЫ ИССЛЕДОВАНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ КОВАЛЕНТНО-СВЯЗАННЫЙ АТОМ СЕРЫ
Впрепаратах органической природы встречается ковалентносвязанный атом серы в виде сульфогруппы, тиольной группы, а также гетероатом серы.
Методы идентификации органических соединений, содержащих ковалентно-связанный атом серы
1. Наличие серы в сульфо-группе молекулы серосодержащего соединения можно установить окислением органической части молекулы кислотой азотной концентрированной или сплавлением с десятикратным количеством калия (натрия) нитрита до сульфат-иона.
Выделившийся сульфат-ион идентифицируют раствором бария сульфата, выпадает белый осадок.
2. Для обнаружения серы в тиольной группе препарат сплавляют с 30% раствором натрия гидроксида, происходит разрушение молекулы серосодержащего соединения с образованием меркаптана и сульфидов.
11
