
ОЯФРиД
.pdf3.4. Энергия отдачи для разных типов ядерных превращений. Метод разделения изотоповСцилларда-Чалмерса
Для обобщения проведенных расчетов и формулировки выводов сведем полученные результаты в одну таблицу и сравним приведенные в ней цифры с энергией теплового движения одноатомного газа (0,025 эВ), с энергией химической связи (1-5 эВ) и рассчитаем условную “температуру” атомов отдачи по формуле
Т=1,16.104 Екин,0К/эВ
Таблица 3.6.
Энергия отдачи для разных типов ядерных превращений
|
|
Энергия отдачи (эВ) |
|
|
|
|
|
|
|
Мя (а.е.м.) |
|
|
|
Еβmax= 1,5 |
|
|
|
Mev, |
|
|
|
|
Ее- = 1 Mev |
|
|
Еγ = 2 Mev |
Еα = 5 Mev |
Eν = 0,5 |
|
|
|
|
|
Mev, |
|
|
|
|
= 0 |
20 |
107 |
106 |
53,8 |
87,63 |
50 |
43 |
0,4.106 |
21,5 |
35,04 |
100 |
21 |
0,2.106 |
10,7 |
17,52 |
200 |
11 |
105 |
5,4 |
8,16 |
Из приведенных в таблице данных можно сделать следующие выводы.
•Энергия отдачи охватывает широкий диапазон от долей эВ до миллионов эВ, во многих случаях значительно превышая энергию химической связи атомов в молекулах (1-5 эВ).
•Условная температура атомов отдачи в момент их образования лежит в диапазоне от десятков до десятков миллиардов градусов К – ядра находятся в перегретом состоянии, поэтому их химическое поведение и называется химией горячих атомов.
Важность знания химии горячих атомов обусловлена:
•возможностью разделения изотопов и изомеров, получаемых с использованием ядерных реакций (n,у), (у,n), (n,р), (n, ), (n,2n), (ИП);
•возможностью выделения радионуклидов из облучаемой мишени без
носителя;
•возможностью осуществления реакций микросинтеза меченых радионуклидами химических соединений;
Кафедра радиохимии и
прикладной экологии© |
71 |
|

• возможностью установления форм состояния радионуклидов (или их продуктов распада) в твердой фазе;
По реакции (n,у) образуются изотопы тех же элементов, которые подвергаются облучению. Поэтому выделение радиоактивных атомов из мишени связано с необходимостью разделения изотопов одного и того же элемента. Трудность разделения изотопных атомов усугубляется еще и исключительно малым содержанием радиоактивных изотопов в облучаемой мишени, а также ограниченной продолжительностыо их жизни.
Единственным методом отделения радиоактивных атомов от стабильных, входящих в состав мишени, является метод атомов отдачи (метод Сцилларда — Чалмерса). Суть метода состоит в следующем. Захват нейтрона ядром активируемого изотопа сопровождается образованием составного возбужденного ядра, которое переходит в основное состояние путем эмиссии гамма-квантов захвата. Например, при облучении C2H5127I нейтронами происходит ядерная реакция 127I(n, )128I с образованием радиоактивного изотопа 128I (Т1/2=25 мин). Получаемая атомом иода энергия отдачи обычно во много раз превышает энергию химической связи атомов элемента в облучаемом соединении. В результате происходит разрушение исходной молекулы, и радиоактивный атом оказывается в химической форме, отличной от исходной. В данном случае происходит преимущественное образование 128I в молекулярном состоянии. При этом чрезвычайно трудная проблема разделения изотопов сводится к разделению различных химических форм одного и того же элемента. Для этого достаточно промыть органическую фазу водой с восстановителем
Na2SO3 +128I2+H2O =Na2SO4+2128I- +2H+
и весь радиоактивный иод перейдет в водную фазу.
Таким образом, метод Сцилларда — Чалмерса позволяет разделять изотопы и получать препараты радиоактивных изотопов с высокой удельной активностью.
Эффективность метода Сцилларда — Чалмерса зависит от природы исходного соединения, условий облучения, метода изолирования радиоактивного изотопа и характеризуется выходом и фактором обогащения. Выход радиоактивного изотопа В определяется отношением числа выделяемых радиоактивных атомов Nв* к общему числу радиоактивных атомов в облученном соединении N* и выражается в процентах:
B NВ* 100
N*
Отсюда может быть вычислена величина удержания У= 100-В,%.
Фактор обогащения К представляет собой отношение массовых удельных
активностей обогащенной фракции (аобог) и облученного вещества до разделения (аИСХ): |
||
Кафедра радиохимии и |
72 |
|
прикладной экологии© |
||
|
||
K aобог 106 aисх
На выход радиоактивного изотопа, образующегося по реакции (n,у), существенное влияние оказывает явление удержания, следствием которого является сохранение части радиоактивных атомов в форме исходного соединения. Причинами удержания могут быть: сохранение молекул, подвергаемых облучению (вклад этого процесса в общее удержание невелик); реакции «горячих» и эпитермальных атомов, которые способствуют переходу радиоактивных атомов в форму исходного соединения; превращение атомов радиоактивного изотопа в форму исходного соединения в результате радиационно-химических и обычных тепловых реакций.
3.5. Удержание. Классификация причин удержания
Известно, что радиоактивные атомы, получающиеся в результат ядерных превращений, частично оказываются в химическом соединении, в котором произошло их образование (в виде так называемого «материнского» соединения). Например, при облучении нейтронами галогенпроизводных органических соединений значительная доля радиоактивного галогена, образующегося по n, -реакции, оказывается в виде исходной молекулы и не может быть отделена от нее. Это явление получило название удержания, (гetention). Оно характеризуется долей радиоактивных атомов, образующихся после ядерного процесса в виде материнского соединения. Иногда удержанием называют долю радиоактивных атомов не только в виде исходного соединения, но и в виде всех других часто неотделимых от исходного простыми способами соединенения («кажущееся» удержание), т.е. образование наряду с материнскими галогенорганическими соединениями других галогенорганических соединений с числом атомов галогена на единицу больше, чем в материнской молекуле (табл.3.7).
Таблица 3.7. Кажущееся удержание после n, -реакций галогенпроизводных органических
соединений.
Облучаемое |
|
|
Удержание в виде |
соединение |
Ядерная реакция |
Кажущееся |
материнской |
|
|
удержание, % |
молекулы, % |
CH5I |
127I (n, )128I |
56 |
44 |
CH2Br2 |
81Br(n, )82Br |
67 |
51 |
CHBr3 |
81Br(n, )82Br |
69 |
49 |
C6H5Cl |
37Cl(n, )38Cl |
50 |
35 |
Кафедра радиохимии и
прикладной экологии© |
73 |
|
3.5.1.Ядерно-физические причины удержания
Кядерно-физическим причинам удержания относят:
1.Соотношение масс ядра (М—масса атома отдачи) и радикала (MR — масса остатка молекулы). Этот вопрос подробно рассмотрен в разделе 3.2.
2.Временное и угловое распределение фотонов (при потере энергии возбуждения путем испускания каскада -квантов). Частично этот вопрос рассмотрен в разделе 3.1., испускание квантов. Будем считать, что -кванты испускаются одновременно, если выполняется условие V t<10-8 см, где V-скорость атома отдачи, см/сек, t –интервал времени между испусканием -квантов, сек. Указанное условие означает, что ядро атома отдачи не покидает пределов своего силового поля, а t=10-14 сек. При выполнении указанного условия можно воспользоваться уравнением (3.12) и показать, что в случае эмиссии фотонов в строго противоположных направлениях ( =1800) и 1= 2 при сколь угодно большой энергии фотонов E =0 и удержание будет полным (У=100%).
Из величин максимального и минимального значения энергии (смотри уравнение
(3.12)), отвечающие эмиссии фотонов в одном ( =00, cos =1) и противоположных ( =1800, cos =-1) направлениях, можно рассчитать энергетический интервал, в котором может находиться ядро атома отдачи
E E max E min 42Mc1 22
3. Внутренние соударения, возникающие в результате действия радиальной компоненты.
Отсутствие разрыва связи в последнем случае является результатом внутренних неупругих соударений атома отдачи с атомами молекулы, в которой он образовался. Энергия отдачи может быть разложена на тангенциальную (Pτ) и радиальную (Pr) компоненты.
P
P
Я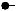 ц.т. R
ц.т. R
Pr
Рис.3.2. Разложение импульса атома отдачи на тангенциальную (Pτ) и радиальную (Pr)
компоненты. Здесь ц.т. – центр тяжести молекулы, состоящей из атома отдачи и его ядра (Я), а так же остатка молекулы R.
Кафедра радиохимии и
прикладной экологии© |
74 |
|
Первая (Pτ) сообщает молекуле вращательное движение относительно центра тяжести и ослабляет химическую связь, а вторая (Pr) — идет на удаление или сближение атома отдачи с другими атомами. При направлении радиальной компоненты от центра тяжести молекулы энергия отдачи затрачивается на разрыв связи. Если Pr>Ех.св, то связь рвется и У=0, при Pr<Ех.св удержание полное (У=100%). Если радиальная компонента направлена внутрь молекулы, к ее центру тяжести, то а) при Pr>Ех.св и упругом соударении У=0, а при неупругом столкновении в случае Pr – Е >Ех.св также У=0, а в случае Pr – Е <Ех.св при неупругих столкновениях происходит возбуждение молекулы без ее диссоциации и имеет место полное удержание (У=100%); б) при Pr<Ех.св удержание будет полным (У=100%).
Расчеты, проведенные чешским исследователем К. Свободой, показывают, что лишь доли процента молекул могут сохраняться вследствие внутренних неупругих соударений. Иногда все эти ядерно-физические причины удержания называют первичным удержанием.
Первичное удержание. Как было показано, химические связи атома отдачи с другими атомами в молекуле в подавляющем большинстве случаев должны рваться. Разрыв связи вследствие явления отдачи может не иметь места в следующих случаях: 1) если энергия связи больше энергии отдачи (изомерный переход, электронный захват, -распад); 2) если доля энергии, затрачиваемая на разрыв связи, меньше энергии связи; 3) если имеет место компенсация суммарной энергии отдачи при испускании нескольких -квантов или - частицы и нейтрино; 4) если направление движения атома отдачи по отношению к связи его с молекулой идет под малым углом внутрь молекулы.
Удержание без разрыва химической связи вновь образовавшегося радиоактивного атома в молекуле называется первичным удержанием.
3.5.2.Физико-химические причины удержания
1.Реакции горячих атомов (вторичное удержание) – реакции между “остывающими” атомами и атомами и молекулами окружающей среды. Удержание не может являться только результатом сохранения молекул. Это следует из величин энергий отдачи, значительно превышающих энергии связи атомов в молекулах, и больших величин удержания в подавляющем большинстве ядерных превращений. Вторичное удержание является результатом химических реакций атомов отдачи с атомами среды, в которой они зарождаются и движутся. Это видно из того, что наряду с материнской молекулой радиоактивные атомы оказываются в виде молекул, которые являются продуктами замещения других атомов и атомных групп в материнской молекуле на атомы отдачи. Например, из анилина при облучении его нейтронами образуются содержащие 14С молекулы
анилина, метиланилина и толуола — продукты замещения на атомы отдачи 14С углерода,
Кафедра радиохимии и
прикладной экологии© |
75 |
|

водорода и азота:
Подобно этому и во всех других случаях атомы отдачи замещают себе подобные атомы в материнской молекуле, образуя материнскую молекулу, включающую атом отдачи.
Удержание, являющееся результатом химических реакций атома отдачи с атомами среды, в которой зарождаются атомы отдачи, называется вторичным удержанием.
Обычные (тепловые) химические реакции подчиняются законам аррениусовской кинетики, которая базируется на максвелл-больцмановском распределении молекул по скоростям. При таком распределении скорость реакции пропорциональна концентрациям реагирующих веществ, т. е. числу эффективных столкновений молекул, столкновений, при которых энергия сталкивающихся частиц превышает пороговую энергию реакции.
При тепловых реакциях скорость исчезновения молекул больших энергий мала и практически мгновенно восстанавливается максвелл-больцмановское распределение молекул по скоростям. При высоких температурах (3000—10000°С) скорость реакций столь велика, что максвелл-больцмановское распределение нарушается, и кинетика таких реакций не может удовлетворительно описываться по Аррениусу. Атомы отдачи после ядерной реакции зарождаются все с одинаковыми энергиями. По мере их столкновений с окружающими молекулами и атомами происходит потеря ими энергии, и к области энергий, при которых могут возникнуть химические связи атомов отдачи с другими атомами, они подходят от высоких энергий. При этом поток атомов отдачи имеет распределение по энергиям, не отвечающее максвелл-больцмановскому. Следовательно, для атомов отдачи кинетика реакций не может описываться по Аррениусу. К таким атомам следует применять методы, разработанные для ядерных реакций.
«Горячими» атомами будем называть атомы, имеющие энергию выше пороговой энергии для данной химической реакции и не максвелл-больцмановское распределение по энергиям. Реакции таких атомов будем называть реакциями горячих атомов («горячими»).
Не все горячие атомы отдачи вступают в химическое взаимодействие с окружающими атомами, часть из них в результате соударений охлаждается до тепловых скоростей. Такие атомы отдачи могут реагировать с продуктами радиолиза (смотри раздел 2) молекул среды, проходящего под действием атомов отдачи, внешнего облучения или облучения вследствие
Кафедра радиохимии и
прикладной экологии© |
76 |
|
радиоактивного распада.
Охлажденные до тепловых скоростей горячие атомы отдачи кроме радиационнохимических превращений могут вступать в обычные тепловые реакции и реакции изотопного обмена. О реакциях изотопного обмена подробнее будет речь идти далее.
Атомы отдачи, порвавшие связи с молекулой, с большой скоростью движутся в среде других молекул и атомов. Взаимодействие таких высокоэнергетических атомов со средой проходит в несколько этапов и может быть приближенно описано следующей моделью. Сначала атом отдачи имеет настолько высокую скорость, что электронные оболочки других атомов для него легко проницаемы и на этом этапе идет замедление атомов отдачи в процессе ионизации и возбуждения ими окружающих атомов. Граничная энергия атома отдачи Е, ниже которой ионизация становится невозможной, определяется из уравнения (3.27), в котором Еэ (энергия связи электрона в атоме) для молекул — потенциал их ионизации, для металлов — энергия перехода электрона ионизируемого атома из валентной зоны в зону проводимости.
После охлаждения атома отдачи до энергий ниже Еэ возможно лишь частичное взаимное проникновение электронных оболочек и происходит возбуждение атомов и молекул. Граничная энергия взаимодействия этого вида во много раз ниже Еэ. Замедление атомов отдачи происходит по механизму кулоновского отталкивания, идет так называемое резерфордовское рассеяние, которое осуществляется без образования химических соединений.
Затем начинаются столкновения по типу жестких сфер. Энергия Е (в эВ) начала столкновений по типу жестких сфер может быть найдена из уравнения
E E |
|
2()m M |
z z |
|
|
|
|
|
|
|
R |
|
z |
2/3 z |
2/3 |
, |
(3.28) |
||||
|
M |
1 |
2 |
1 |
2 |
|
||||
где ER — энергия Ридберга (13,6 эВ); m — масса атомов замедляющей среды; Z1 и Z2 — заряды ядер атома отдачи и атомов замедляющей среды.
Только на этапе соударений по типу жестких сфер начинается химическое взаимодействие атомов отдачи с окружающими молекулами. В этой области для приближенного расчета выхода реакций горячих атомов можно воспользоваться простой механической моделью соударений, предложенной Либби и развитой Миллером и Додсоном, Капроном и Ошимой, которая для реакций замещения атомами отдачи атомов близких масс, а также галоген-галогенидных замещений дает удовлетворительные согласия с опытом.
Атомы отдачи, охладившиеся до скоростей, при которых столкновения атом — атом
по типу жестких сфер становятся невозможными, взаимодействуют с окружающими
Кафедра радиохимии и
прикладной экологии© |
77 |
|
молекулами по механизму неупругих соударений атом — молекула. Область энергий, в которой происходят неупругие столкновения, исследована мало, очевидно, она лежит несколько выше энергии связи атома в молекуле. Неупругое соударение атома отдачи с молекулой вызывает возбуждение молекулы (очевидно, локальное) или образование возбужденного комплекса, затем следует разрыв одной-двух связей и образование молекулы или радикала, включающих атом отдачи.
Атомы отдачи, избежавшие химического взаимодействия в области упругих и неупругих соударений (высокоэнергетических – горячих и надтепловых реакций), охлаждаются до тепловых скоростей и могут взаимодействовать с окружающими молекулами по обычным тепловым или радиационно-химическим реакциям или стабилизируются в виде атомов и ионов.
Продуктами реакций горячих атомов могут быть:
а) молекулы исходного вещества с радиоактивным атомом, вошедшим на место стабильного – в этом случае говорят об истинном вторичном удержании, или об удержании в форме исходного соединения;
б) новые химические вещества, образовавшиеся при реакции горячего атома с молекулам исходного вещества (при вхождении их на новое место в молекуле, например, C2H5Br+Br*=C2H4BrBr*+H) или с молекулами растворителя (CH3COOH+Br*= CH3Br*+COOH) – в этом случае идут реакции микросинтеза и если их продукты не извлекаются, то говорят о “кажущемся удержании” или удержании за счет микросинтеза;
в) радиоактивный атом в отличном от исходного атомарном или ионном состоянии – если это не используется для извлечения, то говорят о “кажущемся удержании”.
2.Радиационно-химический синтез и распад как причина удержания (третичное удержание). Если облучаемая мишень состоит из простых молекул, то говорят о радиационно-химическом синтезе, если из сложных, то говорят о радиационно-химическом распаде.
3.Удержание за счет изотопного обмена (смотри раздел 3.9) и тепловых реакций радиоактивных атомов.
3.6.Химические последствия изомерного перехода
Энергия отдачи при изомерном переходе может быть результатом испускания - квантов низкой энергии и электронов конверсии. Величина энергии отдачи оказывается в большинстве случаев ниже энергии связи атомов в молекулах, и, следовательно, в процессе
изомерного перехода не должно происходить нарушения химических связей атома отдачи с
Кафедра радиохимии и
прикладной экологии© |
78 |
|
другими атомами молекулы. Например, для 80mВr энергия отдачи равна 0,015 эВ при излучении -кванта и 0,34 эВ при испусканий электрона конверсии, для 127mТе — 0,034 эВ при излучении -кванта и 0,42 эВ при испускании электрона конверсии и для 69mZn при испускании -кванта — 1,55 эВ и электрона конверсии — 5 эВ. Так как у 69mZn лишь 6% - переходов конвертировано, то 69Zn после -распада 69mZn в его диэтилпроизводном практически весь остается в виде материнского соединения. В то же время имеет место нарушение химических связей 127Те в его диэтилпроизводном, несмотря на то, что энергия отдачи после перехода на низший энергетический уровень ниже энергии связи. Та же картина наблюдается в бромопроизводных, содержащих 80mВr.
Разрушение связей в молекулах при изомерном переходе имеет место во всех случаях, когда изомерный переход сопровождается конверсией электронов независимо от их энергии. Это связано с эффектом Оже, в результате которого атом теряет все или часть внешних электронов. Положение такого атома в молекуле становится неустойчивым и молекула распадается. Известно, например, что при изомерном переходе 80mВr 15% атомов теряют все внешние электроны, 60% — четыре электрона, 10% — два электрона и 2% — один электрон. Если, например, эффект Оже имеет место в соединении НВr, то сначала образуется молекулярный ион НВrz+, затем происходит перераспределение заряда и образуется молекулярный ион Н+Вr(z-1)+, который неустойчив и распадается с образованием возбужденных положительно заряженных ионов брома с высокой кинетической энергией. Затем идут реакции образования ионов брома с окружающими молекулами.
3.7. Химические изменения в результате электронного захвата
Электронный захват, так же как изомерный переход, сопровождается эффектом Оже. Энергия отдачи в этом процессе получается за счет испускания нейтрино. Онa мала, меньше энергии связи у атомов в молекуле и кристаллической решетке, поэтому химические изменения целиком определяются эффектом Оже. Испускание электронов Оже приводит, как было описано, к многократной ионизации атомов. Например, по теоретическим оценкам электронный захват 57Со, находящегося в свободном состоянии, приводит к образованию 57Fe с зарядами от +1 до +7. Высокозарядные атомы взаимодействуют с окружающими ионами. Это является источником энергии для инициирования различного рода химических процессов. Высокий заряд атомов, претерпевших захват электрона, может перераспределяться внутри молекулы и приводить к кулоновскому расталкиванию ее фрагментов.
Кафедра радиохимии и
прикладной экологии© |
79 |
|
Однако в ряде случаев удержание имеет высокое, вплоть до 100%, значение. В комплексных соединениях кобальта, например с лигандами, имеющими сопряженные связи (фталоцианин, витамин В12), железо стабилизируется в аналогичном исходному соединению 57Со виде, что, возможно, связано с нейтрализацией заряда по системе сопряженных связей.
Другое объяснение воссоздания материнской молекулы в твердых веществах — реакции в «гнезде» радикалов, созданных атомом отдачи или путем атом-атомных замещений в сложных молекулах. Эмиссионный спектр Мёссбауэра 57Co3[Co(CN)6]•12Н2О и спектр поглощения Fe3[Co(CN6)]•12Н2О (зеркальный эксперимент) одинаковы. Это показывает, что 57Fe после электронного захвата 57Со стабилизируется только во внешней сфере комплекса. Переход железа во внутреннюю сферу комплекса отсутствует, а следовательно, отсутствует кулоновское расталкивание и образование фрагментов, имеющих большую энергию отдачи, достаточную для прямого замещения атома на атом при столкновении. Электроны Оже способны к радиационному воздействию на окружающие молекулы. Наиболее вероятно образование радикалов, окислительно-восстановительные свойства которых определяют конечные состояния стабилизирующихся атомов. Это модель, предложенная в 1963 г. Виллардом, была названа моделью авторадиолиза.
Втвердых веществах возможен переход процесса Оже с оболочки атома, претерпевшего захват электрона, на соседние атомы. Этот процесс тем вероятнее, чем ближе энергия электронных уровней ионизированного атома совпадает с энергией электронных уровней лигандов. Так как химическая связь изменяет энергетические уровни валентных электронов, то она должна быть ответственна за степень ионизации окружающих атомов.
Ионизированный атом может образовать возбужденный комплекс, который самопроизвольно распадается на фрагменты. Число ионизированных атомов, зависящее от характера протекания процесса Оже, будет определять протекание химических процессов.
Впростых бинарных соединениях роль ионизационных процессов отступает на второй план по сравнению с термодинамическими условиями образования определенного состояния атомов. Условием стабилизации атома железа после захвата электрона 57Со, например в состоянии окисления +3, может являться присутствие катионных вакансий, что имеет место в окислах, или подходящего электростатического потенциала кристаллического поля, создаваемого лигандами. В ряду фторидов металлов: Mn, Fe, Zn, Co, Ni, Mg, начиная с цинка, появляется при распаде 57Со, входящего в виде примеси в соответствующий фторид Fe3+, выход которого монотонно увеличивается в соответствии с электростатическим потенциалом на атоме железа в этих соединениях.
Кафедра радиохимии и
прикладной экологии© |
80 |
|
